
ARTÍCULO ESPECIAL
Oxigenación por Membrana Extracorpórea (ECMO): Experiencia en una Unidad de Cuidado Intensivo Neonatal
Extracorporeal Membrane Oxygenation (ECMO): Experience in a Neonatal Intensive Care Unit
Dr. Eduardo D. Domíngueza, Dra. Gisella Salasa, Dr. Martín Valdésa, Dra. Cecilia Rubioa, Dra. Patricia Bellania, Lic. Sonia Rodasa y Dra. Diana Fariñaa
a. Hospital de Pediatría SAMIC "Profesor Dr. Juan P Garrahan",Área Terapia Intensiva Neonatal, Buenos Aires, Argentina.
Correspondencia: Dr. Eduardo Domínguez: eduecmo@gmail.com
Conflicto de intereses: Ninguno que declarar.
Recibido: 13-4-2012
Aceptado: 4-7-2012
http://dx.doi.org/10.5546/aap.2012.xxx
RESUMEN
La Oxigenación por Membrana Extracorpórea
(ECMO), aún poco desarrollada en la Argentina, es una terapia de rescate altamente invasiva,
destinada a pacientes críticamente enfermos, con
insuficiencia respiratoria grave y fallo cardiovascular asociado o sin él, y una probabilidad de
mortalidad cercana al 80%. Este estudio comunica los primeros pacientes tratados con ECMO
en el Área de Terapia Intensiva Neonatal (UCIN)
del Hospital Garrahan, Buenos Aires.
Desde abril 2008 a enero 2012 fueron tratados
17 pacientes con ECMO veno-arterial, con una
supervivencia del 59%, similar a los informes
internacionales. Los pacientes se encuentran en
seguimiento, evaluándose la evolución a largo plazo.
Palabras clave: ECMO; Neonatos; Lactantes; Insuficiencia respiratoria.
SUMMARY
Extracorporeal Membrane Oxygenation (ECMO),
a poorly developed resource in Argentina, is a
highly invasive rescue therapy, for critically ill
patients with severe respiratory failure with or
without associated cardiovascular failure and
mortality probability near to 80%. This article
reports the experience obtained with first patients treated with ECMO in the Neonatal Intensive Care Unit (NICU) of Hospital Garrahan
at Buenos Aires.
From April 2008 to January 2012, 17 patients
were treated with veno-arterial ECMO. Survival rate was 59%, similar to international reports.
Patients are being monitored to evaluate their
long-term outcome.
Key words: ECMO; Neonates; Infants; Respiratory failure.
INTRODUCCIÓN
La Oxigenación por Membrana
Extracorpórea (ECMO) es una técnica
de asistencia circulatoria desarrollada
para asegurar un adecuado aporte de
oxígeno a pacientes que sufren fallo
respiratorio o cardiovascular (o ambos). En estos pacientes, cuando las
terapéuticas convencionales fracasan,
:la mortalidad supera el 80%.1,2 Esta estrategia terapéutica mantiene las variables respiratorias y hemodinámicas
dentro de límites normales, mientras
los órganos afectados, principalmente, el pulmón y el corazón se mantienen en reposo relativo hasta lograr su
recuperación. La ECMO provee una
entrega de oxígeno adecuada, minimiza el daño que producen las presiones
empleadas en la asistencia respiratoria
mecánica (ARM), brinda una elevada
fracción inspirada de oxígeno y altas
dosis de fármacos vasoactivos. Es un
procedimiento altamente invasivo; requiere la canulación de venas y arterias importantes que luego son ligadas
definitivamente. Las complicaciones
del circuito, y las del paciente pueden
poner en riesgo la vida.
El primer caso exitoso de ECMO
fue practicado en 1972 por Hill, en
un hombre de 24 años con un Síndrome de Dificultad Respiratoria del
Adulto y ruptura de la aorta por un
accidente.3 En mayo de 1975, Bartlett
logró el primer tratamiento exitoso
con ECMO en un recién nacido (RN)
de sexo femenino con un Síndrome
de Aspiración de Líquido Amniótico
Meconial.4,5
Desde entonces, según los datos
de la Organización para el Apoyo Vital Extracorpóreo (Extracorporeal Life
Support Organization, ELSO), existen
en el mundo más de 30 000 pacientes
tratados con ECMO. Luego de más de
30 años del primer informe del caso
neonatal, la ECMO se convirtió en laúltima opción terapéutica para pacientes críticamente enfermos, cuando los
tratamientos convencionales y la terapia máxima han fracasado.
El Grupo de Estudio de ECMO del Reino Unido publicó, en 1996, los resultados de un estudio
clínico aleatorizado que comparó la eficacia de la
ECMO contra la terapia convencional; el estudio
fue detenido antes de completar el reclutamiento
acordado debido a que la mortalidad con la ECMO era de 32% contra el 59% en el grupo convencional, es decir que, por cada 3-4 pacientes
tratados con ECMO se lograba la supervivencia
de un paciente.6 Otras publicaciones han demostrado la eficacia de la ECMO en el tratamiento de
RN con fallo cardiorrespiratorio refractario a las
terapias convencionales.7,8
El Programa de ECMO de la UCIN del Hospital Garrahan comienza en 1998 con un entrenamiento multidisciplinario a través de la
realización de talleres teórico-prácticos y procedimientos de ECMO en porcinos de la raza Landrace.9,10 Luego de una fase de entrenamiento
intensiva se inició la etapa clínica. En el año 2008
se practicó ECMO al primer paciente neonatal en
la Unidad.11
El objetivo de este estudio es presentar los resultados de los primeros 17 pacientes tratados con
ECMO en la UCIN del Hospital Garrahan.
MATERIAL Y MÉTODO
Diseño: estudio descriptivo de informe de serie de casos. Los datos se resumen mediante frecuencias, medias y medianas y desvíos estándar
(DE) o intervalos.
Población: todos los pacientes ingresados en
ECMO, desde el 1 de abril de 2008 hasta el 31
enero de 2012. Los criterios de inclusión al tratamiento figuran en la Tabla 1, adoptados por nuestra Unidad, basados en las guías de tratamiento
de la ELSO.12
Tabla 1: Indicaciones de ECMO - Criterios de inclusión

Variables incluidas en el estudio: edad gestacional (EG), edad al ingreso (EI), peso de nacimiento (PN), peso al ingreso a ECMO (PI),
diagnóstico clínico, índice de oxigenación (IO) al
ingreso a ECMO, días de internación, duración en
horas del procedimiento, supervivencia, complicaciones del paciente y del circuito.
Descripción del Programa de ECMO: el equipo
de ECMO está a cargo de un coordinador médico
y uno de enfermería; cuatro médicos neonatólogos
y doce enfermeros neonatales. Además, cirujanos
cardiovasculares, perfusionistas e integrantes de
los Servicios de: Hematología, Hemoterapia, Cardiología, Farmacia y Diagnóstico por Imágenes.
Durante las 24 h del día el paciente está a cargo de
un neonatólogo y dos enfermeros, uno, asistiendo
al paciente y el otro, al cuidado del circuito. La decisión del ingreso y egreso del paciente a ECMO
es consensuado entre el coordinador médico de
ECMO y el médico a cargo del paciente. En todos
los casos, los pacientes ingresaron con el consentimiento informado de los padres. Los criterios de
suspensión anticipada de la ECMO incluyeron situaciones en las que la continuación del procedimiento agravaba el cuadro del paciente.
Descripción del equipamiento y procedimientos: en todos los casos se practicó ECMO veno-arterial. Se utilizó una bomba oclusiva de rodillos
(Cobe
El paciente se colocaba en una servocuna con
sistema de elevación, en decúbito dorsal, con la
cabeza ubicada a los pies para la canulación de
los vasos del cuello, monitorizado con tensión arterial invasiva, T° corporal central, oximetría de
pulso y registro electrocardiográfico. El circuito se
ensambló en un área separada del sector de internación bajo estrictas normas de asepsia y luego se
purgó secuencialmente con CO2, solución salina
normal, albúmina y finalmente con sangre (cebado del sistema).
En la Figura 1, se observa un esquema del circuito y del sistema de cebado. En la Figura 2, se aprecia una fotografía del equipo y otra, durante
un procedimiento.
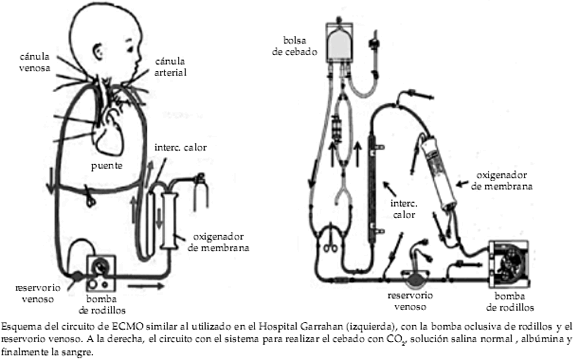
Figura 1. Esquema del circuito ECMO veno-arterial y circuito de cebado
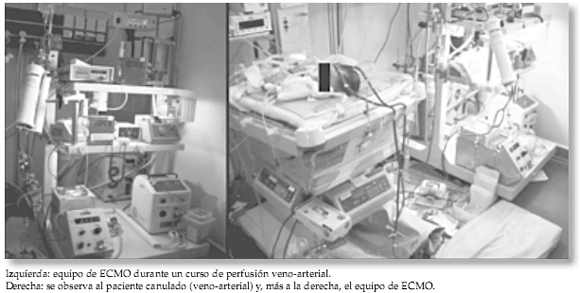
Figura 1. Equipo de ECMO
La anticoagulación se controló con el Tiempo
de Coagulación Activada (TCA) (Medtronic®);
se practicó con infusión continua de heparina
(1 ml= 5000 UI) preparada en una solución de
dextrosa al 5%, equivalente a 0,1 ml/h= 2,5 UI/kg/h. La dosis de inicio fue de 15-25 UI/kg/h,
si el primer TCA en el curso de ECMO era < 300
seg; los controles se efectuaron cada 30-60 min,
con el objetivo de mantener valores de TCA de
180-200 seg. Cada 6 h, se efectuaba el recuento
de plaquetas y, diariamente, factor anti Xa, antitrombina III, coagulograma, fibrinógeno y dímero D.
Se realizó diariamente ecocardiograma y ecografías cerebral y abdominal.
La canulación, en todos los casos, fue realizada
por un cirujano cardiovascular, quien decidía el
tamaño de las cánulas al exponerse los vasos. Se
canuló la vena yugular interna derecha, ubicando
la cánula unos 7,5 cm dentro de la aurícula derecha
(con el extremo 1-2 cm por encima del diafragma)
y la arteria carótida derecha, introducida alrededor de 2,5 cm, con el extremo en la desembocadura de la arteria innominada en el arco aórtico. En
todos los casos se practicó radiografía de tórax y
ecocardiografía para confirmar la normoposición
de las cánulas.
El flujo de ingreso de bomba se incrementó paulatinamente y al alcanzar 80 ml/kg/min
se disminuyeron los parámetros respiratorios al
nivel de "reposo pulmonar": presión inspiratoria máxima= 25/30 cmH2O, presión positiva al
final de la espiración= 10 cmH2O, tiempo inspiratorio= 0,5/0,6 seg, frecuencia respiratoria= 15
ciclos por min y FiO2 = 0,21/0,30. Luego se incrementó el flujo hasta alcanzar 120-140 ml/kg/min según el estado clínico del paciente, con el
objetivo de alcanzar el 80% del gasto cardíaco del
paciente, o sea que se mantenía, estimativamente, un 20% del gasto cardíaco del corazón nativo.
Según la respuesta clínica, SvO2, la radiografía
de tórax y el ecocardiograma se realizaron decrementos graduales del flujo, hasta llegar a valores mínimos (30-60 ml/kg/min), momento en
que se iniciaron las pruebas de suspensión de
ECMO. Si la respuesta era adecuada y luego de
dos pruebas exitosas, se descanulaba al paciente,
finalizando el procedimiento.
Se efectuó hemofiltración/hemodiafiltración
(hemofiltro Argimed®), en caso de insuficiencia
renal o balance hidroelectrolítico inadecuado sin
respuesta a los diuréticos.
RESULTADOS
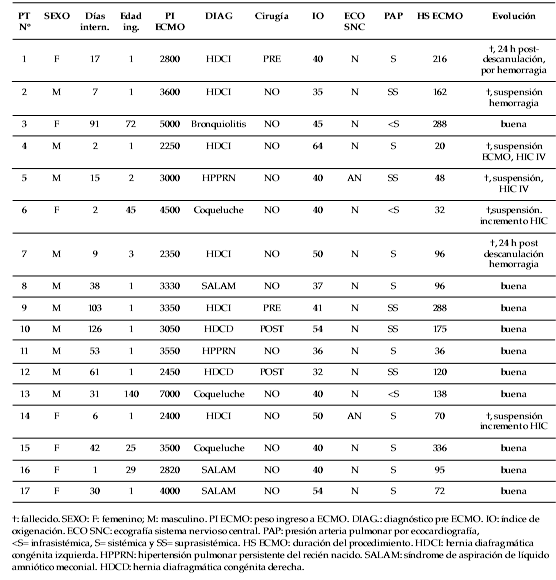
Las características generales de los 17 pacientes al ingreso a ECMO se describen en la Tabla 2. Se excluyó un paciente de 45 días con neumonía por Pertussis que ingresó a ECMO luego de 25 min de paro cardiorrespiratorio, suspendiéndose el procedimiento a los 15 min. La Tabla 3 (ver versión electrónica), presenta la evolución de los 17 pacientes. Antes de ingresar a ECMO, todos los pacientes requirieron fármacos vasoactivos y óxido nítrico. Las cánulas arteriales utilizadas fueron: 8 Fr en 2 pacientes, 10 Fr en 9 y 12 Fr en 6. Las venosas fueron, 14 Fr en 10, 12 Fr en 4 y 10 Fr en 3. Se administró surfactante en 7 pacientes, 4 antes del ingreso y 3 previo al egreso de ECMO.
Tabla 2. Resultados

Tabla 3. Evolución de los pacientes
La dosis de heparina fue variable, con requerimientos de hasta 100 UI/kg/h. Se administró, en
la mayoría de los pacientes, una o más transfusiones diarias de plaquetas.
Las complicaciones del circuito se limitaron
al cambio del oxigenador de membrana debido a
su ruptura (n= 2). Las complicaciones de los pacientes fueron: neumotórax (n= 1); hemorragia del
sistema nervioso central (n= 4); hemoperitoneo
(n= 1); hematoma extenso subcutáneo por infiltración de acceso vascular percutáneo (n= 1); hipertensión arterial (n= 1); sepsis tardía (n= 1). Se
realizó hemofiltración (n= 3) y hemodiafiltración
(n= 2); la mayoría requirió furosemida.
No hubo diferencias entre los sobrevivientes (n= 10) y el grupo de paciente fallecidos
(n= 7) en el peso de ingreso (3360 ± 1245 contra
3360 ± 1291), en el índice de oxigenación (43,4 ± 8
contra 43,4 ± 8) ni en el flujo máximo de bomba
alcanzado (124 ml/k/min contra 131 ml/k/min).
La supervivencia en ECMO fue según diagnóstico:
3/8 hernia diafragmática congénita, 2/3 coqueluche, 1/1 bronquiolitis, 3/3 síndrome de aspiración
de líquido amniótico meconial y 1/2 hipertensión
pulmonar persistente del recién nacido.
Seis de los 8 pacientes con hernia diafragmática congénita (HDC), tenían diagnóstico prenatal.
De los siete pacientes fallecidos, en cinco se
realizó la descanulación electiva, en tres, por
hemorragia intracraneana; otro, presentó una
hemorragia subcutánea de gran extensión secundaria a la infiltración por ruptura de un acceso percutáneo y el quinto, neumonía grave por Bordetella pertussis con arritmia refractaria. Los
dos restantes, fallecieron, luego de la suspensión
electiva de ECMO, uno, por hemorragia abdominal masiva y el otro por fallo multiorgánico
luego de cerrado el ductus (en la necropsia se
constató coartación de aorta grave no diagnosticada por ecocardiografía).
Todos los sobrevivientes concurren al Consultorio de Seguimiento Neonatal de Alto Riesgo.
DISCUSIÓN
La ECMO es una terapia altamente invasiva y
costosa que debe estar reservada para pacientes
con patologías reversibles refractarias a terapias
convencionales máximas, como ventilación de alta frecuencia, óxido nítrico y fármacos vasoactivas
a dosis máximas. A partir de los estudios de Barlett,4,13 esta tecnología se desarrolló en distintos
países para el tratamiento del fallo respiratorio-cardíaco en RN de término o casi término.
Mugford (2008) publicó un metaanálisis de
cuatro estudios con el objetivo de determinar la
eficacia en términos de mortalidad y discapacidad
en la infancia, de la ECMO contra el tratamiento
convencional e incluían la evaluación de la costo-eficacia de esta tecnología; los estudios compartían los criterios de ingreso a ECMO, pero diferían
en la inclusión de pacientes con HDC, traslado y
datos del seguimiento a largo plazo. Se demostró un claro beneficio a favor de la ECMO en la mortalidad (RR 0,44; IC95% 0,31-0,61), que mejoraba
aún más, si se excluían los pacientes con HDC (RR
0,33; IC95% 0,21-0,53).14
El estudio del Reino Unido es el único que
aportó datos de evolución alejada (óbito o discapacidad grave) a los 4 y 7 años (RR 0,62; IC95%
0,45-0,86) y (RR 0,64; IC95% 0,47-0,86) respectivamente, así como el estudio de costo-eficacia.15,16
Nuestro Programa de ECMO Neonatal es el
primero realizado en el país en forma orgánica.
La mayoría de los centros que han desarrollado
ECMO, lo han hecho como continuación del soporte cardiovascular (postcirugía de cardiopatías
congénitas) o en forma aislada. Para el entrenamiento del grupo involucrado se realizaron, en el
bioterio del Hospital Garrahan, catorce sesiones
experimentales en animales y numerosos talleres
teórico-prácticos.9,10
El equipamiento permitió practicar ECMO
sin mayores complicaciones y, pese a la utilización de una bomba oclusiva, no se presentaron
inconvenientes relacionados con la producción de hemólisis ni la presencia de aire.
En nuestra unidad ingresaron a ECMO 17 pacientes, con una supervivencia global del 59%.
Estos resultados son similares a los comunicados
por la ELSO para este conjunto de patologías. En
el caso de los RN con HDC, la supervivencia fue
del 38%, menor a la comunicada, del 52%, en la
ELSO;17 los dos pacientes con HDC derecha sobrevivieron, pese a que esta forma anatómica tiene
peor pronóstico.18
El 75% de los pacientes con malformaciones pulmonares presentaba diagnóstico prenatal. El Hospital Garrahan y la Maternidad Sardá comparten un Programa de Diagnóstico y Tratamiento Fetal, por lo cual, diagnosticadas las
malformaciones, el RN es derivado al nacimiento.
La mayoría de los pacientes fallecidos se encuentran entre los primeros ingresos al Programa,
lo que denota la curva de aprendizaje de neonatólogos, enfermeros y cirujanos. En los primeros
7 pacientes están 6 de los fallecidos, 4, con HDC.
Se asistieron 3 pacientes con neumonía y sepsis por Pertussis, con una supervivencia del 66%.
La gravedad y la mayor morbimortalidad en neonatos y lactantes pequeños por Bordetella pertussis,
fue descripta por varios autores con una mortalidad superior al 50%.19,20
Los 3 pacientes que presentaron SALAM sobrevivieron, coincidente con los informes de la
ELSO en el 200617 y, recientemente, por Singhy.21
Cabe destacar que, en solo un paciente (6%)
de los 17, se aisló un germen (Klebsiella sensible a
cefalosporinas). Constituyó un hallazgo entre los
hemocultivos seriados que se efectúan por protocolo. La incidencia de infecciones durante la ECMO, según distintas publicaciones es variable,
oscilan en 6-50%.22,23
Los aspectos pendientes del programa de ECMO incluyen mejorar los resultados en HDC, disminuir los casos de hemorragias, especialmente
del SNC, y la presentación de los resultados del
neurodesarrollo, a los 18 meses y 3 años de vida
de estos primeros diez sobrevivientes.
Concluimos que, dado los datos presentados,
el desarrollo de la ECMO en el Hospital Garrahan
logró resultados satisfactorios, en un grupo de pacientes cuya predicción de mortalidad superaba el
80%. La curva de aprendizaje aún se encuentra en
desarrollo, pero el Programa se encuentra afianzado y un grupo creciente de profesionales del área se está incorporando al Programa de ECMO.
La introducción de tecnologías nuevas y complejas requiere un fuerte compromiso del recurso
humano y de la institución donde se lleva a cabo. El Programa de ECMO se encuentra en funcionamiento y constituye una oportunidad terapéutica
eficaz para RN gravemente enfermos, quienes no
responden a los tratamientos convencionales.
Agradecimientos
Enfermeras y médicos del Equipo profesional de ECMO del Área de Neonatología, Hospital Garrahan.
Dr. Jorge Barretta; Dr. Javier Cornellis; Dr. Pablo Ruffa: cirujanos cardiovasculares, Hospital
Garrahan, quienes practicaron la canulación de
los pacientes.
Médicos del Área de Neonatología que intervinieron en la primera fase experimental y desarrollo
de la actividad teórico-práctica, Dra. María T. Mazzucchelli, Dr. Daniel Wright y Dr. Jorge Morales
(médicos principales del Área de Neonatología,
Hospital Garrahan).
Dr. Pedro de Sarasqueta () (ex Jefe del Área
de Neonatología, Hospital Garrahan).
Médicos veterinarios: Dres. Marcelo Asprea y
Gustavo Williams (Hospital Garrahan).
Médicos cirujanos cardiovasculares pediátricos y cirujanos pediátricos, que realizaron las primeras canulaciones en Medicina Experimental:
Dr. Horacio Vogelfang, Dr. Gerardo Naiman, Dr.
Mariano Boglione y Dr. Marcelo Martínez Ferro
(Hospital Garrahan).
Servicios y Áreas de Hemoterapia, Farmacia,
Hematología, Cardiología e Imágenes (Hospital
Garrahan).
Perfusionista Estela Carmona (Hospital Garrahan).
Perfusionista Sr. Hugo D. Cardoso (Hospital
Garrahan).
Dr. Carlos Blanco (Profesor en Pediatría/Director de Neonatología, Hospital Académico de
Maastricht, Maastricht, Países Bajos).
Dr. Reese H. Clark (Profesor Asistente de Pediatría, Facultad de Medicina de la Universidad
Emory, Atlanta, Georgia, EE.UU.).
Perfusionista Jorge Ogito (Jefe de Perfusionistas
del Hospital de Niños de Miami, Miami, EE.UU.).
Dr. Ricardo Rodríguez (Jefe de Neonatología
de la Clínica Cleveland, Ohio, EE.UU.).
Empresa Coto.
Fundación Guido Candolfi.
Fundación del Hospital Garrahan.
1. Ortiz RM, Cilley RE, Batlett RH. Extracorporeal membrane oxigenation in pediatric respiratory failure. Pedatric Clin North Am 1987;34:39-46.
2. Beck R, Anderson KD, Pearson GD, Cronin J, et al. Criteria for extracorporeal membrane oxygenation in a population of infants with persistent pulmonary hypertension of the newborn. J Pediatr Surg 1986;21:297-302.
3. Hill JD, O´Brien TG, Murray JJ, Dontigny L, et al. Extracorporeal oxygenation for acute post traumatic respiratory failure (shock-lung syndrome): use the Bramson membrane lung. N Eng J Med 1972;286:629-34.
4. Bartlett RH, Gazzaniga AB, Jeffries MR, Huxtable RI, et al. Extracorporeal membrane oxygenation (ECMO) cardiopulmonary support in infancy. Trans Am Soc Artif Intern Organs 1976;22:80-93.
5. Bartlett RH, Esperanza (ASAIO Presidential Address). Trans ASAIO 1985;30:723-5.
6. UK Collaborative ECMO Trial Group. UK collaborative randomized trial of neonatal extracorporeal membrane oxygenation. Lancet 1996;348:75-82.
7. Walker G, Liddell M, Davis C. Extracorporeal Life Support-state of the art. Pediatr Respirat Rev 2003;4:147-52.
8. Douglas R, Hansel RRT. Extracorporeal membrane oxygenation for perinatal and pediatric patients. Respiratory Care 2003;48(4):352-62.
9. Domínguez ED. Conferencia: "Implementación de ECMO en nuestro país". 9° Jornadas Nacionales de Neonatología; 6° Jornadas Interdisciplinarias de Seguimiento Neonatal de Alto Riesgo. Sociedad Argentina de Pediatría. Buenos Aires, 21-23 de agosto de 2008. Disponible en: http://www.sap.org.ar/stractifles/actividades/congresos/.../dominguez.pdf.
10. Domínguez ED, Salas GL, Bellani PA, Rodas S, et al. Utilización de un modelo animal para entrenamiento en oxigenación por membrana extracorpórea (ECMO). Medicina Infantil 2008;XVI(3):248-54.
11. Domínguez ED, Rodas S, Bellani PA, Rubio C, et al. Oxigenación de Membrana Extracorpórea, reporte de los primeros pacientes tratados en el Área de Terapia Intensiva Neonatal del Hospital de Pediatría SAMIC "Prof. Dr Juan P. Garrahan". Resúmenes de trabajos libres. 1° Congreso Argentino de Neonatología. Octubre de 2010. Disponible en http://www.sap.org.ar/images/stories/Neo_Res2010.pdf.
12. Short BL, Williams L. ECMO specialist training manual. 3rd ed. Extracorporeal Life Support Organization; 2010.
13. Bartlett RH. Surgery, science and respiratory failure. J Pediatr Surg 1997;32:1401-7.
14. Mugford M, Elbourne D, Field D. Extracorporeal membrane oxygenation for severe respiratory failure in newborn infants. Cochrane Database Syst Rev 2008; Issue 3: CD001340 Review.
15. Bennett C, Johnson A, Field D, Elbourne D for UK Collaborative ECMO trial group. UK collaborative randomised trial of neonatal extracorporeal membrane oxygenation: follow up to age 4 years. Lancet 2001;357:1094-6.
16. Petrou S, Bischof M, Bennett C, Elbourne D, et al. Cost-effectiveness of neonatal extracorporeal membrane oxygenation based on 7-year results from the United Kingdom Collaborative ECMO Trial. Pediatrics 2006;117(5):1640-9.
17. ELSO, Extracorporeal Life Support Organization, Ann Arbor, MI. Pediatric Respiratory Care Statistics. International Summary as of January; 2006.
18. Fisher JC, Jefferson RA, Arkovitz MS, Stolar CJ. Redefining outcomes in right congenital diaphragmatic hernia. J Pediatr Surg 2008;43:373-9.
19. De Berry BB, Lynch JE, Chung DH, Zwischenberger JB. Pertussis with severe pulmonary hypertension and leukocytosis treated with extracorporeal membrane oxygenation. Pediatr Surg Int 2005;21(8):692-4.
20. Castagnini L, Munoz F. Clinical characteristics and outcomes of neonatal pertussis: a comparative study. J Pediatr 2010;156:498-500.
21. Singh BS, Clark RH, Powers RJ, Spitzer AR. Meconium aspiration syndrome remains a signifcant problem in the NICU: outcomes and treatment patterns in term neonates admitted for intensive care during a ten-year period. J Perinatol 2009;29(7):497-503.
22. Lequer L. Extracorporeal life support in pediatric and neonatal critical care: A Review. J Intensive Care Med 2004; 19:243-58.
23. Segura S, Cambra FJ, Moreno M, Thio M, et al. ECMO: experiencia en edad pediátrica. An Pediatr (BARC) 2009; 70(1):12-19.