
Figura 1. Unidad de remodelamiento óseo.
BIOQUÍMICA CLÍNICA
Marcadores bioquímicos del remodelamiento óseo. Utilidad clínica
Biochemical markers of bone remodelling. Clinical utility
Belen Reynaga Montecinos1, Susana Noemí Zeni2
1. Bioquímica
2. Dra. Ciencias Químicas
Sección Osteopatías Médicas. Hospital de Clínicas. Facultad de Medicina. Universidad de Buenos Aires y CONICET. Buenos Aires. Argentina.
Resumen
El esqueleto se renueva continuamente mediante el proceso de remodelamiento óseo, reemplazando hueso viejo y dañado por hueso nuevo. Este proceso es llevado a cabo en pequeños paquetes celulares denominados "unidades de remodelamiento óseo" (URO) por acción combinada de las células óseas. Los osteocitos iniciarían y la parathormona determina el nivel del proceso. El remodelamiento de todo el esqueleto puede evaluarse mediante los marcadores bioquímicos del remodelamiento óseo. Los marcadores de formación (fosfatasa alcalina ósea, osteocalcina y propéptidos del colágeno tipo I amino y carboxilo terminal) provienen de la actividad de osteoblastos y los de resorción (fosfatasa ácida tartrato resistente 5b, telopéptidos carboxilo y amino terminales, piridinolinas, hidroxiprolina y calciuria) de los osteoclastos. La utilidad clínica de los marcadores consiste en determinar cambios en el remodelamiento óseo ya que al ser más rápida la resorción que la formación, todo aumento llevaría a pérdida de masa ósea. Si bien no sirven para diagnosticar, la identificación de individuos con alto remodelamiento permitiría comenzar con una terapia preventiva que evite la pérdida de hueso. Los más sensibles y específicos pueden determinar el riesgo relativo de fracturas. Para interpretar su valor correctamente se deben considerar las variaciones preanalítica, analítica y biológica del marcador bioquímico utilizado.
Palabras clave: Marcadores bioquímicos óseos; Remodelamiento óseo; Osteoporosis; Marcadores óseos de formación y de resorción; Utilidad clínica
Summary
Bones are continuously undergoing remodeling as a result of the coordinated actions of bone cells. This process occurs in discrete regions or basic multicellular units (BMUs) and ensures the maintenance of skeletal integrity and bone mass. The rate of bone remodelling can be monitored quantitatively by measuring biochemical markers of bone turnover. Bone formation markers (bone alkaline phosphatase, osteocalcin, type I collagen extension propeptides) reflect osteoblast activity and bone resorption markers (pyridinium crosslinks, N-terminal type I collagen C-crosslinking telopeptides, tartrate resistant acid phosphatase 5-b, hydroxyproline and urinary calcium) reflect osteoclast activity. Bone markers are useful to detect changes in bone turnover. As bone resorption is faster than bone formation, the increase in bone turnover markers can be regarded as a risk factor for rapid bone loss. Although bone markers provide little information in osteoporosis diagnosis, they can identify fast bone losers who will benefit from a preventive therapy and thereafter monitor the efficacy of the treatment. The most sensitive and specific markers may predict fractures risk, independently of bone density. For interpreting the results of the bone marker test used, it is necessary to consider the main sources of variability which include preanalytical, analytical and biological conditions.
Key words: Biochemical bone markers; Bone remodelling; Osteoporosis; Bone formation and resorption markers; Clinical utility
Introducción
Remodelamiento óseo
Una correcta salud ósea es indispensable para que
el esqueleto pueda cumplir con sus tres funciones
fundamentales: mecánica, como soporte del cuerpo;
protectora de los órganos internos que delimita y metabólica
como reserva de iones, principalmente calcio
(Ca) y fósforo (P) (1). Para ello, el esqueleto cuenta
con la habilidad de renovarse continuamente mediante
el proceso de remodelamiento óseo (del inglés
turnover) que comienza tempranamente, en el útero, y continúa hasta la muerte del individuo.
El remodelamiento óseo no es más que el reemplazo
periódico de hueso viejo y dañado por hueso
nuevo, en el mismo sitio, reparando el daño por fatiga
del material que pudiera producirse por la acumulación
de mineral. Este proceso es el responsable de
la completa regeneración del esqueleto adulto cada
10 años (2).
El recambio óseo comprende dos etapas: resorción
y formación ósea que son llevadas a cabo por el esfuerzo
colaborativo y secuencial de un grupo de células que
se encuentran dentro de una estructura temporaria denominada "unidad de remodelamiento óseo" (URO)
(Fig. 1) (3). Es decir, la resorción del hueso viejo y su
reemplazo por hueso nuevo es producto de la acción
principal de dos tipos celulares diferentes: osteoclastos
y osteoblastos que, a pesar de no encontrarse separados,
son independientes.

Figura 1. Unidad de remodelamiento óseo.
El remodelamiento es un proceso cíclico que comienza con el hueso en estado de reposo y culmina de igual manera. En todo el esqueleto y en un período de tiempo dado millones de estas UROs se encuentran operando en diferentes estadios del ciclo (4). Cada URO permanece inactiva aproximadamente de 6 a 8 meses aunque continúa acumulándose mineral con lo cual el hueso se endurece y pierde elasticidad. Las alteraciones biomecánicas producidas por este envejecimiento hacen que comiencen a producirse "microfracturas" las que, por una señal no del todo clara, son detectadas por células inmersas en la matriz mineralizada. Estas células liberan factores hacia la superficie ósea desencadenando el inicio del ciclo de remodelamiento en el que se evidencian 4 fases: activación, resorción, reversión y formación (Fig. 2).

Figura 2. Ciclo de remodelamiento óseo (5).
La activación produce la atracción desde la circulación
de precursores osteoclásticos mononucleares
(provenientes de progenitores hematopoyéticos) cuya
diferenciación celular a preosteoclastos multinucleados
es realizada por citoquinas provenientes de las células
en reposo que tapizan la superficie ósea y otras células
del mesénquima. Los preosteoclastos se pegan a
la superficie a resorber mediante receptores de integrinas
presentes en sus membranas que tienen la particularidad
de unirse a determinados péptidos presentes
en la matriz extracelular que contienen la secuencia arginina-
glicina-aspártico (RGD). Dicha unión delimita
un compartimento denominado "laguna de resorción" y desencadena la polarización del osteoclasto que emite
prolongaciones citoplasmáticas llamadas "ribete en
cepillo" a través de las cuales volcarán sus productos
iniciando la siguiente fase denominada de resorción
propiamente dicha.
Durante la fase resortiva una bomba de protones
(H+) específica y otros canales iónicos presentes en la
membrana del ribete en cepillo del osteoclasto producen
una disminución considerable del pH en la laguna
de resorción. Esta acidificación es acompañada por la
secreción de una serie de enzimas lisosomales tales como
fosfatasa ácida tartrato resistente (TRAP) y catepsina
K, así como metaloproteasas de la matriz (MMP)
entre las que se encuentran colagenasas como la
MMP-9. La disminución del pH en forma conjunta
con la liberación de enzimas que presentan actividad
máxima a pH ácidos produce la degradación del cristal
de hidroxiapatita y en forma subsiguiente la del colágeno
creando cavidades denominadas "lagunas de
Howship" en el hueso trabecular y túneles cilíndricos
en el hueso cortical (6).
Generalmente se encuentra sólo uno o a lo sumo
dos osteoclastos en el mismo sitio resortivo pero, en
condiciones de resorción exagerada, es posible encontrar
hasta cuatro o cinco células resortivas (7)(8). La
resorción es un proceso rápido que dura aproximadamente
10 a 12 días, finaliza con la apoptosis del osteoclasto
y es seguida por la fase reversa.
Durante la etapa de reversión la laguna de resorción
es reemplazada por monocitos y osteocitos, que fueron
liberados de la matriz mineralizada durante la resorción,
y por preosteoblastos que fueron reclutados
para comenzar a formar nuevo hueso. En esta etapa es
donde se producen las señales de acoplamiento más
importantes y aunque, hasta el momento, la naturaleza
exacta de dichas señales es desconocida existen una
serie de hipótesis respecto a ello. Una sugiere que, durante
la resorción, los osteoclastos liberarían ciertos
factores de crecimiento que habían quedado inmersos
en la matriz ósea mineralizada, los que actuarían como
factores quimiotácticos osteoblásticos estimulando su
proliferación y diferenciación. Alguno de los candidatos
potenciales sugeridos son factor de crecimiento tumoral
beta (TGFb); factor de crecimiento insulínico I
y II (IGF I y II); proteínas morfogenéticas (BMPs); factor
de crecimiento y diferenciación plaquetario
(PDGF) y factor de crecimiento fibroblástico (FGF).
Entre todos ellos el principal candidato es el TGFb, ya
que diversos estudios demostraron que prolonga la vida
media de los osteoblastos inhibiendo su apoptosis,
a la vez que inhibe la producción por dichas células de
otros factores que aumentan la resorción (9)(10).
Otra de las teorías sugeridas es que el propio osteoclasto
jugaría un rol en el acoplamiento (4) donde estarían
implicadas señales bidireccionales entre osteoblastos
y osteoclastos vía receptores de efrina (11).
En el adulto, y debido al proceso de acoplamiento,
los osteoblastos son atraídos al lugar donde se generó previamente la resorción. Esta etapa es la menos conocida de todo el ciclo de remodelamiento, no se observa
durante el crecimiento, por ello se denomina de
"modelamiento". A diferencia del remodelamiento, el
modelamiento no se encuentra acoplado en el sentido
de que la formación puede producirse donde previamente
no existió resorción, siendo así el responsable
del crecimiento en largo y ancho de los huesos.
La formación comprende dos etapas en las que los
osteoblastos sintetizan primeramente la matriz del osteoide
y luego regulan su mineralización. Los osteoblastos
provienen de progenitores mesenquimáticos
que pueden proliferar y diferenciarse a precursores osteoblásticos,
preosteoblastos y osteoblastos maduros
(12). A diferencia del osteoclasto que llega al hueso
desde la circulación, los precursores osteoblásticos mayoritariamente
lo alcanzan por migración de progenitores
desde los tejidos conectivos circundantes (2).
Cuando el hueso está inactivo los osteoblastos se encuentran
sobre la superficie ósea y se las denomina células
en reposo. Estas células presentan una forma alargada,
plana que se modifica hacia una forma cúbica
cuando existe formación activa. Dentro de la cavidad
de resorción los osteoblastos primeramente forman
una capa sintetizando proteínas de la matriz, principalmente
colágeno tipo I y otras proteínas no colágenas
(osteocalcina, osteonectina, factores de crecimiento,
citoquinas, etc), todas ellas importantes para el proceso
de mineralización. A continuación se incorporan
factores locales y citoquinas produciendo la maduración
del osteoide. Sobre las fibras de colágeno maduro
comienza el proceso de calcificación correspondiente
a la incorporación de cristales de hidroxiapatita.
Todos estos procesos determinan que, a diferencia de
la resorción, la formación sea más lenta (3 meses).
Los osteoblastos gatillan la mineralización liberando
pequeñas vesículas pegadas a su membrana denominadas
vesículas matriciales, que establecen condiciones óptimas para iniciar la deposición de mineral. Dichas
vesículas concentran iones calcio y fosfato y enzimas
que degradan a los inhibidores de la mineralización como
pirofosfatos y proteoglicanos presentes en la matriz
extracelular. A medida que la mineralización continúa,
los osteoblastos quedan inmersos en la matriz y cambian
su morfología transformándose en osteocitos
(4)(13). Es decir, que al cumplir su función, sólo aproximadamente
el 20% de los osteoblastos muere por
apoptosis, el resto queda inmerso dentro de la matriz
mineralizada que ellos mismos produjeron transformándose
en osteocitos. Estas células no proliferativas
corresponden al último estadio de diferenciación de
las células del linaje osteoblástico, son relativamente
inertes metabólicamente y como se ubican dentro de
lagunas osteocíticas rodeadas de un tejido mineralizado
duro pierden su capacidad migratoria.
Los osteocitos han tomado un interés creciente en
los últimos años ya que se ha descubierto que participan
activamente en la regulación homeostática del remodelamiento óseo. Estas células se caracterizan por
tener una morfología estrellada que recuerda la trama
dendrítica del sistema nervioso. Son las células más
abundantes del hueso (10 osteocitos cada 1 osteoblasto)
y se comunican entre sí o con células de la superficie ósea mediante múltiples extensiones de sus membranas
citoplasmáticas. Mediante estas proyecciones
forman un sincisio celular estratégico de redes de conexión
(uniones "gap") que representarían un sistema
muy eficiente en la transmisión metabólica de señales
a través de enormes distancias (14). Su localización las
transforma en excelentes células mecanosensoras capaces
de detectar señales de "estrés mecánico" (15),
las que traducen en señales químicas (citoquinas), son
enviadas a la superficie iniciando así el proceso del remodelado óseo (Fig. 1) (9). El osteocito se polariza en
el sentido de que sus prolongaciones son más numerosas
hacia la superficie del hueso para conectarse con
células en reposo y/o con osteoblastos. Los osteocitos
también participan en la finalización del proceso de
formación ya que secretan una citoquina denominada
esclerostina que tiene la particularidad de suprimir la
función osteoblástica (16).
Control del remodelamiento óseo
Para que se inicie el remodelamiento óseo debe
existir una correcta comunicación osteoblasto-osteoclasto
asociados en tiempo y espacio en la misma
URO. Existen tres modelos sugeridos de comunicación
celular; uno de ellos determina una comunicación
directa entre estas dos células mediante ligandos
y receptores unidos a las membranas celulares que interaccionan
iniciando señales intracelulares; otro sugiere
la existencia de interconexiones tipo uniones "gap" permitiendo el pasaje de pequeñas moléculas
entre ambas células, y finalmente el tercero señala que
las comunicaciones podrían efectuarse por factores
parácrinos difusibles como citoquinas, factores de crecimiento,
quimioquinas u otras moléculas.
El remodelamiento óseo se inicia en respuesta a diferentes
estímulos entre los que se encuentran: generación
de microfracturas con pérdida de carga mecánica,
baja concentración del Ca++ en el líquido
extracelular (LEC) y alteración en la concentración de
hormonas y citoquinas.
La apoptosis del osteocito produce señales regulatorias
que desencadenan la diferenciación osteoclástica
para iniciar la reparación del hueso dañado. Los osteocitos
determinarán qué parte del hueso se degradará ya
que censan microfracturas y pérdida de carga mecánica
y mediante sus prolongaciones dendríticas envían señales
químicas (citoquinas) que se encuentran involucradas
en la interacción celular hacia la superficie ósea. En este sentido, dos de las señales osteociticas
potenciales involucradas en la iniciación del remodelamiento
son el TGF-b y el óxido nítrico (NO), las que
inducirían en las células de la progenie osteoblástica la
secreción del factor estimulante de colonia de macrófagos
(f-SCM), citoquina indispensable para el reclutamiento,
diferenciación y sobrevida de células del linaje
osteoclástico, ya que controla la migración celular y
la reorganización del citoesqueleto.
La homeostasis del Ca++ del LEC está regulada por la
parathormona (PTH), principal factor hormonal que
determina el nivel del remodelamiento óseo. El rol homeostático
de dicha hormona induce un aumento en la
resorción del hueso para mantener la concentración de
Ca++ constante. Sin embargo, los osteoclastos no presentan
receptores para PTH, por lo cual, el reclutamiento,
maduración y actividad de estas células por parte
de PTH es indirecto. Son los osteoblastos quienes
poseen receptores para PTH, por ello son activados por
la hormona liberando citoquinas que favorecen la diferenciación
y sobrevida, a la vez que inhiben la apoptosis
del osteoclasto. Este grupo de citoquinas pertenece al
sistema regulador del remodelamiento óseo llamado:
Sistema RANK - RANKL - OPG (11) (Fig. 3).
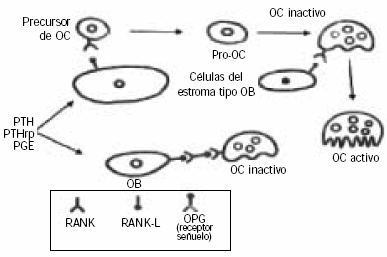
Figura 3. Sistema RANK-RANKL-OPG (19).
La PTH estimula la liberación al medio del ligando
del receptor activador del factor nuclear NF-kB
(RANKL). Este factor es una proteína sintetizada por
osteoblastos, células en reposo y células del estroma
que puede encontrarse unida a la membrana plasmática
o en forma soluble. En forma soluble también es
secretada por los linfocitos T activados. El RANKL se
unirá al receptor-activador del factor nuclear NF-kB
(RANK) que se encuentra presente en la membrana
del preosteoclasto favoreciendo su diferenciación, activación
a osteoclasto maduro y sobrevida inhibiendo
su apoptosis.
La osteoprotegerina (OPG) es un receptor trampa
(decoy) que actúa como antagonista del RANKL. Es
una proteína liberada por los osteoblastos en forma soluble
para proteger al esqueleto de una excesiva resorción ósea. Al unirse al RANKL lo bloquea para su
unión al RANK inhibiendo la diferenciación y activación
del precursor osteoclástico y aumentando su
apoptosis, por lo cual la relación RANKL/OPG es indicativa
de la osteoclastogénesis en una serie de enfermedades
del remodelamiento óseo (11)(17) (Fig. 3).
Por otra parte, varias quimioquinas son utilizadas
por los osteoblastos para comunicarse con los precursores
osteoclásticos. Entre ellas la Proteína Quimiotáctica
Monocítica-1 (MCP-1), también conocida como CCL2
es producida por los osteoblastos y es una de las principales
candidatas para actuar en el reclutamiento de precursores
osteoclásticos. La expresión osteoblástica de
MCP-1 es activada por citoquinas proinflamatorias como
factor de necrosis tumoral beta (TNF-b) e interleuquina
1 alfa (IL-1a) y por PTH, mientras que la de sus
receptores osteoclásticos es activada por RANKL. Asimismo,
las células en reposo expresan moléculas de adhesión
intercelular-1 (ICAM-1) que podrían predisponer
o limpiar la superficie ósea mediante la activación
de MMP previo a la resorción osteoclástica (18).
Marcadores bioquímicos del remodelamiento óseo
En un determinado período de tiempo se estima que
sólo el 10% de la superficie ósea se encuentra en remodelación,
sin embargo los distintos tipos de hueso no poseen
la misma actividad remodelatoria. El 80% del esqueleto
está formado por hueso cortical y sólo el 20%
del volumen óseo por hueso trabecular, siendo este último
el metabólicamente más activo y el que aporta el mayor
porcentaje al recambio óseo de todo el esqueleto. La
frecuencia con que la superficie ósea se activa, o sea la
frecuencia de activación, determinará el número de sitios
de remodelamiento presentes en el hueso, por lo
cual la sumatoria de actividad de todas esas UROs, o sea
la actividad remodelatoria de todo el esqueleto, puede
evaluarse bioquímicamente a través de la medición de
los marcadores bioquímicos del remodelamiento óseo.
Estos marcadores bioquímicos óseos son productos
secretados por la actividad de las células óseas que se
liberan al torrente sanguíneo y pueden ser determinados
en sangre y/o orina (20). Los que provienen de la
actividad de los osteoblastos se denominan "marcadores
de formación" y todos ellos se evalúan en sangre.
Los provenientes de la actividad de los osteoclastos se
denominan "marcadores de resorción" y aunque en
un principio se determinaban en orina, actualmente
es posible evaluarlos en suero (3)(20).
En la Tabla I se enumeran los marcadores bioquímicos
del remodelamiento óseo actualmente disponibles
en forma comercial.
Tabla I. Marcadores bioquímicos óseos disponibles comercialmente.

Los marcadores de formación provienen de enzimas propias del osteoblasto y su progenie, de proteínas derivadas del colágeno tipo I y de otras proteínas no-colágenas.
FOSFATASA ALCALINA TOTAL (FAL) Y FOSFATASA ALCALINA ÓSEA (FAO)
La FAL es una glicoproteína tetramérica que pertenece
a una gran familia de proteínas unidas a las membranas
celulares plasmáticas mediante un grupo glicano-fosfatidil-inositol carboxilo terminal. La FAL tiene
una vida media de 1-2 días, lo que contribuye a que su
variación diurna sea mínima.
La FAL en suero circula como un dímero con dos
sitios activos simétricos y su actividad comprende a la
de varias isoformas que se originan en diferentes tejidos
(hígado, hueso, intestino, bazo, riñón, placenta o
por expresión de tumores) (13)(21) siendo las dos
fracciones mayoritarias las fosfatasas ósea (FAO) y hepática.
En condiciones normales los niveles sanguíneos
de FAO corresponden a sólo el 40% de la FAL total,
el resto es fundamentalmente hepático aunque en
ciertos casos pueden encontrarse fracciones significativas
de naturaleza intestinal o placentaria (4). En niños
y adolescentes la isoenzima predominante es la
FAO que puede alcanzar un nivel entre 70% y 90% de
la FAL (13)(21).
Las isoenzimas hepáticas y ósea son idénticas en su
composición aminoacídica pero modificaciones postraslacionales
hacen que presenten distinta movilidad
electroforética, reactividad frente a la leptina de germen
de trigo, susceptibilidad al calor e inhibición química.
Estos métodos se utilizan para separarlas (4)(21).
Una vez descartada la falla hepática, los niveles de
FAL ofrecen certeza de la actividad osteoblástica (13),
sin embargo es un marcador inespecífico de hueso. La
actividad poblacional sérica de FAL presenta una variación
mayor que la intra-individual, por ello no es
posible detectar cambios menores en su concentración.
Esto hace que carezca de sensibilidad y especificidad
en condiciones en las que el nivel de incremento
del remodelamiento óseo es mediano, como en la
osteoporosis. Por su fácil realización y bajo costo se
continúa utilizando para evaluar cambios en el remodelamiento
en sujetos con función hepática normal.
Contrariamente, es un muy buen marcador óseo para
determinar la actividad y realizar el seguimiento terapéutico
de la enfermedad de Paget (21).
La isoforma ósea es sintetizada por los osteoblastos
maduros y sus precursores. Aunque su función precisa
no ha sido aún bien establecida es sabido que juega un
rol importante en la formación e iniciación de la mineralización ósea. Por ello, la medición de su actividad
en suero es una medida indirecta del proceso de formación,
más sensible y específica que la de FAL.
La determinación sérica de FAO presenta poca variabilidad
entre sujetos, baja variabilidad metodológica
y biológica (4). En osteoporosis con bajo remodelado
no es muy sensible aunque su mayor utilidad radica
en detectar el incremento del remodelamiento óseo
durante la postmenopausia (21). En la actualidad, la
sensibilidad y especificidad clínica de FAO se ha incrementado
por la disponibilidad comercial de inmunoensayos
con anticuerpos monoclonales específicos.
Osteocalcina
La osteocalcina (OC) es el constituyente proteico no colágeno más importante de la matriz ósea con un porcentaje que ronda el 15%. Corresponde a un pequeño péptido de 49 aminoácidos sintetizado por los osteoblastos en los últimos estadios de la formación ósea como una molécula precursora llamada pro-osteocalcina y bajo el control de la vitamina D. Este propéptido contiene tres residuos de ácido glutámico (glu) en las posiciones 17, 21 y 24 que se carboxilan postraslacionalmente a ácido carboxiglutámico (gla) en una reacción dependiente de vitamina K. La fracción propeptídica se elimina de la molécula al mismo tiempo que la proteína carboxilada se vuelca al espacio extracelular donde se une a la hidroxiapatita vía Ca++ a través de los residuos de gla (Fig. 4).
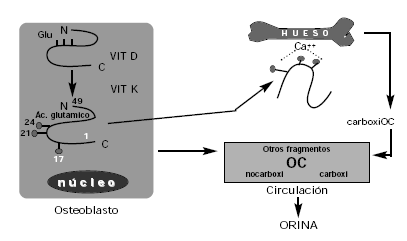
Figura 4. Metabolismo de la osteocalcina.
Los niveles de OC no carboxilada se encuentran suprimidos
en individuos bajo tratamiento con glucocorticoides
lo que podría reflejar, en parte, la acción de
estos compuestos sobre la expresión del gen de OC
(20). Asimismo, recientemente se la ha señalado como
una "hormona" del osteoblasto que regularía el metabolismo
lipídico y energético (23).
Por otra parte, la medición de OC no carboxilada
es considerada un índice de deficiencia de vitamina K
y podría jugar un rol, en el futuro, para predecir la masaósea y el riesgo de fracturas (24).
Propéptidos de colágeno tipo I
Los propéptidos de procolágeno derivan del colágeno
tipo I, principal proteína extracelular de la matriz ósea. Aunque el colágeno tipo I no es exclusivo del
hueso, el que se encuentra en tejido óseo tiene ciertas
características propias. Es un heterodímero constituido
por dos cadenas a1 (I) y una cadena a2 (I) que presenta
una larga cadena media helical y dos regiones
cortas no helicoidales propeptídicas a cada extremo
de la cadena. Los osteoblastos sintetizan el colágeno tipo
I en una fase temprana de su diferenciación en forma
de una cadena prepro-alfa. El gen COL1A1 que
se encuentra en el cromosoma 17 y el gen COL1A 2
presente en el cromosoma 7 codifican para ambas cadenas.
El preprocolágeno en el retículo endoplasmático
rugoso pierde la fracción N-terminal y se transforma
en procolágeno el cual será modificado
post-traslacionalmente por varias enzimas específicas
del tejido óseo. Estas modificaciones incluyen la hidroxilación
de residuos de lisina y prolina; glicosilación
de la hidroxilisina a galactosil-lisina o gluco-galactosil-
hidroxilisin y por último, la fosforilación de
residuos de serina. Mientras la glicosilación ocurre en
la fracción C-terminal, la fosforilación ocurre en el extremo
N-terminal de los propéptidos.
Las tres cadenas alfa se ensamblan mediante puentes
disulfuro dando el propéptido de colágeno tipo I
que se caracteriza por tener largas extensiones terminales
propeptídicas amino (N-) y carboxilo (C-) terminal.
Mientras el propéptido C-terminal (PICP) es globular,
el propéptido N-terminal (PINP) es parte
globular y parte helical. El procolágeno tipo I es secretado,
vía el complejo de Golgi, al espacio extracelular
donde es degradado por endopeptidasas. El PICP es
separado en primer lugar por la Proteína Morfogénica
1 (BMP1) (25), mientras el PINP es liberado luego
por otras enzimas. El colágeno tipo I se incorpora a la
matriz ósea y los propéptidos pasan a la circulación
donde pueden evaluarse como marcadores de formación
por inmunoensayos específicos (13) (Fig. 5).

Figura 5. Fracciones propeptídicas del colágeno tipo I.
El colágeno tipo I no es específico del hueso pero,
entre aquellos que lo contienen, este tejido es el que
presenta mayor remodelamiento por ello sus propéptidos,
en concordancia con estudios histomorfométricos,
reflejan la actividad total de formación ósea. Distintos estudios avalan este concepto y demuestran que
la fracción N-terminal es la de mayor utilidad clínica.
Existen varios ensayos para la medición de PINP,
uno de ellos es un ELISA (P1NP) que utiliza anticuerpos
policlonales dirigidos contra una secuencia sintética
de la cadena proalfa 1 (26) obtenida de liquido
amniótico (27); otro es un RIA donde el antígeno se
obtiene de cultivos celulares de osteosarcoma (28). En
el primer caso la concentración de PINP obtenida es
100 veces mayor que la del PICP, ya que este ensayo
mide tanto la fracción intacta como un pequeño fragmento
del Col1 que se obtiene por metabolización renal
del PINP y que, por lo tanto, se acumula en IRC.
El método RIA sólo mide la fracción intacta. Su medición
es utilizada en la menopausia para detectar cambios
en la remodelación ósea y para el seguimiento en
la terapia con estrógenos (21).
El PICP puede medirse por RIA (29) o ELISA. Sin
embargo, presenta poca especificidad y falta de respuesta
en condiciones de bajo recambio óseo (30).
MARCADORES DE RESORCIÓN
Con excepción de la fosfatasa ácida tartrato resistente 5b (TRAP5b) que es una enzima propia del osteoclasto, la mayoría de los marcadores de resorción ósea son productos de degradación del colágeno óseo tipo I. Otros marcadores de resorción ósea evaluados, pero que hasta el momento no son utilizados clínicamente, son las proteínas no colagenosas como sialoproteína ósea (BSP) que, si bien no es un producto proveniente del osteoclasto, se incorpora a la matriz y se libera durante el proceso de resorción. Recientemente se ha ensayado como marcador de resorción a la catepsina K derivada de la actividad osteoclástica.
Calciuria
El calcio urinario de 24 h proviene del metabolismo general y representa la cantidad filtrada por los glomérulos y no reabsorbida a nivel de los túbulos renales, siendo los valores de referencia de hasta 250 mg/24 h en la mujer y hasta 300 mg/24 h en el hombre. La calciuria de 2 h se mide en la 2º orina de la mañana recogida en ayunas después de ingerir 200 cm3 de agua destilada. Se expresa en mg/mg de creatinina. Ambas muestras son poco específicas y sensibles pero como se trata de un marcador muy económico y accesible a cualquier laboratorio de rutina se lo utiliza actualmente para detectar cambios en el recambio óseo (21).
Hidroxiprolinuria
La hidroxiprolina (OHP) se forma intracelularmente. Es un aminoácido no esencial que proviene de la hidroxilación post-traslacional de prolina y constituye el 10% del contenido de colágeno maduro (Fig. 6).

Figura 6. Molécula de hidroxiprolina.
El 90% de OHP es liberada durante la degradación
del colágeno tipo I, pasa a circulación, se metaboliza
en el hígado y posteriormente es excretada en la orina
donde se encuentra en forma libre sólo en un 10%. El
mayor porcentaje corresponde a OHP unida a péptidos
por lo cual para su determinación colorimétrica es
indispensable una hidrólisis previa. Su excreción es
mayor en niños que en adultos y además puede estar
influida por el contenido de carne o gelatina de la dieta,
por lo que debe realizarse una dieta exenta de productos
que la aporten durante las 48 h previas a la recolección
de orina (31).
Sólo el 10% de la OHP proviene del colágeno tipo
I degradado del hueso ya que otras proteínas la aportan,
entre ellas el componente C1q del complemento
o bien de colágeno recientemente sintetizado. Parte
de este aminoácido se metaboliza y reutiliza para la
síntesis de nuevas proteínas lo que determina que sea
un marcador inespecífico para determinar la degradación
del tejido óseo (4).
La mayoría de los métodos utilizados para su detección
son engorrosos lo que aumenta su variabilidad
con un coeficiente de variación entre 10 a 12%. Puede
determinarse por HPLC (cromatografía de alta presión
líquida) (13), aunque dicha metodología no se
encuentra disponible para cualquier laboratorio de
análisis clínicos.
Como los niveles de OHP urinaria reflejan básicamente
la cantidad de este aminoácido proveniente de
la resorción ósea de colágeno sintetizado recientemente,
esto hizo que su uso primordial haya sido determinar
la actividad y seguimiento de la enfermedad
de Paget. En osteoporosis presenta baja sensibilidad ya
que existe gran sobre-exposición con los valores obtenidos
en muestras de sujetos normales (21) y si bien la
determinación de HOP urinaria fue el marcador de
resorción histórico, con el tiempo ha sido reemplazado
por otros más sensibles y específicos de hueso.
Piridinolinas
Cuando el procolágeno tipo I pierde sus fracciones
propeptídicas y se transforma en colágeno tipo I se deposita en forma de fibrillas longitudinales sobre la matriz ósea. Éstas se contactan con otras fibrillas dando lugar a
una fibra colágena que se estabiliza por medio de puentes
de entrecruzamiento entre ellas denominados cross-links.
Su formación comienza con la desaminación del
grupo ε-amino de la lisina e hidroxilisina presentes en la
región telopeptídica de una molécula de colágeno a su
aldehído correspondiente. Este compuesto desaminado
reacciona con otros residuos de lisina o hidroxilisina localizados
en una molécula de colágeno vecina formando
estructuras cíclicas llamada piridinolinas.
Los residuos de hidroxilisina son mucho menos
abundantes en el tejido óseo respecto de otros tejidos,
lo contrario ocurre con los residuos de lisina. Se conocen
dos formas de piridinolinas: si el residuo que interactúa
dentro de la molécula de colágeno es la hidroxilisina
el producto de entrecruzamiento maduro se
denomina piridinolina (Pir), mientras que si el residuo
es la lisina se denomina deoxipiridinolina (D-Pir)
(Fig. 7) (4). Estos productos de entrecruzamiento son
importantes ya que determinan las propiedades biomecánicas
y estructurales del hueso (32).

Figura 7. Productos de entrecruzamiento del colágeno tipo I (Pir y D-Pir).
La Pir y la D-Pir, también llamadas Hidroxilisilpiridinolina
(HP) y Lisilpiridinolina (LP), estabilizan la
molécula de colágeno maduro y constituyen uniones únicas para las moléculas de colágeno y elastina. Cuando
el colágeno es degradado por osteoclastos, ambas
se vuelcan a la circulación y, a diferencia de la OHP, no
sufren metabolización posterior y son excretadas directamente
en la orina (21).
Estos cross-links no son exclusivos del hueso: la Pir
está presente en el colágeno tipo II del cartílago y
otros tejidos conectivos, mientras que D-Pir se ubica
casi exclusivamente en hueso y dentina. Por ello la D-Pir
urinaria es más específica como marcador de resorción ósea. Como el tejido óseo es el mayor reservorio
de colágeno tipo I del cuerpo y se remodela más rápidamente
que el resto de los tejidos conectivos se considera
que la mayoría de la D-Pir presente en la orina
de un adulto será la que provenga de la resorción ósea. La D-Pir se encuentra en orina tanto en forma libre
(40%) como unida a péptidos (60%). Una ventaja
respecto de la determinación de HOP es que no es necesaria
una dieta previa a la toma de muestra (31).
Inicialmente la determinación de Pir se realizaba
por HPLC, previa hidrólisis de la muestra de orina, utilizando
un detector de fluorescencia; luego se desarrollaron
inmunoensayos que miden Pir libre o unida a
péptidos en orina (13)(21). En la actualidad existen
inmunoensayos que utilizan anticuerpos monoclonales
para la detección de D-pir (26) o métodos de electroquimioluminiscencia
(EQL) automatizados (33).
Telopéptidos amino y carboxilo terminal del colágeno tipo 1
La degradación de la matriz ósea es esencial para
que se produzca el remodelamiento óseo. Dos tipos de
enzimas proteolíticas se encuentran involucradas en
dicho proceso, la catepsina K lisosomal y las MMPs cuya
actividad depende del estado de remodelamiento y
del tipo de hueso a ser remodelado (34).
Actualmente se considera que la catepsina K, cuya
actividad es máxima a pH ácido, es la principal colagenasa
del proceso de resorción ósea. Esta enzima es capaz
de degradar al colágeno en varios sitios dando lugar
a pequeños péptidos N- y C-terminales, dejando así expuesta a la molécula de colágeno para la acción de
otras colagenasas que actúan a pH neutro, entre ellas
las MMPs (16).
Se considera en la actualidad que los telopéptidos
N- y C-terminal, conocidos como NTX y CTX, respectivamente
son los marcadores más sensibles y específicos
de la resorción ósea (Fig. 8). Estos fragmentos se forman por la actividad de la catepsina K y aparecen
en cantidades significativas, tanto en sangre como en
orina, donde pueden medirse por inmunoensayos específicos
(4)(35). La medición sérica proporciona una
ventaja con respecto al ensayo en orina porque evita el
efecto aditivo de la variabilidad biológica de la excreción
de creatinina urinaria (36).

Figura 8. Telopéptidos carboxilo (C-) y amino (N-) terminal del colágeno tipo I.
Existen dos ensayos para el NTX, uno urinario por
ELISA y el otro automatizado tanto en suero como en
orina por EQL; en ambos casos se utiliza un anticuerpo
monoclonal dirigido contra la cadena a2 (I) que
no reacciona con la parte lineal de la secuencia peptídica
ya que necesita de la existencia de un producto de
entrecruzamiento (Pir o D-Pir) entre dos moléculas de
colágeno vecinas N-terminal.
El antígeno utilizado para la evaluación del CTX es
un octapéptido con la secuencia: Glu-Lys-Ala-His-Asp-Gly-Gly-Arg correspondiente a la región de entrecruzamiento
de la fracción a1 (I) de la fracción telopeptídica
C-terminal del colágeno tipo I. En dicho octapéptido
se encuentra la secuencia Asp-Glu que es capaz de sufrir
isomerizaciones espontáneas. En el hueso recién
formado el Asp se encuentra en la estructura espacial a y cuando el hueso envejece se transforma espontáneamente
en la forma b (37)(38). De ello, el a-CTX
corresponde a hueso degradado de menor edad biológica
que el b-CTX. Ambas formas pueden evaluarse independientemente
por ensayos específicos (Fig. 9).
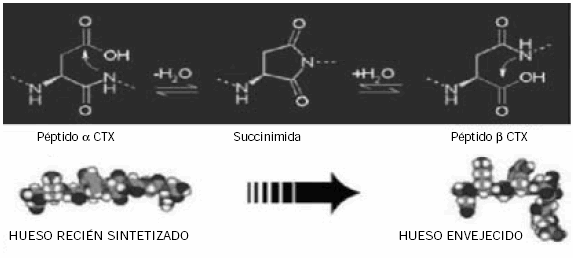
Figura 9. Cambio conformacional espontáneo de a−CTX → b-CTX.
El b-CTX o crosslaps es uno de los marcadores óseos
que presenta mayor sensibilidad y especificidad en este
momento y puede evaluarse en suero u orina en forma
manual o automatizada. Recientemente se ha desarrollado
un método ELISA para evaluar a-CTX en
orina.
Para ejemplificar la diferencia entre la medición de
las formas isoméricas a y b-CTX, se pueden tomar dos
patologías óseas como la enfermedad de Paget y el hiperparatiroidismo
primario (HPT 1º). En el primero
caso, como el hueso degradado es el recientemente
sintetizado, la medición de b-CTX no es útil, mientras
que la a-CTX sería la adecuada. En el HPT1º, en cambio,
el hueso degradado es más viejo, por ello el a-CTX
determina en forma más sensible el aumento en la resorción ósea.
En la región telopeptídica C-terminal se produce
por acción enzimática otro telopéptido denominado
anteriormente ICTP, en la actualidad CTX-MMP. Este
fue el primer marcador de resorción evaluado en suero
pero como proviene de la actividad de MMPs, específicamente
de la MMP-9, es menos sensible y específico
que NTX y CTX para evaluar cambios en el remodelamiento óseo inducido por osteoporosis. Se considera, en cambio, que el CTX-MMP sería útil para medir
cambios agudos de la resorción ósea por neoplasias.
El anticuerpo utilizado para el ensayo de ICTP requiere
de los entrecruzamientos trivalentes, de Pir o
D-pir, y de la fracción telopeptídica rica en fenilalanina
que se encuentran presenten en los dominios C-terminal
de las dos cadenas a1 del colágeno tipo I (26).
Este dominio es destruido por la catepsina K, por ello
se ha propuesto recientemente la denominación de
CTX-MMP (39).
Fosfatasa ácida tartrato resistente
La fosfatasa ácida (FA) consiste en una familia de
isoenzimas que se expresan en diferentes tejidos y células
tales como próstata, hueso, hígado, riñón, bazo,
plaquetas, eritrocitos, macrófagos y osteoclastos.
En sangre la FA circula como dos fracciones diferenciadas
por su sensibilidad al tartrato. Todas las fosfatasas ácidas son inhibidas por L(+)-tartrato, excepto
la banda 5 que se denomina fosfatasa ácida tartrato resistente
(TRAP). Existen dos subtipos conocidos de
TRAP: 5a y 5b que se diferencian en que la 5a contiene ácido siálico y la 5b no. Esta última proviene de los
osteoclastos; el origen de TRAP-5a es desconocido, pero
podría ser expresada por los macrófagos.
Los niveles de TRAP-5b representan el número y actividad
de los osteoclastos más que el nivel de degradación ósea, aún así su actividad en suero aumenta en las
condiciones clínicas en que el remodelamiento óseo
se encuentra aumentado (4) y un cambio en su concentración
sérica se considera un índice específico de
alteración aguda de la resorción ósea (35).
La mayoría de los ensayos para la medición de
TRAP utilizaban métodos colorimétricos donde no era
posible diferenciar ambas isoformas (13). En la actualidad
existen inmunoensayos con anticuerpos monoclonales
específicos para TRAP-5b.
Catepsina K
La Catepsina K es un miembro de la familia de las
cisteínas proteasas que, a diferencia de otras catepsinas,
tiene la capacidad única de cortar las regiones helicoidales
y telopeptídicas del colágeno tipo I. Su relevancia
clínica fue apreciada con el descubrimiento de
Pycnodysostosis, una enfermedad autosómica recesiva
caracterizada por osteopetrosis, debido a mutaciones
en el gen que codifica a la catepsina K. Este fenotipo
clínico ha sido confirmado en ratones knock-out en catepsina
K, mostrando disfunciones en la digestión de
la matriz ósea.
Estudios inmunocitoquímicos demostraron que la
catepsina K se encuentra intracelularmente en vesículas,
gránulos y vacuolas en el citoplasma de los osteoclastos
y es secretada dentro de las lagunas de resorción ósea donde participa de la degradación extracelular
del colágeno. Debido al hecho de que la catepsina K
es expresada y secretada por osteoclastos durante la resorción ósea activa actualmente es considerada un
marcador de la actividad osteoclástica (13).
Utilidad clínica de los marcadores de remodelamiento óseo
La certeza con que un marcador refleje el remodelamiento óseo va a depender, entre otros factores, de
su especificidad. Por ello, un marcador óseo ideal para
determinar cambios en la velocidad de remodelamiento
sería aquel que sólo sea producido por las células óseas.
Se debe recordar que el proceso de resorción es
más rápido que el de formación, por ello todo aumento
en el ciclo de remodelamiento lleva a una pérdida
de masa ósea. El diagnóstico de una baja masa ósea se
realiza mediante la medición de la densidad mineral ósea (DMO) que, de acuerdo con el número de desviaciones
estándares respecto del valor de DMO en columna
y fémur de un sujeto joven normal sano (T-Score),
determinará la presencia de osteopenia y distintos
grados de osteoporosis (11)(40)(41). En la Tabla II se
enumeran las pautas del comité de expertos de la Organización
Mundial de la Salud (OMS) para el diagnóstico
de osteoporosis en un paciente individual.
Tabla II. Clasificación de osteoporosis/osteopenia según la OMS.

En la Figura 10 se grafican los niveles individuales de CTX urinario obtenidos en un grupo de sujetos con diferentes características (42). Este estudio evidencia que alguno de los valores de CTX urinario obtenido en mujeres postmenopáusicas osteoporóticas presenta sobreexposición con aquellos obtenidos en mujeres postmenopáusicas sanas, premenopáusicas y aun en hombres. Esto hace que aun los marcadores más sensibles y específicos no sirvan para diagnosticar.

Figura 10. Falta de utilidad diagnóstica de los marcadores óseos (42).
Si bien los marcadores no sirven para el diagnóstico, son útiles para identificar a los sujetos denominados "perdedores rápidos" que se caracterizan por niveles aumentados del remodelamiento óseo. De aquí que la utilidad clínica más importante de los marcadores óseos consista en diferenciar un alto índice de recambio óseo de uno bajo. En este sentido, niveles elevados de marcadores óseos sensibles y específicos indicarían una pérdida acelerada de masa ósea que si continúa en el tiempo puede conducir a osteoporosis e incremento en el riesgo de fracturas. Por ello, identificar individuos con elevado remodelamiento permitiría aplicar en forma preventiva un tratamiento antirresortivo que disminuya el remodelamiento, evitando así la pérdida de hueso (21). La Figura 11 ejemplifica este concepto mediante los resultados obtenidos en un estudio realizado en un grupo de mujeres sanas postmenopáusicas. En dicho estudio en forma basal las mujeres se dividieron en cuartilos de resorción ósea mediante la medición del NTX urinario. De acuerdo con esta división se determinó el cambio en la DMO de columna entre los tiempos finales del estudio (12 meses) y basal, sin que las mujeres hayan recibido algún tipo de tratamiento. Se evidencia que las mujeres que se encontraban en el mayor cuartilo de resorción ósea, presentaron la mayor pérdida de masa ósea al año del estudio.

Figura 11. Porcentaje de cambio en la DMO al año de acuerdo con el cuartilo inicial de NTX en orina (43).
El uso de marcadores óseos en pacientes individuales
puede ser apropiado en algunas situaciones, sobre
todo en mujeres peri o postmenopáusicas con mediciones de DMO dentro de la normalidad (44). Un aumento
en los niveles de marcadores puede sugerir un
tratamiento preventivo para evitar, en un futuro, la
pérdida de hueso.
La masa ósea, la velocidad de pérdida de hueso y el
riesgo de fracturas osteoporóticas se encuentran relacionadas
y por lo tanto una baja masa ósea así como
un aumento en la pérdida de hueso evaluada por incremento
en el remodelamiento óseo, son predictores
independientes del riesgo relativo de fracturas de cadera
y vertebrales. El valor predictivo es mayor para los
marcadores de resorción que para los de formación, es
también mayor en las mujeres adultas que en las jóvenes
(25)(45) mientras que en hombres los distintos estudios
no mostraron resultados concluyentes.
En principio, si el ciclo de remodelamiento óseo se
encuentra acoplado, tanto el aumento en un marcador
de resorción como en uno de formación podría
predecir la futura pérdida de masa ósea. Sin embargo,
en la actualidad los marcadores más específicos y sensibles
son el NTX y el CTX, ambos de resorción. Asimismo,
sus niveles aumentados, tal como lo demuestra
el estudio de Garnero et al., independientemente de la
DMO son predictores de riesgo de fractura de cadera
y vertebral (40)(46). Sujetos con niveles elevados de
CTX muestran un riesgo relativo similar a aquellos
que presentan una baja DMO. Asimismo, individuos
que sumen la baja masa ósea a una resorción elevada
medida por CTX duplican el riesgo relativo de fracturas
de cadera (Fig. 12) (47).

Figura 12. Riesgo relativo de fracturas evaluado por DMO y por marcadores bioquímicos específicos
de resorción ósea (47).
La ventaja más importante de la medición de los
marcadores es que se trata de métodos poco invasivos
que si son aplicados e interpretados correctamente se
convierten en herramientas útiles que ayudan al diagnóstico
y seguimiento terapéutico de las enfermedades
metabólicas óseas (13)(40). En este sentido determinan,
en un corto periodo de tiempo, la adherencia
y efectividad del tratamiento (48). Una caída en los niveles
de los marcadores de resorción de alrededor del
50% entre el tercero y sexto mes de una terapia antirresortiva
predice una buena respuesta (46).
Los niveles de los marcadores pueden identificar
problemas en la absorción de la medicación o carencia
de respuesta al tratamiento (individuos no respondedores)
pero también pueden indicar, por parte del
paciente, disconformidad y falta de adherencia a la terapia
instituida (Fig. 13).
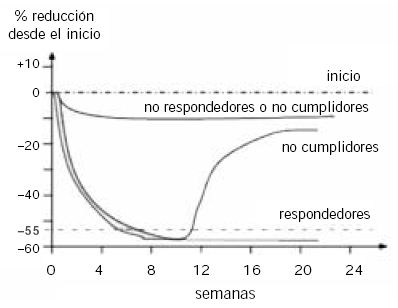
Figura 13. Diferentes respuestas de un marcador de resorción específico
ante un tratamiento instituido.
Si el objetivo es controlar la eficacia terapéutica, lo
más adecuado sería utilizar un marcador de resorción
para aquellos tratamientos con anticatabólicos ya que
en un periodo corto de tiempo (entre 1 a 3 meses) determinan
los cambios que al año podrían recién observarse
en la DMO (21)(31). En caso de tratamientos
anabólicos, como la inyección en forma de pulsos de
PTH, lo más apropiado sería utilizar marcadores de
formación ósea (3).
La respuesta "clínicamente significativa" al tratamiento
puede ser evaluada mediante el denominado "Minino Cambio Significativo" (LSC) el cual, mediante
una fórmula en la que se contempla tanto la variabilidad
biológica como la variabilidad analítica, determinará si los cambios son específicos del tratamiento o no
(ruido)(42). Para evaluar el LSC se debe realizar la medición
basal del marcador en dos muestras tomadas en
forma consecutiva a la primera y la 12a. semana. Con dichos
valores se obtendrá un valor promedio del marcador
bioquímico utilizado que disminuirá la variabilidad
individual. Asimismo, se deberá contar con una muestra
postratamiento cuya extracción dependerá del marcador
usado y del tipo de tratamiento (rápidamente
efectivos o de efectividad más lenta). En este sentido se
considera tres meses como un período adecuado para
el tratamiento con bisfosfonatos y de seis meses para un
tratamiento con terapia hormonal de reemplazo (21).
El LSC dependerá de la sensibilidad y especificidad
del marcador utilizado, es decir cuanto más específico y sensible sea el marcador, los porcentajes de cambio
para determinar una respuesta positiva al tratamiento
son menores. Por supuesto, los valores de LSC menores
se presentan en los marcadores óseos evaluados en
sangre.
Otra de las formas de evaluar la efectividad del tratamiento
es comparar el nivel actual del marcador óseo con un rango predefinido como de "referencia" o de "normalidad". En general se toma como rango
normal al obtenido en mujeres premenopáusicas sanas:
promedio ± 2DE. Para ello, cada laboratorio debería
contar con un valor de referencia independientemente
del suministrado por el fabricante del
equipo. Respecto de las mujeres postmenopáusicas
con remodelamiento normal se considera que el nivel
del marcador óseo evaluado no debe sobrepasar los
2DE del correspondiente a mujeres premenopáusicas
sanas. Todo valor por encima del mismo se tomará como
remodelamiento aumentado.
Interpretación clínica de un marcador bioquímico óseo
En un sujeto individual, la interpretación del valor
de un marcador bioquímico de remodelamiento óseo es complicada debido a los distintos factores
que podrían influir en sus resultados y que, por lo
tanto, deben tenerse en cuenta. Entre ellos se encuentran
la influencia de las condiciones preanalíticas,
sus características analíticas de sensibilidad y especificidad
y su variabilidad biológica. Asimismo, la
falta de estandarización hace aún más engorrosa la
comparación entre los resultados obtenidos por los
distintos laboratorios.
La variación preanalítica incluye la preparación del
paciente antes de la obtención de la muestra (horas de
ayuno, necesidad de dieta diaria) y tipo de muestra
(suero-orina), anticoagulantes utilizados, temperatura
de manipulación y almacenamiento, ciclos de congelamiento
y descongelamiento, entre otros. Todas estas
fuentes de variabilidad técnicas son importantes y pueden
ser controladas (49).
La variación analítica es función de la reproducibilidad
y exactitud de las técnicas empleadas (50). Las
muestras sanguíneas presentan menos variación analítica
que las urinarias ya que a estas últimas se le debe
sumar el error de la determinación de creatinina. Aunque
el error de precisión analítica de los marcadores
es alto (10 a 20%), el porcentaje de descenso por efecto
del tratamiento utilizando un marcador sensible y
específico es mayor (40 a 60% luego de 3 a 6 meses),
esto hace que los marcadores sean útiles para determinar
la eficacia de la terapia instituída (21).
La variabilidad biológica depende de la regulación
del remodelado óseo relacionado con factores mecánicos
(actividad física y fuerza muscular) y humorales
(concentración de Ca++ y fosfatos, hormonas, vitamina
D, citoquinas) que actúan sobre la células óseas para el
reclutamiento, proliferación y función celular (50).
Ciertos factores biológicos como la edad, género, etnicidad,
etc., no pueden modificarse; en cambio, otros
factores pueden ser modificables y, por lo tanto, deben
tenerse en cuenta para tratar de disminuir su influencia
al máximo posible.
Distintos estudios han investigado diversas condiciones
que influirían en los resultados de los marcadores óseos tales como la dieta, tipo de muestra, cambio
diario (ritmo circadiano), ciclo menstrual, menopausia,
estación anual, edad, sexo, crecimiento (44). A
continuación se enumeran los más importantes.
- Variación diaria (circadiana): salvo las determinaciones
enzimáticas, los marcadores bioquímicos
presentan variación diaria con valores más elevados
en las primeras horas de la mañana y más bajos
en horas de la tarde. En general, la amplitud
de la variación se encuentra entre el 20-30%,
aunque el mayor o menor valor dependerá del
marcador utilizado. La etiología de esta variación
es desconocida aunque varias hormonas
que presentan ritmo diario (PTH, hormona de
crecimiento, cortisol, etc) podrían estar involucradas
parcialmente en dicho cambio.
- Edad: las concentraciones de marcadores óseos,
tanto en suero como en orina, no son estables a
través de la vida. Son altas al nacimiento y descienden
en la niñez siguiendo la curva de velocidad
de crecimiento; se incrementan nuevamente
en la pubertad debido a la 2° etapa de
velocidad de crecimiento. Es más temprano y de
menor intensidad en las niñas. A partir de ahí,
decrecen y se mantienen estables hasta la menopausia,
en que se incrementan, en la mujer, nuevamente
en relación directa a la deficiencia de
estrógenos. En los hombres, en cambio, permanecen
sin grandes variaciones. A partir de los 70
años se observa un incremento que es independiente
del género (48).
- Variación en días consecutivos: En general, la variación
para un mismo individuo observada al evaluar
un marcador en sangre es menor a la observada en
la medición de los marcadores bioquímicos evaluados
en orina.
- Variación estacional (circoanuales): En climas templados,
en general, se observan valores más altos
en otoño-invierno (20-30%) debido, en parte, a
la influencia que presenta sobre el metabolismo óseo el estado fisiológico de la vitamina D.
- Ciclo menstrual: La mayoría de los marcadores óseos presentan variación durante el ciclo menstrual.
La resorción es de mayor amplitud (10-
20%) durante el período medio y tardío de la fase
folicular y temprano de la fase luteal. Por tal
motivo se recomienda la extracción de la muestra
entre el 3er. y 7mo. día del ciclo menstrual.
- Dieta: La ingestión de alimentos reduce la resorción ósea en forma postprandial posiblemente
mediada por la liberación de péptidos intestinales
y/o pancreáticos. La composición de la dieta
por largos período de tiempo (ingestión de Ca,
vitamina D, proteínas y fosfatos) pueden modificar
el remodelamiento óseo. Por ello, la medición
de marcadores en sangre debería ser evaluada
en ayunas y, si es posible, permanecer con
una dieta estable durante una o dos semanas
previas a la recolección.
- Estilo de vida: El ejercicio moderado reduce el recambio óseo. Asimismo el alcoholismo y tabaco
alteran los valores.
- Funcionamiento hepático y renal: Un mal funcionamiento
hepático puede alterar marcadores que
se metabolizan en hígado mientras que la insuficiencia
renal crónica produce acumulación de
los marcadores óseos que por su estructura química
no pueden filtrar en dichas condiciones
por el glomérulo.
- Actividad física: la ingravidez o la inmovilización
prolongada da lugar a un aumento acelerado
de la resorción ósea, con aumento de los marcadores.
- Otras causas: raza, embarazo y lactancia.
Conclusiones
Desde el punto de vista fisiopatológico, la osteoporosis
se define como "pérdida cuantitativa de la DMO
que causa una disminución de la resistencia biomecánica
del hueso, por consiguiente, facilita la aparición
de fracturas ante traumatismos que no serian suficientes
para causarla, si el esqueleto hubiera conservado
sus características iniciales". En esta patología no se
observan anormalidades en la estructura de la matriz
orgánica del hueso, sino que se presenta una reducción
de la masa ósea, indicativa de una mayor tasa de
resorción del hueso, menor formación o ambas. Para
prevenirla es de suma utilidad determinar el nivel de
remodelamiento óseo, ya que todo aumento lleva a la
pérdida de masa ósea. Los marcadores bioquímicos de
resorción y formación son una herramienta atractiva
no sólo para identificar aumentos exagerados del remodelamiento
sino para controlar la eficacia de una
terapia en un corto período de tiempo. Sin embargo,
la interpretación de los resultados exige contar con niveles
de referencia adecuados.
Los marcadores no sirven para diagnosticar osteoporosis
porque aun los marcadores más sensibles y específicos
presentan valores que se superponen en
condiciones de normalidad o de osteoporosis. Sin embargo,
la medición de los marcadores óseos en conjunto
con las de DMO provee información adicional
que ayuda a optimizar el control de la osteoporosis.
CORRESPONDENCIA
PROF. DRA. SUSANA N. ZENI
Sección Osteopatías Médicas. Hospital de Clínicas
Córdoba 2351- 8vo. Piso
1120 CIUDAD AUTÓNOMA DE BUENOS AIRES
Argentina
1. Canalis E. Effect of insuline like growth factor I on DNA and protein synthesis in cultures rat calvariae. J Clin Invest 1980; 66: 709-19.
2. Manolagas SC. Birth and death of bone cells: basic regulatory mechanisms and implications for the pathogenesis and treatment of osteoporosis. Endocr Rev 2000; 21: 115-37.
3. Camozzi V, Tossi A, Simoni E, Pagani F, Francucci CM, Moro L. Role of biochemical markers of bone remodelling in clinical practices. J Endocrinol Invest 2007; 30: 13-7.
4. Ross PF, Christiano AM. Nothing but skin and bone. J Clin Invest 2006; 116: 1140-9.
5. Allison´s Restrospection. Bone remodelling. Physiology by Alliraph 2007. Disponible en: http://alliraph.wordpress.com/2007/11/03/bone-remodelling/. Fecha de acceso 2 de noviembre de 2008.
6. Mundy GR. Bone-Resorbing Cells. In: Favus MJ editor. Primer on the metabolic bone diseases and disorders of mineral metabolism. 3st. ed. New York: Lippincott- Raven publishers; 1996.
7. Davies J, Warwick J, Tatty N, Philip R, Helfrich M, Horton M. The osteoclast functional antigen, implicated in the regulation of bone resorption, is biochemically related to vitronectin receptor. J Cell Biol 1989; 109: 1817-26.
8. Baron R. Anatomy and ultrastructure of bone. In: Favus MJ, Ed. Primer on Metabolic Bone diseases and disorders of mineral metabolism. New York: Raven Press; 1993.
9. Cordova A. Compendio de Fisiología para Ciencias de la Salud Interamericana de España - Madrid: Mc- GRAW - HILL; 1996.
10. Dempster D. Bone remodeling and its regulation. En: ECTX training course in bone markers. 35 th European Symposium on Calcified Tissues (ECTS) 24 de mayo de 2008. Barcelona - España; 2008. p.9.
11. McCormick RK. Osteoporosis: intergrating biomarkers and other diagnostic correlates into the management of bone fragility. Altern Med Rev 2007; 12: 113-45.
12. Oliveri B, Wittich A, Nadal M, Zeni SN. Telopéptido carboxilo terminal del colágeno tipo I (=-CTX) sérico y compromiso óseo en la insuficiencia renal crónica. Medicina (Buenos Aires) 2005; 65: 321-8.
13. Seibel MJ. Biochemical markers of bone turnover. Part II: Clinical applications in the management of osteoporosis. Clin Biochem Rev 2006; 27: 123-38.
14. Noble BS. The osteocyte lineage. Arch Biochem Biophys 2008; 473: 106-11.
15. Behnke B, Kemper M, Kruse HP, Muller-Weifel D. Bone alkaline phosphatase in children with chronic renal failure. Nephrol Dial Transplant 1998; 13: 662-7.
16. van Bezooijen RL, Roelen BA, Visser A, van der Wee- Pals L, de Wilt E, Karperien M, et al. Sclerostin is an osteocyte-expressed negative regulator of bone formation, but not a classical BMP antagonist. J Exp Med 2004; 199: 805-14.
17. Boyce BF, Xing L. Biology of RANK, RANKL, and osteoprotegerin. Arthritis Res Ther 2007; 9:S1 (doi: 10.1186 - 2165).
18. Tanaka Y, Maruo A, Fujii K, Nomi M, Nakamura T, Eto S, et al. Intercellular adhesion molecule 1 discriminates functionally different populations of human osteoblasts: characteristic involvement of cell cycle regulators. J Bone Miner Res 2000; 15: 1912-23.
19. Yasuda H, Shima N, Nakagawa N, Yamaguchi K, Kinosaki M, Mochizuki S, et al. Osteoclast differentiation factor is a ligand for osteoprotegerin/osteoclastogenesis- inhibitory factor and is identical to TRANCE/RANKL. Proc Natl Acad Sci U S A 1998; 95: 3597-602.
20. Watts WS. Clinical utility of biochemical markers of bone remodelling. Clin Chem 1999; 45: 1359-68.
21. Jamal SA, Leiter RE, Bayoumi AM, Bauer DC, Cummings SR. Clinical utility of laboratory testing in women with osteoporosis. Osteoporos Int 2005; 16: 534-40.
22. Vasikaran SD. Utility of biochemical markers of bone turnover and bone mineral density in management of osteoporosis. Crit Rev Clin Lab Sci 2008; 45: 221-58.
23. Lee NK, Sowa H, Hinoi E, Ferron M, Ahn JD, Confavreux C, et al. Endocrine regulation of energy metabolism by the skeleton. Cell 2007; 130: 456-69.
24. Khosla S, Kleerekoper M. In: Favus MJ editor. Primer on the metabolic bone diseases and disorders of mineral metabolism. 5th. ed. Whashington DC: American Society for Bone and Mineral Research publishers; 2003.
25. Kessler E, Takahara K, Biniaminov L, Brusel M, Greenspan DS. Bone morphogenetic protein-1: The type I procollagen C-proteinase. Science 1996; 271: 360-2.
26. Robins SP, Woitge H, Hesley R, Ju J, Seyedin S, Seibel MJ. A direct, enzyme-linked immunoassay for urinary deoxypyridinoline as a specific marker for measuring bone resorption. J Bone Miner Res 1994; 9: 1643-9.
27. Orum O, Hansen M, Jensen CH, Sorensen HA, Jensen LB, Horslev-Petersen K, et al. Procollagen type I N-terminal propeptide (PINP) as an indicator of type I collagen metabolism: ELISA development, reference interval, and hypovitaminosis D induced hyperparathyroidism. Bone 1996; 19: 157-63.
28. Melkko J, Kauppila S, Risteli L, Niemi S, Haukipuro K, Jukkola A, et al. Immunoassay for intact aminoterminal propeptide of human type I procollagen. Clin Chem 1996; 42: 947-54.
29. Melkko J, Niemi S, Risteli L, Risteli J. Radioimmunoassay of the carboxyterminal propeptide of human type I procollagen. Clin Chem 1990; 36: 1328-32.
30. Kanis JA, Delmas PD. European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int 2008; 19: 99-428.
31. Manjón Llorente G, Fernández Espuelas C. Normal values of bone turnover markers in childhood. An Pediatr (Barc) 2004; 60: 330-6.
32. Wassen MHM, Lammens J, Tekoppele JM, Sakkers RJB, Liu Z, Verbout Aj, et al. Collagen structure regulates fibril mineralization in osteogenesis as revealed by crosslink patterns in calcifying callus. J Bone Miner Res 2000; 15: 1776-85.
33. Rosano TG, Peaston RT, Bone HG, Woitge HW, Francis RM, Seibel MJ. Urinary free deoxypyridinoline by chemiluminescence immunoassay: analytical and clinical evaluation. Clin Chem 1998; 44: 2126-32.
34. Everts V, Delaisse JM, Korper W, Beertsen W. Cysteine proteinases and matrix metalloproteinases play distinct roles in the subosteoclastic resorption zone. J Bone Miner Res 1998; 13: 1420-30.
35. Bjoerm H, Christian E, Feld M, Zichner L, Kurth A. Tartrate-resistant acid phosphatase 5b (TRAP 5b) as a marker of osteoclast activity in the early phase after cement less total hip replacement. Acta Orthopaedic 2007; 78: 221-5.
36. Scariano JK, Garry PJ, Montoya GD, Wilson JM, Baumgartner RN. Critical differences in the serial measurement of three biochemical markers of bone turnover in the sera of pre - and postmenopausal women. Clin Biochem 2001; 34: 639-44.
37. Fledelius C, Johnsen AH, Cloos PAC, Bonde M, Qvist P. Characterization of urinary degradation products derived from type I collagen. Identification of a b-isomerized Asp-Gly sequence within the C-terminal telopeptide (a1) region. J Biol Chem 1997; 272: 9755-63.
38. Pedersen BJ, Ravn P, Bonde M. Type I collagen Ctelopeptide degradation products as bone resorption markers. J Clin Ligand Assay 1998; 21: 118-27.
39. Delmas PD, Committee of Scientific Advisors of the International Osteoporosis Foundation. Bone marker nomenclature. Bone 2001; 28: 575-6.
40. Garnero P, Delmas PD. Contribution of bone mineral density and bone turnover markers to the estimation of risk of osteoporotic fracture in postmenopausal women. J Musculoskelet Neuronal Interact 2004; 4: 50-63.
41. Kanis A. Diagnosis of osteoporosis and assessment of fracture risk. The Lancet 2002; 359: 9321.
42. Zeni S, Wittich A, Di Gregorio S, Casco C, Oviedo A, Somoza J, et al. Utilidad clínica de los marcadores de formación y resorción ósea. Acta Bioquím Clín Latinoam 2001; 35: 3-36.
43. Srivastava AK, Vliet EL, Lewiecki EM, Maricic M, Abdelmalek A, et al. Clinical use of serum and urine bone markers in the management of osteoporosis. Curr Med Res Opin 2005; 21: 1015-26.
44. Abe Y, Ishikawa H, Fukao A. Higher efficacy of urinary bone resorption marker measurements in assessing response to treatment for osteoporosis in postmenopausal women. Tohoku J Exp Med 2008; 214: 51-9.
45. Ross PD, Knowlton W. Rapid bone loss is associated with increased levels of biochemical markers. J Bone Miner Res 1998; 13: 297-302.
46. Allende Vigo MZ. The use of biochemical markers of bone turnover in osteoporosis. P R Health Sci J 2007; 26: 91-5.
47. Garnero P, Hausherr E, Chapuy MC, Marcelli C, Grandjean H, et al. Markers of bone resorption predict hip fracture in elderly women: the EPIDOS Prospective Study. J Bone Miner Res 1996; 11: 1531-8.
48. Souberbielle JC, Cormier C, Kindermans C. Bone markers in clinical practice. Curr Opin Rheumatol 1999; 11: 312-9.
49. Seibel MJ, Lang M, Geilenkeuser WJ. Interlaboratory variation of biochemical markers of bone turnover. Clin Chem 2001; 47: 1443-50.
50. Alvarez H, Santana M, Casas E. Variabilidad Analítica y Biológica de los Marcadores de Osteoporosis. Rev Cub Reumatol 2006; 8 (9,10): 86-7.
Aceptado para su publicación el 17 de marzo de 2009