

TEMAS DE INTERÉS
Guías de prácticas de laboratorio clínico
Biomarcadores de síndromes coronarios agudos y falla cardíaca
EDITADO POR
Robert Christenson
Copyright©2007 The American Association for Clinical Chemistry
Este documento ha sido traducido con permiso de la National Academy of Clinical Biochemistry (NACB), Washington, DC. La NACB no se hace responsable de la exactitud de la traducción. Los puntos de vista presentados son los de los autores y no necesariamente los de la NACB.
Preámbulo
Capítulo I
Características clínicas y utilización de marcadores bioquímicos en
síndromes coronarios agudos
Capítulo II
Aspectos analíticos de los marcadores bioquímicos de síndromes
coronarios agudos
Capítulo III
Características clínicas y utilización de marcadores cardíacos en la
falla cardíaca
Capítulo IV
Aspectos analíticos de los biomarcadores de falla cardíaca
Capítulo V
Pruebas en el sitio de atención, vigilancia y administración de
marcadores cardíacos en síndromes coronarios agudos
Capítulo VI
Uso de troponina cardíaca y péptido natriurético tipo B o NT proBNP
en otras etiologías que no son síndromes coronarios agudos o falla
cardíaca
Aspectos analíticos de los marcadores bioquímicos de los síndromes coronarios agudos
II. ASPECTOS ANALÍTICOS DE LOS BIOMARCADORES
A. Especificaciones de la troponina cardíaca
B. Tiempo de respuesta del biomarcador cardíaco
C. Biomarcadores ya no recomendados para el uso en el contexto de SCA
D. Determinación de las características del valor de corte para la decisión médica de los biomarcadores para SCA
E. Recomendaciones de la European Society of Cardiology (ESC) y del American College of Cardiology (ACC)
I. Generalidades de los aspectos analíticos relacionados con los biomarcadores del Síndrome Coronario Agudo (SCA)
En 1999, la National Academy of Clinical Biochemistry (NACB)1 publicó los primeros estándares de prácticas del laboratorio abordando recomendaciones analíticas y clínicas para el uso de los marcadores cardíacos en enfermedades de las arterias coronarias (1). Los objetivos eran recomendar la implementación y utilización adecuadas de los biomarcadores cardíacos, específicamente la troponina cardíaca (cTn), que había sido autorizada recientemente por la Food and Drug Administration (FDA) de los Estados Unidos como marcador cardíaco para ayudar en el diagnóstico del infarto agudo del miocardio (IAM). En 2001, el Comité de Estandarización de Marcadores de Daño Cardíaco de la IFCC (C-SMCD) recomendó especificaciones de calidad para los factores analíticos y pre-analíticos de los ensayos de cTn (2). Los objetivos fueron pensados para uso de los fabricantes de ensayos comerciales y de los laboratorios clínicos que utilizan ensayos de cTn. El objetivo general fue establecer criterios uniformes para que todos los ensayos de cTn pudieran ser evaluados objetivamente por sus calidades analíticas y rendimiento clínico. Estos principios generales también se pueden aplicar a los ensayos de creatinquinasa MB (CK-MB) masa y mioglobina mediante el uso de las recomendaciones analíticas de este documento. En este informe se incluyen los antecedentes para establecer guías de prácticas actualizadas con recomendaciones que abordan los aspectos analíticos relacionados con los biomarcadores cardíacos en base a 8 años de observaciones médicas y científicas, basadas en la evidencia, transcurridos desde la publicación de las recomendaciones iniciales (1).
1 Abreviaturas no estándares: NACB, National Academy of Clinical Biochemistry; SCA, síndrome coronario agudo; cTn, troponina cardíaca; FDA, Food and Drug Administration de los Estados Unidos; IAM, infarto agudo del miocardio; C-SMCD, Comité de Estandarización de Marcadores de Daño Cardíaco; CK-MB, creatina quinasa MB; cTnI, troponina cardíaca I; cTnT, troponina cardíaca T; CLSI, Clinical Laboratory Standards Institute; POC point-of-care; TAT, tiempo de respuesta; IM, infarto de miocardio; AHA, American Heart Association; ESC, European Society of Cardiology; ACC, American College of Cardiology y WHF, World Heart Federation.
II. Aspectos analíticos de los biomarcadores


A. Especificaciones sobre la troponina cardíaca (cTn)
En primer lugar, en el contexto de la cTn, se deben delinear los epitopes reconocidos por los anticuerpos. Los epitopes ubicados en la parte estable de la molécula de la cTnI deben ser prioritarios. Deben describirse las respuestas relativas específicas para las siguientes formas de la cTnI: cTnI libre, el complejo binario I-C, el complejo ternario T-I-C y las isoformas oxidadas, reducidas y fosforiladas de las 3 formas de la cTnI. También deben abordarse los efectos de los distintos anticoagulantes en la unión de la cTnI. En segundo lugar, debe informarse el origen del material utilizado para calibrar los ensayos de cTn, específicamente para la cTnI. Un subcomité de estandarización de cTnI de la AACC, en colaboración con el NIST, ha desarrollado un material de referencia primario (SRM#2921) (3). A pesar de que este material demostró conmutabilidad con sólo el 50% de los ensayos actuales de cTn, será útil para armonizar las concentraciones de cTnI entre los distintos ensayos (4) (5). En la actualidad, parece que la única forma de lograr una estandarización completa de la cTnI sería que todos los fabricantes acordaran utilizar los mismos pares de anticuerpos para todos los ensayos comerciales así como un material de referencia común para la calibración (6) (7). El C-SMCD de la IFCC actualmente está investigando el desarrollo de un material de referencia secundario en base a suero. Para la cTnT, como hay solamente un fabricante de ensayos, la armonización entre las generaciones de ensayos ha sido consistente. En tercer lugar, los fabricantes deben usar métodos aconsejados por el CLSI para caracterizar el límite de detección, la sensibilidad funcional y la imprecisión total (8) (9). Las características clave para los ensayos de cTn incluyen la determinación de la distribución de valores en una población de referencia sana, la determinación estadística del punto de corte del percentil 99 para la población de referencia y la determinación de la concentración correspondiente al CV 10% (imprecisión total). Los factores pre-analíticos que deberían describirse incluyen el efecto del tiempo de almacenamiento y de la temperatura, el efecto de los tubos de vidrio versus los de plástico y los tubos separadores de gel, así como la influencia de los anticoagulantes en las mediciones de plasma y sangre. A medida que se conciban más sistemas de ensayo para las pruebas point-of-care (POC), se deben aplicar criterios analíticos idénticos en las metodologías de los laboratorios de referencia y en sistemas de pruebas POC. Al medir la cTn mediante diferentes metodologías dentro de la misma institución, se deben armonizar los resultados de los ensayos o se debe implementar una estrategia para evitar la confusión interpretativa por parte de los médicos.
B. Tiempo de respuesta del biomarcador cardíaco
Los médicos y los técnicos de laboratorio continúan tras el objetivo de tiempos de respuesta (TAT) <60 minutos para los biomarcadores cardíacos, pero el estudio más importante que se ha publicado a la fecha ha demostrado que las expectativas del TAT no se están cumpliendo en un gran número de hospitales (10). Un estudio del College of American Pathologists de 7020 determinaciones de cTn y 4368 determinaciones de CK-MB en 159 hospitales predominantemente de América del Norte demostró que el TAT medio y el percentil 90 para la troponina fue 74,5 y 129 min, y para la CK-MB, 82 y 131 min. De hecho, menos del 25% de los hospitales pudieron cumplir con el TAT <60 minutos, definido como el período de tiempo indicado para realizar el informe. No se informó ningún análisis de los sistemas de prueba POC. Los datos recientemente publicados han demostrado que la implementación de las pruebas de cTn POC puede disminuir el TAT <30 min en unidades de cardiología de cuidados intensivos y de internaciones cortas (11). Estos datos subrayan la necesidad de que los servicios de laboratorio y los proveedores del cuidado de la salud trabajen en conjunto en el desarrollo de mejores procesos para cumplir con el TAT <60 min requerido por los médicos.
C. Biomarcadores que ya no se recomiendan para el uso en la evaluación del SCA
No se recomienda el uso de la aspartato aminotransferasa, la lactato deshidrogenasa total y las isoenzimas de la lactato deshidrogenasa para la evaluación del daño cardíaco y la detección del infarto del miocardio (IM). El uso de la actividad de la CK total o de la CK-MB es una alternativa aceptable para evaluar el daño cardíaco en instituciones donde los ensayos de cTn o CK-MB masa no están disponibles o no son posibles. La CK total también puede ayudar a mejorar la especificidad del tejido del miocardio cuando la proporción de la CK-MB a CK total es mayor que los intervalos de referencia previamente establecidos. Este concepto está reforzado por una declaración del Consejo de Epidemiología y Prevención de la American Heart Association (AHA) con respecto a definiciones de casos de enfermedad coronaria aguda en estudios de investigación epidemiológicos y clínicos (12). Se realizaron las siguientes recomendaciones para permitir una interpretación más precisa de las tendencias recientes del SCA durante la implementación de ensayos de cTn y el uso de la definición de IM consensuada por la European Society of Cardiology (ESC) y el American College of Cardiology (ACC) (13) (14) atribuido a la cTn: (a) el uso simultáneo de biomarcadores tradicionales con cTn para determinar el rendimiento de los biomarcadores nuevos; y (b) el uso de los factores de ajuste en bases de datos y estudios retrospectivos buscando determinar la incidencia y las tendencias del IM antes y después de los estudios derivados de la cTn.
D. Determinación de las características del punto de corte para la decisión clínica en los biomarcadores de SCA
Cada laboratorio debe determinar el percentil 99 de
un límite de decisión de referencia (punto de corte de
decisión médica) para los ensayos de cTn, mediante estudios
internos que utilicen el ensayo específico usado
en la práctica clínica o la validación de un intervalo de
referencia basado en los hallazgos de la literatura (13) (16). Se definió la imprecisión deseable (expresada como
%CV) de cada ensayo de cTn (y ensayo de CK-MB
masa) como CV <10% en el percentil 99 del límite de
referencia (13) (16). Desafortunadamente, la mayoría
de los laboratorios no tiene los recursos necesarios para
realizar estudios importantes del percentil 99 ni la capacidad
de realizar los protocolos del CLSI para establecer
los criterios de imprecisión total para el ensayo de cTn
que planean usar en la práctica (17). Por lo tanto, los laboratorios
clínicos deben confiar en la literatura publicada
revisada por pares para el establecimiento de límites
de referencia locales y características de imprecisión.
Se debe tener cuidado al comparar los hallazgos registrados
en los insertos de los equipos diagnósticos, autorizados
por la FDA, con los hallazgos informados en las
publicaciones científicas, debido a la diferencia en el tamaño
total de la muestra, las distribuciones por sexo y
etnicidad, los rangos etarios y los métodos estadísticos
utilizados para calcular el percentil 99 en cuestión.
A la fecha, muy pocas compañías de diagnóstico in
vitro han publicado el percentil 99 de los límites en los
insertos de los equipos. No hay una guía establecida por
la FDA u otro organismo de regulación que exija una
evaluación consistente del percentil 99 del límite de referencia
para las cTn. El estudio de valores de referencia
más grande y más diverso registrado a la fecha muestra
el percentil 99 de los límites de referencia en plasma
(heparina) en ensayos de 8 cTn (7 cTnI y 1 cTnT) y 7
ensayos de CK-MB masa (18). Este estudio se realizó en
696 adultos sanos (edades 18-84) estratificados por sexo
y raza. Hubo una diferencia de 13 veces entre el límite
medido del percentil 99 de cTnI más bajo y el más alto.
La falta de estandarización de ensayos de cTn (no hay
material de referencia primario que sea conmutable
con todos los métodos comerciales, como se observó anteriormente)
y las diferencias en el reconocimiento de
epitopes-anticuerpos entre ensayos (diferentes ensayos
utilizan distintos anticuerpos, como se observó anteriormente)
dan como resultado concentraciones substancialmente
discrepantes. Lo que suele reconocerse, sin
embargo, es que mientras se comprendan las características
de un ensayo individual y no se intente comparar
las concentraciones absolutas entre los diferentes ensayos,
la interpretación clínica debería ser aceptable en todos
los ensayos.
Para la CK-MB (como se reconoció durante años
para la CK total), todos los ensayos demuestran un límite
de percentil 99, 2 a 3 veces más alto en hombres
que en mujeres (18). Además, la CK-MB puede demostrar
concentraciones hasta 2 ó 3 veces más altas
para los afroamericanos que para los caucásicos, atribuidas
a las diferencias fisiológicas de masa muscular
entre las razas. Estos datos condujeron a la recomendación
clase I de que los laboratorios clínicos deben
establecer diferentes límites de referencia para CKMB
en base al sexo. Los laboratorios deberían considerar
hacerlo por grupos étnicos.
Para la cTn, el consenso de los expertos surgió en
apoyo de que el punto de corte de referencia sea el
percentil 99, independientemente de si la imprecisión
total del ensayo <10%. Esto ha sido apoyado por
un estudio reciente que demostró que la clasificación
errónea de pacientes que son excluidos utilizando ensayos
de cTn con imprecisión variable (10%-25%) en
el percentil 99 no conduce a una clasificación errónea
significativa de los pacientes sobre órdenes de cTn seriales
(19). Además, mientras que la literatura ha sido
enriquecida con estudios que abordan de manera
adecuada la imprecisión total de ensayos de cTn, con
respecto a cuál será la menor concentración para alcanzar
un CV 10%, los insertos de los fabricantes generalmente
publican datos de imprecisión principalmente
basados en la precisión intra-ensayo o entre
días. Una vez más, no hay especificaciones consistentes
que regulen los datos de precisión que deban ser informados en los insertos de los fabricantes. Para
abordar mejor la práctica diaria del laboratorio clínico,
los hallazgos tempranos de un estudio del CSMCD
de la IFCC demostraron que la imprecisión total
de 13 ensayos comerciales [en base a un protocolo
CLSI de 20 días (20)] no pudo alcanzar experimentalmente
un CV 10% en el percentil 99 de su límite. Sin
embargo, los ensayos mejorados de segunda generación
han demostrado recientemente un CV de 10%
en el percentil 99 (21). El objetivo final será que los
ensayos de cTn alcancen un CV de 10% en el percentil
99 del límite de referencia para reducir los resultados
analíticos, potenciales falsos-positivos, atribuidos
a la imprecisión en el rango de concentración bajo.
En los ensayos clínicos, para evitar la confusión de
que varios centros utilicen ensayos múltiples, se recomiendan
varios abordajes para las pruebas de cTn
(15) (16). Primero, analizar todas las muestras de los
centros de estudios clínicos en un laboratorio de referencia
con un ensayo preciso y bien definido. Segundo,
proveer a todos estos centros con los mismos ensayos
bien definidos y autorizados por la FDA. Tercero,
definir uniformemente los ensayos de cada centro utilizando
la concentración del percentil 99 (dependiente
del ensayo), reduciendo así la confiabilidad de los
criterios de laboratorios locales para los puntos de cortes
de decisión de cTn. Cuarto, utilizar un múltiplo del
percentil 99 (multiplicado por 2 a 3 veces). Quinto, si
las pruebas deciden utilizar valores de corte definidos
en estudios anteriores, debe ser informado el grado de
imprecisión en estas concentraciones.
E. Recomendaciones de la European Society of Cardiology (ESC) y del American College of Cardiology (ACC)
Un documento consensuado por la ESC y el ACC
junto con las guías de la AHA y el ACC para diferenciar
el IAM y la angina inestable codificó el papel de la
cTn recomendando que el diagnóstico del IAM debe
basarse en aumentos de la cTnI o T (preferentemente)
o de la CK-MB masa por encima del percentil 99
del punto de corte en la situación clínica adecuada
(14) (22). Las guías reconocieron la realidad de que ni
la presentación clínica ni el electrocardiograma presentaban
una sensibilidad y especificidad clínica adecuadas.
Las guías no sugieren que todos los aumentos
de estos biomarcadores deban conducir a un diagnóstico
de IM o a un perfil de alto riesgo, solamente aquellos
asociados con los hallazgos clínicos, patológicos,
del electrocardiograma o del diagnóstico por imágenes.
Cuando los aumentos de cTn no se deben a una
isquemia aguda, el médico se ve obligado a buscar otra
etiología para la elevación (6) (23). Pronto se publicarán
las guías actualizadas que abordan la definición
universal revisada de IM co-auspiciadas por la Joint
ESC-ACC-AHA-World Heart Federation (WHF) Task Force
for the Redefinition of MI [Comisión Conjunta para la
Redefinición del IM de la SEC-ACC-AHA-Federación
Mundial del Corazón (WHF)]. Este documento avalará y coincidirá con las recomendaciones propuestas en
el documento conjunto actual de la NACB y la IFCC.
Los autores y los miembros del comité de la
NACB y el C-SMCD de la IFCC declaran que han recibido
financiamiento para proyectos de investigación,
honorarios, gastos en reuniones auspiciadas o
tarifas de consultoría de al menos un fabricante de
ensayos de cTn.
Presentación de información financiera: El Comité de Guías para la Práctica en el Laboratorio Clínico
de la National Academy of Clinical Biochemistry para
la Utilización de Biomarcadores en Síndromes Coronarios
Agudos e Insuficiencia Cardíaca informa todas
las relaciones publicadas dentro de los 2 años
anteriores a esta publicación que puedan ser relevantes
para este documento de guías. Se puede consultar
el documento de aquellas relaciones en el Suplemento
de Datos online en http://www.clinchem.org/content/vol53/issue4.
Utilización clínica de los biomarcadores en la falla cardíaca
I. GENERALIDADES DE LA FALLA CARDÍACA
A. Contexto de las pruebas de marcadores bioquímicos en la falla cardíaca
B. Antecedentes y definición de los términos.
C. Metabolismo y medición del péptido natriurético tipo B (BNP) y del fragmento N terminal del propéptido natriurético cerebral (NT-proBNP)
II. USO DE MARCADORES BIOQUÍMICOS EN LA EVALUACIÓN INICIAL DE LA FALLA CARDÍACA
A. Diagnóstico de falla cardíaca.
1. BNP y NT-proBNP para el diagnóstico de falla cardíaca aguda descompensada.
2.BNP o NT-proBNP para la confirmación del diagnóstico de falla cardíaca.B. Estratificación del riesgo de falla cardíaca.
1.Estratificación del riesgo de los pacientes con y sin falla cardíaca por medio del BNP o NT-proBNP.
2.Estratificación del riesgo de los pacientes con falla cardíaca por medio de la troponina cardíaca.
III. USO DE MARCADORES BIOQUÍMICOS EN EL SCREENING DE DISFUNCIÓN CARDÍACA
A. BNP o NT-proBNP para el screening de falla y disfunción cardíacas.
B. Abordajes del screening para la disfunción cardíaca.
IV. USO DE MARCADORES BIOQUÍMICOS EN LAS GUÍAS DE MANEJO DE LA FALLA CARDÍACA.
A. Terapia de monitoreo por medio de las Guías de BNP o NT-proBNP.
I. Generalidades de la falla cardíaca
A. Contexto de las pruebas de marcadores bioquímicos en la falla cardíaca
Las pruebas de marcadores bioquímicos han revolucionado
el abordaje para el diagnóstico y el manejo
de la falla cardíaca durante la última década. Quienes
se dedican a estudiar la falla cardíaca tienen la clara
certeza de que los avances significativos en la comprensión
de los biomarcadores cardíacos disponibles
en la actualidad y de los que surjan en el futuro, van a
mejorar la caracterización de los estados de la enfermedad
por falla cardíaca, así como promover terapias
individualizadas en esos casos.
Sin embargo, como en la mayoría de las nuevas
pruebas diagnósticas, los hallazgos prometedores que
surgen de estas pruebas se enfrentan a desafíos al ser
aplicados en el entorno clínico.
El material que se discute en este documento de
guías aborda el uso clínico de las pruebas de BNP/NT-proBNP
y troponina cardíaca en el contexto del diagnóstico
de falla cardíaca, estratificación y manejo del
riesgo, incluidas las guías terapéuticas en pacientes
adultos (> 18 años). Junto con el documento asociado
titulado "National Academy of Clinical Biochemistry and
IFCC Committee for Standardization of Markers of Cardiac
Damage Laboratory Medicine Practice Guidelines:Analytical
Issues for Biomarkers of Heart Failure", estas recomendaciones
tienen como objetivo que tanto los médicos en
su práctica clínica como los profesionales del laboratorio
realicen una correcta utilización de estas pruebas.
El comité siente que la divulgación de estas guías en el área de la clínica médica y del laboratorio va a mejorar
la comunicación, la atención y los resultados de los pacientes
que presenten falla cardíaca. A pesar de que es
complicado proporcionar las herramientas específicas
para su implementación, las guías están diseñadas de
manera directa y sucinta para que ésta se vea facilitada.
El comité siente que la educación y la divulgación
son las barreras más importantes que provocan un sobre-
o sub- uso de las mediciones de péptidos natriuréticos.
Por este motivo, existen planes de realizar una
amplia divulgación de las recomendaciones que se encuentran
presentes aquí; el comité cree que esa divulgación
ayudará a educar a los usuarios acerca de las
ventajas y advertencias acerca de la medición de BNP
y NT-proBNP. Con relación a los costos, por ejemplo,
el costo directo por prueba de BNP o NT-proBNP es
de aproximadamente USD 50 (moneda corriente de
los Estados Unidos de 2007).
A pesar de que es en parte controvertido, existe evidencia
de que el uso de las pruebas de péptidos natriuréticos
dentro del contexto de la falla cardíaca disminuye
los costos sin que aumenten los riesgos para el
paciente (1) (2). EL comité consideró los costos al formular
las recomendaciones; sin embargo, éstos fueron
modestos si se los compara con el costo total de la
atención de los pacientes con falla cardíaca, visión que
se puede probar (1) (2).
Es muy importante poner énfasis en que la validez de
los resultados de las pruebas debe complementarse con
los hallazgos clínicos para definir el proceso de una enfermedad.
Por lo tanto, las pruebas de marcadores bioquímicos
(como la medición de BNP y NT-proBNP) no
son aisladas y deben usarse e interpretarse en un contexto clínico más amplio, en el que los factores confusos
deben tomarse en cuenta. Si se las utiliza de manera
apropiada en este contexto, los beneficios de las pruebas
superan en gran medida los efectos secundarios y
los riesgos de tener conocimiento de los niveles de BNP
y NT-proBNP. El uso de las pruebas de troponina cardíaca
en cuanto a la población con falla cardíaca también
se va a discutir en primer lugar en cuanto al papel que
tiene en la estratificación del riesgo.
B. Antecedentes y definición de los términos
La falla cardíaca es un síndrome clínico que puede
originarse en cualquier alteración cardíaca, estructural
o funcional, que detenga la capacidad de los ventrículos
de llenarse con sangre o de expulsarla (3). Es un
problema creciente y costoso, que afecta al 2-3% del
total de la población de los Estados Unidos. Además,
se estima que sólo un 50% de los pacientes sobrevive
hasta 4 años (4). La creciente prevalencia de la falla
cardíaca se debe al envejecimiento de la población, así como al marcado incremento de la sobrevida de los
pacientes que sufrieron un infarto de miocardio.
Las estimaciones conservadoras sugieren que más
del 50% de los casos tiene un origen isquémico, mientras
que en hasta un 75% de los casos la hipertensión
es el factor más importante. El costo de la falla cardíaca
está estimado en 100.000 millones de dólares por
año en Europa y en los Estados Unidos, 70% del cual
se origina por las internaciones (3-5).
El diagnóstico de la falla cardíaca es un diagnóstico
al lado del paciente, que se basa en señales y síntomas
clínicos y no sólo en resultados de pruebas de laboratorio.
Sin embargo, una importante cantidad de los pacientes
derivados al cardiólogo luego de la consulta
con el clínico recibió un diagnóstico erróneo originariamente
de alguna afección distinta a la falla cardíaca.
Por consiguiente, la realización de pruebas de biomarcadores
clínicos en el marco de la falla cardíaca
apunta a tres importantes fines: 1) identificar las posibles -y potencialmente reversibles- causas subyacentes
de la falla cardíaca; 2) confirmar la presencia o ausencia
del síndrome de falla cardíaca; y 3) estimar la severidad
de la falla cardíaca y el riesgo de progresión de
la enfermedad.
Durante la última década, los péptidos natriuréticos,
en particular el BNP y su co-metabolito amino-terminal,
el NT-proBNP, han sido presentados como de
particular utilidad para la confirmación o refutación
del diagnóstico de la falla cardíaca así como para la estratificación
de los perfiles de riesgo a largo plazo. En
la literatura han surgido varios biomarcadores cardíacos
nuevos, metabólicos e inflamatorios acerca de la
falla cardíaca, como es el caso del péptido natriurético
tipo C (6), la endotelina-1 (7), la troponina cardíaca
(8), la proteína C reactiva de alta sensibilidad (hs-
PCR) (9) (10), la apelina (11) (12), la miotrofina
(13), la urotensina-II (14-16), la adrenomedulina (17) (18) y la proadrenomedulina de la región media (19),
la cardiotrofina-1 (20) (21), la urocortina (22), el receptor
de ST2 soluble (23), la mieloperoxidasa
(MPO) (24), la copeptina (19) (25), el factor de diferenciación
de crecimiento 15 (GDF-15) (26), las quinasas
del receptor ligadas a la proteína G del linfocito
(GRK-2) (27), la galectina 3 (28), el péptido natriurético
pro tipo A de la región media y otras formas circulantes
(19) (29), y muchos otros. Sin embargo, su papel
clínico todavía tiene que ser determinado y
validado (Tabla I). Por lo tanto, vamos a centrar nuestra
discusión en la utilidad de la realización de pruebas
de BNP y su metabolito asociado NT-proBNP asociado
en la falla cardíaca, con alguna mención a otros
biomarcadores cardíacos en contextos específicos.
Tabla III-1. Marcadores bioquímicos seleccionados actualmente
disponibles o en estudio para el diagnóstico clínico, el manejo y
la estratificación del riesgo de falla cardíaca.


C. Metabolismo y medición de BNP y NT-proBNP
Debido a que un gran cuerpo del conocimiento en
la realización de pruebas de marcadores bioquímicos
específicos para pacientes con falla cardíaca involucrará al BNP y NTproBNP, vamos a discutir específicamente
el metabolismo y medición de estos marcadores.
El BNP y el NT-proBNP pertenecen a una familia
de hormonas conocidas como péptidos natriuréticos.
A pesar de que el BNP se co-expresa en las vesículas secretoras
con un péptido natriurético del tipo A y los estímulos
para la expresión son complejos, la expresión
de BNP aumenta primariamente por el incremento en
la tensión de las paredes en respuesta a una sobrecarga
de presión (y volumen) de los atrios y de los ventrículos.
Por consiguiente, niveles elevados de BNP y NT-proBNP
en sangre ocurren en el contexto de
presiones de llenado elevadas en pacientes con disfunción
cardíaca, y pueden proporcionar información
diagnóstica y pronóstica relativamente confiable (30).
Queda claro, a partir de la literatura existente, que
los niveles de péptido natriurético en sangre disminuyen
luego de seguir tratamientos largos con los inhibidores
de la enzima convertidora de la angiotensina
(ACE) (31) (32), los bloqueadores del receptor de la
angiotensina II (33) y la espironolactona (34) (35). Es
muy probable que este hallazgo se deba a una reducción
en las presiones del rellenado y/o a una inversión
en el sentido del proceso de remodelación patológica
que tiene lugar luego del bloqueo neurohormonal.
Sin embargo, las respuestas en los niveles de péptidos
natriuréticos a los bloqueadores beta-adrenérgicos
han sigo dispares -mientras que la mayoría de la literatura
apunta a una reducción en los niveles de los péptidos natriuréticos en sangre con tratamientos a
largo plazo con bloqueadores beta-adrenérgicos, se
han observado elevaciones transitorias en los niveles
de los péptidos natriuréticos en sangre al iniciar tratamiento
con ellos (36).
Han surgido varios ensayos comerciales de laboratorio
así como pruebas point-of-care y están disponibles
para la realización de pruebas de BNP en el entorno
clínico como ayuda para el diagnóstico de la falla cardíaca
y para proporcionar información pronóstica
(Tabla 3-1). Por ejemplo, un BNP <100 pg/mL o un
NT-proBNP <300 pg/mL tienen altos valores predictivos
negativos al descartar el diagnóstico de falla cardíaca
entre pacientes que presentan disnea (37) (38).
Como se explicó anteriormente, en este documento,
el término "péptido natriurético" se referirá, en futuras
discusiones, tanto a BNP como a NT-proBNP, a
menos que se especifique lo contrario.
Existen varias consideraciones prácticas relativas al
uso de las pruebas de péptidos natriuréticos en los entornos
clínicos. En primer lugar, los rangos de referencia
para los ensayos de péptidos natriuréticos varían en
relación al método de ensayo empleado y a la naturaleza
de la población control. Las unidades expresadas
en la literatura acerca de los péptidos natriuréticos incluyen
mol/L y pg/mL, y el ensayo tan comúnmente
utilizado (Shionogi) a menudo informa valores que se
encuentran entre un 15-20% por debajo del valor de
los ensayos comerciales (Biosite y Abbot) (39).
Las diferencias en los resultados entre estos ensayos
han sido atribuidas a los distintos epitopes que identifican
los anticuerpos que se utilizan en cada uno de los
inmunoensayos (40). Estas variaciones han hecho que
la comparación directa entre estudios resulte difícil, y
deba realizarse una consideración cuidadosa del tipo o
los tipos de ensayo que se usan al interpretar los valores
que se informan en la literatura (Ver Guías de la National
Academy of Clinical Biochemistry y del Comité de Estandarización
de Marcadores de Daño Cardíaco de la IFCC
para las Prácticas en el Laboratorio Clínico: Aspectos analíticos
de los marcadores bioquímicos de la falla cardíaca).
En segundo lugar, una amplia variedad de factores
clínicos han demostrado que influyen en los niveles de
péptidos natriuréticos, entre los que se encuentran la
edad y el sexo (39) (41-43), la función renal (43-48),
la predisposición del cuerpo (49-51), la función tiroidea
(52) (53) y la anemia (54). La obesidad, en particular,
ha estado asociada con niveles de BNP y NT-proBNP
en sangre más bajos en todo el espectro de la
falla cardíaca, y debe interpretarse con precaución, especialmente
al descartar las causas cardíacas de la disnea.
Las afecciones cardíacas pre-existentes como una
historia previa de falla cardíaca (55), anomalías rítmicas
(42) (56-58), y una etiología subyacente de falla
cardíaca (59) también pueden influir en un diagnóstico
preciso. La influencia relativa de estos factores en
relación al grado de disfunción cardíaca continúa
siendo un tema ampliamente debatido y puede diferir
en distintos entornos clínicos (en términos generales,
los efectos confusos son menos aparentes en el entorno
de una exacerbación aguda de falla cardíaca). Además,
la disfunción diastólica, la regurgitación mitral, la
disfunción ventricular derecha, una cirugía cardíaca
reciente y otras anomalías cardíacas ventriculares o
funcionales pueden influir de manera significativa sobre
los niveles de péptidos natriuréticos en sangre
(60-63).
En tercer lugar, a pesar de que distintos estudios
han demostrado correlaciones estadísticas excelentes
entre los ensayos de BNP y NT-proBNP (64) (65), hubo
diferencias muy claras, en particular con respecto a
sus medias vidas, a la variabilidad intra e inter individual
(66) (67), y a las diferencias en su producción y
en el clearance renal. Sin embargo, sus capacidades
diagnósticas y pronósticas generales pasaron a ser
comparables en el entorno clínico. También existen
diferencias en la estabilidad del péptido. En la actualidad,
no existe "conversión" directa entre los dos tipos
de ensayo, mucho menos entre los distintos ensayos
del mismo péptido.
Cuando se los aplica en conjunción con la historia
clínica, el examen físico y otras herramientas que los
médicos tienen a su disposición, los biomarcadores
cardíacos sirven para lograr objetivos clínicos tal como
se presenta a continuación.
II. Uso de marcadores bioquímicos en la evaluación inicial de falla cardíaca
A. Diagnóstico de falla cardíaca

1. BNP Y NT-PROBNP PARA EL DIAGNÓSTICO DE LA FALLA CARDÍACA DESCOMPENSADA AGUDA
La mayoría de los estudios tempranos de péptidos natriuréticos han estado enfocados al papel diagnóstico de las pruebas de BNP o NT-proBNP entre los pacientes que presentan signos y síntomas de falla cardíaca. Varios estudios clínicos prospectivos de distintos centros han establecido la utilidad de la prueba en sangre de BNP o NT-proBNP en la evaluación inicial de los pacientes con falla cardíaca en el entorno agudo. En el estudio de centros múltiples Breathing-Not- Properly Study, el uso de un nivel de BNP de 100 pg/mL como punto de corte diagnóstico proporcionó una sensibilidad del 90%, una especificidad del 76% y una precisión diagnóstica del 81% para determinar la etiología de falla cardíaca de la disnea aguda, que fue superior a la evaluación clínica sola en una serie de 1.586 pacientes que concurrieron a la guardia con disnea aguda (68) (Figura 3-1A). En una prueba controlada aleatoria reciente que comparaba una estrategia diagnóstica en la que se incluían pruebas de BNP en sangre, con la evaluación clínica sola, la prueba de BNP en sangre en la sala de guardia mejoraba la evaluación y el tratamiento de los pacientes con disnea aguda, con lo que el alta médica se daba antes y se reducía el costo total del tratamiento (1). Los médicos informaron hallazgos similares en el entorno de la atención primaria, en los cuales la prueba de NT-proBNP mejoró la precisión del diagnóstico (69). El papel equivalente que tiene el NT-proBNP se confirmó con la prueba PRIDE (ProBNP Investigation of Dyspnea in the Emergency Department), en la que se le realizó una prueba de NT-proBNP a 600 pacientes que ingresaron para atenderse en la sala de guardia con disnea aguda. Los NT-proBNP con puntos de corte >450 pg/mL (edades<50 años) y >900 pg/mL (edades ≥50 años) fueron ampliamente sensibles y específicos para el diagnóstico de falla cardíaca aguda, mientras que <300 pg/mL fue óptimo para descartar falla cardíaca aguda (valor predictivo negativo de 99%, Figura 3-1B) (70). Es lógico comparar los niveles de péptidos natriuréticos de manera longitudinal en pacientes previamente estables con falla cardíaca pre-existente, a pesar de que no se ha establecido la precisa dimensión del incremento que podría considerarse clínicamente significativo. En la actualidad, no existen guías nacionales para el diagnóstico y manejo de los síndromes de falla cardíaca aguda en los Estados Unidos.
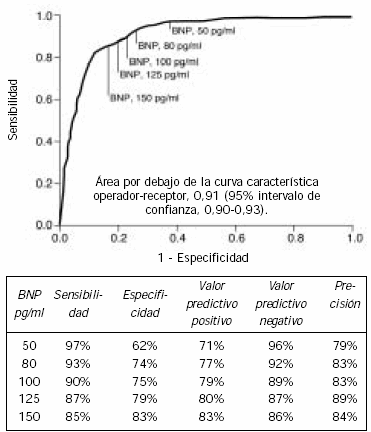
Figura 3-1A. Curva Característica Operador-Receptor (ROC) para la
prueba del péptido natriurético tipo B en el diagnóstico de la falla
cardíaca con disnea aguda (68). Con permiso de Maisel A, et al."Rapid measurement of B-type natriuretic peptide in the emergency
diagnosis of heart failure." N Engl J Med 2002; 347(3):
161-7; Copyright © 2002 Massachusetts Medical Society. Todos
los derechos reservados.
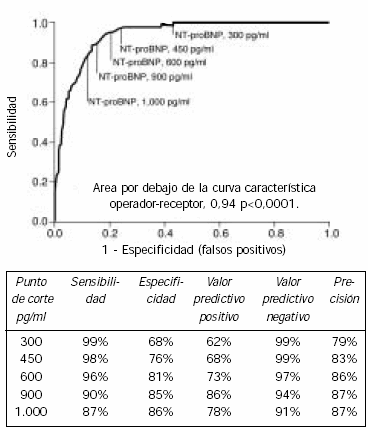
Figura 3.1B. Curva característica operador-receptor (ROC) para la
prueba del péptido natriurético aminoterminal tipo proB en el
diagnóstico de falla cardÍaca con disnea aguda (70). Reimpreso
de Januzzi JL Jr et al. "The N-terminal Pro-BNP investigation of
dyspnea in the emergency department (PRIDE) study." Am J Cardiol
2006; 95(8): 948-954; Copyright © 2006, con permiso de
Elsevier.
Ha surgido algo de escepticismo con respecto a las indicaciones clínicas para el uso de rutina de la prueba de péptidos natriuréticos en sangre, en la evaluación inicial de los pacientes que presentan signos y síntomas de falla cardíaca, particularmente en el contexto no-agudo (71). Además, una medición de un solo punto del péptido natriurético en sangre con niveles entre 80 y 300 pg/mL utilizando el ensayo Biosite se ha informado como menos confiable en el contexto de la falla cardíaca aguda con edema pulmonar relámpago debido a que el nivel de BNP o NT-proBNP probablemente no haya tenido suficiente tiempo para elevarse (72). Estas "zonas grises" de los péptidos natriuréticos en el diagnóstico de la falla cardíaca pueden también verse influidas por la presencia de una historia subyacente de falla cardíaca, donde el nivel "seco" de péptido natriurético puede descender dentro de este rango (55) (73) (74). Los "puntos de corte" específicos presentan desafíos en ciertas poblaciones como la de los mayores de edad (75). Además, los valores absolutos y los cambios en los niveles de péptidos natriuréticos pueden correlacionarse con los parámetros clínicos o ecocardiográficos, pero tales correlaciones pueden variar de manera considerable. Se han presentado informes que ilustran la falta de relación estrecha entre los niveles de péptidos natriuréticos en sangre y la evaluación del volumen de sangre (76), la fracción de eyección ventricular izquierda (60), y los parámetros hemodinámicos (77) (79). Por consiguiente, en este momento, la prueba de péptidos natriuréticos todavía debería considerarse sólo parte de la evaluación diagnóstica en la falla cardíaca, y no la definición diagnóstica.
2. BNP O NT-PROBNP PARA LA CONFIRMACIÓN DEL DIAGNÓSTICO DE FALLA CARDÍACA
Existe consenso entre las últimas guías de la American
College of Cardiology (ACC)/American Heart Association (AHA), la Heart Failure Society of America (HFSA), entre
otras, en relación al manejo de la falla cardíaca
crónica, que recomiendan que las pruebas de péptidos
se realicen para confirmar el diagnóstico de la falla cardíaca
entre aquellos pacientes con diagnóstico sospechoso
de falla cardíaca, pero solamente en aquellos que
presentan signos y síntomas que son ambiguos o que
ocurren en el contexto de estados confusos de la enfermedad
(como las enfermedades pulmonares obstructivas
crónicas) (80). Tales niveles pueden ser valiosos para
mejorar la precisión diagnóstica en la detección de
la falla cardíaca. Además, se encontró que la prueba
de péptidos natriuréticos es útil para diferenciar los
distintos mecanismos de disfunción cardíaca (miocardiopatía
restrictiva versus miocardiopatía constrictiva
(81)), y para identificar el compromiso cardíaco en las
enfermedades sistémicas (82) (83).
No se ha llevado a cabo ninguna evaluación cuidadosa
de la utilidad de la prueba de péptidos natriuréticos
en el contexto de los cuidados ambulatorios no
agudos. Se deduce que la utilidad clínica de la prueba
de péptidos natriuréticos para confirmar el diagnóstico
de falla cardíaca en los pacientes sintomáticos en el ámbito
de los cuidados ambulatorios deberá ser comparable
con el entorno agudo de donde derivan la mayor
parte de los datos existentes relativos a la prueba de
péptidos natriuréticos. Vale la pena resaltar que entre
los pacientes mínima o crónicamente sintomáticos en
el entorno de los cuidados ambulatorios no agudos, los
niveles de péptidos natriuréticos pueden variar, y los
rangos diagnósticos pueden ser diferentes de los del
entorno agudo (ver Sección III acerca del Screening).
Por ende, los valores del punto de corte que se utilizan
en el entorno agudo es probable que no se traduzcan
de manera confiable al contexto del cuidado ambulatorio,
entre los pacientes con falla cardíaca crónica estable.
También se han producido informes referidos a
que, en el ámbito de los cuidados ambulatorios, los pacientes
con falla cardíaca crónica estable pero sintomática
pueden tener niveles de péptidos natriuréticos que
son relativamente inferiores a los que normalmente se
considerarían como "diagnósticos" de falla cardíaca
(por ejemplo, BNP Biosite<100 pg/mL) (59). Esto se
encuentra en oposición directa con más del 90% de los
pacientes que presentan niveles de BNP en sangre > 100 pg/mL en el entorno de los cuidados agudos (84).
Sin embargo, este punto de corte es todavía útil probablemente
para excluir un diagnóstico de falla cardíaca
cuando se lo verifica por intermedio de una historia
cuidadosa y un examen físico.
B. Estratificación del riesgo de falla cardíaca

1. ESTRATIFICACIÓN DEL RIESGO EN PACIENTES CON Y SIN FALLA CARDÍACA UTILIZANDO BNP O NT-PROBNP
Existe una cantidad creciente de literatura segura
que apoya la utilidad de la prueba de los péptidos natriuréticos
para la estratificación del riesgo en pacientes
con falla cardíaca, o inclusive en aquellos sin historia
previa de falla cardíaca (85). Esto se aplica a una
amplia variedad de entornos clínicos, entre los que se
incluyen los síndromes coronarios agudos (86-89), la
enfermedad de las arterias coronarias estables (90-92),
la falla cardíaca descompensada (93) (94), la falla cardíaca
crónica estable (95), e inclusive las alteraciones
no cardíacas como el embolismo pulmonar (96) (97) o a la población en general sin historia previa de falla
cardíaca (85) o a aquellos en riesgo de desarrollar falla
cardíaca (98). Ha habido estudios también que defienden
el papel de la prueba de los péptidos natriuréticos
para la selección de pacientes para trasplante
cardíaco (8) (99) (100), así como para la implantación
de desfibriladores cardíacos (101) o para terapia de resincronización
cardíaca (102-104). Además, se ha descubierto
que los niveles de los péptidos natriuréticos
son predictores independientes importantes de muerte
súbita (105) y equivalente, en la estratificación del
riesgo, al Heart Failure Survival Score (106). Los péptidos
natriuréticos también tienen un valor pronóstico
adicional con indicadores pronósticos clínicos y de laboratorio
(98) (107).
Es importante también resaltar que los cambios en
los niveles sanguíneos de los péptidos natriuréticos
han estado asociados con las diferencias en los resultados
clínicos a largo plazo (ver Sección IV acerca de "Manejo Guiado"). Además, también vale la pena reconocer
que los valores absolutos de los rangos en los
diferentes estratos de riesgo informados en la literatura
varían considerablemente, dependiendo de la población
de pacientes. De hecho, inclusive cuando los
niveles sanguíneos de los péptidos natriuréticos fueron
intermedios, sus valores pronósticos a largo plazo
siguieron siendo robustos (74) (108). Sin embargo, el
valor pronóstico de las pruebas del péptido natriurético
está todavía limitado por la falta de una utilidad clara
en el manejo clínico de las guías. El desafío consiste
en definir mejor las situaciones específicas en las
cuales la estratificación del riesgo puede ser beneficiosa
clínicamente, y el hecho de qué se considera "falso positivo" o "falso negativo" puede revelar las manifestaciones
fisiopatológicas subyacentes que todavía no
son clínicamente aparentes (109).
El manejo actual de los pacientes con falla cardíaca
depende de la evaluación clínica subjetiva hecha por
los pacientes y por los médicos y en distintas mediciones
de laboratorio no específicas de la disfunción de órganos y del estado de los fluidos. Los niveles del péptido
natriurético disminuyen de manera rápida luego
de la terapia con diuréticos en aquellos pacientes con
falla cardíaca descompensada (131-133), a pesar de
que estos cambios pueden variar en gran medida y
pueden ser independientes de los cambios hemodinámicos
(77). Además, los péptidos natriuréticos pueden
correlacionarse con los síntomas en el entorno del paciente
externo (134). La variabilidad intra-individuo
de los niveles seriados de péptidos natriuréticos sigue
siendo un tema ampliamente debatido (135-137). La
literatura más reciente que surge de los cohortes de
pacientes con falla cardíaca crónica (138) y con síndromes
coronarios agudos (139) ha ilustrado en más
detalle que la reducción en los niveles de los péptidos
natriuréticos a través del tiempo puede estar directamente
asociada con correspondientes reducciones de
los episodios clínicos en el largo plazo. Por consiguiente,
las concentraciones sanguíneas seriadas de BNP o
NT-proBNP también podrían usarse para seguir los
cambios en los perfiles de riesgo y en el estado clínico
de los pacientes con falla cardíaca en situaciones particulares
en las que se necesita una estratificación del
riesgo adicional.
2. ESTRATIFICACIÓN DEL RIESGO EN PACIENTES CON FALLA CARDÍACA POR MEDIO DE LA TROPONINA
Los niveles de troponina cardíaca en suero constituyen una evidencia de la existencia de necrosis del miocardio, y se los ha utilizado en gran medida en el contexto de los síndromes coronarios agudos (SCA). En aquellos pacientes que presentan falla coronaria aguda, la realización de pruebas de troponina cardíaca se ha utilizado como parte de las prácticas de rutina dentro del contexto agudo para descartar la isquemia de miocardio como etiología primaria (ver las recomendaciones en el Capítulo I). Sin embargo, en el contexto de una falla cardíaca avanzada (8) (110) o en descompensaciones (111-113) algunos pacientes pueden presentar elevación transitoria o persistente de los niveles de troponina cardíaca I o de troponina T sin presencia de ninguna isquemia de miocardio obvia. Los niveles elevados de troponina han estado asociados con un mal pronóstico a largo plazo. Varias series clínicas han ilustrado en mayor detalle un fuerte efecto pronóstico adverso frente a una elevación sostenida de los niveles seriados de troponina en suero que podría indicar daño de miocardio en curso (114) (115). Sin embargo, sigue todavía sin determinarse la utilidad de la evaluación de rutina de los niveles de troponina en los pacientes con falla cardíaca aguda o crónica, así como el enfoque diagnóstico y terapéutico de los niveles elevados de troponina en el entorno de no-SCA. Esto en parte se debe a la falta de conocimiento acerca de si los niveles de troponina cardíaca como marcadores de necrosis del miocito representan un marcador de riesgo o un factor de riesgo.
III. Uso de marcadores bioquímicos en el screening de disfunción cardíaca
A. BNP o NT-proBNP para el screening de falla y disfunción cardíaca
La utilidad diagnóstica de los niveles sanguíneos de
péptidos natriuréticos en el contexto de la falla cardíaca
aguda ha despertado el interés por evaluar a estos
biomarcadores como herramientas para el screening de
pacientes con una disfunción cardíaca subyacente pero
sin signos o síntomas claros (la así llamada "disfunción
ventricular izquierda asintomática") (ALVD). De
acuerdo a las más recientes guías de la ACC/AHA para
el manejo de la falla cardíaca crónica, una gran mayoría
de los pacientes que desarrollan falla cardíaca
pueden padecer anomalías cardíacas estructurales
precedentes ("falla cardíaca estadío B") que pueden
reconocerse antes de la progresión de la enfermedad
(116). Datos recientes obtenidos de la población común
del Condado Olmsted sugieren que la prevalencia
de anomalías estructurales cardíacas subyacentes
(entre las que se incluye ALVD, disfunción diastólica,
anomalías valvulares, hipertrofia ventricular izquierda,
y anomalías en la motricidad de la pared cardíaca motriz
regional) fue más alta entre los individuos dentro
del tercil más alto tanto de BNP como de NT-proBNP.
Los niveles más altos de NT-proBNP también han estado
asociados con una mayor probabilidad de detectar
falla cardíaca incidental en una población con enfermedad
estable de la arteria coronaria (117). No obstante,
han existido datos inconcluyentes relativos al
papel del screening para ALVD utilizando la prueba de
péptidos natriuréticos en distintos estudios (85) (118)
(119). En general, las precisiones diagnósticas son mucho
más bajas comparadas con la detección de la falla
cardíaca clínica, que es probable que se deba a la asociación
relativamente no específica con la ALVD en
rangos de niveles de péptidos natriuréticos observados
en la población en general (120) (121).
B. Abordajes para el screening de disfunción cardíaca
Existen dos abordajes para el uso de la prueba de
péptidos natriuréticos con fines de screening. En el primer
abordaje, la realización de pruebas de péptidos natriuréticos
puede ser de utilidad en el contexto de infarto
agudo de miocardio, sin que exista falla cardíaca
explícita. En este caso, los niveles sanguíneos de péptidos
natriuréticos han estado asociados de manera inversa
con la fracción de eyección ventricular izquierda
post-infarto. Sin embargo, debido a la heterogeneidad
de las poblaciones en estudio y al tiempo de toma de la
muestra, ha variado la precisión del screening del péptido
natriurético. Es probable que la ecocardiografía siga
siendo el método principal para evaluar las anomalías
estructurales y funcionales del ventrículo izquierdo
luego de un infarto de miocardio.
El segundo abordaje es el que combina la prueba
de péptidos natriuréticos con otras modalidades de screening para mejorar la precisión diagnóstica de cualquier
prueba. Este abordaje de "marcadores múltiples" ha sido muy estudiado para la estratificación del
riesgo en el contexto de los síndromes coronarios agudos.
En este caso, parecieron prometedoras las combinaciones
de las pruebas de péptidos natriuréticos con
mieloperoxidasa o electrocardiografía (122) (123),
pero se necesita realizar más estudios que definan mejor
estos abordajes. En este momento, la mayoría de
las guías no apoyan la realización de pruebas de rutina de péptidos natriuréticos en el screening para disfunción
sistólica ventricular izquierda de grandes poblaciones
de pacientes asintomáticos.
Algunos investigadores han intentado aumentar la
detección de la disfunción cardíaca asintomática poniendo énfasis en los subgrupos de alto riesgo, estrategia
que probablemente sea más costo-efectiva (124). Se
ha observado una alta prevalencia de niveles elevados
de péptidos natriuréticos en sangre en una población
de pacientes en riesgo de desarrollar falla cardíaca
("Falla cardíaca estadio A"), particularmente entre
quienes tienen una historia de hipertensión de larga
data, diabetes mellitus (125) (126), enfermedad de las
arterias coronarias (92) (127), y entre los mayores de
edad (128-130). Se puede considerar que la prueba de
péptidos natriuréticos es de utilidad para el screening de
estas poblaciones que se encuentran en alto riesgo y
quienes, de otro modo, serían derivados para la realización
de más screenings ecocardiográficos para detectar
disfunción ventricular izquierda asintomática, a pesar
de que los niveles de corte puedan ser distintos en diferentes
poblaciones de pacientes. Otros investigadores
han combinado varios biomarcadores cardíacos para
incrementar la especificidad del screening utilizando
marcadores inflamatorios como MPO o hsPCR (122).
Todavía no se encuentra garantizada la aplicación clínica
amplia de estos abordajes hasta tanto no se lleven a
cabo estudios prospectivos que establezcan la evidencia
para estratificar a los pacientes de acuerdo con los niveles
de péptidos natriuréticos o para validar un abordaje
de marcadores múltiples con ensayos clínicamente
disponibles con justificaciones costo-efectivas.
IV. Uso de marcadores bioquímicos para guiar el manejo de la falla cardíaca

A. TERAPIA DE MONITOREO UTILIZANDO GUÍAS PARA BNP O NT-PROBNP
Más allá de sus capacidades diagnósticas, las pruebas
de péptidos natriuréticos son para guiar la terapia
de un modo objetivo. De hecho, esta hipótesis ha sido
estudiada en un pequeño estudio piloto entre pacientes
con falla cardíaca crónica de leve a moderada. En
este estudio, los inhibidores de la ACE y la terapia con
diuréticos se titularon para lograr un nivel de NT-proBNP <200 pmol/L por el ensayo Christchurch (equivalente
a 1.680 pg/mL) sin comprometer la función
de los otros órganos (por ejemplo con hipotensión, insuficiencia
renal) (140). Este estudio halló un número
significativamente menor de eventos cardiovasculares
totales (muertes, internaciones o episodios de falla
cardíaca descompensada basado en los criterios de
Framingham modificados) en el grupo aleatorio para
terapia guiada por NT-proBNP. Estos resultados han sido
confirmados en un estudio francés de centros múltiples
que indicaba una significativa mejora en los episodios
clínicos posteriores a un abordaje guiado por
péptidos natriuréticos, en comparación con la evaluación
clínica estándar (141). Sin embargo, se observaron
también resultados neutros cuando se comparó al
abordaje guiado por péptidos natriuréticos con la evaluación
clínica estándar (142) (143). Por consiguiente,
el concepto de manejo de la falla cardíaca guiado por péptidos natriuréticos todavía es objeto de debate
y no existe consenso general en la opinión de los expertos
en relación a este tema.
Otro uso potencial de la prueba de los péptidos natriuréticos
en el monitoreo del tratamiento es la evaluación
de la adecuación de la terapia en la falla cardíaca
descompensada. Los niveles sanguíneos de
péptidos natriuréticos antes de darle de alta al paciente,
pero no los iniciales, han estado firmemente asociados
y de manera consistente con los resultados posteriores
al alta médica (93) (144), a pesar de que los
rangos de los cambios en los péptidos natriuréticos
luego de las intervenciones terapéuticas también varían
ampliamente. Sin embargo, sigue siendo difícil
determinar los niveles de péptidos natriuréticos "secos",
los que son distintos de paciente a paciente. La
diuresis sobre-agresiva basada solamente en los niveles
de péptidos natriuréticos en sangre puede aumentar
el riesgo de azotemia renal o prolongar la estadía en el
hospital sin reducir la morbilidad y la mortalidad.
También han surgido varios problemas en relación
a la probabilidad clínica de una estrategia terapéutica
guiada por péptidos natriuréticos. La amplia variación
de sus niveles simples o secuenciales en la falla
cardíaca crónica luego de una prolongada terapia
médica ha ocasionado dificultades para establecer un
solo nivel "meta" (59) (60) (136) (145) (146). La frecuencia
de la realización de las pruebas de péptidos
natriuréticos y la utilidad de las mismas para monitorear
a los pacientes con falla cardíaca sigue aún sin
determinarse.
Es muy promisoria la posibilidad de guías terapéuticas
utilizando un abordaje guiado por los biomarcadores.
En la actualidad se están llevando a cabo varios
estudios prospectivos para confirmar la utilidad de
una estrategia terapéutica guida por los péptidos natriuréticos
(147) (148).
Sin embargo, hasta que estos resultados estén disponibles,
todas las guías clínicas coinciden en que la
realización de rutina de pruebas de BNP o NTproBNP
en sangre no está todavía garantizada para decisiones
terapéuticas en pacientes con falla cardíaca aguda o
crónica, en primer lugar debido a los resultados mezclados
provenientes de estudios clínicos y a la variabilidad
intraindividual, interindividual e interensayos.
1. Wu AHB, Apple FS, Gibler Wb, Jesse RL, Warshaw MM, Valdes R Jr. National Academy of Clinical Biochemistry Standards of Laboratory Practice: recommendations for use of cardiac markers in coronary artery diseases. Clin Chem 1999; 45: 1104-21.
2. Panteghini M, Gerhardt W, Apple FS, Dati F, Ravkilde J, Wi AH. Quality specifications for cardiac troponin assays. Clin Chem Lab Med 2001; 39: 174-8.
3. National Institute of Standards and Technology. Certificate of analysis. Standard reference material 2921: human cardiac troponin complex. Gaithersburg, MD; NIST, 2004.
4. Christenson RH, Duh SH, Apple FS, Bodor GS, Bunk DM, Dalluge J, et al. Standardization of cardiac troponin I assays: round robin performance of ten candidate reference materials. Clin Chem 2001; 47: 431-7.
5. Christenson RH, Duh SH, Apple FS, Bodor GS, Bunk DM, Panteghini M, et al. Toward standardization of cardiac troponin I measurements. Part II: Assessing commutability of candidate reference materials and harmonization of cardiac troponin I assays. Clin Chem 2006; 52: 1685-92.
6. Jaffe AS, Babuin L, Apple FS. Biomarkers in acute coronary disease: the present and the future. J Am Coll Cardiol 2006; 48: 1-11.
7. Panteghini M. Standardization of cardiac troponin I measurements: The way forward? Clin Chem 2005; 51: 1594-7.
8. Clinical and Laboratory Standards Institute. Protocols for determination of limits of detection and limits of quantitation; Approved guideline. CLSI document EP17-A. 2004.
9. Clinical and Laboratory Standards Institute. Evaluation of precision performance of quantitative measurement methods; approved guideline, 2nd ed. CLSI document EP5-A2. 2004.
10. Novis DA, Jones BA, Dale JC, Walsh MK. Biochemical markers of myocardial injury test turnaround time: a College of American Pathologists Q-probe Study. Arch Path Lab Med 2004; 128: 158-64.
11. Apple FS, Chung AY, Kogut ME, Bubany S, Murakami MM. Decreased patient charges following implementation of point-of-care cardiac troponin monitoring in acute coronary syndrome patients in a community hospital cardiology unity. Clin Chim Acta 2006; 370: 191-5.
12. Luepker RV, Apple FS, Christenson RH, Crow RS, Fortmann Sp, Goff D, et al. Case definitions for acute coronary heart disease in epidemiology and clinical research studies. Circulation 2003; 108: 2543-9.
13. Jaffe AS, Ravkilde J, Roberts R, Naslund U, Apple FS, Galvani M, Katus H. It's time for a change to a troponin standard. Circulation 2000; 102: 1216-20.
14. Alpert JS, Thygesen K, Antman E, Bassand JP. Myocardian infarction redefined: a consensus document of the Joint European Society of Cardiology/American College of Cardiology Committee for the redefinition of myorcardial infarction. J Am Coll Cardio 2000; 36: 959-69.
15. Newby LK, Alpert JS, Ohman EM, Thygesen K, Califf RM. Changing the diagnosis of acute myocardial infarction: implications for practice and clinical investigations. Am Heart J 2002: 144: 957-80.
16. Apple FS, Wu AHB, Jaffe AS. European Society of Cardiology and American College of Cardiology guidelines for redefinition of myocardial infarction: how to use existing assays clinically and for clinical trials. Am Heart J 2002; 144: 981-6.
17. Clinical and Laboratory Standards Institute. How to define and determine reference interval sin the clinical laboratory; approved guideline, 2nd ed. CLSI document C28-A2. 2000.
18. Apple FS, Quist HE, Doyle PJ, Otto AP, Murakami MM. Plasta 99th percentile reference limits for cardiac troponin and creatine kinase MB mass for use with European Society of Cardiology/American College of Cardiology consensus recommendations. Clin Chem 2003; 49: 1331-6.
19. Apple FS, Parvin CA, Buechler KF, Christenson RH, Wu AHB, Jaffe AS. Validation of the 99th percentile cutoff independent of assay imprecision (%CV) for cardiac troponin monitoring for ruling out myocardial infarction. Clin Chem 2005; 51: 2198-200.
20. Panteghini M, Pagani F, Yeo KT, Apple FS, Christenson RH, Dati F, et al. Evaluation of the imprecision at low range concentrations of the assays for cardiac troponin determination. Clin Chem 2004; 50: 327-32.
21. Christenson RH, Cervelli DR, Bauer RS, Gordon M. Stratus CS cardiac troponin I method: performance characteristics including imprecision at low concentrations. Clin BIochem 2004; 37: 679-83.
22. Braunwald E, Antman EM, Beasley JW, Califf RM, Cheitlin MD, Hochman, JS, et al. American College of Cardiology/American Heart Association Task Force on practice guidelines (Committee on the Management of Patients With Unstable Angina). ACC/AHA guideline update for the management of patients with unstable angina and non-ST-segment elevation myocardial infarction - 2002: summary article: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Commitee on the Management of Patients With Unstable Angina). Circulation 2002; 106: 1893-2000.
23. Jaffe AS. Elevations in cardiac troponin measurements: false false-positive. Cardiovasc Tox 2001; 1: 87-92.
1. Mueller C, Scholer A, Laule-Kilian K, Martina B, Schindler C, Buser P, Pfisterer M, Perruchoud AP. Use of B-type natriuretic peptide in the evaluation and management of acute dyspnea. N Engl J Med 2004; 350: 647-54.
2. Mueller C, Laule-Kilian K, Schindler C, Klima T, Frana B,Rodriguez D, Scholer A, Christ M, Perruchoud AP. Cost-effectiveness of B-type natriuretic peptide testing in patients with acute dyspnea. Arch Intern Med 2006; 166: 1081-7.
3. Hunt SA, Abraham WT, Chin MH, Feldman AM, Francis GS, Ganiats TG, Jessup M, Konstam MA, Mancini DM, Michl K, Oates JA, Rahko PS, Silver MA, Stevenson LW, Yancy CW, Antman EM, Smith SC, Jr., Adams CD, Anderson JL, Faxon DP, Fuster V, Halperin JL, Hiratzka LF, Jacobs AK, Nishimura R, Ornato JP, Page RL, Riegel B. ACC/AHA 2005 Guideline Update for the Diagnosis and Management of Chronic Heart Failure in the Adult: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Update the 2001 Guidelines for the Evaluation and Management of Heart Failure): developed in collaboration with the American College of Chest Physicians and the International Society for Heart and LungTransplantation: endorsed by the Heart Rhythm Society. Circulation 2005; 112: e154-235.
4.Rosamond W, Flegal K, Friday G, Furie K, Go A, Greenlund K, Haase N, Ho M, Howard V, Kissela B, Kittner S, Lloyd-Jones D, McDermott M, Meigs J, Moy C, Nichol G, O'Donnell CJ, Roger V, Rumsfeld J, Sorlie P, Steinberger J, Thom T, Wasserthiel-Smoller S, Hong Y. Heart disease and stroke statistics-2007 update: a report from the American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Circulation 2007; 115: e69-171.
5. Bhalla V, Willis S, Maisel AS. B-type natriuretic peptide: the level and the drug-partners in the diagnosis of congestive heart failure. Congest Heart Fail 2004; Suppl 1: 3-27.
6. Kalra PR, Clague JR, Bolger AP, Anker SD, Poole-Wilson PA, Struthers AD, Coats AJ. Myocardial production of C-type natriuretic peptide in chronic heart failure. Circulation 2003; 107: 571-3.
7. Kinugawa T, Kato M, Ogino K, Osaki S, Igawa O, Hisatome I, Shigemasa C. Plasma endothelin-1 levels and clinical correlates in patients with chronic heart failure. J Card Fail 2003; 9: 318-24.
8. Horwich TB, Patel J, MacLellan WR, Fonarow GC. Cardiac troponin I is associated with impaired hemodynamics, progressive left ventricular dysfunction, and increased mortality rates in advanced heart failure. Circulation 2003; 108: 833-8.
9. Berton G, Cordiano R, Palmieri R, Pianca S, Pagliara V, Palatini P. C-reactive protein in acute myocardial infarction: association with heart failure. Am Heart J 2003; 145: 1094-101.
10. Alonso-Martinez JL, Llorente-Diez B, Echegaray-Agara M, Olaz-Preciado F, Urbieta-Echezarreta M, Gonzalez- Arencibia C. C-reactive protein as a predictor of improvement and readmission in heart failure. Eur J Heart Fail 2002; 4: 331-6.
11. Chen MM, Ashley EA, Deng DX, Tsalenko A, Deng A, Tabibiazar R, Ben-Dor A, Fenster B, Yang E, King JY, Fowler M, Robbins R, Johnson FL, Bruhn L, McDonagh T, Dargie H, Yakhini Z, Tsao PS, Quertermous T. Novel role for the potent endogenous inotrope apelin in human cardiac dysfunction. Circulation 2003; 108: 1432-9.
12. Foldes G, Horkay F, Szokodi I, Vuolteenaho O, Ilves M, Lindstedt KA, Mayranpaa M, Sarman B, Seres L, Skoumal R, Lako-Futo Z, deChatel R, Ruskoaho H, Toth M. Circulating and cardiac levels of apelin, the novel ligand of the orphan receptor APJ, in patients with heart failure. Biochem Biophys Res Commun 2003; 308: 480-5.
13. O'Brien RJ, Loke I, Davies JE, Squire IB, Ng LL. Myotrophin in human heart failure. J Am Coll Cardiol 2003; 42: 719-25.
14. Ng LL, Loke I, O'Brien RJ, Squire IB, Davies JE. Plasma urotensin in human systolic heart failure. Circulation 2002; 106: 2877-80.
15. Richards AM, Nicholls MG, Lainchbury JG, Fisher S, Yandle TG. Plasma urotensin II in heart failure. Lancet 2002; 360: 545-6.
16. Douglas SA, Tayara L, Ohlstein EH, Halawa N, Giaid A. Congestive heart failure and expression of myocardial urotensin II. Lancet 2002; 359: 1990-7.
17. Richards AM, Doughty R, Nicholls MG, MacMahon S, Sharpe N, Murphy J, Espiner EA, Frampton C, Yandle TG. Plasma Nterminal pro-brain natriuretic peptide and adrenomedullin: prognostic utility and prediction of benefit from carvedilol in chronic ischemic left ventricular dysfunction. Australia-New Zealand Heart Failure Group. J Am Coll Cardiol 2001; 37: 1781-7.
18. Richards AM, Nicholls MG, Yandle TG, Frampton C, Espiner EA, Turner JG, Buttimore RC, Lainchbury JG, Elliott JM, Ikram H, Crozier IG, Smyth DW. Plasma N-terminal pro-brain natriuretic peptide and adrenomedullin: new neurohormonal predictors of left ventricular function and prognosis after myocardial infarction. Circulation. 1998; 97: 1921-9.
19. Gegenhuber A, Struck J, Dieplinger B, Poelz W, Pacher R, Morgenthaler NG, Bergmann A, Haltmayer M, Mueller T. Comparative evaluation of B-type natriuretic peptide, midregional pro-A-type natriuretic peptide, midregional proadrenomedullin,and Copeptin to predict 1-year mortality in patients with acute destabilized heart failure. J Card Fail 2007; 13: 42-9.
20. Talwar S, Squire IB, Downie PF, O'Brien RJ, Davies JE, Ng LL. Elevated circulating cardiotrophin-1 in heart failure: relationship with parameters of left ventricular systolic dysfunction. Clin Sci (Lond) 2000; 99: 83-8.
21. Ng LL, O'Brien RJ, Demme B, Jennings S. Non-competitive immunochemiluminometric assay for cardiotrophin- 1 detects elevated plasma levels in human heart failure. Clin Sci (Lond) 2002; 102: 411-6.
22. Ng LL, Loke IW, O'Brien RJ, Squire IB, Davies JE. Plasma urocortin in human systolic heart failure. Clin Sci (Lond) 2003.
23.Weinberg EO, Shimpo M, Hurwitz S, Tominaga S, Rouleau JL, Lee RT. Identification of serum soluble ST2 receptor as a novel heart failure biomarker. Circulation 2003; 107: 721-6.
24. Tang WH, Brennan ML, Philip K, Tong W, Mann S, Van Lente F, Hazen SL. Plasma myeloperoxidase levels in patients with chronic heart failure. Am J Cardiol 2006; 98: 796-9.
25. Stoiser B, Mortl D, Hulsmann M, Berger R, Struck J, Morgenthaler NG, Bergmann A, Pacher R. Copeptin, a fragment of the vasopressin precursor, as a novel predictor of outcome in heart failure. Eur J Clin Invest 2006; 36: 771-8.
26. Kempf T, Horn-Wichmann R, Brabant G, Peter T, Allhoff T, Klein G, Drexler H, Johnston N, Wallentin L, Wollert KC.Circulating concentrations of growth-differentiation factor 15 in apparently healthy elderly individuals and patients with chronic heart failure as assessed by a new immunoradiometric sandwich assay. Clin Chem 2007; 53: 284-91.
27. Iaccarino G, Barbato E, Cipolletta E,De Amicis V, Margulies KB, Leosco D, Trimarco B, Koch WJ. Elevated myocardial and lymphocyte GRK2 expression and activity in human heart failure. Eur Heart J 2005; 26: 1752-8.
28. Sharma UC, Pokharel S, van Brakel TJ, van Berlo JH, Cleutjens JP, Schroen B, Andre S, Crijns HJ, Gabius HJ, Maessen J, Pinto YM. Galectin-3 marks activated macrophages in failure-prone hypertrophied hearts and contributes to cardiac dysfunction. Circulation 2004; 110: 3121-8.
29. Liang F, O'Rear J, Schellenberger U, Tai L, Lasecki M, Schreiner GF, Apple FS, Maisel AS, Pollitt NS, Protter AA. Evidence for functional heterogeneity of circulating B-type natriuretic peptide. J Am Coll Cardiol 2007;49:1071-8.
30. Richards AM. The natriuretic peptides in heart failure. Basic Res Cardiol. 2004; 99: 94-100.
31. Murdoch DR, McDonagh TA, Byrne J, Blue L, Farmer R, Morton JJ, Dargie HJ. Titration of vasodilator therapy in chronic heart failure according to plasma brain natriuretic peptide concentration: randomized comparison of the hemodynamic and neuroendocrine effects of tailored versus empirical therapy. Am Heart J 1999; 138: 1126-32.
32. Brunner-La Rocca HP, Weilenmann D, Kiowski W, Maly FE, Candinas R, Follath F. Within-patient comparison of effects of different dosages of enalapril on functional capacity and neurohormone levels in patients with chronic heart failure. Am Heart J 1999; 138: 654-62.
33. Latini R, Masson S, Anand I, Judd D, Maggioni AP, Chiang YT, Bevilacqua M, Salio M, Cardano P, Dunselman PH, Holwerda NJ, Tognoni G, Cohn JN. Effects of valsartan on circulating brain natriuretic peptide and norepinephrine in symptomatic chronic heart failure: the Valsartan Heart Failure Trial (Val HeFT). Circulation. 2002; 106: 2454-8.
34. Tsutamoto T, Wada A, Maeda K, Mabuchi N, Hayashi M, Tsutsui T, Ohnishi M, Sawaki M, Fujii M, Matsumoto T, Matsui T, Kinoshita M. Effect of spironolactone on plasma brain natriuretic peptide and left ventricular remodeling in patients with congestive heart failure. J Am Coll Cardiol. 2001; 37: 1228-33.
35. Rousseau MF, Gurne O, Duprez D, Van Mieghem W, Robert A, Ahn S, Galanti L, Ketelslegers JM. Beneficial neurohormonal profile of spironolactone in severe congestive heart failure: results from the RALES neurohormonal substudy. J Am Coll Cardiol. 2002; 40: 1596-601.
36. Davis ME, Richards AM, Nicholls MG, Yandle TG, Frampton CM, Troughton RW. Introduction of metoprolol increases plasma B-type cardiac natriuretic peptides in mild, stable heart failure. Circulation. 2006; 113: 977-85.
37. Maisel AS. The diagnosis of acute congestive heart failure: role of BNP measurements. Heart Fail Rev. 2003; 8: 327-34.
38. Januzzi JL, van Kimmenade R, Lainchbury J, Bayes- Genis A, Ordonez-Llanos J, Santalo-Bel M, Pinto YM, Richards M. NTproBNP testing for diagnosis and short-term prognosis in acute destabilized heart failure: an international pooled analysis of 1256 patients: the International Collaborative of NT-proBNP Study. Eur Heart J 2006; 27: 330-7.
39. Redfield MM, Rodeheffer RJ, Jacobsen SJ, Mahoney DW, Bailey KR, Burnett JC, Jr. Plasma brain natriuretic peptide concentration: impact of age and gender. J Am Coll Cardiol. 2002; 40: 976-82.
40. Tetin SY, Ruan Q, Saldana SC, Pope MR, Chen Y, Wu H, Pinkus MS, Jiang J, Richardson PL. Interactions of two monoclonal antibodies with BNP: high resolution epitope mapping using fluorescence correlation spectroscopy. Biochemistry. 2006; 45: 14155-65.
41. Emdin M, Passino C, Del Ry S, Prontera C, Galetta F, Clerico A. Influence of gender on circulating cardiac natriuretic hormones in patients with heart failure. Clin Chem Lab Med 2003; 41: 686-92.
42. Loke I, Squire IB, Davies JE, Ng LL. Reference ranges for natriuretic peptides for diagnostic use are dependent on age, gender and heart rate. Eur J Heart Fail 2003; 5: 599-606.
43. McLean AS, Huang SJ, Nalos M, Tang B, Stewart DE. The confounding effects of age, gender, serum creatinine, and electrolyte concentrations on plasma B-type natriuretic peptide concentrations in critically ill patients. Crit Care Med 2003; 31: 2611-8.
44. McCullough PA, Duc P, Omland T, McCord J, Nowak RM, Hollander JE, Herrmann HC, Steg PG, Westheim A, Knudsen CW, Storrow AB, Abraham WT, Lamba S, Wu AH, Perez A, Clopton P, Krishnaswamy P, Kazanegra R, Maisel AS. B-type natriuretic peptide and renal function in the diagnosis of heart failure: an analysis from the Breathing Not Properly Multinational Study. Am J Kidney Dis 2003; 41: 571-9.
45. Vesely DL. Natriuretic peptides and acute renal failure. Am J Physiol Renal Physiol 2003; 285: F167 77.
46. McCollough PA, Kuncheria J, Mathur VS. Diagnostic and therapeutic utility of B-type natriuretic peptide in patients with renal insufficiency and decompensated heart failure. Rev Cardiovasc Med 2003; 4 Suppl 7: S3-S12.
47. Herrmann Z, Uhl W, Steinberg HW, Dworschack R. The influence of renal function on NT-proBNP levels in various disease groups. Clin Lab 2003; 49: 649-56.
48. Anwaruddin S, Lloyd-Jones DM, Baggish A, Chen A, Krauser D, Tung R, Chae C, Januzzi JL, Jr. Renal function, congestive heart failure, and amino-terminal probrain natriuretic peptide measurement: results from the ProBNP Investigation of Dyspnea in the Emergency Department (PRIDE) Study. J Am Coll Cardiol 2006; 47: 91-7.
49.Wang TJ, Larson MG, Levy D, Benjamin EJ, Leip EP, Wilson PW, Vasan RS. Impact of obesity on plasma natriuretic peptide levels. Circulation 2004; 109: 594-600.
50. Taylor JA, Christenson RH, Rao K, Jorge M, Gottlieb SS. Btype natriuretic peptide and N-terminal pro B-type natriuretic peptide are depressed in obesity despite higher left ventricular end diastolic pressures. Am Heart J 2006; 152: 1071-6.
51. Krauser DG, Lloyd-Jones DM, Chae CU, Cameron R, Anwaruddin S, Baggish AL, Chen A, Tung R, Januzzi JL, Jr. Effect of body mass index on natriuretic peptide levels in patients with acute congestive heart failure: a ProBNP Investigation of Dyspnea in the Emergency Department (PRIDE) substudy. Am Heart J 2005; 149: 744-50.
52. Schultz M, Faber J, Kistorp C, Jarlov A, Pedersen F, Wiinberg N, Hildebrandt P. N-terminal-pro-B-type natriuretic peptide (NT-pro-BNP) in different thyroid function states. Clin Endocrinol (Oxf) 2004; 60: 54-9.
53. Missouris CG, Grouzmann E, Buckley MG, Barron J, MacGregor GA, Singer DR. How does treatment influence endocrine mechanisms in acute severe heart failure? Effects on cardiac natriuretic peptides, the renin system, neuropeptide Y and catecholamines. Clin Sci (Lond) 1998; 94: 591-9.
54. Ralli S, Horwich TB, Fonarow GC. Relationship between anemia, cardiac troponin I, and B-type natriuretic peptide levels and mortality in patients with advanced heart failure. Am Heart J 2005; 150: 1220-7.
55. Chung T, Sindone A, Foo F, Dwyer A, Paoloni R, Janu MR, Wong H, Hall J, Freedman SB. Influence of history of heart failure on diagnostic performance and utility of B-type natriuretic peptide testing for acute dyspnea in the emergency department. Am Heart J 2006; 152: 949-55.
56. Albage A, Kenneback G, van der Linden J, Berglund H. Improved neurohormonal markers of ventricular function after restoring sinus rhythm by the Maze procedure. Ann Thorac Surg 2003; 75: 790-5.
57. Inoue S, Murakami Y, Sano K, Katoh H, Shimada T. Atrium as a source of brain natriuretic polypeptide in patients with atrial fibrillation. J Card Fail 2000; 6: 92-6.
58. Rossi A, Enriquez-Sarano M, Burnett JC, Jr., Lerman A, Abel MD, Seward JB. Natriuretic peptide levels in atrial fibrillation: a prospective hormonal and Doppler- echocardiographic study. J Am Coll Cardiol 2000; 35: 1256-62.
59. Tang WH, Girod JP, Lee MJ, Starling RC, Young JB, Van Lente F, Francis GS. Plasma B-type natriuretic peptide levels in ambulatory patients with established chronic symptomatic systolic heart failure. Circulation 2003; 108: 2964-6.
60. Troughton RW, Prior DL, Pereira JJ, Martin M, Fogarty A, Morehead A, Yandle TG, Richards AM, Starling RC, Young JB, Thomas JD, Klein AL. Plasma B-type natriuretic peptide levels in systolic heart failure: importance of left ventricular diastolic function and right ventricular systolic function. J Am Coll Cardiol 2004; 43: 416-422.
61. Lubien E, DeMaria A, Krishnaswamy P, Clopton P, Koon J, Kazanegra R, Gardetto N, Wanner E, Maisel AS. Utility of B-natriuretic peptide in detecting diastolic dysfunction: comparison with Doppler velocity recordings. Circulation 2002; 105: 595-601.
62.Maisel AS, McCord J, Nowak RM, Hollander JE, Wu AH, Duc P, Omland T, Storrow AB, Krishnaswamy P, Abraham WT, Clopton P, Steg G, Aumont MC, Westheim A, Knudsen CW, Perez A, Kamin R, Kazanegra R, Herrmann HC, McCullough PA. Bedside B-Type natriuretic peptide in the emergency diagnosis of heart failure with reduced or preserved ejection fraction. Results from the Breathing Not Properly Multinational Study. J Am Coll Cardiol 2003; 41: 2010-7.
63. Cheung BM. Plasma concentration of brain natriuretic peptide is related to diastolic function in hypertension. Clin Exp Pharmacol Physiol. 1997; 24: 966-8.
64. Masson S, Vago T, Baldi G, Salio M, De Angelis N, Nicolis E, Maggioni AP, Latini R, Norbiato G, Bevilacqua M.Comparative measurement of N-terminal pro-brain natriuretic peptide and brain natriuretic peptide in ambulatory patients with heart failure. Clin Chem Lab Med 2002; 40: 761-3.
65. Yeo KT, Wu AH, Apple FS, Kroll MH, Christenson RH, Lewandrowski KB, Sedor FA, Butch AW. Multicenter evaluation of the Roche NT-proBNP assay and comparison to the Biosite Triage BNP assay. Clin Chim Acta 2003; 338: 107-15.
66.Wu AH, Smith A, Wieczorek S, Mather JF, Duncan B, White CM, McGill C, Katten D, Heller G. Biological variation for N-terminal pro- and B-type natriuretic peptides and implications for therapeutic monitoring of patients with congestive heart failure. Am J Cardiol 2003; 92: 628-31.
67.Wang TJ, Larson MG, Levy D, Benjamin EJ, Corey D, Leip EP, Vasan RS. Heritability and genetic linkage of plasma natriuretic peptide levels. Circulation 2003; 108: 13-6.
68. Maisel AS, Krishnaswamy P, Nowak RM, McCord J, Hollander JE, Duc P, Omland T, Storrow AB, Abraham WT, Wu AH, Clopton P, Steg PG, Westheim A, Knudsen CW, Perez A, Kazanegra R, Herrmann HC, McCullough PA. Rapid measurement of B-type natriuretic peptide in the emergency diagnosis of heart failure. N Engl J Med 2002; 347: 161-7.
69.Wright SP, Doughty RN, Pearl A, Gamble GD, Whalley GA, Walsh HJ, Gordon G, Bagg W, Oxenham H, Yandle T, Richards M, Sharpe N. Plasma amino-terminal pro-brain natriuretic peptide and accuracy of heart-failure diagnosis in primary care: a randomized, controlled trial. J Am Coll Cardiol 2003; 42: 1793-800.
70. Januzzi JL, Jr., Camargo CA, Anwaruddin S, Baggish AL, Chen AA, Krauser DG, Tung R, Cameron R, Nagurney JT, Chae CU, Lloyd-Jones DM, Brown DF, Foran- Melanson S, Sluss PM, Lee-Lewandrowski E, Lewandrowski KB. The N-terminal Pro-BNP investigation of dyspnea in the emergency department (PRIDE) study. Am J Cardiol 2005; 95: 948-54.
71. Packer M. Should B-type natriuretic peptide be measured routinely to guide the diagnosis and management of chronic heart failure? Circulation 2003; 108: 2950-3.
72. Logeart D, Saudubray C, Beyne P, Thabut G, Ennezat PV, Chavelas C, Zanker C, Bouvier E, Solal AC. Comparative value of Doppler echocardiography and B-type natriuretic peptide assay in the etiologic diagnosis of acute dyspnea. J Am Coll Cardiol 2002; 40: 1794-800.
73. Coste J, Jourdain P, Pouchot J. A gray zone assigned to inconclusive results of quantitative diagnostic tests: application to the use of brain natriuretic Peptide for diagnosis of heart failure in acute dyspneic patients. Clin Chem 2006; 52: 2229-35.
74. Brenden CK, Hollander JE, Guss D, McCullough PA, Nowak R,Green G, Saltzberg M, Ellison SR, Bhalla MA, Bhalla V, Clopton P, Jesse R, Maisel AS. Gray zone BNP levels in heart failure patients in the emergency department: results from the Rapid Emergency Department Heart Failure Outpatient Trial (REDHOT) multicenter study. Am Heart J 2006; 151: 1006-11.
75. Berdague P, Caffin PY, Barazer I, Vergnes C, Sedighian S, Letrillard S, Pilossof R, Goutorbe F, Piot C, Reny JL. Use of Nterminal prohormone brain natriuretic peptide assay for etiologic diagnosis of acute dyspnea in elderly patients. Am Heart J 2006; 151: 690-8.
76. James KB, Troughton RW, Feldschuh J, Soltis D, Thomas D, Fouad-Tarazi F. Blood volume and brain natriuretic peptide in congestive heart failure: a pilot study. Am Heart J 2005; 150: 984.
77. O'Neill JO, Bott-Silverman CE, McRae AT, 3rd, Troughton RW,Ng K, Starling RC, Young JB. B-type natriuretic peptide levels are not a surrogate marker for invasive hemodynamics during management of patients with severe heart failure. Am Heart J 2005; 149: 363-9.
78. Dokainish H, Zoghbi WA, Lakkis NM, Al-Bakshy F, Dhir M, Quinones MA, Nagueh SF. Optimal noninvasive assessment of left ventricular filling pressures: a comparison of tissue Doppler echocardiography and B-type natriuretic peptide in patients with pulmonary artery catheters. Circulation 2004; 109: 2432-9.
79. Cioffi G, Tarantini L, Stefenelli C, Azzetti G, Marco R, Carlucci S, Furlanello F. Changes in plasma N-terminal proBNP levels and ventricular filling pressures during intensive unloading therapy in elderly with decompensated congestive heart failure and preserved left ventricular systolic function. J Card Fail 2006; 12: 608-15.
80. Le Jemtel TH, Padeletti M, Jelic S. Diagnostic and therapeutic challenges in patients with coexistent chronic obstructive pulmonary disease and chronic heart failure. J Am Coll Cardiol 2007; 49: 171-80.
81. Leya FS, Arab D, Joyal D, Shioura KM, Lewis BE, Steen LH, Cho L. The efficacy of brain natriuretic peptide levels in differentiating constrictive pericarditis from restrictive cardiomyopathy. J Am Coll Cardiol 2005; 45: 1900-2.
82. McKie PM, Rodeheffer RJ, Cataliotti A, Martin FL, Urban LH, Mahoney DW, Jacobsen SJ, Redfield MM Burnett JC, Jr. Amino-terminal pro-B-type natriuretic peptide and B-type natriuretic peptide: biomarkers for mortality in a large communitybased cohort free of heart failure. Hypertension 2006; 47: 874-80.
83. Karadag O, Calguneri M, Yavuz B, Atalar E, Akdogan A, Kalyoncu U, Kiraz S, Aksoyek S, Ozmen F, Ertenli AI. B-type natriuretic peptide (BNP) levels in female systemic lupus erythematosus patients: what is the clinical significance? Clin Rheumatol 2007.
84. Hogenhuis J, Voors AA, Jaarsma T, Hillege HL, Hoes AW, van Veldhuisen DJ. Low prevalence of B-type natriuretic peptide levels _ 100 pg/mL in patients with heart failure at hospital discharge. Am Heart J 2006; 151: 1012 e1-5.
85.Wang TJ, Larson MG, Levy D, Benjamin EJ, Leip EP, Omland T, Wolf PA, Vasan RS. Plasma natriuretic peptide levels and the risk of cardiovascular events and death. N Engl J Med 2004; 350: 655-63.
86. James SK, Lindahl B, Siegbahn A, Stridsberg M, Venge P, Armstrong P, Barnathan ES, Califf R, Topol EJ, Simoons ML, Wallentin L. N-terminal pro-brain natriuretic peptide and other risk markers for the separate prediction mortality and subsequent myocardial infarction in patients with unstable coronary artery disease: a Global Utilization of Strategies To Open occluded arteries (GUSTO)-IV substudy. Circulation 2003; 108: 275-81.
87. Richards AM, Nicholls MG, Espiner EA, Lainchbury JG, Troughton RW, Elliott J, Frampton C, Turner J, Crozier IG, Yandle TG. B-type natriuretic peptides and ejection fraction for prognosis after myocardial infarction. Circulation 2003; 107: 2786-92.
88. Omland T, Persson A, Ng L, O'Brien R, Karlsson T, Herlitz J,Hartford M, Caidahl K. N-terminal pro-B-type natriuretic peptide and long-term mortality in acute coronary syndromes. Circulation 2002; 106: 2913-8.
89. de Lemos JA, Morrow DA. Combining natriuretic peptides and necrosis markers in the assessment of acute coronary syndromes. Rev Cardiovasc Med 2003; 4 Suppl 4: S37-46.
90. Kragelund C, Gronning B, Kober L, Hildebrandt P, Steffensen R. N-terminal pro-B-type natriuretic peptide and long-term mortality in stable coronary heart disease. N Engl J Med 2005; 352: 666-75.
91. Poge U, Gerhardt TM, Woitas RP. N-terminal pro-B-type natriuretic peptide and mortality in coronary heart disease. N Engl J Med 2005; 352: 2025-6; author reply 2025-6.
92. Richards M, Nicholls MG, Espiner EA, Lainchbury JG, Troughton RW, Elliott J, Frampton CM, Crozier IG, Yandle TG, Doughty R, MacMahon S, Sharpe N. Comparison of B-type natriuretic peptides for assessment of cardiac function and prognosis in stable ischemic heart disease. J Am Coll Cardiol 2006; 47: 52-60.
93.Cheng V, Kazanagra R, Garcia A, Lenert L, Krishnaswamy P, Gardetto N, Clopton P, Maisel A. Arapid bedside test for B-type peptide predicts treatment outcomes in patients admitted for decompensated heart failure: a pilot study. J Am Coll Cardiol 2001; 37: 386-91.
94. Januzzi JL, Jr., Sakhuja R, O'Donoghue M, Baggish AL, Anwaruddin S, Chae CU, Cameron R, Krauser DG, Tung R, Camargo CA, Jr., Lloyd-Jones DM. Utility of aminoterminal pro-brain natriuretic peptide testing for prediction of 1-year mortality in patients with dyspnea treated in the emergency department. Arch Intern Med 2006; 166: 315-20.
95. Anand IS, Fisher LD, Chiang YT, Latini R, Masson S, Maggioni AP, Glazer RD, Tognoni G, Cohn JN. Changes in brain natriuretic peptide and norepinephrine over time and mortality and morbidity in the Valsartan Heart Failure Trial (Val-HeFT). Circulation 2003; 107: 1278-83.
96. Pruszczyk P, Kostrubiec M, Bochowicz A, Styczynski G, Szulc M, Kurzyna M, Fijalkowska A, Kuch-Wocial A, Chlewicka I,Torbicki A. N-terminal pro-brain natriuretic peptide in patients with acute pulmonary embolism. Eur Respir J 2003; 22: 649-53.
97. Kruger S, Graf J, Merx MW, Koch KC, Kunz D, Hanrath P, Janssens U. Brain natriuretic peptide predicts right heart failure in patients with acute pulmonary embolism. Am Heart J 2004; 147: 60-5.
98. Blankenberg S, McQueen MJ, Smieja M, Pogue J, Balion C, Lonn E, Rupprecht HJ, Bickel C, Tiret L, Cambien F, Gerstein H, Munzel T, Yusuf S. Comparative impact of multiple biomarkers and N-Terminal pro-brain natriuretic peptide in the context of conventional risk factors for the prediction of recurrent cardiovascular events in the Heart Outcomes Prevention Evaluation (HOPE) Study. Circulation 2006; 114: 201-8.
99. Gardner RS, Ozalp F, Murday AJ, Robb SD, McDonagh TA. Nterminal pro-brain natriuretic peptide. A new gold standard in predicting mortality in patients with advanced heart failure. Eur Heart J 2003; 24: 1735-43.
100. Koglin J, Pehlivanli S, Schwaiblmair M, Vogeser M, Cremer P, Von Scheidt W. Clinical value of brain natriuretic peptide for candidate selection before cardiac transplantation. J Heart Lung Transplant 2001; 20: 164.
101. Verma A, Kilicaslan F, Martin DO, Minor S, Starling R, Marrouche NF, Almahammed S, Wazni OM, Duggal S, Zuzek R, Yamaji H, Cummings J, Chung MK, Tchou PJ, Natale A.Preimplantation B-type natriuretic peptide concentration is an independent predictor of future appropriate implantable defibrillator therapies. Heart 2006; 92: 190-5.
102. Pitzalis MV, Iacoviello M, Di Serio F, Romito R, Guida P, De Tommasi E, Luzzi G, Anaclerio M, Varraso L, Forleo C, Pansini N. Prognostic value of brain natriuretic peptide in the management of patients receiving cardiac resynchronization therapy. Eur J Heart Fail 2006; 8: 509-14.
103. Yu CM, Fung JW, Zhang Q, Chan CK, Chan I, Chan YS, Kong SL, Sanderson JE, Lam CW. Improvement of serum NTProBNP predicts improvement in cardiac function and favorable prognosis after cardiac resynchronization therapy for heart failure. J Card Fail 2005; 11: S42-6.
104. Sinha AM, Filzmaier K, Breithardt OA, Kunz D, Graf J, Markus KU, Hanrath P, Stellbrink C. Usefulness of brain natriuretic peptide release as a surrogate marker of the efficacy of long-term cardiac resynchronization therapy in patients with heart failure. Am J Cardiol 2003; 91: 755-8.
105. Berger R, Huelsman M, Strecker K, Bojic A, Moser P, Stanek B, Pacher R. B-type natriuretic peptide predicts sudden death in patients with chronic heart failure. Circulation 2002; 105: 2392-7.
106. Koglin J, Pehlivanli S, Schwaiblmair M, Vogeser M, Cremer P, vonScheidt W. Role of brain natriuretic peptide in risk stratification of patients with congestive heart failure. J Am Coll Cardiol 2001; 38: 1934-41.
107. van Kimmenade RR, Januzzi JL, Jr., Baggish AL, Lainchbury JG, Bayes-Genis A, Richards AM, Pinto YM. Amino-terminal pro-brain natriuretic Peptide, renal function, and outcomes in acute heart failure: redefining the cardiorenal interaction? J Am Coll Cardiol 2006; 48: 1621-7.
108. van Kimmenade RR, Pinto YM, Bayes-Genis A, Lainchbury JG, Richards AM, Januzzi JL, Jr. Usefulness of intermediate aminoterminal pro-brain natriuretic peptide concentrations for diagnosis and prognosis of acute heart failure. Am J Cardiol 2006; 98: 386-90.
109. Drazner MH, de Lemos JA. Unexpected BNP levels in patients with advanced heart failure: a tale of caution and promise. Am Heart J 2005; 149: 187-9.
110. Perna ER, Macin SM, Canella JP, Augier N, Stival JL, Cialzeta JR, Pitzus AE, Garcia EH, Obregon R, Brizuela M, Barbagelata A. Ongoing myocardial injury in stable severe heart failure: value of cardiac troponin T monitoring for high-risk patient identification. Circulation 2004; 110: 2376-82.
111. Macin SM, Perna ER, Cimbaro Canella JP, Augier N, Riera Stival JL, Cialzeta J, Pitzus AE, Obregon R, Garcia E, Medina F, Badaracco RJ. Increased levels of cardiac troponin-T in outpatients with heart failure and preserved systolic function are related to adverse clinical findings and outcome. Coron Artery Dis 2006; 17: 685-91.
112. Perna ER, Macin SM, Cimbaro Canella JP, Alvarenga PM, Rios NG, Pantich R, Augier N, Farias EF, Jantus E, Brizuela M, Medina F. Minor myocardial damage detected by troponin T is a powerful predictor of long-term prognosis in patients with acute decompensated heart failure. Int J Cardiol 2005; 99: 253-61.
113. You JJ, Austin PC, Alter DA, Ko DT, Tu JV. Relation between cardiac troponin I and mortality in acute decompensated heart failure. Am Heart J 2007; 153: 462-70.
114. Stanton EB, Hansen MS, Sole MJ, Gawad Y, Packer M, Pitt B, Swedberg K, Rouleau JL. Cardiac troponin I, a possible predictor of survival in patients with stable congestive heart failure.Can J Cardiol 2005; 21: 39-43.
115. Taniguchi R, Sato Y, Nishio Y, Kimura T, Kita T. Measurements of baseline and follow-up concentrations of cardiac troponin-T and brain natriuretic peptide in patients with heart failure from various etiologies. Heart Vessels 2006; 21: 344-9.
116. Goldberg LR, Jessup M. Stage B heart failure: management of asymptomatic left ventricular systolic dysfunction. Circulation 2006; 113: 2851-60.
117. Bibbins-Domingo K, Gupta R, Na B, Wu AH, Schiller NB, Whooley MA. N-terminal fragment of the prohormone brain type natriuretic peptide (NT-proBNP), cardiovascular events,and mortality in patients with stable coronary heart disease. JAMA 2007; 297: 169-76.
118. Vasan RS, Benjamin EJ, Larson MG, Leip EP, Wang TJ, Wilson PW, Levy D. Plasma natriuretic peptides for community screening for left ventricular hypertrophy and systolic dysfunction: the Framingham heart study. JAMA 2002; 288: 1252-9.
119. Nakamura M, Tanaka F, Yonezawa S, Satou K, Nagano M,Hiramori K. The limited value of plasma B-type natriuretic peptide for screening for left ventricular hypertrophy among hypertensive patients. Am J Hypertens 2003; 16: 1025-9.
120. Luchner A, Burnett JC, Jr., Jougasaki M, Hense HW, Heid IM,Muders F, Riegger GA, Schunkert H. Evaluation of brain natriuretic peptide as marker of left ventricular dysfunction and hypertrophy in the population. J Hypertens 2000; 18: 1121-8.
121. Costello-Boerrigter LC, Boerrigter G, Redfield MM, Rodeheffer RJ, Urban LH, Mahoney DW, Jacobsen SJ, Heublein DM, Burnett JC, Jr. Amino-terminal pro-B-type natriuretic peptide and B-type peptide in the general community: determinants and detection of left ventricular dysfunction. J Am Coll Cardiol 2006; 47: 345-53.
122. Ng LL, Pathik B, Loke IW, Squire IB, Davies JE.Myeloperoxidase and C-reactive protein augment the specificity of B-type natriuretic peptide in community screening for systolic heart failure. Am Heart J 2006; 152: 94-101.
123. Jeyaseelan S, Goudie BM, Pringle SD, Donnan PT, Sullivan FM, Struthers AD. A critical re-appraisal of different ways of selecting ambulatory patients with suspected heart failure for echocardiography. Eur J Heart Fail 2007; 9: 55-61.
124. Nielsen OW, McDonagh TA, Robb SD, Dargie HJ. Retrospective analysis of the cost-effectiveness of using plasma brain natriuretic peptide in screening for left ventricular systolic dysfunction in the general population. J Am Coll Cardiol 2003; 41: 113-20.
125. Epshteyn V, Morrison K, Krishnaswamy P, Kazanegra R,Clopton P, Mudaliar S, Edelman S, Henry R, Maisel A. Utility of B-type natriuretic peptide (BNP) as a screen for left ventricular dysfunction in patients with diabetes. Diabetes Care 2003; 26: 2081-7.
126. Silver MA, Pisano C. High incidence of elevated B-type natriuretic peptide levels and risk factors for heart failure in an unselected at-risk population (stage A): implications for heart failure screening programs. Congest Heart Fail 2003; 9: 127-32.
127. Tang WH, Steinhubl SR,Van Lente F, Brennan D, McErlean E,Maroo A, Francis GS, Topol EJ. Risk stratification for patients undergoing nonurgent percutaneous coronary intervention using N-terminal pro-B-type natriuretic peptide: a Clopidogrel for the Reduction of Events During Observation (CREDO) substudy. Am Heart J 2007; 153 36-41.
128. Groenning BA, Raymond I, Hildebrandt PR, Nilsson JC, Baumann M, Pedersen F. Diagnostic and prognostic evaluation of left ventricular systolic heart failure by plasma N-terminal pro-brain natriuretic peptide concentrations in a large sample of the general population. Heart 2004; 90: 297-303.
129. Alehagen U, Lindstedt G, Eriksson H, Dahlstrom U. Utility of the amino-terminal fragment of pro-brain natriuretic peptide in plasma for the evaluation of cardiac dysfunction in elderly patients in primary health care. Clin Chem 2003; 49: 1337-46.
130. Hutcheon SD, Gillespie ND, Struthers AD, McMurdo ME. Btype natriuretic peptide in the diagnosis of cardiac disease in elderly day hospital patients. Age Ageing 2002; 31: 295-301.
131. Richards AM, Crozier IG, Yandle TG, Espiner EA, Ikram H,Nicholls MG. Brain natriuretic factor: regional plasma concentrations and correlations with haemodynamic state in cardiac disease. Br Heart J 1993; 69: 414-7.
132. Kazanegra R, Cheng V, Garcia A, Krishnaswamy P, Gardetto N,Clopton P, Maisel A. A rapid test for B-type natriuretic peptide correlates with falling wedge pressures in patients treated for decompensated heart failure: a pilot study. J Card Fail 2001; 7: 21-9.
133. Johnson W, Omland T, Hall C, Lucas C, Myking OL, Collins C,Pfeffer M, Rouleau JL, Stevenson LW. Neurohormonal activation rapidly decreases after intravenous therapy with diuretics and vasodilators for class IV heart failure. J Am Coll Cardiol 2002; 39: 1623-9.
134. Lee SC, Stevens TL, Sandberg SM, Heublein DM, Nelson SM,Jougasaki M, Redfield MM, Burnett JC, Jr. The potential of brain natriuretic peptide as a biomarker for New York Heart Association class during the treatment of heart failure.J Card Fail 2002; 8: 149-54.
135. Schou M, Gustafsson F, Nielsen PH, Madsen LH, Kjaer A,Hildebrandt PR. Unexplained week-to-week variation in BNP and NT-proBNP is low in chronic heart failure patients during steady state. Eur J Heart Fail 2007; 9: 68-74.
136. Wu AH. Serial testing of B-type natriuretic peptide and NTpro-BNP for monitoring therapy of heart failure: the role of biologic variation in the interpretation of results. Am Heart J 2006; 152: 828-34.
137. O'Hanlon R, O'Shea P, Ledwidge M, O'Loughlin C, Lange S,Conlon C, Phelan D, Cunningham S, McDonald K. The biologic variability of B-type natriuretic peptide and N-terminal pro-B-type natriuretic peptide in stable heart failure patients. J Card Fail 2007; 13: 50-5.
138. Lindahl B, Lindback J, Jernberg T, Johnston N, Stridsberg M,Venge P, Wallentin L. Serial analyses of N-terminal pro-B-type natriuretic peptide in patients with non-ST-segment elevation acute coronary syndromes: a Fragmin and fast Revascularisation during In Stability in Coronary artery disease (FRISC)-II substudy. J Am Coll Cardiol 2005; 45: 533-41.
139. Morrow DA, de Lemos JA, Blazing MA, Sabatine MS, Murphy SA, Jarolim P, White HD, Fox KA, Califf RM, Braunwald E.Prognostic value of serial B-type natriuretic peptide testing during follow-up of patients with unstable coronary artery disease. JAMA 2005; 294: 2866-71.
140. Troughton RW, Frampton CM, Yandle TG, Espiner EA, Nicholls MG, Richards AM. Treatment of heart failure guided by plasma aminoterminal brain natriuretic peptide (N-BNP) concentrations. Lancet 2000; 355: 1126-30.
141. Jourdain P, Jondeau G, Funck F, Gueffet P, Le Helloco A, Donal E, Aupetit JF, Aumont MCG, M., Eicher JC, Cohen-Solal A, Juillière Y. Plasma Brain Natriuretic Peptide-Guided Therapy to Improve Outcome in Heart Failure: The STARS-BNP Multicenter Study. J Am Coll Cardiol 2007; 49: 1733-9.
142. Shah MR, Claise KA, Bowers MT, Bhapkar M, Little J, Nohria A, Gaulden LH, McKee VK, Cozart KL, Mancinelli KL,Daniels H, Kinard T, Stevenson LW, Mancini DM, O'Connor CM, Califf RM. Testing new targets of therapy in advanced heart failure: the design and rationale of the Strategies for Tailoring Advanced Heart Failure Regimens in the Outpatient Setting: BRain NatrIuretic Peptide Versus the Clinical CongesTion ScorE (STARBRITE) trial. Am Heart J 2005; 150: 893-8.
143. Beck-da-Silva L, de Bold A, Fraser M, Williams K, Haddad H.BNP-guided therapy not better than expert's clinical assessment for beta-blocker titration in patients with heart failure. Congest Heart Fail 2005; 11: 248- 53; quiz 254-5.
144. O'Brien RJ, Squire IB, Demme B, Davies JE, Ng LL. Pre-discharge,but not admission, levels of NT-proBNP predict adverse prognosis following acute LVF. Eur J Heart Fail 2003; 5: 499-506.
145. Melzi d'Eril G, Tagnochetti T, Nauti A, Klersy C, Papalia A,Vadacca G, Moratti R, Merlini G. Biological variation of N-terminal pro-brain natriuretic peptide in healthy individuals. Clin Chem 2003; 49: 1554-5.
146. McGeoch G, Lainchbury J, Town GI, Toop L, Espiner E,Richards AM. Plasma brain natriuretic peptide after long-term treatment for heart failure in general practice. Eur J Heart Fail 2002; 4: 479-83.
147. Lainchbury JG, Troughton RW, Frampton CM, Yandle TG,Hamid A, Nicholls MG, Richards AM. NTproBNP-guided drug treatment for chronic heart failure: design and methods in the"BATTLESCARRED" trial. Eur J Heart Fail 2006; 8: 532-8.
148. Brunner-La Rocca HP, Buser PT, Schindler R, Bernheim A,Rickenbacher P, Pfisterer M. Management of elderly patients with congestive heart failure-design of the Trial of Intensified versus standard Medical therapy in Elderly patients with Congestive Heart Failure (TIME-CHF). Am Heart J 2006; 151: 949-55.