CARDIOLOGÍA INTERVENCIONISTA
Resultados hospitalarios y factores asociados con morbimortalidad del Registro Argentino de Angioplastia Coronaria (RAdAC)
Primary Outcomes and Morbi-mortality Associated Factors in the Coronary Angioplasty Argentine Registry - RAdAC
Alejandro CherroMTSAC, Carlos Fernández PereiraMTSAC, Ernesto Torresani?, Daniel O. Mauro?, Carlos A. InginoMTSAC, José A. G. ÁlvarezMTSAC, Raúl A. BorracciMTSAC *, Jorge G. Allin, Miguel A. MiceliMTSAC, Ricardo A. SarmientoMTSAC, en representación del grupo RAdAC
Consejo de Hemodinamia y Cardiología Intervencionista de la Sociedad Argentina de Cardiología (SAC), Federación Argentina de Cardiología (FAC),
Colegio Argentino de Cardioangiólogos Intervencionistas (CACI) y Consejo Nacional de Residentes de Cardiología (CONAREC)
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
? Para optar a Miembro Titular de la Sociedad Argentina de Cardiología
*Bioestadística, Ciencias Biomédicas, Universidad Austral, Argentina.
Recibido: 21/01/2012
Aceptado: 03/07/2012
Dirección para separatas
Dr. Daniel O. Mauro Avda. Acoyte 930 - Piso 4° B Buenos Aires, Argentina Tel. +54 11 5409-9727 e-mail: dmauro@intramed.net
Declaración de conflicto de intereses
Los autores no tienen conflicto de intereses que declarar.
RESUMEN
Introducción En el Registro CONAREC V, de 1996, se recopilaron los resultados obtenidos con angioplastia
transluminal coronaria (ATC) y posteriormente, durante 2005, se recabaron datos con similar
metodología generándose el Registro CONAREC XIV. Desde entonces no se cuenta con
datos nacionales generales en relación con la revascularización coronaria percutánea, por lo
que la Sociedad Argentina de Cardiología, en conjunto con el CACI, la FAC y el CONAREC,
implementó el Registro Argentino de Angioplastia Coronaria (RAdAC).
Objetivo Evaluar a escala nacional los resultados intrahospitalarios y la morbimortalidad de pacientes
sometidos a ATC según los distintos escenarios clínicos.
Material y métodos En un período de 7 meses se incluyeron 1.905 pacientes en forma prospectiva y consecutiva
en 67 centros de la Argentina. Se analizaron factores de riesgo, antecedentes cardiovasculares
y cuadro clínico. La ATC se consideró programada, de urgencia y de emergencia, y se estimó
el número de vasos enfermos y la intención de vasos a tratar y la cantidad y tipo de stents [convencionales (SC) y liberadores de droga (SLD)]. Se analizó el empleo de aterectomía,
Cutting Balloon®, tromboaspiración, ultrasonido intravascular (IVUS), antiagregantes y balón
de contrapulsación intraaórtico (BCIA). El éxito angiográfico se definió como lesión residual
< 20% y flujo normal (TIMI 3).
Resultados La edad promedio fue de 63,8 años. Un total de 752 pacientes (39,5%) presentaban infarto
agudo de miocardio (IAM) y 834 pacientes (43,8%) angina inestable (AI). Se utilizó acceso
femoral en el 92,8% de los casos. El 44,3% de las intervenciones fueron programadas, el
37,8%, de urgencia y el 17,9%, de emergencia. Se implantaron 2.753 stents (1,4 por paciente)
con 33,2% de SLD. El éxito primario fue del 97% y la mortalidad global observada, del 1,6%;
la asociada con infarto ascendió al 3,2% (con ST 4,3%, sin ST 1,7%), la de AI fue del 0,8%
y la de angina crónica estable, del 0,3%. Las variables asociadas con el óbito fueron shock
cardiogénico, necesidad de BCIA, Killip y Kimball 3-4, ATC de emergencia, ATC del tronco,
mala función ventricular, insuficiencia renal o diabetes, mayor número de vasos enfermos,
mayor edad y fracaso de la ATC.
Conclusiones En nuestro medio, la mayoría de las ATC se realizan en síndromes coronarios agudos y casi
exclusivamente por vía femoral, con éxito primario comparable a datos internacionales pero
con menor utilización de SLD. El empleo de Rotablator®, Cutting Balloon®, tromboaspiración,
IVUS y BCIA fue más bajo que el esperado, mientras que la edad, el shock cardiogénico, la
emergencia y la ATC fallida resultaron factores asociados con mayor morbimortalidad.
Palabras clave: Infarto del miocardio; Angina inestable; Angioplastia; Stents; Factores de riesgo; Mortalidad.
ABSTRACT
Primary Outcomes and Morbi-mortality Associated Factors in the Coronary Angioplasty Argentine Registry - RAdAC
Background Percutaneous transluminal coronary angioplasty (PTCA)
outcomes were compiled in the 1996 V CONAREC Registry,
and in 2005, data collection was repeated using a similar
methodology, giving rise to the XIV CONAREC Registry. As
no general national PTCA results have been reported since,
the Argentine Society of Cardiology, together with CACI,
FAC and CONAREC carried out the Coronary Angioplasty
Argentine Registry (RAdAC).
Objective The aim of this Registry was to evaluate intrahospital
outcome and morbi-mortality of patients submitted to PTCA
according to different clinical scenarios.
Methods One thousand nine hundred and five patients were prospectively
and consecutively included in 67 centers of Argentina
during a 7-month period. Cardiovascular risk factors and clinical
history were analyzed. PTCA procedures were classified
as: planned, urgent or emergent and the number of affected
and intended-to-treat vessels, as well as the number and
type of stents implanted [bare metal (BMS) or drug-eluting
stents (DES)] were estimated. Use of atherectomy, Cutting
Balloon?, thrombus aspiration, intravascular ultrasound
(IVUS), antiplatelet drugs and intra-aortic balloon pump
(IABP) was analyzed. Angiographic success was defined as
residual lesion <20% and normal flow (TIMI 3).
Results Mean age was 63.8 years. A total of 752 patients (39.5%)
presented with acute myocardial infarction (AMI) and 834
patients (43.8%) with unstable angina (UA). Femoral access
was used in 92.8% of the cases. Overall, 44.3% of the interventions
were planned, 37.8% were urgent and 17.9% emergent.
A total of 2753 stents were implanted (1.4 per patient), 33.2%
of which were DES. The primary success rate was 97% and
overall mortality 1.6%: 3.2% associated to AMI, (4.3% STEMI
and 1.7% non-STEMI), 0.8% to UA and 0.3% to chronic stable
angina. Death-associated variables were: cardiogenic shock,
need of IAPB, Killip-Kimball class 3-4, emergency PTCA, left
main PTCA, ventricular function impairment, renal failure or
diabetes, number of affected vessels, age and PTCA failure.
Conclusions In our setting, most PTCAs are performed in acute coronary
syndromes, almost exclusively by femoral access, with primary
success comparable to that of international reports, but
employing less DES. Use of Rotablator?, Cutting Balloon?,
thrombus aspiration, IVUS and IABP implementation was
lower than expected, while age, cardiogenic shock, emergency
and PTCA failure were factors associated with increased
morbi-mortality.
Key words: Myocardial Infarction; Unstable angina; Angioplasty; Stents; Risk Factors; Mortality.
ACE Angor crónico estable
IAM Infarto agudo de miocardio
ACV Accidente cerebrovascular
IC Insuficiencia cardíaca
AI Angina inestable
IR Insuficiencia renal
ATC Angioplastia transluminal coronaria
IVUS Ultrasonido intravascular
BCIA Balón de contrapulsación intraaórtico
KK Clase funcional de Killip y Kimball
CACI Colegio Argentino de Cardioangiólogos
RAdAC Registro Argentino de Angioplastia
Intervencionistas Coronaria
CONAREC Consejo Nacional de Residentes de Cardiología
SAC Sociedad Argentina de Cardiología
CRM Cirugía de revascularización miocárdica
SC Stent convencional
EPOC Enfermedad pulmonar obstructiva crónica
SCA Síndrome coronario agudo
FAC Consejo de Hemodinamia de la Federación
SLD Stent liberador de droga
INTRODUCCIÓN
La intervención coronaria percutánea fue introducida
por Grüentzig en 1978. (1) La experiencia en el procedimiento
y los avances tecnológicos han permitido
notables mejoras en los resultados, posibilitando el tratamiento
de lesiones más complejas y con mayor riesgo
anatómico. (2, 3) Estudios aleatorizados y controlados
mostraron que los stents liberadores de drogas (SLD)
comparados con los convencionales (SC) presentan una
reducción significativa de la reestenosis, (4, 5) lo que
permitió ampliar aún más las indicaciones.
En 1996, el Consejo Nacional de Residentes de
Cardiología realizó el Registro CONAREC V, (6) en el
que se recopilaron los resultados obtenidos con angioplastia
coronaria durante 6 meses en 1.295 pacientes
consecutivos en centros con residencia de cardiología;
se concluyó que el éxito y la morbimortalidad eran
comparables a lo observado en la bibliografía. Posteriormente,
durante el año 2005, con similar metodología
se recabaron los datos de 1.500 pacientes, generándose
el Registro CONAREC XIV. (7)
Desde entonces no contamos con datos nacionales
generales en relación con la revascularización coronaria
percutánea. Por tal motivo, el Consejo de Hemodinamia
y Cardiología Intervencionista "Dr. Isaac Berconsky"
de la Sociedad Argentina de Cardiología (SAC), en
conjunto con el Colegio Argentino de Cardioangiólogos
Intervencionistas (CACI), el Consejo de Hemodinamia
de la Federación Argentina de Cardiología (FAC) y
el Consejo Nacional de Residentes de Cardiología
(CONAREC), implementó el Registro Argentino de
Angioplastia Coronaria (RAdAC).
El objetivo fue recabar información relacionada
con la revascularización percutánea en nuestro país,
haciendo hincapié en las características de la población,
los resultados intrahospitalarios, la modalidad de revascularización
(tronco, bifurcación, múltiples vasos,
etc.) tipos de stents utilizados y los factores asociados
con morbimortalidad.
MATERIAL Y MÉTODOS
En mayo de 2010 se invitó a participar vía e-mail y/o telefónica
a 146 Servicios de Cardiología Intervencionista acreditados
por el CACI, a lo que respondió un total de 67 centros (45%)
(véase Apéndice).
Se confeccionó una base de datos a completarse por Internet.
La inclusión de cada paciente fue realizada por cada
uno de los investigadores de los centros participantes y la
información volcada fue confidencial.
Se incluyeron en forma prospectiva y consecutiva pacientes
con enfermedad coronaria aguda o crónica, mayores
de 21 años, tratados mediante angioplastia coronaria y que
prestaran su consentimiento informado por escrito para
participar en el registro. Dicho consentimiento fue revisado
y aprobado previamente por el Comité de Ética de la SAC.
Se consignaron los siguientes factores de riesgo coronario:
hipertensión arterial, diabetes, tabaquismo, extabaquismo,
antecedentes familiares de coronariopatía, hipercolesterolemia
y obesidad-sobrepeso.
Los antecedentes clínicos evaluados fueron: cirugía de
revascularización miocárdica (CRM) o ATC previas, insuficiencia
cardíaca (IC) y su clase funcional, insuficiencia renal
(IR), vasculopatía periférica, infarto agudo de miocardio
(IAM), accidente cerebrovascular (ACV) y enfermedad pulmonar
obstructiva crónica (EPOC).
Para un mejor análisis, los procedimientos de ATC se
dividieron en: a) programado, realizado en forma electiva, b) de urgencia, realizado dentro de las 24 horas del diagnóstico
clínico de un síndrome coronario agudo (SCA) y c) de emergencia,
realizado en el menor tiempo posible ante un cuadro
de IAM o de angina inestable (AI) de alto riesgo.
La forma de presentación clínica se consideró según
lo habitual como: angor crónico estable (ACE), AI o IAM
supra-ST, infra-ST o indeterminado según correspondiera,
consignándose la clase funcional (Killip y Kimball -KK-)
en cada caso y el shock cardiogénico cuando estuviera
presente.
Las pruebas funcionales fueron relevadas como realizadas
o no.
La troponina y la CK-MB se consignaron
como no realizadas, positivas o negativas. La creatinina
plasmática se expresó en mg/dl. La función del ventrículo
izquierdo se consignó como no evaluada, normal, leve,
moderada o grave.
En el informe angiográfico se hizo constar: a) la dominancia,
b) los segmentos proximal, medio y distal con obstrucciones
= 70% correspondientes a los vasos principales (coronaria
derecha, descendente anterior y circunfleja), c) obstrucciones
= 70% en ramas secundarias = 2 mm de coronaria derecha o
circunfleja (descendente posterior y posteroventricular), de
descendente anterior (primera diagonal y segunda diagonal)
o de circunfleja (primera y segunda lateroventricular), d)
obstrucciones = 70% en puentes venosos y/o mamarios y e)
obstrucción = 50% en el tronco de la coronaria izquierda, distribución por sexo y los antecedentes clínicos se
resumen en la Tabla 1. El tipo de angina al ingreso, el
resultado de las pruebas funcionales para isquemia y la
premura de la intervención se muestran en la Tabla 2.
El 84,9% de las intervenciones se realizaron en el
contexto de AI o IAM.
Si bien es motivo de otra publicación, adicionalmente
se analizaron los resultados del infarto por separado.
La mortalidad global del IAM fue del 3,1%, 4,3%
con ST y 1,7% sin ST.
consignándose además el/los segmento/s comprometidos
(proximal, medio y distal). La reestenosis intrastent también
se señaló cuando comprometía la luz del vaso en un 70% o
más. En todos los segmentos antes mencionados se consignó
si fueron tratados o no.
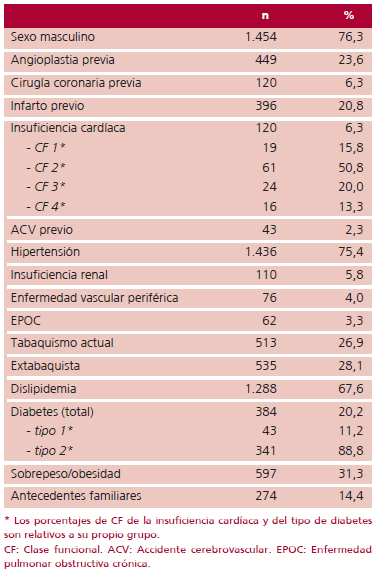
Tabla 1. Características de la población (n = 1.905)

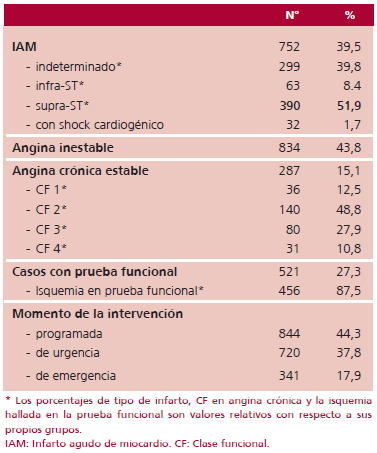
Tabla 2. Características clínicas al ingreso (n = 1.905)
Se cuantificó la cantidad de vasos coronarios enfermos por
paciente y también la cantidad de vasos enfermos en el total de
la población. Se consideró enfermedad en uno, dos o tres vasos
en base a la presencia de obstrucciones = 70% en la coronaria
derecha, la descendente anterior y/o la circunfleja y de más de
tres vasos cuando además hubiera obstrucción en al menos
una rama diagonal (de la descendente anterior), lateral (de la
circunfleja), descendente posterior o posteroventricular (de la
coronaria derecha o la circunfleja) con diámetro = 2 mm. Con
igual sistemática se consignó la intención de tratamiento. En
esta etapa se calculó y se consignó el puntaje SYNTAX. (8) La relación de vasos enfermos por paciente correspondió al
cociente entre el número total de vasos enfermos y la cantidad
total de pacientes, mientras que la relación de angioplastia
o stenting por paciente correspondió a los cocientes entre el
número total de angioplastias o stents usados y la cantidad
total de pacientes.
Se analizó el número de vasos enfermos y vasos tratados
por paciente durante la misma internación. Los que sólo recibieron
tratamiento de un vaso a pesar de presentar lesiones
múltiples se adicionaron a los pacientes con lesión de un solo
vaso para el cálculo de porcentajes.
Se realizó un relevamiento del número y el tipo de stents utilizados por paciente según fueran convencionales o liberadores
de droga y también de la cantidad total de stents en
la población general. Debido a las diferentes características
de los SLD en cuanto a su estructura metálica, polímero,
droga, biodisponibilidad, etc., se hizo consignar el nombre
comercial de cada uno.
Con respecto al empleo de clopidogrel y prasugrel, de
uso habitual en estos procedimientos, se consignaron las
dosis de carga y de mantenimiento para cada una de las
drogas
.
En relación con los aspectos técnicos del procedimiento, se
consideraron: a) la vía de abordaje (radial, humeral o femoral),
b) el uso de inhibidores IIb/IIIa (sí /no), c) la necesidad de
balón de contrapulsación (sí/no), d) el empleo de IVUS (sí/no),
e) la preparación de placa con Cutting Balloon® o Rotablator®
(sí/no) y f) y la tromboaspiración (sí/no).
Se consideró éxito angiográfico la obtención de una lesión
residual < 20% con flujo normal (tipo TIMI 3).
Análisis estadístico
Las variables categóricas se expresaron como valores absolutos,
porcentajes y relaciones, mientras que las cuantitativas,
como media y desviación estándar y, eventualmente,
con sus máximos, mínimos y rangos. La normalidad de las
variables métricas se comprobó con la prueba de bondad
de ajuste de K-S. La comparación estadística entre variables
cualitativas se realizó con la prueba de chi cuadrado
ajustada o no por Yates o con la prueba de probabilidad
exacta de Fisher, según correspondiera. Por su parte, las
variables cuantitativas se compararon con la prueba de la
t de Student bajo los supuestos de normalidad e igualdad
de varianzas. En estos casos, el valor significativo de p
se estableció en 0,05 para pruebas de dos colas. Para el
análisis multivariado de regresión logística se incorporaron
todas las variables que en el análisis univariado
tuvieron una significación estadística igual o menor de
0,05. Se usó el método condicional forward stepwise y se
ajustó el modelo en base a la reducción del valor del logaritmo
de la verosimilitud (-2 log likelihood). Se realizó
una primera regresión con 1.905 pacientes, excluyendo las variables clase de KK y función ventricular, ya que el
registro contenía datos ausentes de estas variables. Una
segunda regresión con 366 pacientes incluyó también
estas dos últimas.
Para los cálculos se utilizó el paquete estadístico SPSS
para Windows versión 11.5® (SPSS Inc., Chicago, Ill, USA).
RESULTADOS
Los resultados que se informan corresponden a 1.905
pacientes intervenidos entre el 1 de mayo de 2010 y el
30 de noviembre de 2010.
La edad promedio fue de 63,8 años (DE, 11,07; rango,
64, mínimo: 28, máximo: 92, distribución normal).
La distribución por sexo y los antecedentes clínicos se
resumen en la Tabla 1. El tipo de angina al ingreso, el
resultado de las pruebas funcionales para isquemia y la
premura de la intervención se muestran en la Tabla 2.
El 84,9% de las intervenciones se realizaron en el
contexto de AI o IAM.
Si bien es motivo de otra publicación, adicionalmente
se analizaron los resultados del infarto por separado.
La mortalidad global del IAM fue del 3,1%, 4,3%
con ST y 1,7% sin ST.
El análisis univariado de las variables asociadas
con mortalidad en la ATC del IAM fueron: existencia
de shock cardiogénico al ingreso (OR: 44,5), necesidad
de balón de contrapulsación intraaórtico (BCIA) (OR:
25,9), clase de KK 3-4 (OR: 18,7), ATC del tronco (OR:
11,4), IR (OR: 3,84), IAM con supra-ST (OR: 2,87),
deterioro moderado a grave de la función ventricular
izquierda (OR: 2,78), diabetes mellitus (OR: 2,64), mayor
número de vasos enfermos del paciente, condición
de éxito o no (OR: 35,7).
En el análisis multivariado, las variables asociadas
fueron el uso de BCIA (OR: 9,57), la tromboaspiración
(OR: 5,17) y el shock (OR: 41,6).
En la Tabla 3 se resumen los datos de la clase KK,
de la función ventricular izquierda y de los marcadores
bioquímicos al ingreso de aquellos de los que fueron
informados los valores.
Tabla 3. Clase de Killip y Kimball, función ventricular izquierda y
marcadores bioquímicos al ingreso

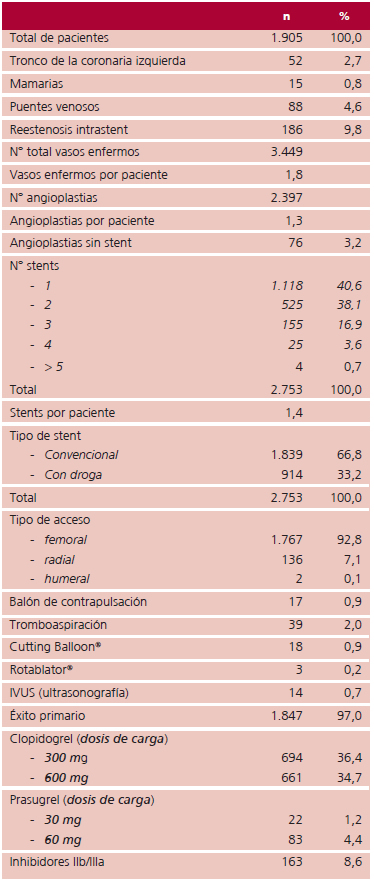
En la Tabla 4 se presenta el análisis descriptivo de los procedimientos realizados, el número de vasos tratados, la utilización y el tipo de stent, los accesos vasculares y procedimientos asociados y el uso de antiplaquetarios.
Tabla 4. Análisis descriptivo de los procedimientos realizados
Por su parte, los porcentajes de empleo de clopidogrel/
prasugrel corresponden a la indicación de dosis
de carga previa a la angioplastia, mientras que el porcentaje
que no recibió carga correspondió a pacientes
que ya estaban bajo tratamiento antiagregante previo.
La relación entre el número de vasos enfermos y
vasos tratados durante la internación se muestra en
la Figura 1. Los porcentajes asociados indican que al
57,7% de quienes tenían lesión de dos vasos les fueron
tratados los dos vasos, y así sucesivamente para el
resto de los porcentajes. Del total de vasos tratados,
el 45% correspondió a la descendente anterior, el 27%
a la coronaria derecha, el 21% a la circunfleja y el 7%
restante, al tronco o ramas diagonales.
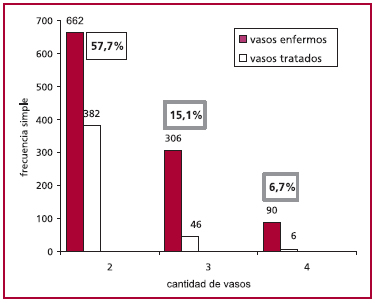
Fig. 1. Relación entre el número de vasos enfermos y vasos tratados
durante la internación. Los porcentajes asociados indican que al
57,7% de quienes tenían lesión de dos vasos les fueron tratados
los dos vasos, y así sucesivamente para el resto de los porcentajes.
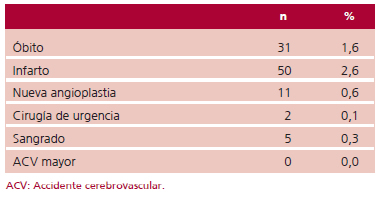
En la Tabla 5 se detallan los resultados hospitalarios en términos de mortalidad global y complicaciones mayores. Si bien la mortalidad global fue del 1,6%, la asociada con el infarto ascendió al 3,2%, mientras que en la AI fue del 0,8% y en la ACE, del 0,3%.
Tabla 5. Mortalidad y complicaciones mayores hospitalarias
El análisis univariado de factores asociados con la mortalidad hospitalaria se muestra en la Tabla 6.
Tabla 6. Análisis univariado de factores asociados con mortalidad hospitalaria de la angioplastia

Las variables asociadas con óbito por orden de peso
de acuerdo con los OR fueron: la existencia de shock
cardiogénico al ingreso, la necesidad de BCIA, la clase
KK 3-4, el tratamiento de emergencia, la presencia de
insuficiencia cardíaca, la angioplastia del tronco, la
necesidad de tromboaspiración, el deterioro moderado
a grave de la función ventricular izquierda, la presencia
de IR o de diabetes, el mayor número de vasos enfermos
por paciente, la mayor edad y la condición de éxito o no.
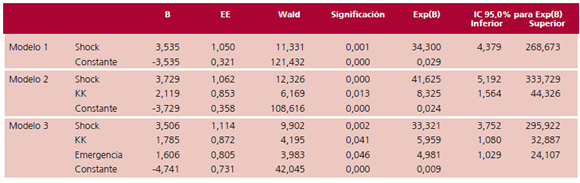
En la Tabla 7 se muestra paso a paso el análisis
multivariado de los factores asociados con mortalidad
hospitalaria de la angioplastia. Este análisis de regresión
logística incluyó todas las variables que en el análisis
univariado tuvieron una significación estadística
igual o menor de 0,05 y a la vez excluyó las siguientes
combinaciones de posibles variables confundidoras:
KK 4 con shock, KK 4 con contrapulsación aórtica y
KK 4 con insuficiencia cardíaca. El mejor modelo que
redujo el valor del -2 log likelihood e incrementó los
coeficientes de determinación fue el que incluyó el
shock, la clase KK y la emergencia.
Tabla 7. Análisis multivariado de los factores asociados con mortalidad hospitalaria de la angioplastia. Resumen de los coeficientes de los
tres modelos sucesivos
DISCUSIÓN
Este Registro Argentino de Angioplastia Coronaria
(RAdAC) se realizó en forma prospectiva durante 7 meses de 2010 e incluyó un número mayor de centros
de hemodinamia que los registros anteriores realizados
en nuestro país. Se logró además una muestra amplia
y representativa de la realidad local al convocar a las
principales entidades científicas que nuclean la especialidad
a nivel nacional.
A diferencia de los registros CONAREC V (6) y
CONAREC XIV, (7) en el RAdAC se incluyeron centros
con y sin residencia en cardiología. Los factores de
riesgo de mayor prevalencia resultaron la hipertensión
arterial y la dislipidemia y tres de cada cuatro pacientes
fueron hombres, coincidiendo con lo observado en los
dos registros mencionados.
Respecto del Registro CONAREC XIV, (7) en el
RAdAC fue mayor el número de angioplastias en pacientes
con síndromes isquémicos agudos, mientras
que la cantidad de pacientes con enfermedad de dos
y tres vasos (55,5%) y la proporción de IAM supra-ST
resultó similar a la de ese registro.
En cuanto a datos de otros países, los resultados
globales observados en el RAdAC son comparables a
los de los registros ACC-NCDR (The American College
of Cardiology-National Cardiovascular Data Registry),
NHLBI Dynamic Registry (The National Heart, Lung,
and Blood Institute Registries), (9) RENAC (Registro
Nacional de Angioplastia de Chile) (10) y el Registro
Español de Hemodinámica y Cardiología Intervencionista.
(11)
Del universo total de pacientes del RAdAC, solamente
el 22,7% fue tratado con angioplastia de dos o tres vasos. Observando este dato con más detalle,
vemos que en aquellos con enfermedad de dos vasos,
el 57,7% recibió tratamiento de ambos, mientras que
sólo el 15,1% de los pacientes con enfermedad de tres
vasos recibieron una revascularización completa.
Consideramos que estos datos corresponden a que la
revascularización mediante ATC en la enfermedad de
múltiples vasos muchas veces es incompleta debido a
lesiones no tratables (oclusiones totales, vasos pequeños
o ausencia de lechos distales) o simplemente por
criterio clínico. Lo observado en el RAdAC coincide
con la evidencia del Euro Heart Survey-PCI Registry
sobre ATC de múltiples vasos en 4.400 pacientes con
SCA sin compromiso hemodinámico. (12) Este trabajo demostró que no hubo diferencias en mortalidad
intrahospitalaria entre la ATC de múltiples vasos y la
ATC al vaso responsable, pero sí una tasa mayor de
IAM no mortal periprocedimiento (8,8% vs. 1,8%) en
la intervención múltiple. En un interesante trabajo de
Bauer y colaboradores sobre este mismo registro (13) se
compararon resultados de la ATC del vaso responsable
versus ATC de múltiples vasos en pacientes con shock
cardiogénico y tampoco demostró beneficios a favor
de la intervención múltiple, concluyendo que sólo se
emplea en la cuarta parte de los pacientes con shock y
que la ATC adicional al vaso no culpable no se asoció
con beneficios en la sobrevida.
En el RAdAC observamos un uso global de stents (94,7%) similar al del Registro CONAREC XIV, con
un aumento de la utilización de stents farmacoactivos:
33,2% vs. 18,67%, respectivamente. Si bien es evidente
un aumento en el empleo de este tipo de stents, la proporción
resulta claramente inferior a la utilizada en
los Estados Unidos y en Europa, donde actualmente
supera el 85-90%. La proporción de SLD utilizados en
el RAdAC recuerda el promedio (32%) observado en el
registro europeo del año 2006. (14) En nuestro registro,
la proporción de SLD utilizados (33,2%) apenas supera
la suma de pacientes diabéticos (20,2%) y aquellos con
reestenosis intrastent (9,8%), lo cual no debería sorprender,
ya que éstas son las principales indicaciones
aceptadas por las financiadoras de salud, generalmente
basadas en el Programa Médico Obligatorio del Ministerio
de Salud de la Nación. (15)
Llama la atención la escasa utilización de sistemas
de tromboaspiración, Cutting Balloon®, aterectomía
rotacional y de IVUS. Las razones que pueden ensayarse
para esto son varias, pero se presume que principalmente
se debe al incremento en la complejidad y
la duración del procedimiento y a que el costo de los
dispositivos no siempre es soportado por el sistema de
cobertura de salud en nuestro medio, lo que limita su
empleo.
Encontramos un 0,9% de empleo global de BCIA, en
comparación con el 1,7% de ATC en shock cardiogénico.
Sin duda, la utilización del BCIA no escapa de las
consideraciones previas sobre el empleo de sistemas de
tromboaspiración y preparación de placa. No obstante
esto, si observamos datos recientes del registro NCDR
(Estados Unidos) sobre 18.990 ATC con BCIA, (16) veremos en el análisis multivariado que la mortalidad
intrahospitalaria cercana al 5% no varió entre los cuartiles
de uso de BCIA por hospital (comprendían desde el
0% al 40% de empleo), sin haberse comprobado mejor
evolución de los pacientes tratados en hospitales con
mayor uso de BCIA respecto de aquellos en los que se
empleó mucho menos. Esto apoyaría la utilización no
sistemática de este dispositivo de asistencia circulatoria
mecánica. También en concordancia, el registro Euro
Heart Survey on PCI, (17) que involucró a 33 países,
informó un empleo del BCIA de sólo el 25% durante la
ATC en IAM con shock cardiogénico, sin que el empleo
del balón se asociara con mejoría en la sobrevida.
La técnica radial aumentó levemente con respecto a
registros previos, pero aún sigue siendo poco utilizada,
salvo en algunos centros donde su empleo resulta más
sistemático.
El éxito primario fue alto, 97%, y la utilización de
antiagregantes como clopidogrel o prasugrel en dosis de
carga fue menor que la esperada. Es probable que esto
corresponda a la población con angina estable que llegó
a la angioplastia con tratamiento antiagregante previo.
El empleo de inhibidores IIb/IIIa resultó escaso
comparativamente con la cantidad de síndromes isquémicos
agudos. Es posible que esto también corresponda
a una cuestión de costos, como ya fuera mencionado.
Los estudios funcionales para determinar isquemia
se hicieron en un porcentaje bajo de pacientes, y mayormente
fueron realizados en quienes presentaron
angina estable o infarto indeterminado.
La mortalidad observada en el IAM (3,2%) es menor
que la comunicada en el Registro CONAREC XIV (8%)
y que la observada en la Encuesta SAC 2005 en el IAM
(9,6%). Es probable que estas diferencias se deban a una
selección previa de los pacientes a quienes se les realizó
ATC primaria. En este sentido, el Swedish Coronary
Angiography and Angioplasty Registry (SCAAR), (18) sobre 3.284 pacientes, demostró una mortalidad a los
7 días del 3,5% cuando la arteria responsable del IAM
se encontraba cerrada (dos tercios de los pacientes) y
del 1,2% cuando el vaso se encontraba permeable; esto
coincidió con el uso previo de hipolipemiantes, pretratamiento
con heparina e inhibidores IIb/IIIa y edad
menor de 80 años. Esta caracterización angiográfica
no se tuvo en cuenta en el RAdAC.
La edad, el shock cardiogénico, la angioplastia de
emergencia y el procedimiento no exitoso se asociaron
significativamente con mayor mortalidad. Estos datos
son similares a lo observado por Chuntao Wu y colaboradores,
(19) quienes mediante un modelo de regresión
logística sobre 46.090 angioplastias realizadas (año
2002) en 41 hospitales del estado de New York pudieron
determinar 9 variables predictoras de mortalidad
intrahospitalaria, y entre ellas los dos factores de riesgo
asociados con un riesgo muy alto de muerte fueron el
shock (OR 19,92, IC 95% 11,92% a 33,30%) y el IAM
dentro de las 24 horas pre-ATC con trombosis del stent (OR 18,75, IC 95% 7,27% a 48,37%). En el RAdAC,
a estas variables se agregan la ATC del tronco de la
coronaria izquierda (práctica no frecuente en el año
2002) y el fracaso de la ATC.
El registro Percutaneous Coronary Intervention
in Europe in 2006, (14) publicado en mayo de 2010,
se realizó sobre 1.001.000 ATC en 23 países. El 70%
fueron realizadas ad hoc. La enfermedad de múltiples
vasos fue tratada en una sola sesión en el 15%, el 18%
fueron IAM y el número de stent/angioplastia fue de
0,85. La tasa promedio de SLD fue del 32%, con gran
disparidad entre países (Italia 88%, Bulgaria 1%). El
uso del BCIA osciló entre el 0% y el 8,7%, con un promedio
cercano al 1%. Algo similar ocurrió con el empleo
del IVUS (1,2% promedio), donde llamativamente en 15 países, incluido el Reino Unido, fue igual o inferior
al 1%. La mortalidad global observada alcanzó el 0,4%.
En líneas generales, estos números coinciden con lo
observado en el RAdAC, con excepción del porcentaje
de IAM tratados, que en nuestro medio se duplica.
Si observamos datos de registros de otros países
en desarrollo, Malasia publicó en 2011 un registro
nacional de 3 años, (20) con 11.498 angioplastias
realizadas en 10.602 pacientes, llamativamente con
edad promedio baja, de 57 años, y alta incidencia de
diabéticos (50%) y de IR (47%). No obstante ello, el éxito
primario resultó idéntico al de nuestro registro (97%) y
su mortalidad global fue del 1%. Lamentablemente, no
menciona la proporción de procedimientos de urgencia,
pero establece que esta condición, la mayor clase KK y
la edad avanzada fueron los factores de peor pronóstico.
Limitaciones
A pesar de la protocolización, como en todo registro, los
datos son aproximados. Las fuentes de error potencial
incluyen la pérdida de validación externa de los datos
crudos provistos por las diversas instituciones y el hecho
de no ser aún representativo del universo total de
angioplastias de nuestro país. No obstante, se procuró
asegurar el registro más preciso de datos, vinculando a
todas las sociedades científicas y para este primer corte
del RAdAC se reunió un número significativo de casos.
Consideramos como aporte principal del RAdAC el
brindar información actualizada sobre el tratamiento
con angioplastia en nuestro medio, con la inclusión de
un número mayor de centros con y sin residencia en
cardiología, a diferencia de los registros anteriores.
CONCLUSIONES
Respecto de registros anteriores, se observa un aumento de ATC en SCA con elevada tasa de éxito primario y baja mortalidad, más aún en procedimientos programados. La vía femoral resulta sin duda la más utilizada y el empleo de dispositivos para preparación de placa, tromboaspiración, IVUS y BCIA es más bajo que el esperado. La proporción de stents farmacológicos sigue en aumento, si bien es muy inferior a la de países del primer mundo. Los análisis univariado y multivariado confirman la edad, el shock cardiogénico, la ATC fallida y la emergencia como los factores asociados con morbimortalidad.
APÉNDICE
Centros asistenciales y médicos participantes agrupados por provincias
BUENOS AIRES, Clínica Constituyentes de Morón (Dr. Miguel Micelli, Dr. Antonio Scuteri, Dr. Martín Swistun),
Clínica de las Mercedes (Dr. Daniel Mauro), Clínica IMA de
Adrogué (Dr. Carlos Fernández Pereyra, Dr. Gastón Rodríguez Granillo), Clínica La Pequeña Familia (Dr. José M. Magni, Dr. Fernando Genna), Clínica San Nicolás (Dr. Roberto Fernández Viña, Dr. Oberdan Andrin), Hospital Carrillo (Dr. Miguel Micelli, Dr. Antonio Scuteri, Dr. Rodrigo Martín), Hospital El
Cruce (Dr. Ricardo Sarmiento, Dr. Raúl Solernó, Dra. Ángeles Videla Lynch), Hospital Gral. de Agudos Gral. San Martín de
La Plata (Dra. María C. Bayón, Dr. Marcelo Ventre, Dr. Diego Ríos), HIGA San José de Pergamino (Dr. Antonio Scuteri),
Hospital Italiano Regional Sur de Bahía Blanca (Dr. Carlos Álvarez Iorio, Dr. Alejandro Álvarez, Dr. Pablo García Pacho),
Hospital Privado del Sur de Bahía Blanca (Dr. Carlos Álvarez Iorio, Dr. Pablo García Pacho), Hospital Privado Ntra. Sra. de
la Merced (Dr. Marcelo Ruda Vega, Dr. Juan Álvarez Sevillano),
Hospital Pte. Perón de Avellaneda (Dr. Marcelo Cetera), Hospital
Regional Español (Dr. Carlos Álvarez Iorio, Dr. Fernando Ordóñez, Dr. Pablo García Pacho), Instituto Cardiovascular
Juncal (Dr. Carlos Gadda Thompson), Instituto Médico Agüero
(Dr. Miguel Micelli, Dr. Antonio Scuteri, Dr. Martín Swistun),
Instituto Médico Central de Ituzaingó (Dr. Alejandro Cherro, Dr. Raúl Solernó), Sanatorio del Pilar (Dr. Alejandro García Escudero), Sanatorio Modelo Quilmes (Dr. Ernesto M. Torresani, Dr. Guillermo R. Martino, Dr. Alejandro F. Moguilner).
CHACO, Cordis Instituto del Corazón (Dr. Manuel Sanjurjo, Dr. Oscar R.Codutti).
CIUDAD AUTÓNOMA DE BUENOS AIRES, CEMIC
Instituto de Investigaciones (Dr. Jorge N. Wisner, Dr. Marcel G. Voos Budal Arrins), Hospital Naval de Buenos Aires (Dr. Rubén Kevorkian), Clínica Adventista de Belgrano (Dr. Alejandro Cherro, Dr. Ernesto M. Torresani), Clínica Bazterrica
(Dr. Jorge H. Leguizamón, Dr. Gustavo J. Schipani), Clínica
del Sol (Dr. Juan M. Ponce, Dr. Víctor Bernardi), Clínica y
Maternidad Suizo Argentina (Dr. Juan R. Alderete, Dr. Luis M. De La Fuente), Hospital Alemán (Dr. José A. Álvarez, Dr. Jorge G. Allín), Hospital Británico (Dr. José A. Álvarez, Dr. Jorge G. Allín), Hospital Carlos G. Durand (Dra. Gloria Mohamed, Dr. César Lopardo, Dra. Sandra S. Zymerman),
Hospital Churruca (Dr. Álvaro Bordenave, Dr. Sebastián Rizzone, Dr. Sergio Zolorsa), Hospital Español (Dr. Miguel Micelli, Dr. Antonio Scuteri, Dr. Martín Swistun), Hospital
Santojanni (Dra. María Carolina Etcheverry), Hospital UAI
(Dr. Juan J. Fernández, Dr. Juan F. Arellano), Instituto Sacre
Coeur (Dr. Marcelo G. Pettinari, Dra. Amalia Descalzo),
Policlínico Bancario (Dr. Daniel Omar Mauro), Policlínico
del Docente OSPLAD (Dr. Jorge D. Entrerríos, Dr. Germán Cafaro), Clínica La Sagrada Familia (Dr. Alejandro Cherro, Dr. Marcelo Halac), Sanatorio de La Trinidad Palermo (Dr. Alejandro Palacios, Dr. Juan F. Arellano, Dra. María D. Coria),
Sanatorio Franchín (Dr. Jorge H. Leguizamón, Dr. Gustavo Andersen), Sanatorio Mater Dei (Dr. Juan J. Fernández, Dr. Juan F. Arellano, Dra. María D. Coria), Sanatorio Otamendi (Dr. Alfredo Rodríguez, Dr. Gastón Rodríguez Granillo, Dra. Bibiana Rubilar), Sanatorio Santa Isabel (Dr. Jorge H. Leguizamón, Dr. Alejandro A. Fernández).
CÓRDOBA, Sanatorio Allende (Dr. Hugo Londero, Dr. Francisco Paoletti, Dra. María J. Cabrera Ferreyra), Unidad
Cardiológica de Río Cuarto (Dr. Rubén Montiel Cocco, Dr. Mauro Paulino).
ENTRE RÍOS, Centro Médico San Lucas (Dr. Marcelo F. Menéndez), Cooperativa Médica Ltda. (Dr. Marcelo F. Menéndez),
Hospital Justo José de Urquiza (Dr. Marcelo F. Menéndez),
Sanatorio La Entrerriana (Dr. Oscar Birollo, Dr. Víctor Moles).
FORMOSA, Hospital de Alta Complejidad Juan D.
Perón (Dr. Alejandro Ramiro Costello, Dr. Aldo Rodríguez Saavedra).
LA PAMPA, Clínica Modelo de Sta. Rosa (Dr. Fernando Nadal, Dr. Leonardo Novaretto), Sanatorio Santa Rosa (Dr. Fernando Nadal).
LA RIOJA, Hospital Regional Dr. Enrique Vera Barros
(Dr. Juan C. Olmos, Dr. Roberto R. Vázquez).
MENDOZA, Clínica de Cuyo (Dr. Miguel A. Larribau),
Hospital Español de Mendoza (Dr. Miguel A. Larribau), Sociedad
Española de Socorros Mutuos (Dr. Gustavo Carosella, Dr. Gustavo Irusta).
MISIONES, Centro Integral de Cardiología IOT (Dr. Elías Eserequis, Dr. Raúl Roman).
RÍO NEGRO, Clínica Pasteur (Dr. Ricardo L. Moreno, Dr. Pablo Ferrari), Instituto Cardiovascular del Sur (Dr. Pedro L. Urdiales, Dr. José Pereyra), Instituto Cardiovascular Juan
XXIII (Dr. Luis M. Flores, Dr. Diego Lavaggi).
SALTA, Hospital Privado Tres Cerritos (Dr. Miguel A. Farah).
SAN LUIS, Instituto Cardiovascular Villa Mercedes (Dr. Alfredo D. Bravo).
SANTA FE, Clínica de Nefrología y Enfermedades
Cardiológicas (Dr. Oscar Birollo, Dr. Víctor Moles), Sanatorio
Garay (Dr. José H. Vicario, Dr. Juan P. Berduc, Dr. Matías Dallo, Dr. Luis Gerardo, Dra. Milagros Capellutto),
Sanatorio Plaza (Dr. Rubén Piraino, Dr. Cristian Calenta),
Sanatorio Rosendo García (Dr. Diego Kirschmann, Dr. Emanuel Luchesi), Sanatorio San Gerónimo (Dr. Oscar Birollo, Dr. Víctor Moles).
TIERRA DEL FUEGO, Sanatorio San Jorge (Dr. Marcelo J. Cardone).
TUCUMÁN, Centro Privado de Cardiología (Dr. Pedro Gallardo Galeas, Dr. Ricardo M. Falú), Instituto de Cardiología
de Tucumán (Dr. Federico Barbaglia).
Agradecimiento
A la Sra. Teresita Peiper, Secretaria de Consejos de la Sociedad Argentina de Cardiología por su esfuerzo y dedicación en la organización y la comunicación con los investigadores.
1. Gruntzig A. Transluminal dilatation of coronary-artery stenosis. Lancet 1978;1:263.
2. Bittl JA. Advances in coronary angioplasty. N Engl J Med 1996;335:1290-302. http://doi.org/dxc4h6
3. Serruys PW, Kutryk MJ, Ong AT. Coronary-artery stents. N Engl J Med 2006;354:483-95. http://doi.org/dpb8cd
4. Stettler C, Wandel S, Allemann S, Kastrati A, Morice MC, Schömig A, et al. Outcomes associated with drug-eluting and bare-metal stents: a collaborative network meta-analysis. Lancet 2007;370:937-48. http://doi.org/bwztfn
5. Stone GW, Moses JW, Ellis SG, Schofer J, Dawkins KD, Morice MC, et al. Safety and efficacy of sirolimus and paclitaxel-eluting coronary stents. N Engl J Med 2007;356:998-1008. http://doi.org/bbzpcx
6. Baratta SJ, Ferroni F, Ho-Bang J, Gonzalez S, Mameluco G, Paredes FA y col, por investigadores CONAREC. CONAREC V. Encuesta sobre ATC coronaria en la República Argentina. Resultados generales. Fase intrahospitalaria. Rev Argent Cardiol 1998;66:43-53.
7. Linetzky B, Sarmiento R, Barceló J, Bayol P, Descalzo M, Rodríguez A y col. Angioplastia coronaria en centros con residencia de cardiología en la Argentina. Estudio CONAREC XIV - Área de Investigación de la SAC. Rev Argent Cardiol 2007;75:249-56.
8. Sianos G, Morel MA, Kappetein AP, Morice MC, Colombo A, Dawkins K, et al. The SYNTAX Score: an angiographic tool grading the complexity of coronary artery disease. EuroIntervention 2005;1:219-27.
9. Shaw RE, Anderson HV, Brindis RG, Krone RJ, Klein LW, McKay CR, et al. Development of a risk adjustment mortality model using the American College of Cardiology-National Cardiovascular Data Registry (ACC-NCDR) experience: 1998-2000. J Am Coll Cardiol 2002;39:1104-12. http://doi.org/frjrgp
10. Dussaliant G, Marchant E, Donoso H, Aninat M, Opazo M, Delgado J y col. Práctica contemporánea de ATC coronaria en Chile. Informe final del Registro Nacional de Angioplastia Coronaria (RENAC) 2001- 2002. Rev Med Chile 2004;132:913-22.
11. Hernández JM, Goicolea J, Durán JM, Augé JM. Spanish Registry on Cardiac Catheterization Interventions. 11th official report of the Working Group on Cardiac Catheterization and Interventional Cardiology of the Spanish Society of Cardiology (years 1990-2001). Rev Esp Cardiol 2002;55:1173-84.
12. Bauer T, Zeymer U, Hochadel M, Möllmann H, Weidinger F, Zahn R, et al. Prima-vista multi-vessel percutaneous coronary intervention in haemodynamically stable patients with acute coronary syndromes: Analysis of over 4.400 patients in the EHS-PCI registry. Int J Cardiol (in press) http://doi.org/fx7crf
13. Bauer T, Zeymer U, Hochadel M, Möllmann H, Weidinger F, Zahn R, et al. Use and outcomes of multivessel percutaneous coronary intervention in patients with acute myocardial infarction complicated by cardiogenic shock (from the EHS-PCI Registry). Am J Cardiol 2012;109:941-6. http://doi.org/fzd3vh
14. Moschovitis A, Cook S, Meier B. Percutaneous coronary interventions in Europe in 2006. EuroIntervention 2010;6:189-94. http://doi.org/b75wwm
15. Resolución 201/2002 del Ministerio de Salud Pública - Boletín Oficial de la República Argentina N° 29881 del 19 de abril de 2002.
16. Curtis JP, Rathore SS, Wang Y, Chen J, Nallamothu BK, Krumholz HM. Use and effectiveness of intra-aortic balloon pumps among patients undergoing high risk percutaneous coronary intervention: insights from the National Cardiovascular Data Registry. Circ Cardiovasc Qual Outcomes 2012;5:21-30. http://doi.org/fct5zm
17. Zeymer U, Bauer T, Hamm C, Zahn R, Weidinger F, Seabra-Gomes R, et al. Use and impact of intra-aortic balloon pump on mortality in patients with acute myocardial infarction complicated by cardiogenic shock: results of the Euro Heart Survey on PCI. EuroIntervention 2011;7:437-41. http://doi.org/bwwn6h
18. Kreutzer M, Magnuson A, Lagerqvist B, Fröbert O. Patent coronary artery and myocardial infarction in the era of primary angioplasty: assessment of an old problem in a new setting with data from the Swedish Coronary Angiography and Angioplasty Registry (SCAAR). EuroIntervention 2010;6:590-5. http://doi.org/dxb7ht1
19. Wu C, Hannan EL, Walford G, Ambrose JA, Holmes DR Jr, King SB 3rd, et al. A risk score to predict in-hospital mortality for percutaneous coronary interventions. J Am Coll Cardiol 2006;47:654-60. http://doi.org/bt2xsr
20. Ahmad WA, Ali RM, Khanom M, Han CK, Bang LH, Yip AF, et al. The journey of Malaysian NCVD-PCI (National Cardiovascular Disease Database-Percutaneous Coronary Intervention) Registry: A summary of three years report. Int J Cardiol 2011. http://doi.org/fwvpdb Epub ahead of print