
ENFERMEDAD DE CHAGAS
Hallazgos ergométricos en pacientes chagásicos, asintomáticos, con electrocardiograma normal y sin cardiopatía evidenciable
Ergometric Findings in Asymptomatic Chagasic Patients, With Normal ECG and Without Evident Heart Disease
Norma Crudo, Juan GagliardiMTSAC, Alfredo PiomboMTSAC, José L. Castellano, Miguel A. RiccitelliMTSAC
División Cardiología, Hospital General de Agudos "Dr. Cosme Argerich". Buenos Aires, Argentina
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
Para optar a Miembro Titular de la Sociedad Argentina de Cardiología
Recibido: 01/06/2012
Aceptado: 16/07/2012
Dirección para separatas
Dr. Juan Gagliardi Av. Alte. Brown 240 - 2.° Piso (C1155ADP) Buenos Aires, Argentina Tel.-Fax: 011 4121-0873 e-mail: jgagliardi@fibertel.com.ar
Declaración de conflicto de intereses
Los autores no tienen conflicto de intereses que declarar.
RESUMEN
Introducción Entre las manifestaciones más precoces de la enfermedad de Chagas se encuentran la disautonomía
y la dispersión de los intervalos QT en el electrocardiograma, que han demostrado ser
predictores de mayor morbimortalidad. Las nuevas tecnologías diagnósticas que posibilitan
el hallazgo temprano de alteraciones endoteliales o disautonómicas deben originar mejores
estrategias de diagnóstico y tratamiento que permitan la detección precoz de pacientes con
riesgo de evolucionar a la miocardiopatía chagásica crónica o de sufrir muerte súbita.
Objetivos 1) Investigar los signos clínicos, electrocardiográficos y ergométricos de pacientes chagásicos
asintomáticos, con electrocardiograma normal y sin patología clínica evidenciable. 2) Comparar
los datos que presentan durante la prueba ergométrica graduada estos pacientes chagásicos con
los de un grupo de características clínicas similares pero con serología negativa para Chagas.
Material y métodos Estudio observacional, retrospectivo, en el que se incluyeron 74 pacientes chagásicos y 28
sujetos sanos en los que se efectuó una ergometría por control clínico entre marzo de 2009
y septiembre de 2011.
Resultados Los pacientes chagásicos presentaron más a menudo frecuencia cardíaca basal = 60 lpm
(27,0% vs. 7,1%; p = 0,02), menor frecuencia cardíaca máxima (129,5 ± 22,8 lpm vs. 145,2 ±
16,5 lpm; p = 0,002), mayor incompetencia cronotrópica con frecuencia máxima < 80% que
la preestablecida (47,3% vs. 14,3%; p = 0,001) y mayor frecuencia de arritmia ventricular
durante el ejercicio y la recuperación (25,7% vs. 0%; p = 0,003).
Durante el ejercicio, mientras que en los pacientes del grupo control el intervalo QTc se acortó
normalmente, en la mayoría de los pacientes del grupo Chagas se prolongó en forma notoria
(grupo Chagas: 412,1 a 432,8 mseg, p = 0,0005; grupo control: 412,4 a 385,8 mseg, p < 0,0001).
Conclusiones Los pacientes chagásicos asintomáticos sin cardiopatía demostrable presentaron durante la
ergometría una alta prevalencia de signos de disautonomía, como la incompetencia cronotrópica
y la prolongación del intervalo QTc durante el esfuerzo. La prueba ergométrica graduada
es un método de diagnóstico incruento, confiable y de relativo bajo costo que puede contribuir
al diagnóstico temprano de las alteraciones disautonómicas y de la repolarización ventricular
y así identificar a los pacientes chagásicos con mayor riesgo de muerte súbita arritmogénica.
Palabras clave Enfermedad de Chagas; Electrocardiografía; Disautonomías primarias; Intervalo QT; Prueba de esfuerzo.
ABSTRACT
Ergometric Findings in Asymptomatic Chagasic Patients, With Normal ECG and Without Evident Heart Disease Background
Dysautonomia and QT interval dispersion are one of the
earliest manifestations of Chagas disease which have proved
to be predictors of increased morbi-mortality. New diagnostic
technologies revealing earlier endothelial or dysautonomic
disorders should provide better diagnostic and treatment
strategies for the premature detection of patients with risk of
developing chronic chagasic cardiomyopathy or sudden death.
Objectives The aims of this study were:
1) To investigate clinical, electrocardiographic and ergometric
characteristics in asymptomatic chagasic patients
with normal electrocardiogram and no clinical evidence of
the pathology. 2) To compare graded exercise testing results
between chagasic patients and subjects with similar clinical
characteristics but negative serological tests for Chagas.
Methods This retrospective, observational study included 74 chagasic
patients and 28 healthy subjects who underwent exercise
testing during clinical check-up between March 2009 and
September 2011.
Results Chagasic patients often presented baseline heart rate£ 60
bpm (27.0% vs. 7.1%, p=0.02), lower maximal heart rate
(129.5±22.8 vs. 145.2±16.5 bpm; p=0.002), prevalence of
chronotropic incompetence, with maximum heart rate < 80%
pre-established value (47.3% vs. 14.3%; p=0.001) and higher
rate of ventricular arrhythmias during exercise and recovery
(25.7% vs. 0%; p=0.003).
While in the control group patients the QTc interval shortened
normally during exercise, in most chagasic patients it
was noticeably prolonged (Chagas group: 412.1 to 432.8 ms;
p = 0.0005; control group: 412.4 to 385.8 ms; p< 0.0001).
Conclusions Asymptomatic chagasic patients without verifiable heart
disease showed a high prevalence of dysautonomia, such as
chronotropic incompetence and QTc interval prolongation during exercise. Stress testing is a noninvasive, reliable and
relatively inexpensive diagnostic method that can contribute
to the early diagnosis of dysautonomic and ventricular
repolarization disorders and thus identify patients with
Chagas disease who are at increased risk of arrhythmogenic
sudden death.
Key words: Chagas Disease; Electrocardiography; Primary Dysautonomia; QT Interval; Exercise Test.
Abreviaturas
ECG Electrocardiograma
FCMT Frecuencia cardíaca máxima total
FC Frecuencia cardíaca
PEG Prueba ergométrica graduada
FC máx Frecuencia cardíaca máxima
TA Tensión arterial
INTRODUCCIÓN
A pesar de haber transcurrido un siglo desde su descubrimiento,
la enfermedad de Chagas continúa siendo
una de las mayores causas de morbilidad y mortalidad
en América Latina y en las últimas décadas, debido a la
migración de personas infectadas, ha llegado a ser un
potencial problema en Europa y en los Estados Unidos.
(1) Según la Organización Mundial de la Salud, se estima
una población mundial de 12 millones de personas
infectadas, 100 millones de pacientes en riesgo y una
mortalidad anual aproximada de 50.000 personas. (2)
Salvo excepciones, la enfermedad de Chagas evoluciona
con: a) una fase aguda que puede ser asintomática
o manifestarse con un síndrome febril autolimitado que
dura 4 a 8 semanas y b) una fase crónica que consta de
dos estadios: un período crónico sin patología demostrada
o período indeterminado, asintomático, que puede
durar 10 a 30 años o toda la vida y un período crónico
con patología demostrada, sintomático, en el que el 10%
de los pacientes infectados desarrolla patología digestiva
y/o neurológica y el 25-30% presenta compromiso
cardíaco, cuya manifestación más importante y grave
es la miocardiopatía, considerada la principal causa de
mortalidad, ya sea por muerte súbita arritmogénica o
por falla mecánica como consecuencia de la insuficiencia
cardíaca congestiva. (3)
Se han propuesto factores vasculares, inflamatorios,
inmunológicos y neurológicos que actuarían
interrelacionándose para desarrollar y desencadenar
la enfermedad muchos años después de la etapa aguda
y así intervendrían para que en determinadas circunstancias
algunos pacientes pasen del período crónico sin
patología demostrada al período crónico sintomático de
la enfermedad de Chagas. (4, 5)
Según el análisis fisiopatológico, Trypanosoma
cruzi posee una neuraminidasa que afecta la función
cardíaca al actuar sobre la membrana de las fibras de
conducción, del sistema autonómico y de las células endoteliales
del miocardio y de los vasos sanguíneos. (6) Se
ha observado que una de las manifestaciones más precoces
de la enfermedad de Chagas es la disautonomía
por la afectación del sistema nervioso autónomo, que
estaría relacionada con la presencia de anticuerpos que
actuarían contra los receptores muscarínicos, primero
estimulando y luego bloqueando, con un claro efecto
símil-acetilcolina. Los anticuerpos antimuscarínicos
aparecen precozmente una vez instalada la parasitosis
y se han detectado en el 30% de los pacientes infectados.
(7-11)
La evolución clínica de la enfermedad de Chagas es
variable e impredecible, por lo cual se torna un desafío
llegar a conocer los indicadores que puedan ayudar a
identificar a pacientes con mayor riesgo de presentar
muerte súbita o una progresión a la fase crónica sintomática
de la enfermedad. Las nuevas tecnologías
diagnósticas que posibilitan el hallazgo temprano de
alteraciones endoteliales o disautonómicas deberán originar
mejores estrategias de diagnóstico y tratamiento al
permitir la detección precoz de los pacientes con riesgo
de evolucionar a la miocardiopatía chagásica crónica o de
sufrir muerte súbita. La prueba ergométrica graduada
(PEG) es un procedimiento incruento, confiable y de
relativo bajo costo que en la metodología de estudio de
la enfermedad de Chagas se constituye en una indicación
de Clase IC en los pacientes que se encuentran en
el período crónico sin cardiopatía evidenciable con los
métodos diagnósticos actualmente disponibles. (12)
En consideración a estas observaciones, los objetivos
del presente trabajo fueron:
a) Investigar los signos clínicos y ergométricos de los
pacientes chagásicos asintomáticos, con electrocardiograma
(ECG) normal y sin patología clínica
evidenciable.
b) Comparar los datos clínicos, ergométricos y las
modificaciones de los parámetros electrocardiográficos
que presentan durante la PEG estos pacientes
chagásicos con los de un grupo de sujetos de características
clínicas similares pero con serología
negativa para Chagas.
MATERIAL Y MÉTODOS
En este estudio observacional, retrospectivo, se incluyeron
102 pacientes que realizaron una ergometría en nuestro hospital
entre marzo de 2009 y septiembre de 2011. En base al
diagnóstico serológico de enfermedad de Chagas, los pacientes
fueron distribuidos en dos grupos:
Grupo Chagas: 74 pacientes con serología positiva para
Chagas, que presentaban ECG, radiografía de tórax y ecocardiograma
bidimensional normales y ausencia de cardiopatía
u otra patología orgánica demostrable con los métodos diagnósticos
actualmente disponibles.
Grupo control: 28 sujetos no chagásicos, seleccionados
entre 100 ergometrías consecutivas, sin antecedentes coronarios
o patología clínica evidenciable y con ECG, radiografía
de tórax y ecocardiograma bidimensional dentro de límites
normales.
Todos los sujetos incluidos en este estudio eran asintomáticos
y realizaron la PEG para ingresar a gimnasio,
realizar actividad física no competitiva o para evaluación
preocupacional.
En los pacientes del grupo Chagas, el diagnóstico de
enfermedad de Chagas se confirmó por la positividad de las
tres reacciones que según los criterios del Instituto Nacional
de Parasitología Dr. Mario Fatala Chabén son: la reacción de
hemaglutinación indirecta, la prueba de inmunofluorescencia
indirecta y el método de enzimoinmunoensayo (ELISA). (12)
Se excluyeron los pacientes con antecedentes de infarto
previo o enfermedad arterial coronaria en estudio, valvulopatías,
miocardiopatías, arritmias supraventriculares y
ventriculares, trastornos de conducción, enfermedad de la
glándula tiroides, medicación y/o patologías que afecten el
automatismo, la conducción y/o la repolarización ventricular
o la interpretación del ECG basal.
De cada paciente se consideraron los siguientes datos:
edad, sexo, frecuencia cardíaca (FC), tensión arterial (TA), se
evaluaron el ECG, la radiografía de tórax y el ecocardiograma
bidimensional realizados en la semana previa al estudio
ergométrico.
La PEG se realizó con una bicicleta ergométrica conectada
a un sistema computarizado que realiza un registro
electrocardiográfico a 25 mm/seg de las 12 derivaciones al
finalizar cada etapa, tanto de la fase de ejercicio como de
la de recuperación, sumado al control de la FC y la TA del paciente. Se empleó un protocolo escaleriforme continuo que
consta de dos fases: la fase activa de ejercicio con etapas de 3
minutos cada una con cargas progresivas de 150 kgm y la fase
de recuperación que tiene tres etapas de 1 minuto seguidas
de dos etapas de 3 minutos.
La PEG se consideró suficiente cuando durante la fase
de ejercicio la FC alcanzaba el 85% de la FC máxima total
(FCMT) según la tabla de Robinson y se definió como incompetencia
cronotrópica cuando la FC máxima (FC máx)
durante el esfuerzo era menor del 80% de los valores preestablecidos.
(13)
Como expresión de disautonomía, se evaluó el número de
pacientes que presentaban FC basal = 60 latidos por minuto
(lpm) o = 100 lpm. También se consideró la TA = 190/100 mm
Hg al final de la carga ergométrica máxima.
Se consideró retardo en la recuperación de la FC cuando
en el segundo minuto del posesfuerzo la FC había descendido
menos de 22 lpm. (14)
Utilizando el sistema computarizado que almacena el
registro electrocardiográfico de cada etapa de la PEG, dos
observadores independientes realizaron un promedio de los
valores en milisegundos (mseg) de tres ciclos consecutivos
de las derivaciones V5 y V6 en el registro basal, al final de
la carga máxima alcanzada y al segundo minuto de la recuperación
de los siguientes parámetros del ECG: intervalo
R-R (RR); intervalo P-R (PR); duración del QRS (QRS); el
intervalo Q-T (QT), que fue medido desde el comienzo del
QRS hasta el fin de la onda T por el método tangencial que
pasa por el vértice de la curva entre la onda T y la onda U
y el punto más declive de la onda; el intervalo QT corregido
(QTc), calculado según fórmula de Bazet; el QTc-máx = 0,47
seg y la presencia de modificaciones del segmento ST a 80
mseg del punto J durante la PEG.
Sobre la base de la FC máx alcanzada durante la fase de
ejercicio activo de la PEG, los pacientes del grupo Chagas se
distribuyeron en:
Con PEG insuficiente: 48 pacientes con FC máx durante
la fase de ejercicio < 85% de la FCMT.
Con PEG suficiente: 26 pacientes que a la carga máxima
la FC alcanzó el 85% de la FCMT preestablecida.
Se compararon los principales datos clínicos, ergométricos y las modificaciones de los parámetros electrocardiográficos durante la fase de ejercicio y de recuperación de la PEG, entre los pacientes chagásicos y el grupo control y dentro del grupo de chagásicos, entre los pacientes con PEG insuficiente y suficiente.
Análisis estadístico
Las variables categóricas se expresan como frecuencia y su
porcentaje. Las variables continuas se expresan como medias
± desviación estándar y mediana (intervalo intercuartil)
según su distribución.
El análisis de las variables discretas se realizó con la
prueba de chi cuadrado y chi cuadrado con partición de
grados de libertad.
Las variables continuas se analizaron con la prueba de
la t para dos grupos o Kruskal-Wallis según su distribución.
La comparación intragrupo de las variables continuas se
realizó con la prueba de la t para datos apareados. Se consideró
significativo un valor de p < 0,05.
RESULTADOS
Se incluyeron 102 pacientes con una edad promedio de 47,6 ± 12,8 años; 59 pacientes (57,8%) eran de sexo masculino.
En la Tabla 1 se detallan las características clínicas y ergométricas generales de los pacientes de cada grupo. No se observaron diferencias estadísticamente significativas entre los grupos respecto de la edad y el sexo de los pacientes.
Tabla 1. Características clínicas
y ergométricas de los pacientes
de cada grupo

La causa de detención anticipada del ejercicio fue el
agotamiento muscular. Durante la PEG, los pacientes
no presentaron síntomas y no se observaron modificaciones
significativas del segmento ST y de la onda T.
Los pacientes del grupo Chagas presentaron más
frecuentemente FC basal = 60 lpm (27,0% vs. 7,1%; p =
0,02) y la FC máx alcanzada durante la PEG fue menor
(129,5 ± 22,8 lpm vs. 145,2 ± 16,5 lpm; p = 0,002).
Los pacientes chagásicos presentaron mayor prevalencia
de FCMT = 80% durante la PEG (incompetencia
cronotrópica) (47,3% vs. 14,3%; p = 0,003) y de arritmia
ventricular durante el ejercicio y la recuperación
(25,7% vs. 0%; p = 0,003).
En la Tabla 2 se presentan los parámetros electrocardiográficos
y su modificación durante la ergometría
de los pacientes de cada grupo. No se observaron diferencias
estadísticamente significativas en los parámetros
del registro electrocardiográfico basal.
Tabla 2. Datos del ECG basal
y su modificación durante la
ergometría de los pacientes de
cada grupo
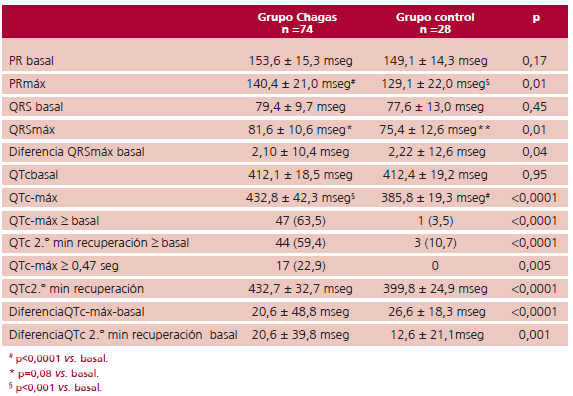
Durante el ejercicio se observó que los pacientes del grupo control acortaron normalmente el intervalo QTc mientras que un número significativo de pacientes del grupo Chagas prolongaron en forma notoria el QTc (grupo Chagas: 412,1 ± 18,5 mseg a 432,8 ± 42,3 mseg; p = 0,0005; grupo control: 412,4 ± 19,2 mseg a 385,8 ± 19,3 mseg; p < 0,0001) (Figura 1). También se observó en el grupo Chagas alta prevalencia de pacientes con QTc-máx = 0,47seg (22,9% vs. 0%; p = 0,005).
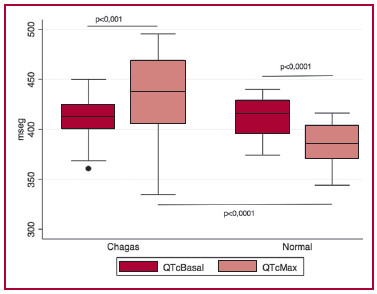
Fig. 1. Variación del QTc con el ejercicio en los pacientes chagásicos
y en los pacientes del grupo control.
En ambos grupos se observó un acortamiento
significativo del PR. Los pacientes del grupo Chagas
mostraron una tendencia a ensanchar el QRS mientras
que en los pacientes del grupo control no se observó
variación.
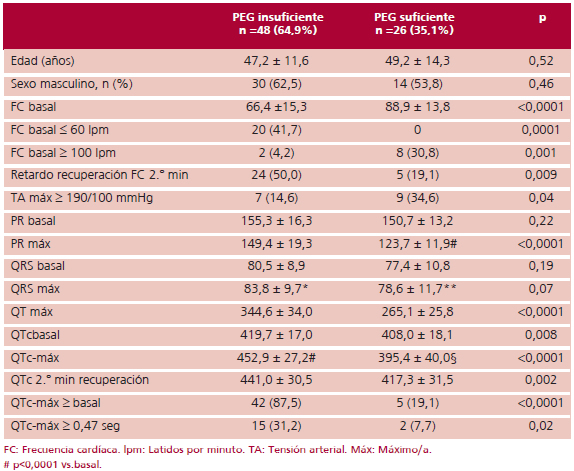
En la Tabla 3 puede observarse que, al analizar a
los pacientes chagásicos según la FC máx alcanzada
durante la fase de ejercicio, los pacientes con PEG
insuficiente tenían una FC basal menor (66,4 ± 15,3
lpm vs. 88,9 ± 13,8 lpm; p < 0,0001), mayor prevalencia
de FC basal = 60 lpm (41,7% vs. 0%; p = 0,0001),
mayor retardo en la recuperación de la FC al segundo
minuto (50% vs. 19,2%; p = 0,009) y una diferencia
significativa en el número de pacientes que mostraron
marcada prolongación del QTc frente a un acortamiento
normal en los pacientes con PEG suficiente (419,7 ±
17,0 mseg a 452,9 ± 27,2 mseg con PEG insuficiente,
p < 0,0001 y 408,0 ± 18,1 mseg a 395,4 ± 40,0 mseg
con PEG suficiente, p = 0,003).
Tabla 3. Comparación de
datos clínicos y ergométricos
entre los pacientes chagásicos
con PEG insuficiente y suficiente.
DISCUSIÓN
Durante el período crónico sin cardiopatía demostrable
de la enfermedad de Chagas, en aproximadamente el
30% de los pacientes infectados se presentan alteraciones
de distinta magnitud, como la disautonomía, la
disfunción del endotelio vascular que afecta la microcirculación miocárdica y el retardo y deshomogeneización
regional de la repolarización ventricular que se pone de
manifiesto con la gran dispersión en la duración de los
intervalos QT y con la prolongación del QTc en el ECG
de base. Todas estas manifestaciones estarían relacionadas
con la presencia de anticuerpos antimuscarínicos y
serían indicadores de un incremento de la morbimortalidad,
lo cual torna relevante la posibilidad de lograr su
detección precoz por métodos diagnósticos incruentos
y de fácil disponibilidad. Se ha comprobado que de los
pacientes que presentaban anticuerpos antimuscarínicos
aproximadamente el 95% tenían manifestaciones de
disautonomía y el 50% mostraban en el ECG dispersión
del intervalo QT > 65 mseg. (9, 15, 16)
Los resultados que se muestran en la Tabla 1 coinciden con los de trabajos que hemos mencionado
(6, 11, 16) al mostrar que un número significativo de
pacientes chagásicos presentaron durante la ergometría
signos que indican la presencia de disautonomía:
la alta prevalencia de PEG insuficiente y de FC basal
= 60 lpm, el significativo menor incremento de la FC
máx a pesar de haber alcanzado cargas ergométricas
similares a la de los pacientes del grupo control y fundamentalmente
el mayor porcentaje de pacientes con
incompetencia cronotrópica durante la fase activa del
ejercicio. La arritmia ventricular frecuente también se
sumó a los signos de desequilibrio autonómico durante
la PEG en los pacientes del grupo Chagas.
La incompetencia cronotrópica se define como la
incapacidad de la FC para incrementarse proporcionalmente
a la intensidad del ejercicio realizado; se evidencia
con una FC máx = 80% de la FCMT y se considera
el mejor indicador de disautonomía. Se atribuye a la
disminución de la sensibilidad del nodo sinusal a la estimulación
simpática y a las catecolaminas circulantes
por la disfunción autonómica subyacente y ha demostrado
que es un predictor independiente de eventos
cardíacos mayores y de aumento de la mortalidad de
todas las causas. (17, 18)
El hallazgo más destacable de nuestro estudio se
muestra en la Tabla 2. Durante la fase de ejercicio, el
ECG de fin de la carga máxima muestra que mientras
los pacientes del grupo control, debido posiblemente a
la descarga adrenérgica, presentaban un acortamiento
normal de los intervalos PR máx, QT máx y QTc-máx,
los pacientes chagásicos mostraron mayor duración del
intervalo PR máx, del complejo QRS máx y fundamentalmente
una prolongación significativa del intervalo
QTc-máx, que se hizo más notoria al compararla con
los registros basales y el grupo control. Es de destacar
que casi el 30% de los pacientes presentaron un QTcmáx
= 0,47 seg, mientras que ninguno de los pacientes
del grupo control presentó un QTc-máx prolongado.
Numerosos estudios han señalado la presencia en
el ECG de los pacientes chagásicos, durante el período crónico sin cardiopatía demostrable, de una amplia dispersión
en la duración de los intervalos QT = 65 mseg,
que sería indicadora de la existencia de una heterogenicidad
regional o localizada en la repolarización de
las fibras miocárdicas y estaría asociada con un riesgo
mayor de taquiarritmias ventriculares complejas y con
un aumento de la morbimortalidad. (19-22) Sin embargo, otros autores (23-26) han demostrado
en población no chagásica que la prolongación del
intervalo QTc de mayor duración (= 458 mseg en derivaciones
V5-V6) tendría una importancia mayor, en
especial cuando es = 0,47 seg, porque se comporta como
un predictor independiente del riesgo de muerte súbita.
Esto se debería a que expresa un retardo localizado de
la repolarización ventricular por la prolongación no
homogénea en la duración de los potenciales de acción
como consecuencia de la dispersión temporal y regional
de los períodos refractarios de las fibras miocárdicas, que
al ser estimulado e incrementado por el desequilibrio
autonómico subyacente crea un terreno favorable a la
reentrada y actividad gatillada. Estos son los mecanismos
electrofisiológicos que intervienen en el desencadenamiento
de las arritmias ventriculares complejas y
la muerte súbita en la enfermedad de Chagas. (27, 28)
Durante una PEG, en especial en los pacientes chagásicos
con PEG insuficiente (véase Tabla 3), se puede
detectar una suma de factores que han demostrado ser
predictores de un riesgo mayor de muerte súbita, como
la alta prevalencia de los parámetros indicadores de
disautonomía, el retardo en la recuperación de la FC en
el segundo minuto de la recuperación junto con la más
significativa prolongación del intervalo QTc-máx frente
al acortamiento evidenciado en los pacientes chagásicos
con PEG suficiente. Estos resultados nos permitirían
explicar por qué en estudios previos la disautonomía se
ha asociado con un riesgo mayor de muerte súbita aun en
etapas tempranas de la enfermedad de Chagas. (7, 9, 19)
El retardo de la recuperación de la FC en el segundo
minuto del posesfuerzo también sería atribuible a la
disautonomía por el desequilibrio autonómico entre
la interrupción de la estimulación simpática al fin del
esfuerzo y la reactivación de la respuesta vagal, y ha
demostrado que es un predictor del incremento de la
mortalidad en la población general. (29) Como limitaciones podemos mencionar el número
reducido de pacientes chagásicos y la falta de un seguimiento
adecuado para comprobar el valor predictivo
de la prolongación significativa del intervalo QTc y los
signos de disautonomía que evidenciaron durante la
ergometría y establecer si estos hallazgos identifican a
los pacientes que tienen mayor riesgo de evolucionar a
la cardiopatía chagásica crónica sintomática.
CONCLUSIONES
Los resultados de nuestro estudio muestran que los
pacientes chagásicos asintomáticos sin cardiopatía
demostrable, durante una PEG, presentan alta prevalencia
de los signos que señalan la presencia de
disautonomía. Asimismo, en un número significativo
de pacientes chagásicos, el desequilibrio autonómico
se asoció con una marcada prolongación de los intervalos
QTc, que expresa la heterogenicidad regional en
la duración de los potenciales de acción de las fibras
miocárdicas y favorece el desarrollo de los mecanismos
electrofisiológicos que desencadenan taquiarritmias
ventriculares complejas y sostenidas.
De esta forma, la PEG podría constituirse en un método
de diagnóstico útil para identificar a los pacientes
chagásicos que tienen mayor riesgo de sufrir muerte
súbita arritmogénica.
Estos hallazgos requieren estudios con un número
mayor de pacientes y seguimiento clínico prolongado
a los fines de comprobar fehacientemente el riesgo
aumentado de eventos mayores.
1. Bern C, Montgomery SP, Herwaldt BL, Rassi A Jr, Marin-Neto JA, Dantas RO, et al. Evaluation and treatment of Chagas disease in the United States: a systematic review. JAMA 2007;298:2171-81. http://doi.org/c9c682
2. World Heart Organization (WHO) information about Chagas disease. En: Fact Sheet N° 340; 2011.
3. Prata A. Clinical and epidemiological aspects of Chagas disease. Lancet Infect Dis 2001;1:92-100. http://doi.org/d7kbms
4. Marin-Neto JA, Cunha-Neto E, Maciel BC, Simoes MV. Pathogenesis of chronic Chagas heart disease. Circulation 2007;115:1109-23. http://doi.org/cnstwr
5. Morris SA, Tanowitz HB, Wittner M, Bilezikian JP. Pathophysiological insights into the cardiomyopathy of Chagas' disease. Circulation 1990;82:1900-9. http://doi.org/bzzg45
6. Marin-Neto JA. Cardiac dysautonomia and pathogenesis of Chagas' heart disease. Int J Cardiol 1998;66:129-31.
7. Sousa L, Rocha MO, Britto RR, Lombardi F, Ribeiro AL. Chagas disease alters the relationship between heart rate variability and daily physical activity. Int J Cardiol 2009;135:257-9. http://doi.org/bnd3z4
8. Herrera RN, Coviello A, Sant Yacumo RA, Callejas CA, Bianchi JM, Rodríguez Maisano E y col. Estudio del sistema nervioso autónomo a nivel central y periférico en estadios precoces de la enfermedad de Chagas crónica. Rev Fed Arg Cardiol 2002;31:434-40.
9. Giménez L, Mitelman J, González C, Borda E, Borda L. Anticuerpos antirreceptores autonómicos, alteraciones de la variabilidad de la frecuencia cardíaca y arritmias en sujetos con enfermedad de Chagas. Rev Argent Cardiol 2003;71:109-13.
10. Goin JC, Borda ES, Auger S, Storino R, Sterin-Borda L. Cardiac M(2) muscarinic cholinoceptor activation by human chagasic autoantibodies: association with bradycardia. Heart 1999;82:273-8.
11. Mitelman J, Giménez L, Acuña L, Tomasella M, Cicarelli F, Pugliese O y col. Anticuerpos antirreceptores a neurotransmisores y su correlación con la alteración de la dispersión del QT y de la variabilidad de la frecuencia cardíaca. Relampa 2006;19:408-15.
12. Consenso de Enfermedad de Chagas-Mazza. Sociedad Argentina de Cardiología. Consejo de Enfermedad de Chagas "Dr. Salvador Mazza". Rev Argent Cardiol 2011;79:544-64.
13. Lauer MS, Okin PM, Larson MG, Evans JC, Levy D. Impaired heart rate response to graded exercise. Prognostic implications of chronotropic incompetence in the Framingham Heart Study. Circulation 1996;93:1520-6. http://doi.org/jjt
14. Vivekananthan DP, Blackstone EH, Pothier CE, Lauer MS. Heart rate recovery after exercise is a predictor of mortality, independent of the angiographic severity of coronary disease. J Am Coll Cardiol 2003;42:831-8. http://doi.org/cd9mrm
15. Giménez L, Mitelman J, González C, Palacios K, Burgos AN. Alteraciones de la dispersión del QT y la fracción de eyección en pacientes chagásicos. Relampa 2007;20:74-8.
16. Rassi A, Jr, Rassi A, Rassi SG. Predictors of mortality in chronic Chagas disease: a systematic review of observational studies. Circulation 2007;115:1101-8. http://doi.org/fkvqf4
17. Chaitman BR. Abnormal heart rate responses to exercise predict increased long-term mortality regardless of coronary disease extent: the question is why? J Am Coll Cardiol 2003;42:839-41. http://doi.org/b645xm
18. Lauer MS, Francis GS, Okin PM, Pashkow FJ, Snader CE, Marwick TH. Impaired chronotropic response to exercise stress testing as a predictor of mortality. JAMA 1999;281:524-9. http://doi.org/bf8t9d
19. Salles G, Xavier S, Sousa A, Hasslocher-Moreno A, Cardoso C. Prognostic value of QT interval parameters for mortality risk stratification in Chagas' disease: results of a long-term follow-up study. Circulation 2003;108:305-12. http://doi.org/c9tzmd
20. Okin PM, Devereux RB, Howard BV, Fabsitz RR, Lee ET, Welty TK. Assessment of QT interval and QT dispersion for prediction of all-cause and cardiovascular mortality in American Indians: The Strong Heart Study. Circulation 2000;101:61-6. http://doi.org/jjv
21. Malik M, Batchvarov VN. Measurement, interpretation and clinical potential of QT dispersion. J Am Coll Cardiol 2000;36:1749-66. http://doi.org/bhvb3r
22. Zabel M, Klingenheben T, Franz MR, Hohnloser SH. Assessment of QT dispersion for prediction of mortality or arrhythmic events after myocardial infarction: results of a prospective, long-term follow-up study. Circulation 1998;97:2543-50. http://doi.org/jjw
23. Straus SM, Kors JA, De Bruin ML, van der Hooft CS, Hofman A, Heeringa J, et al. Prolonged QTc interval and risk of sudden cardiac death in a population of older adults. J Am Coll Cardiol 2006;47:362- 7. http://doi.org/c9vn4h
24. Wong KY, Mac Walter RS, Douglas D, Fraser HW, Ogston SA, Struthers AD. Long QTc predicts future cardiac death in stroke survivors. Heart 2003;89:377-81. http://doi.org/fcs2ft
25. Schouten EG, Dekker JM, Meppelink P, Kok FJ, Vandenbroucke JP, Pool J. QT interval prolongation predicts cardiovascular mortality in an apparently healthy population. Circulation 1991;84:1516-23. http://doi.org/jjx
26. Karjalainen J, Reunanen A, Ristola P, Viitasalo M. QT interval as a cardiac risk factor in a middle aged population. Heart 1997;77:543-8.
27. Fuenmayor AJ, Fuenmayor AM. Sudden death in patients with chagasic myocarditis. Arch Inst Cardiol Mex 1996;66:157-61.
28. Bexton RS, Vallin HO, Camm AJ. Diurnal variation of the QT interval influence of the autonomic nervous system. Br Heart J 1986;55:253-8. http://doi.org/dcvj8h
29. Cole CR, Blackstone EH, Pashkow FJ, Snader CE, Lauer MS. Heart-rate recovery immediately after exercise as a predictor of mortality. N Engl J Med 1999;341:1351-7. http://doi.org/c3k9z2