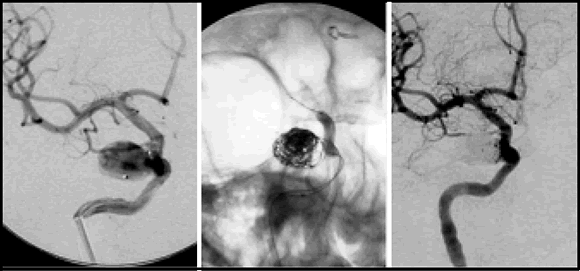
Fig. 1. Aneurisma paraclinoideo derecho de cuello amplio donde se observa la técnica de remodelado del cuello con balón, lo que contiene la canasta de coil en el saco aneurismático.
Reconstrucción de arteria portadora en aneurismas cerebrales de cuello amplio con técnica de micro stent autoexpandible
Walter Casagrande, Luis Lemme Plaghos, Silvia Garbugino, Julio Fernández, Javier Goland
Centro Endovascular Neurológico Buenos Aires, Argentina
Correspondencia: Cenba.neuro@arnet.com.ar
Recibido: agosto 2007;
aceptado: septiembre 2007
RESUMEN
Objetivo. Analizar en forma retrospectiva en el presente trabajo, la efectividad y complicaciones de esta técnica en treinta y cinco
aneurismas de cuello amplio tratados con un micro stent de tipo autoexpandible modelo Neuroform (Boston Scientific).
Población y métodos. En un lapso de cincuenta meses hemos tratado por vía endovascular quinientos treinta aneurismas
cerebrales, en treinta y cinco de los cuales, por sus características anatómicas, se practicó la técnica de coils asistidos con stent, para
reconstruir la arteria. Previa antiagregación y bajo anticoagulación sistémica, el stent Neuroform fue liberado a nivel del cuello del
aneurisma y luego a través del mismo se realizó la oclusión del saco aneurismático con coils desprendibles.
Resultados. En un solo caso no fue posible liberar el stent; treinta y dos casos se trataron con stent seguidos de la oclusión con coils
y a dos aneurismas se los trató sólo con stent. Nueve de los aneurismas habían sido tratados inicialmente sólo con coils y en un
segundo tiempo para completar la oclusión del cuello se les colocó el stent y coils. Un paciente falleció por una hemorragia
subaracnoidea secundaria al procedimiento; otro paciente sufrió accidente tromboembólico sin morbilidad definitva a los doce días
del procedimiento y un paciente sufrió un hematoma retroperitoneal por hemorragia en el sitio de punción femoral. Veinticinco
pacientes tuvieron seguimiento angiográfico y estos casos fueron analizados encontrando en cuatro casos mínima compactación de
los coils, observando en otros tres casos signos de estenosis en el segmento donde se había colocado el stent; uno revirtió ésta en
forma completa y en los otros dos en forma parcial a los 12 meses.
Conclusión. El stent intracraneano autoexpandible Neuroform permite la reconstrucción arterial en aneurismas de cuello amplio en
el 97% de los casos tratados, incrementando significativamente la estabilidad de la oclusión lograda con coils. La técnica, si bien
reproducible, presenta aún riesgos de isquemia y estenosis tardía intrastent, por lo que sólo debe ser utilizada en aquellos casos en
los cuales la anatomía del cuello aneurismático así lo exija.
Palabras clave: Aneurisma cerebral; Coils; Embolización; Stent.
ABSTRACT
Introduction. Main limitation for complete occlusion of wide
neck brain aneurysms is a major challenge for the Endovascular
Technique. Stent assisted reconstruction of the parent vessel
associated with coils embolization has been proposed as a
solution. Retrospective analysis of effectiveness and complications
in a series of thirty five wide neck aneurysms using the self
expandable brain vessel dedicated stent Nueroform (Bostos
Scientific) is described.
Material and methods. In the tern of fifty months 530 brain
aneurysms were treated by endovascular approach. Due to
their anatomy in 35 of these, stent assisted reconstruction of
the parent artery with or without coiling of the aneurysm sac
was performed. Under antiplatelet therapy and anticoagulation
Neuroform stents were deployed in the artery at the neck
of the aneurysm followed by detachable coil occlusion of the
sac itself.
Results. Only in one case stent deployment could not be
achieved. In thirty two cases stent assisted aneurysm coil
embolization was performed while in two cases single stent
deployment was done. In nine cases coil embolization had been
performed previously and stent assisted coil embolization was
performed in order to occlude the aneurysm neck. One patient
died after a subarachnoid hemorrhage secondary to the treatment;
another patient presented with a transient ischemic
episode twelve days after the procedure and one patient had a
retroperitoneal hematoma related to the artery puncture at the
groin. Twenty five patients had three and twelve months follow
up angiograms performed showing minimal compaction in four
cases, and arterial stenosis at the site where stent has been
deployed in three of them. In the twelve month angiogram one
of these cases showed complete regression while the other two
showed a mild reversion.
Conclusions. Neuroform self expandable stent system allowed
arterial wall reconstruction in 97% of cases of wide neck brain
aneurysms increasing the rate of stabilization of coil occlusion.
This technique still carries risks of ischemia and delayed intra
stent stenotic phenomena reason for which it should be performed
solely in those cases in which neck anatomy precludes
sole coil embolization.
Key words: Brain aneurysm; Embolization; Stent; Coils
INTRODUCCIÓN
El tratamiento de un aneurisma cerebral depende
básicamente de su localización y de su morfología.
Hasta hace una década el tratamiento quirúrgico era
considerado el tratamiento de elección de los aneurismas.
Publicaciones más recientes avalan el tratamiento
endovascular para ciertas localizaciones de los
aneurismas y en pacientes con alto grado en la escala
de Hunt y Hess. El Estudio randomizado Interanational
Subarachnoid Aneurysm Traial (ISAT)1 ha demostrado
en casos de aneurismas factibles de ser tratados
por ambas vías, una mejor evolución clínica del paciente
en el primer año postprocedimiento para el
tratamiento endovascular versus la cirugía a cielo
abierto.
Desde el comienzo de la técnica de espirales la
compactación de los mismos continúa siendo un desafío
a vencer. Publicaciones previas remarcan la incidencia
del tamaño del cuello en la recanalización del
aneurisma embolizado, el cual también limita la indicación
cuando la relación saco/cuello no es la adecuada2.
Previamente se ha intentado reconstruir la pared
arterial utilizando métodos como la técnica de remodelado
con balón de oclusión transitoria propuesta y difundida
por Moret3 y la técnica de colocación de stents coronarios
en la arteria cubriendo el cuello de aneurisma4. En la
primera (Fig. 1), se llega con un microcatéter al interior del
aneurisma y una vez dentro del saco, por una segunda vía
de abordaje, se llega con un balón a la boca del aneurisma,
insuflando intermitentemente el mismo para la contención
durante el armado de la canasta de coils en el saco
aneurismático. La técnica de stent, no específicamente
diseñado para arterias intracraneanas como son los stent
coronarios, fue utilizada para asistir el tratamiento de
aneurismas de cuello amplio, con las limitaciones propias
de los stent no diseñados para la anatomía vascular
cerebral como lo son el perfil de la malla del stent, la
limitación que produce el hecho de que se encuentran en
su mayoría premontados a un balón, lo que limita la
navegabilidad del mismo, y la necesidad de expandirlos
con la asistencia de un balón, lo que promueve una sobre
dilatación del vaso portador en muchos casos, con el
consecuente riesgo de ruptura.

Fig. 1. Aneurisma paraclinoideo derecho de cuello amplio donde se observa la técnica de remodelado del cuello con balón, lo que contiene la canasta de coil en el saco aneurismático.
Actualmente se han desarrollado sistemas de micro stent intracraneano autoexpandible (Fig. 2), que permiten una correcta navegación de los vasos intracraneanos y la reconstrucción de la arquitectura vascular en aneurismas de cuello amplio5. En este trabajo analizamos nuestra experiencia con los stent Neuroform en la reconstrucción del cuello aneurismático.
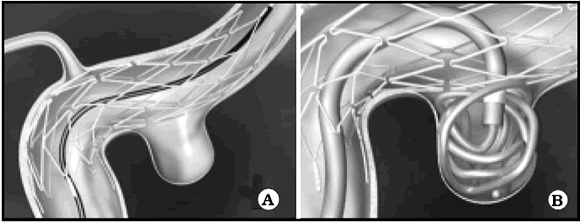
Fig. 2. A. Esquema de la morfología del Microstent Neuroform. B: se observa como se ocluye el saco aneurismático una vez liberado el Microstent. (Gentileza Boston Scientific®)
MATERIAL Y MÉTODOS
Población
En un lapso de cincuenta meses nuestro equipo de
neurocirugía endovascular trató un total de quinientos
treinta aneurismas cerebrales, de los cuales treinta y
cinco presentaron una relación de tamaño entre el saco
y el cuello no apta para la técnica de embolización con
coils, motivo por el que fueron seleccionados para tratamiento
con coils asistidos con stent autoexpandible.
En los pacientes analizados se utilizaron tres generaciones
de microstent Neuroform: Neuroform 1, tres
casos, stent Neuroform 2, ocho casos y stent Neuroform
3, veintitrés casos. En un solo caso el procedimiento fue
discontinuado debido a la imposibilidad de subir el
stent (Tabla 1).
Tabla 1. Pacientes tratados
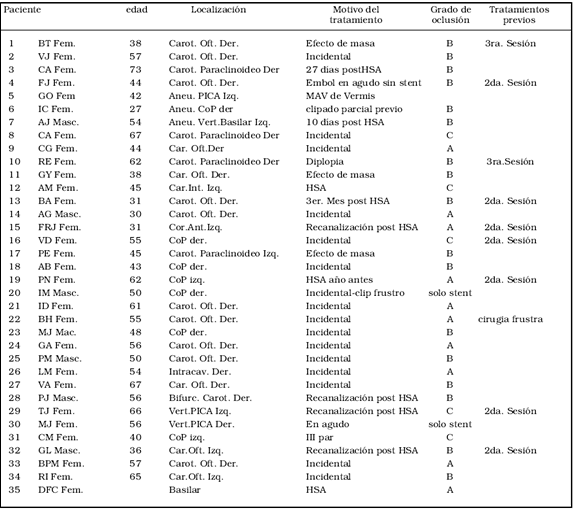
Liberación del stent
El stent Neuroform® es un stent autoexpandible de
Nitinol que se encuentra en un catéter 3 French con el
cual se llega al sitio de colocación donde se libera con un
estabilizador 2 French.
En los de primera y segunda generación, el stent se
presentaba premontado en un catéter sobre el cual se
ensamblaba un estabilizador. En el modelo de tercera
generación el stent y el estabilizador se encuentran ya
ensamblados, habiéndose mejorado la rigidez tanto del
catéter portador como el estabilizador. Este stent propiamente
dicho presenta menor número de soldaduras entre
las celdas, lo que mejora también su navegabilidad.
En cada uno de los procedimientos se utilizó catéter
guía de 6 French; por el que se ascendió un microcatéter
Excel 0,014 sobre una microguía Transend 0,014 de
300 cm de longitud, y una vez en posición con la
microguía distal al saco aneurismático, se procedió al
recambio del microcatéter por el microcatéter con el
microstent premontado.
Oclusión endovascular
Mediante la colocación del stent, el redireccionamiento del flujo en el vaso portador y el hipoflujo en el saco aneurismático no son suficientes para evitar la ruptura aneurismática, motivo por el cual se debe completar el tratamiento con la oclusión del saco con coils. En 33 casos de esta serie, el tratamiento fue completado con la embolización del saco aneurismático utilizando coils biológicamente activos (Figs. 3 y 4).

Fig. 3. A. Aneurisma carotidooftálmico derecho de cuello ancho. B: Control angiográfico sin sustracción digital postembolización donde se visualiza el stent con los marcadores proximales y distales (flechas negras)

Fig. 4. Aneurisma carotidooftálmico tratado con técnica de stent y coils se remarca cómo el cuello aneurismático compromete la mitad del diámetro arterial.
En dos casos se utilizó sólo stent debido a que la
morfología del saco no permitía la colocación de coils
dentro del mismo, uno de estos pacientes se trataba de
un aneurisma carotídeo en el que no se pudo colocar un
clip quirúrgico por su morfología y el otro se trataba de
un pseudoaneurisma vertebral adyacente al origen de
la PICA secundario a disección y hemorragia subaracnoidea
del mismo.
El grado de oclusi ón fue evaluado considerando
como A a la oclusión total, B oclusión subtotal con coils
en el cuello aneurismático, C subtotal sin coils a nivel
del cuello y D oclusión parcial (Tabla 1).
Todos los pacientes fueron antiagregados con Clopidogrel
75 mgr/d ía y AAS 325 mgr/día durante noventa
y seis horas previas al procedimiento, excepto en el caso
referido anteriormente en que se realizó el tratamiento en
agudo y se administró la dosis de carga equivalente a
través de sonda nasogástrica durante el procedimiento6.
Controles postoperatorios
Luego de finalizado el procedimiento se continuó la anticoagulación con Heparina hasta la metabolización de la misma, momento en que se retiraron los catéteres introductores femorales continuando en todos los casos la antiagregación con Clopidogrel y AAS por 3 meses y AAS en forma permanente. Los pacientes tratados sólo con stent sin coils fueron antiagregados en el postoperatorio sólo con AAS.
RESULTADOS
La oclusión aneurismática se realizó con stent
Neuroform y se completó en treinta y tres pacientes la
oclusión con coils Matrix biológicamente activos. En
nueve casos fueron aneurismas previamente tratados
con coils con signos de recanalización del cuello aneurismático
de los cuales cinco fueron tratados previamente
en agudo con técnica de coils en el contexto de
hemorragia subaracnoidea. Dos pacientes fueron tratados
con técnica de stent únicamente debido al
tamaño del aneurisma y en un caso fue discontinuado
el procedimiento por imposibilidad de liberar el stent.
En dos de los casos los coils quedaron atrapados en el
ángulo de una celda del stent y debieron ser desprendidos
en esa situación. En un caso de aneurisma
intracavernoso durante el intento de realizar el posicionamiento
del microcatéter previo al ascenso del
stent se produjo una perforación del saco aneurismático,
lo que produjo una fístula carotidocavernosa
directa, por lo que tratado el aneurisma se ascendió
por vía venosa y se ocluyó la misma, sin consecuencias
clínicas para el paciente. En un aneurisma cartidooftálmico
se produjo durante la liberación del stent la
perforación de un ramo silviano con la microguía
Transend 300 sobre la cual se ascendió el stent, la
oclusión aneurismática fue completada y se instauró
tratamiento de la hemorragia subaracnoidea a pesar
de lo cual la paciente falleció a las 48 hs de finalizado
el procedimiento. Un paciente presentó fenómenos
tromboembólicos al duodécimo día postratamiento y
otro presentó un hematoma retroperitoneal que remitió
espontáneamente.
Se realizó control angiográfico diferido a veinticinco
pacientes, observando recanalización parcial en cuatro
casos, uno de los cuales requirió retratamiento. En
nueve pacientes hubo progresión de la oclusión; de los
tratados únicamente con stent, se realizó seguimiento
evolutivo con angiografía a uno de ellos, observando
oclusión total del pseudoaneurisma. En la evaluación
angiográfica a los tres meses se observaron, en tres
casos, signos de estenosis en el segmento cubierto por
el stent: en estos pacientes se continuó la antiagregación
y reevaluados angiográficamente a los seis meses,
se observó remisión total de la estenosis en un caso y
parcial en dos.
DISCUSIÓN
El tratamiento endovascular de los aneurismas comenzó
a fines del siglo pasado con la oclusión del vaso
portador con microbalones desprendibles en los casos
en que la cirugía por la morfología aneurismática o la
localización del mismo no era posible7.
El objetivo de la técnica endovascular fue excluir el
aneurisma de la circulación sin afectar el vaso portador.
Es así como se trataron aneurismas colocando balones
desprendibles en el saco aneurismático o espirales8.
Estos últimos fueron desarrollados logrando espirales de
liberación controlada por electrolisis o por medios mecánicos
que permiten ocluir con mayor precisión y seguridad
los aneurismas cerebrales9. A partir de allí, comenzó
una competencia entre la neurocirugía convencional y la
endovascular por el tratamiento de los aneurismas cerebrales,
evolucionando además los protocolos de inclusión
de los mismos en los diferentes tipos de tratamiento.
Desde el punto de vista endovascular, se comenzaron a
tratar como indicación primaria los aneurismas intracavernosos
y de circuito posterior por considerar a esta
técnica de menor morbimortalidad que la cirugía a cielo
abierto; en la actualidad se ha realizado sólo un trabajo
controlado randomizado comparando ambas técnicas, el
ISAT1, que indica que la morbimortalidad al primer año
y calidad de vida de un aneurisma que debuta con una
hemorragia subaracnoidea es superior en el paciente
tratado por vía endovascular.
A pesar de lo antes enunciado se continúa discutiendo
al tratamiento endovascular por la durabilidad
y estabilidad de la oclusión obtenida con el concerniente
riesgo de recanalización y resangrado. Nuestro
equipo ha comunicado recientemente la mayor recanalización
de aneurismas de cuello mayor a cuatro
milímetros tratados en la etapa temprana de la hemorragia2.
Con el objeto de disminuir el índice de recanalización
se han desarrollado coils biológicamente activos,
los cuales cuentan con un recubrimiento de ácido
poliláctico poliglicólico que promueve la agregación
plaquetaria y fibrosis intraaneurismática para promover
la endotelización del cuello. De todas maneras es
una limitante tanto para la cirugía convencional como
la endovascular el tratamiento de los aneurismas de
cuello amplio y los aneurismas fusiformes.
En los últimos años se ha intentado la reconstrucción
de la pared arterial con stent, basados en la
experiencia desarrollada en la patología obstructiva
de vasos coronarios y periféricos. Se han colocado
stent coronarios en vasos cerebrales, encontrando
como limitaciones en estos la navegabilidad, debido a
que se liberan premontados en un balón que los
impacta en la arteria pudiendo esto provocar una
ruptura del vaso portador o disección del mismo; otra
limitante es el fenómeno tromboembólico generado
por el stent lo que puede desencadenar la oclusión del
vaso problema o sus ramas4-10. En gran medida, las
limitaciones descriptas son en parte por intentar
extrapolar la patología coronaria de la de vasos intracraneales
cuando la anatomía y la fisiología de los
mismos son diferentes.
En base a esta experiencia se desarrollaron microstent
para uso cerebral adaptados a las necesidades de
reconstruir arterias intracraneanas. Éstos son de tipo
autoexpandibles por lo que no requieren que se infle un
balón para su expansión y liberación evitando posible
daño vascular, mejorando la navegabilidad del stent. El
perfil de la malla del stent es cuatro veces menor que en
los stent cardiológicos, lo que disminuye el riesgo de
tromboembolia a punto de partida del implante.
Uno de estos implantes es el stent Neuroform Boston
Scientific®, producto que ha sido utilizado por nuestro
equipo y del que analizado las sucesivas versiones.
En los stent Neuroform de primera y segunda generación
observamos dificultad en la navegación y liberación
de los mismos, problema realmente mejorado en la
tercera generación. El único caso de perforación arterial
producido fue con un stent de segunda generación, los
que presentaban para su avance una mayor fricción
acumulando tensión sobre la cuerda guía, con bruscos
avances de su extremo distal con lesión de la pared
arterial. Este problema fue mejorado en los stent de
tercera generación debido a que presentan un catéter y
estabilizador del sistema de mayor rigidez, lo que disminuye
el roce del sistema sin limitar la navegabilidad. Se
disminuyó además el número de soldaduras entre las
tramas del stent lo que brinda mayor flexibilidad del
stent durante su ascenso.
Está comprobado que la colocación de stent sin
completar la oclusión del aneurisma con coils no evita
el resangrado. De todas maneras, en los casos en que
la morfología del aneurisma no permitió colocar coils,
se ha intentado reconstruir el segmento arterial sólo
con stent11.
En nuestra serie los pacientes tratados de esta manera
presentaban en un caso, el segmento vascular afectado
por una disección vertebral y un pseudoaneurisma
asociado en el cual se observa oclusión total del aneurisma
en el control diferido. El otro caso fue un aneurisma
pequeño que no permitía colocar coils por su tamaño por
lo que se liberó sólo el stent y el control angiográfico
diferido del paciente aún no se ha realizado.
Es una limitante en la utilización de los stent
intracraneanos la necesidad de antiagregación previa,
lo que limita su utilidad en el contexto de una hemorragia
subaracnoidea.
En el seguimiento angiográfico diferido se observa
una mayor estabilidad y progresión de la oclusión
aneurismática en algunos casos en proporción mayor a
la observada en la embolización de aneurismas sin la
asistencia de stent. En un 8,6% de los casos se observó
fenómeno de estenosis a nivel del stent el cual en un
2,8% remitió totalmente. Esto indica, a pesar de que el
número de la muestra no es estadísticamente significativo,
una mayor estabilidad en la oclusión en aneurismas
de cuello amplio.
La técnica de stent nos permite tratar no sólo el
aneurisma cerebral sino también en casos seleccionados
el segmento arterial afectado, intentando prevenir
el fenómeno evolutivo que en ciertos pacientes significa
la enfermedad aneurismática12.
CONCLUSIONES
Los stent intracraneanos Neuroform originales han mostrado dificultades en la navegabilidad y liberación, la que ha sido mejorada en las distintas generaciones, mostrando además la posibilidad de reconstruir la anatomía vascular cerebral en aneurismas de cuello amplio con una importante estabilidad en la oclusión aneurismática. La técnica de stent y coils, si bien reproducible, presenta aún riesgos de isquemia y estenosis tardía intrastent, por lo que sólo debe ser utilizada en aquellos casos en los cuales la anatomía del cuello aneurismático así lo exija.
COMENTARIO
El trabajo presentado posee un gran valor científico
ya que aporta una alternativa de tratamiento más a un
problema de muy difícil resolución como son los aneurismas
de cuello amplio. Expone claramente la técnica
endovascular utilizada y muestra con total transparencia
los resultados obtenidos, considerando más lo anatomico-
morfologico que los resultados de morbi-mortalidad.
Es una interesante población de 35 pacientes,
que si bien como dicen los autores no alcanza a ser
significativa, nos da una idea suficiente de las ventajas
y desventajas de su utilización.
Queda demostrado que las técnicas endovasculares
no son mínimamente invasivas como habitualmente
se trata de hacer creer a la población en general y queda
acabadamente demostrado en la minuciosa y sincera
evaluación de los resultados de este trabajo donde se
observa que existen importantes complicaciones relacionadas
a la técnica.
Hubo un 2,8% de mortalidad y no se constató la
morbilidad de la serie si bien se describe un paciente con
fenómenos trombo embólicos a los 12 días del procedimiento
sin presentar las consecuencias clínicas y tres
estenosis del segmento arterial en el lugar del stent. Un
caso fallido. Entre otras complicaciones relacionadas a la
técnica se mencionaron dos casos con coils desprendidos
parte por fuera del stent, un caso de ruptura
aneurismática y otro caso de ruptura arterial.
Finalmente existió una franca recanalización de 4
pacientes que significa un 12% y una tasa de oclusión
total sólo del 30% (10/33)
Se trataron dos casos sólo con stents sin coils,
siendo uno un seudoaneurisma por disección arterial
que se trata de una patología distinta con otra fisiopatogenia
y quizás no seria recomendable su inclusión
dentro de los resultados y sí su inclusión en el manejo
de las disecciones arteriales intracerebrales. El otro
caso no tiene control angiográfico por lo que tampoco se
debiera tener en cuenta en los resultados finales.
En resumen existió una tasa de complicaciones
relacionadas a la técnica cercana al 25% ( 8/33 ) y una
tasa de recanalización aneurismática del 13,7% ( 4/29)
y una tasa de oclusión total solo del 30% (10/33). Se
debe señalar que, de esta población, 9 aneurismas
tratados con coils solamente en sesiones previas sufrieron
el fenómeno de recanalizacion y se les indicó
nuevamente la técnica endovascular de stent + coils.
Finalmente se dejo explicito los inconvenientes de
indicar este tipo de abordajes endovasculares en las
etapas en agudo de una HSA por ruptura aneurismática.
Coincido con los autores en que no es una técnica
exenta de riesgos y por lo expuesto, tanto las complicaciones
relacionadas a la técnica como las tasas de
recanalización son todavía altas y hacen pensar que no
estamos en presencia de la solución al problema de los
aneurismas de cuello amplio y mucho menos de aquellos
que son grandes o gigantes. Estos últimos son un
real y actual problema tanto para las técnicas endovasculares
como las microquirúrgicas. Sin embargo estas
ultimas no debieran ser absolutamente descartadas
sobre todo para los aneurismas que siendo de cuello
amplio, son de pequeño tamaño y pertenecientes a la
circulación anterior; ya que han demostrado ser eficaces
tanto en sus resultados anatómicos como clínicos.
Se citó en varias oportunidades el ISAT I y II que son
trabajos que debieran ser cotejados solo en el marco de
pacientes con aneurismas tratados en agudo con HSA
reciente y en donde se evalúe no la técnica en sí misma
sino solo la evolución clínica.
A pesar de las apreciaciones y criticas constructivas
realizadas a este trabajo debo remarcar y resaltar que
se trata de un gran aporte al manejo de una patología
que tiene muchas aristas sin resolver y que ha sido
realizado con enorme rigor científico y con altísima
seriedad y transparencia en sus resultados finales.
Quisiera felicitar al autor y al grupo de trabajo que
dirige el Dr Luis Leme Plagos por seguir adelante
intentando buscar dentro de las técnicas endovasculares
la mejor de las opciones para estos pacientes.
Carlos Guido Gioino
1. Molyneux AJ, Kerr RS, Yu L-M, Clarke M, Senade M, Yarnould JA et al. International Subarachnoid Aneurysm Trial (ISAT) of neurosurgical clipping versus endovascular coiling in 2143 patients with ruptured intracranial aneurysms: a randomised comparison of effects on survival, dependency, seizures, rebleeding, subgroups, and aneurysm occlusion. Lancet 2005; 366: 809-17.
2. Casagrande W, Garbugino S, Lemme Plaghos L. Tratamiento endovascular con sistema de GDC de aneurismas del segmento carotideo de la arteria comunicante posterior: experiencia en 100 casos. Rev Argent Neuroc 2004; 18: 1-9.
3. Moret J, Cognard C, Weill A, Castaings L, Rey A. Recontruction technique in the treatment of wide-neck intracranial aneurysms: Long-term angiographic and clinical results- Report of 56 cases (in French). J Neuroradiol 1997; 24: 30-44.
4. Wakhloo AK, Schellhammer F, de Vries J, Haberstroh J, Schumacher M. Self-expanding and balloon expandable stents in the treatment of carotid aneurysms: An experimental study in a canine model. AJNR Am J Neuroradiol 1994; 15: 493-502.
5. Wakhloo AK, Lanzino G, Lieber BB, Hopkins LN. Stents for intracranial aneurysms: The beginning of a new endovascular era? Neurosurgery 1998; 43: 377-9.
6. Fiorella D Thiabolt L, Albuquerque FC, Deshukh VR, McDougall CG, Rasmussen PA. Anti-platelet therapy in neuroendovascular therapeutics. Neuosurg Clin N Am 2005; 16: 517-40.
7. Debrun G, Lacour P, Caron JP, Hurth M, Comoy J, Keravel Y. Detachable balloon and calibrated-leak balloon techniques in the treatment of cerebral vascular lesions. J Neurosurg 1978; 49: 635-49.
8. Casasco A, Aymard A, Gobin P, Houdart E, Rogopoulos A, George B et al. Selective endovascular treatment of 71 intracranial aneurysms with platinum coils. J Neurosurg 1993; 79: 3-9.
9. Byrne JV, Sohn MJ, Molyneux AJ Chir B. Five year experience in using coil embolization for ruptured intracranial aneurysms: Otcomes and incidence of late rebleeding. J Neurosurg 1999; 90: 653-63.
10. Lylyk P, Ferrario A, Pasbon B, Miranda C, Doroszuk G. Buenos Aires experience with the Neuroform self-expanding stent for the treatment of intracranial aneurysms. J Neurosurg 2005; 102: 235-41.
11. Fiorella D, et al. Endovascular reconstruction with the Neuroform stent as monotherapy for the treatment of uncoilable intradural pseudoaneurysms. Neurosurgery 2006; 59: 291-300.
12. Higashida RT, Smith W, Gress D, Urwin R, Dowd CF, Balousek PA, Halbach VV. Intravascular stent and endovascular coil placement for a ruptured fusiform aneurysm of the basilar artery: Case report and review of the literature. J Neurosurg 1997; 87: 944-9.