
Figura 1
Cambios clínicos, hemáticos y coagulativos consecuentes al aumento de anticuerpos en equinos productores de suero antiofídico
Bogado, F.1; Núñez, S 2; Mussart, N.B.3; Leiva, L.4; Acosta, O.C.1
1 Departamento Clínicas,
2 Cátedra de Inmunología,
3 Cátedra de Fisiología, Facultad de Ciencias Veterinarias,
UNNE, Sargento Cabral 2139, Corrientes (3400), Argentina.
4 Cátedra de
Química Biológica I, Facultad Ciencias Exactas, UNNE.
E-mail: patmed@vet.unne.edu.ar.
Resumen
El objetivo del trabajo consistió en estudiar los efectos clínicos, hemáticos y coagulativos, así como la producción de anticuerpos en tres equinos inmunizados para la producción de suero antiofídico monovalente contra Bothrops alternatus y evaluar los resultados obtenidos correlacionando la respuesta inmune humoral con el estado de salud de los animales. Los resultados indicaron que la inmunización de los equinos con el protocolo utilizado, indujo alteraciones clínicas menores y cambios en ciertos parámetros del hemograma y pruebas coagulativas. Se registraron variaciones de la capacidad neutralizante sobre distintos componentes del veneno, en especial las toxinas que afectan la coagulación de la sangre. Asimismo, se constató una correlación directa entre las tasas séricas de leucocitos y la producción de inmunoglobulinas. Los resultados indicaron que el período de descanso de un trimestre resulta extenso y causa una franca disminución del título de anticuerpos, perdiendo el suero capacidad neutralizante de la toxicidad del veneno; no obstante, al reanudar las inoculaciones los equinos presentaron una rápida reposición de los anticuerpos anti-toxinas de B. alternatus, tolerando altas dosis de veneno en el segundo período de inmunización.
Palabras clave: Equino; Inmunización; Bothrops alternatus; Hemograma; Coagulación.
Clinical, hematological and coagulative changes consequent to antibody level increase in horses destined to antivenom production.
The aim of this work consisted to study the clinical and hematological effects that included blood coagulation and antibody production of a group of three horses immunized for the production of monovalent serum against Bothrops alternatus venom, in order to correlate the results with the humoral immune response of the animals. The results showed that immunization of horses with the essayed protocol induce slight clinic alterations and discrete changes in some parameters of the hemogram. Results also showed variations in the neutralizing capacity of the serum on different venom components, particularly toxins that affect blood coagulation. Also, it was verified a direct relationship between the rate of white blood cells and serum immunoglobulin production. Furthermore, they also indicate that the three-month rest period may be considered as too long as it causes a marked decrease in antibody titles, losing the serum its neutralizing capacity to venom compounds. Nevertheless, after re-administration of venom horses provided a rapid reposition of anti-toxins against B. alternatus venom, tolerating high venom doses during this second period of immunization.
Key words: Horse; Immunization; Bothrops alternatus; Hemogram; Coagulation.
Recibido: 27 diciembre 2012
Aceptado: 7 mayo 2013
Proyecto PFIP/2005 - COFECyT
INTRODUCCIÓN
El litoral argentino es habitado por varias especies de serpientes de la familia Viperidae, entre ellas Bothrops alternatus (yarará grande, víbora de la cruz), responsable de la mayoría de los accidentes que ocurren en dicha región cuando la serpiente muerde descargando su secreción salival (veneno) en la víctima
14.
El tratamiento de la intoxicación ofídica consiste en la
administración de inmunoglobulinas, anticuerpos que
neutralizan las toxinas del veneno. Tales anticuerpos
se obtienen del suero de equinos previamente inmunizados, por ello se lo conoce como suero antiofídico
hiperinmune equino
10.
Para estimular la producción de estos anticuerpos
los caballos son sometidos a dosis sub-letales progresivas de veneno, las cuales no causan la muerte del animal sino que estimulan al sistema inmune para producir
inmunoglobulinas contra las distintas proteínas inoculadas. La administración del antiveneno específico para
el tratamiento de las mordeduras por ofidios ponzoñosos es una práctica mundialmente aceptada
8, 9, 12.
Los antígenos que reciben los equinos en el proceso
de inmunización les generan cambios fisiopatológicos
no bien evaluados hasta la fecha. Estudios realizados
por otros investigadores han demostrado alteraciones
en el medio interno, evidenciadas a través de pruebas
hematológicas y bioquímicas
1. Es importante identificar tales anomalías sistémicas porque la composición
de los venenos varía con la región geográfica que habitan las serpientes
3, de allí la sugerencia de la OMS en
el sentido que los sueros sean producidos por inmunización de mamíferos a partir del veneno de serpientes
de la región en que serán utilizados los sueros hiperinmunes obtenidos
8, 10.
El propósito del trabajo fue estudiar los efectos de la
inmunización con veneno de B. alternatus sobre algunos parámetros semiológicos, sanguíneos y hemostáticos del caballo, y correlacionarlos con la magnitud de la
respuesta inmune humoral (producción de anticuerpos).
MATERIAL Y MÉTODOS
Animales. Se utilizaron tres equinos adultos de 3 a
4 años de edad, con pesos de 450 a 550 kg. Previamente
a la inmunización los animales fueron desparasitados
y sometidos a controles semiológicos y de laboratorio,
incluyendo el test de Coggins (Immunology Lab.) para
descartar la presencia de anemia infecciosa equina.
Luego de cada vacunación los animales fueron nuevamente objeto de controles clínicos y extracciones de
sangre para distintos estudios.
Preparación de la vacuna. El veneno de B. alternatus fue obtenido de ejemplares adultos del serpentario
del Zoológico de la Ciudad de Corrientes (Argentina).
Luego de la extracción, el pool de veneno fue centrifugado para descartar residuos y desecado, manteniéndose a -20°C hasta el momento de su uso. Para la inmunización, se disolvió en buffer fosfato (PBS, pH 7,2)
y se filtró a través de una membrana de nitrocelulosa
de 0,22 µm (Millipore). Finalmente fue mezclado con adyuvante de Freund completo en la primera vacunación y adyuvante de Freund incompleto en las restantes.
Protocolo de inmunización. El volumen inoculado
en cada animal fue de 10 ml, los que se aplicaron por
vía SC en dosis de 2 ml en 5 puntos diferentes de la
tabla del cuello, acorde al siguiente detalle: dosis inicial
de 0,75 mg más adyuvante de Freund completo, continuándose con dosis sucesivas crecientes a intervalos de
21 días a razón de 1,5; 5,0; 5,5; 10; 15; 22; 30; 45 y 45 mg
(dosis expresadas en mg de veneno), en estos casos con adyuvante de Freund incompleto. Luego de un período
de descanso de 3 meses se realizó la revacunación con
dosis de 15 y 30 mg de veneno con adyuvante Freund
incompleto para medir la respuesta inmunológica.
Estudio clínico. Inicialmente y durante el proceso
de inmunización se controló el estado clínico de cada
equino, incluyendo la exploración del área de vacunación, auscultación de los sistemas cardíaco, respiratorio y digestivo, así como examen de mucosas y conjuntivas aparentes.
Hemograma. Previamente al inicio de las vacunaciones y 24 horas después de cada una de ellas, se tomaron muestras de sangre de los equinos con anticoagulante EDTA (1 gota cada 5 ml de sangre), para obtener los valores del hemograma. Tal estudio comprendió las determinaciones de hematocrito (capilares centrifugados a 12.000 rpm), hemoglobina (método fotocolorimétrico de Drabkin, lecturas a 540 nm), recuento de
leucocitos (en analizador electrónico Sequoia-Turner
500) y fórmula leucocitaria (recuento microscópico diferencial de 200 células a partir de frotis coloreados
con Giemsa, reactivos Biopur).
Cuantificación de anticuerpos. Para la determinación de los títulos de anticuerpos, las muestras sanguíneas fueron obtenidas previamente a cada administración del inóculo (sin anticoagulante) cada 21 días. La
valoración sérica se realizó mediante enzimoinmunoensayo (ELISA). Para ello, en policubetas de 9x12 fosas se
fijaron moléculas de antígeno (veneno) por interacciones
hidrofóbicas a las paredes de las cubetas, colocándose
100 µl de una solución antigénica de 10 µg/ml y se incubó 1 h a 37C°. Luego se efectuaron diluciones seriadas
de los sueros equinos. El revelado se realizó por el agregado de una anti-gammaglobulina de equino conjugada
a una peroxidasa (Anti-Horse Immunoglobulin Conjugate-AIgG, Sigma 6154) en una dilución de 1/10.000.
Como sustrato de la enzima se utilizó una solución de
orto fenilendiamina (1 mg/ml en buffer sustrato). La
reacción se detuvo con el agregado de una solución de
H2SO4 3N luego del desarrollo de color. La densidad óptica se midió en un lector de microplaca a 492 nm
16.
Pruebas de coagulación. Empleando plasma citratado obtenido de equinos en estado basal, a las 1, 3,
6 y 24 h posteriores a la inyección de cada dosis de
veneno, se realizaron pruebas de laboratorio para determinar el tiempo de protrombina (método de Quick),
recalcificación plasmática (Howell) y fibrinógeno (von
Clauss). Finalizado el protocolo se evaluó la capacidad
neutralizante del suero del equino inmunizado sobre la
actividad coagulante del veneno botrópico.
Pruebas de neutralización. Las muestras ensayadas consistieron en mezclas de veneno (4 mg/ml) preincubadas con igual volumen de suero equino hiperinmune de cada instancia del sangrado. El veneno entero
preincubado con PBS fue utilizado como control de referencia (máxima actividad) para calcular el porcentaje
de neutralización de cada actividad.
Neutralización de la actividad hemolítica. La neutralización de la actividad hemolítica se evaluó a través de hemólisis radial indirecta. Las muestras se sembraron en placas de agar-sangre enriquecidas con lecitina
de huevo, los halos de hemólisis fueron valorados luego
de 20 h de incubación a 37ºC 5. Como control positivo
de la actividad se sembró una mezcla en la cual se omitió el suero equino reemplazándolo por igual volumen
de PBS.
Neutralización de la actividad proteolítica. Para
evaluar la capacidad neutralizante de la actividad proteolítica se empleó como sustrato azocaseína
18. En un
espectrofotómetro se midió la absorbancia a 450 nm,
utilizándose un blanco de reacción en el cual se omitió la fracción de veneno, reemplazada por igual volumen
de PBS. Como control positivo de la actividad se omitió el suero equino reemplazándolo por igual volumen
de PBS.
Neutralización de la actividad coagulante. La actividad coagulante se midió en coagulómetro (Fibrintimer Wiener Lab.) con suero hiperinmune pre-incubado
con veneno entero, posteriormente adicionado con
igual volumen de plasma humano citratado. Se tomó como control positivo la misma dosis de reto de veneno
incubada con PBS
17.
Estadísticas. Los cálculos estadísticos fueron enmarcados en un diseño completamente aleatorizado,
con arreglo factorial 4 por 7 (4 tiempos de control postinoculación 7 dosis diferentes de veneno). Se efectuó estadística descriptiva (media aritmética, desvío estándar), a los fines de estimar el comportamiento de los datos. Posteriormente los resultados fueron sometidos a
comprobación de los supuestos de normalidad (Wilk-Shapiro) y homocedasticidad de las variancias (Levene) y por las características del diseño se cumplió con
el supuesto de independencia. El grado de asociación
lineal entre variables se evaluó mediante el coeficiente
de correlación de Pearson. Por último se procedió a realizar el análisis de la varianza (ANOVA), teniendo en
cuenta la aparición de interacción entre la dosis aplicada y el tiempo post-inoculación, por lo cual se realizan
particiones según el tiempo transcurrido desde la aplicación del veneno. Para aquellas variables en las que
se detectaron diferencias, las medias se compararon
mediante la prueba de Tukey. Para todas las inferencias
se estableció un riesgo alfa del 5%.
RESULTADOS
Cuadro clínico. Todos los animales sometidos al
test de Coggins resultaron negativos y durante toda la
experiencia se mantuvieron con coprología cuantitativa menor de 100 huevos/g. La inmunización de los
equinos con veneno de B. alternatus causó reacciones
orgánicas que se manifestaron a nivel local, además
de modificaciones de los valores del hemograma, de la
coagulación de la sangre y de los tenores de anticuerpos. Los signos clínicos más relevantes se iniciaron a
pocos minutos de la aplicación de la vacuna, siendo
bien evidentes a los 10 min, con edema en el sitio de
aplicación, inquietud, hipotensión leve valorada por el decaimiento, anorexia y en algunos casos adopción
de la posición de decúbito. El edema se limitó a las áreas de vacunación y transcurridas 2-3 h se intensificó extendiéndose a regiones vecinas (gran parte del
cuello, pecho y miembros), resolviéndose en el término
aproximado de 72 h.
La intensidad de la respuesta local se atenuó en las
sucesivas vacunaciones (desde la cuarta en adelante),
limitándose a una reacción intensa que duraba poco
tiempo y se resolvía en menos de 24 h. El estado de
hipotensión se presentó únicamente tras la primera vacunación. Las inoculaciones provocaron molestias en
el cuello dificultando la aprehensión de los alimentos
sin afectar el apetito, ya que los animales comían sin
dificultad al ofrecerle la pastura sin necesidad de inclinar el cuello.
La frecuencia cardíaca reveló bradicardia a los 10
min post-inoculación, registrándose valores de hasta
18 rpm, que se normalizaban luego de transcurrir la
primera hora. Se verificó incremento de la frecuencia respiratoria (taquipnea de tipo costo-abdominal
superficial), que alcanzó valores de hasta 55 cpm. La
temperatura registró un aumento de hasta 1,5ºC en los pacientes vacunados, regularizándose dentro de las 24
h. En uno de los animales se constató incremento de la
coloración de la mucosa palpebral.
Los equinos inoculados mostraron disminución de
los movimientos intestinales (borborigmos), sin presentar íleo adinámico ni manifestaciones de cólico. Es
importante destacar que los signos clínicos relacionados a los aparatos circulatorio y respiratorio se mantuvieron estables a pesar del aumento de la dosis del
inóculo.
Parámetros de la coagulación. Las primeras vacunas causaron incoagulabilidad sanguínea en todos los
animales a partir de las 3 h post-inoculación, manteniéndose así durante 24 h para luego retornar a la normalidad. Posteriormente se verificó la normalización
de los tiempos de protrombina (Figura 1) y de recalcificación (Figura 2). Los niveles de fibrinógeno (Figura
3) variaron en forma concordante con los tiempos de
protrombina y recalcificación. El tercer refuerzo solo
afectó ligeramente los parámetros hemostáticos, comportamiento que se repitió a lo largo de todo el protocolo, indicando que los anticuerpos formados neutralizaron los componentes del veneno causantes de las
alteraciones coagulativas.

Figura 1
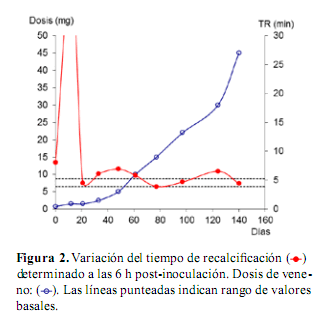
Figura 2

Figura 3
Hemograma. Luego de las inmunizaciones se observaron algunas modificaciones en el hemograma
de los equinos vacunados, tanto en la serie roja como
blanca. El hematocrito disminuyó a partir de la primera dosis de veneno, pero luego reveló una recuperación
gradual. El promedio de los valores basales del hematocrito de los tres equinos bajo ensayo fue de 33,67±2,1%, valor que ante la primera dosis de veneno (1,5 mg) se
redujo a 30,2% y se acentuó ante las dosis siguientes de
2,5 mg (28,0%) y 5,5 mg (27,33%). A partir de la dosis
de 15 mg se advirtió una recuperación (30,6%) que continuó con la dosis de 45 mg (31,33%, p<0,0001).
Los valores de hemoglobina (Figura 4) no se redujeron luego de las dos primeras vacunas a pesar de
las posibles pérdidas de sangre por hemorragia. Luego,
su evolución fue coincidente con los valores del hematocrito: disminuyó ligeramente con las dosis de 2,5 y
5,5 mg de veneno para mostrar luego una recuperación
gradual. A pesar de que el protocolo de vacunación se
extendió hasta el día 160, en la figura se grafican los
resultados hasta el día 120 debido a que desde allí en
adelante se mantuvieron sin modificaciones.
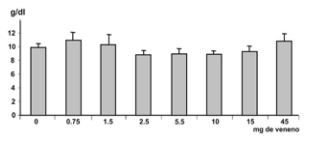
Figura 4. Variaciones de la hemoglobina (media aritmética y desvío estándar) según la dosis de veneno
inoculado.
La concentración de leucocitos totales (Figura 5) reveló un pronunciado ascenso inicial después de la primera vacunación y luego, con algunas fluctuaciones, se mostró moderadamente elevada hasta el final de la inmunización. La fórmula leucocitaria exhibió un marcado predominio de neutrófilos y consecuente disminución de linfocitos, cuyos más bajos porcentajes ocurrieron luego de la segunda dosis de veneno (Figura 6). Pese a que las inoculaciones prosiguieron hasta el día 160, en la figura se consignan las tasas obtenidas hasta el día 120 debido a que posteriormente no se registraron grandes modificaciones

Figura 5. Concentración de leucocitos (media aritmética y desvío estándar) según la dosis de veneno
inoculado.

Figura 6. Porcentajes de neutrófilos y linfocitos (media aritmética y desvío estándar) según la dosis de
veneno inoculado.
Títulos de anticuerpos. Durante el plan de inoculación se presentaron variaciones plasmáticas de los títulos de anticuerpos, en función de las dosis y tiempos de vacunación (Figura 7). En las re-vacunaciones, realizadas luego de un periodo de descanso, se observó una rápida respuesta en la producción de anticuerpos. Se advirtió que el período de tres meses de descanso resulta muy extenso y conduce a una franca disminución de los títulos de anticuerpos, con pérdida de la capacidad neutralizante del suero para ciertos componentes del veneno. Sin embargo, la reposición de los anticuerpos anti-toxinas de B. alternatus fue rápida, tolerándose dosis de 15 y 30 mg de veneno en el segundo periodo de inmunización.

Figura 7
Los ensayos de neutralización, donde el veneno preincubado con suero del equino inmunizado tornó incoagulable un plasma normal citratado, demostraron una efectiva respuesta inmunológica de los anticuerpos generados por los equinos (Tabla 1).
Tabla 1. Variaciones en la capacidad neutralizante del
suero equino hiperinmune.

R: reinoculación. Los números indican porcentaje de neutralización.
DISCUSIÓN
El caballo ha sido reportado como el mejor animal
productor de sueros hiperinmunes por su fácil manejo y
alto rendimiento de plasma
10. Para la producción de inmunoglobulinas, los animales son sometidos a vacunaciones sucesivas, con dosis crecientes de veneno. Cada
vacuna implica la administración de un paquete enzimático altamente nocivo que si bien no causa intoxicación severa, genera reacciones locales y sistémicas
que deben ser tenidas en cuenta. En Argentina existen
pocas investigaciones acerca de las alteraciones clínicas y hematológicas en animales sometidos a vacunaciones con venenos de serpientes para la producción de
anticuerpos. Sin embargo son bien conocidos los daños locales y sistémicos causados en seres humanos y
animales por la mordedura de serpientes como las del
género Bothrops ("yararás")
4, 14, 15.
En el presente trabajo las vacunaciones se efectuaron con un solo veneno e inicialmente con dosis bajas, por lo cual se registraron escasas manifestaciones
clínicas propias de la intoxicación botrópica leve. Los
animales bajo ensayo presentaron un ligero sangrado
local que cesó rápida y espontáneamente. Respecto a
los parámetros hemostáticos, cabría inferir que en la
primera dosis la cantidad de veneno presumiblemente
no haya sido suficiente para modificar el tiempo de coagulación. Sin embargo en la segunda dosis se evidenció un sensible aumento de esta prueba, para retornar a la
normalidad en el término de 24 h. El tercer refuerzo
sólo afectó ligeramente los parámetros coagulativos, comportamiento que se repitió a lo largo de todo el protocolo, indicando que los anticuerpos formados fueron
capaces de neutralizar los componentes del veneno que
afectan la coagulación sanguínea. En consecuencia no
se manifestaron coagulopatías sistémicas pese a que
tanto el tiempo de recalcificación del plasma como el
tiempo de protrombina, indicaron incoagulabilidad
sanguínea hasta las 24 h.
Tales resultados se correspondieron con los obtenidos en los ensayos de neutralización, donde el veneno
pre-incubado con suero del equino inmunizado tornó incoagulable un plasma citratado normal, demostrando
efectiva respuesta inmunológica por parte del equino,
al neutralizar proteínas tipo trombina contenida en el
veneno. Concomitantemente, en la segunda vacunación se verificó una brusca disminución del fibrinógeno sanguíneo, aunque las vacunaciones subsiguientes
solo causaron ligero consumo de dicha proteína. Ello
refuerza la certeza de la ausencia de trastornos hemostáticos en los equinos.
No obstante, utilizando bajas dosis de veneno para
la producción de sueros antiofídicos polivalentes con vacunas que se elaboran con mezclas de distintos venenos, otros investigadores habrían registrado efectos
más intensos
1. Por tales razones se han sugerido técnicas para minimizar la acción tóxica de los venenos en el proceso de inmunización, modificando sus propiedades químicas a través de métodos físicos; sin embargo
este proceso puede causar alteraciones estructurales
en las proteínas del veneno, con modificaciones de los
epítopos y consecuente alteración en los anticuerpos
formados contra las toxinas modificadas 6, 7, interfiriendo la eficiencia terapéutica de los anticuerpos en el
paciente accidentado. Por tales razones, en el presente
ensayo se utilizó únicamente veneno entero no modificado.
Las disminuciones del hematocrito aquí registradas luego de las primeras inoculaciones de veneno deberían atribuirse a pequeñas hemorragias indetectables
a la exploración clínica. Sin embargo, la hemoglobina
mantuvo inicialmente su nivel basal, quizás debido a
que el dolor causado por las inoculaciones interfirió con la ingestión de agua, generando hemoconcentración. Otros investigadores detectaron importantes disminuciones de hematocrito y hemoglobina en las fases
finales del protocolo de vacunación para la producción
de suero polivalente, utilizando mezclas de venenos de
diferentes serpientes del género Crotalus 1, situación
no observada en este trabajo.
Reducciones de hematocrito y hemoglobina también fueron registrados en el envenenamiento humano,
posiblemente a consecuencia de hemorragias ya que en
accidentes naturales la cantidad de veneno inoculado
puede superar, en mucho, a la dosis utilizada como vacuna en nuestro caso
2, 11, 13. En la presente experiencia,
las vacunas sucesivas estimularon la producción de
anticuerpos que impidieron efectos adversos sobre la
serie roja hacia el final del protocolo de vacunación.
La leucocitosis registrada a partir de la primera vacuna en los equinos aquí estudiados se debió al aumento de neutrófilos, los cuales permanecieron elevados
durante todo el proceso de inmunización. En accidente
humanos es típico, como en este caso, encontrar leucocitosis con neutrofilia
11, aunque en otros trabajos se
hallaron incrementos simultáneos de linfocitos
1.
Luego del período de descanso de 3 meses se comprobó que el suero de los caballos no presentaba capacidad neutralizante y que el título había descendido a
1:8000. No obstante, luego de la primer re-vacunación se constató una rápida elevación del título de anticuerpos, detectándose capacidad neutralizante parcial sobre las actividades proteolítica, hemolítica indirecta y
coagulante, mientras que en el segundo refuerzo, el
título alcanzó valores de 1:70000, con neutralización
total de las actividades coagulante y proteolítica, así como capacidad neutralizante parcial de la actividad
hemolítica indirecta. Estos resultados demuestran que
la respuesta inmunológica de los equinos frente a las
distintas toxinas del veneno es variable, dependiendo
probablemente de la capacidad inmunogénica de cada
antígeno, así como de su abundancia relativa en la composición del veneno total, por ello algunas antitoxinas
alcanzan títulos sensiblemente mayores que otras.
En conclusión, los resultados indican que la inmunización de los equinos con el protocolo utilizado para la producción de suero antiofídico monovalente contra B. alternatus, induce alteraciones clínicas y cambios en ciertos parámetros del hemograma. El estudio
también pone de relieve la variabilidad de la respuesta
inmune en su capacidad neutralizante sobre distintos
componentes del veneno, en especial las toxinas que
afectan la coagulación de la sangre, ya que dosis muy
bajas pueden poner en riesgo la salud de un animal de
más de 400 kg de peso. Asimismo, se constató correlación entre los niveles de glóbulos blancos circulantes
y la producción de inmunoglobulinas. Se destaca que
un trimestre es un periodo de descanso extenso, que
conduce a una franca disminución sérica del título de
anticuerpos y pérdida de la capacidad neutralizante de
la toxicidad del veneno, aunque el equino es capaz de
desplegar una veloz reposición de los anticuerpos antitoxinas de B. alternatus y tolerar altas dosis de veneno
en el segundo período de inmunización.
Agradecimientos. A la Dra M.E. García Denegri por su colaboración en la elaboración de algunas de las vacunas. Al MV J. Picot por su participación en los análisis estadísticos. A la Lic L. Rey y al serpentario del Zoológico de la Ciudad de Corrientes por aportar el veneno utilizado en el trabajo.
1. Angulo Y, Estada R, Gutiérrez JM. 1997. Clinical and laboratory alterations in horses during immunization with snake venoms for the production of polyvalent (Crotalinae) antivenom. Toxicon 35: 81-90.
2. Bolaños R. 1982. Las serpientes venenosas de centroamérica y el problema del ofidismo. Rev Cost Cien Med 3: 165-184.
3. Chippaux JP, Goyffon M. 1998. Venoms, antivenoms and immunotherapy. Toxicon 36: 823-846.
4. Esteso SC. 2005. Ofidismo en la República Argentina, Ed. Arpon, Córdoba (Argentina), 176 p.
5. Gutiérrez JM, Chávez F, Elizondo J, Ávila C, Cerdas L. 1988. Production of monovalent anti-Bothrops asper antivenom: development of immune response in horses and neutralizing ability. Rev Biol Trop 36: 511-517.
6. Hati RN, Mandal M, Hati AK. 1990. Active immunization of rabbit with gamma irradiated Russell's viper venom toxoid. Toxicon 28: 895-902.
7. Higashi HG, Guidolin R, Nishikawa AK, Yamaguchi IK, Lima ML, Diaz W. 1989. Venenos botrópicos pretratados com inibidores ativos para os sitios enzimáticos de proteases e com substancias quelantes preservam seu poder inmunogénico. Mem Inst Butatan 51: 107-115.
8. Organización Mundial de la Salud. 1969. Normas para los sueros inmunes de origen animal. Serie de Informes Técnicos Nº 413, Ed. OMS, Ginebra, p. 49-64.
9. Organización Mundial de la Salud. 1980. WHO Guidelines for the production control and regulation snake antivenoms immunoglobulins. http://who.int/bloodproduc ts/snake_antivenoms/snakeantivenomguideline.pdf.
10. Organización Panamericana de la Salud. 1977. Producción y pruebas de control en la preparación de antisueros difitérico, tetánico, botulínico, antivenenosos y gangrena gaseosa. Publ. OPS, Washington, p. 104-141.
11. Otero R, Tabón GS, Gómez LF, Osorio R, Valderrama R, Hoyos D, Urreta JE, Molina S, Arboleda JJ. 1992. Accidente ofídico en Antioquia y Chocó. Aspectos clínicos y epidemiológicos. Acta Méd Colomb 17: 229-249.
12. Reid HA, Theakston RD. 1984. Les morsures de serpent. Bull Org Mond Santé 62: 27-38.
13. Russell FE. 1980. Snake venom poisoning, Ed. J.B. Lippincott, Philadelphia, 562 p.
14. Ruiz RM, Ulón SN, Sario HM. 2004. Epidemiología del accidente ofídico en la Provincia de Corrientes. Sesión Comunic Científ Tecnol UNNE (Argentina), V-029.
15. Sanchez EF, Freitas TV, Ferreira DL, Velarde DT, Diniz MR, Cordeiro MN, Agostini G, Diniz CR. 1992. Biological activities of venoms from South American snakes. Toxicon 30: 95-103.
16. Theakston RD, Warrell DA, Griffiths E. 2003. Report of a WHO workshop on the standardization and control of antivenoms. Toxicon 41: 541-557.
17. Vieira DF, Watanabe L, Santana CD, Marcussi S, Sampaio SV, Soares AM, Arni RK. 2004. Purification and characterization of jararassin-I, a thrombin-like enzyme from Bothrops jararaca snake venom. Acta Biochim Biophys 36: 798-802.
18. Wang WJ, Huang TF. 2002. Purification and characterization of a novel metalloproteinase, acurhagin, from Agkistrodon acutus venom. Thromb Haemost 87: 641-650.