ARTÍCULOS
Evaluación morfológica y fenológica de 10 clones de yerba dulce (Stevia rebaudiana) según el tiempo térmico
Guerrero, D. R.1; Bär, A. 2; Kryvenki, M.1 y Domínguez, M.1
1Área Biotecnología Vegetal, EEA INTA Cerro Azul. guerrero.diego@inta.gob.ar
2Ing. Agr. Independiente.
Recibido 31 de octubre de 2013
Aceptado 06 de julio de 2015
publicado online 25 de noviembre de 2015
Resumen
El cultivo de la yerba dulce se está consolidando como una alternativa productiva para la provincia de Misiones. Este trabajo tiene como objetivo comparar variables morfológicas y tiempo térmico de las diferentes etapas y fases fenológicas en 10 clones de yerba dulce (tratamientos). Las observaciones se registraron desde septiembre de 2010 a abril de 2011. El cálculo del tiempo térmico se realizó con el método residual tomándose como temperatura base 10 ºC. Las variables morfológicas mostraron diferencias significativas entre algunos de los tratamientos para el número de hojas expandidas, número de tallos secundarios, número de entrenudos y altura de planta en cm; sin embargo no se registraron diferencias para el número de tallos primarios en ninguno de los clones. El clon T9-STK12 requirió el mayor tiempo térmico para completar la etapa vegetativa (1993 grados día). Para iniciar la etapa reproductiva (inicio de botón floral) los clones necesitaron acumular entre 1596 (T9-STK12) y 857 (T1-STE21) grados día desde el inicio de la brotación, habiendo además superposición de estas etapas en todos los clones. La etapa reproductiva se dividió en tres fases (botón floral, flor abierta y fructificación). Para finalizar esta última se requirieron entre 1664 (T1-STE21) y 925 (T9-STK12) grados día. El presente trabajo permitió cuantificar variables morfológicas de los clones desconocidas anteriormente y evaluar su comportamiento fenológico. Estos resultados podrían ser utilizados para establecer diferentes técnicas apropiadas de manejo del cultivo (cosecha de hojas y semillas) y para la selección de nuevos materiales genéticos a partir de cruzamientos controlados.
Palabras claves: Grados-día; Fase; Etapa; Método residual.
ABSTRACT
Sweet herb crop is consolidating as a productive alternative for Misiones province. The aim of this work was to compare ten clones of Stevia (treatments) with respect to morphological variables and thermal time accumulation in the different phenological stages and phases. Observation period was September 2010 to April 2011. Residual method was used to calculate degree-days, taking 10 °C as base temperature. Morphological variables showed significant differences between treatments for number of expanded leaves, number of secondary stems, number of internodes and plant height in cm, and not for number of primary stems. Clone T9-STK12 required the greatest thermal time accumulation to complete vegetative stage (1993 degree days). To inicciate reproductive stage (flower bud) clones needed to accumulate between 1596 (T9-STK12) and 857 (T1-STE21) degree-days. Overlapping stages were observed in all treatments. Reproductive stage was divided into three stages (flower bud, open flower and fruit) and required to be complete between 1664 (T1-STE21) and 925 (T9- STK12) degree-days. This work allowed us to quantify morphological variables previous unknown for these clones and to evaluate their phenological behaviour. These results could be useful to establish appropriate crop management (leaves or seeds harvesting) and selection of new genetic material from controlled crossing.
Keywords: Degree-days; Phase; Stage; Residual method.
INTRODUCCIÓN
En los últimos años, en la provincia de Misiones se ha
generado la necesidad de diversificar la producción agrícola
basada fundamentalmente en los cultivos de yerba mate,
té y tabaco. Una de las alternativas que ha surgido es la
producción de yerba dulce.
La yerba dulce es una planta perenne y herbácea, posee
una raíz poco profunda que se distribuye cerca de la superficie
del suelo (Bondarev et al., 2003) y su tallo es subleñoso,
con tendencia a inclinarse. Durante su desarrollo
inicial no posee ramificaciones tornándose multicaule después
del primer ciclo vegetativo. En condiciones óptimas,
el tallo puede llegar hasta un metro y medio de altura
(Sagakuchi y Tatasuiko, 1982; Guedes et al., 2014). Las
hojas son elípticas, ovales o lanceoladas, simples, de bordes
dentados, algo pubescentes, distribuidas en verticilos
alternos; de color verde oscuro brillante y superficie rugosa,
de hasta 5 cm de largo por 2 cm de ancho. Esta es la parte
vegetal mayormente utilizada como endulzante (Sojearto
et al., 1983, Melis et al., 2009), siendo unas 30 veces más
dulces que el azúcar de caña (Rojas Montoya 2009). De
estas se extraen, a partir de diversas técnicas, los distintos
componentes que contienen propiedades edulcorantes (Lv
et al., 2014), siendo los más importantes el esteviósido y
el rebaudiósido A (Midmore y Rank, 2002), que en su forma
pura son 200 a 300 veces más dulces que la sacarosa
(Cardello et al., 1999; Prakash et al., 2008; Lorenzo
et al., 2014). Sin embargo se siguen registrando nuevos
glicósidos de diterpeno, los cuales también pueden adquirir
importancia (Ibrahim et al., 2014). La flor es hermafrodita
tubular, chica y blanquecina, sin fragancia perceptible,
encontrándose en capítulos pequeños terminales o axilares,
agrupados en panículas corimbosas (Rojas Montoya,
2009, Shock, 1982). La planta es autoincompatible; para
desarrollar embriones fértiles es necesaria la polinización
cruzada principalmente realizada por insectos. El fruto es
un aquenio que se disemina fácilmente por el viento, estos
se clasifican en: claro estéril, oscuro fértil y oscuro estéril
(Carneiro 1990). La multiplicación de esta planta puede
realizarse en forma sexual partiendo de semillas o asexual
a partir de estacas (Casaccia y Álvarez, 2006), división de
matas o porciones de hojas y ápices (Nower, 2014). Para
esto se utiliza macropropagación (Kryvenki et al., 2007) o
cultivo de tejidos a través de la micropropagación (Jain et
al., 2012; Vázquez-Baxcajay et al., 2014). Esta última técnica
es muy estudiada por muchos investigadores porque
permite una alta tasa de multiplicación en períodos cortos
de tiempo (Singh y Dwivedi, 2013; Razak et al., 2014;
Fakhrul et al., 2014).
El crecimiento y desarrollo de la yerba dulce está influenciado
en forma directa por los factores climáticos (Molero,
1984), por este motivo el conocimiento fenológico es relevante
ya que permite generar información sobre las variaciones
que ocurren en las plantas (Bello, 1988). Analizando
la importancia del conocimiento de los eventos fenológicos,
sumada a la falta de información de estos en yerba dulce,
se advierte el valor de su estudio. A partir de lo mencionado
se plantea el siguiente objetivo de trabajo: comparar variables
morfológicas y el tiempo térmico de las diferentes etapas
y fases fenológicas en 10 clones de yerba dulce. Las
variables morfológicas seleccionadas presentan una relevante
importancia a nivel productivo (obtención de hojas
secas y plantines a partir de semillas) y el conocimiento de
las diferentes etapas y fases fenológicas permitirá realizar
apropiados manejos en futuros huertos semilleros policlonales
como: selección de diferentes clones con fenologías
similares para ser implantados, cruzamientos dirigidos utilizando
clones que, en condiciones de campo, no se polinizarían
y manejo de la recolección, almacenamiento y siembra
de semillas para la obtención de plantines de calidad.
MATERIALES Y MÉTODOS
El experimento se realizó en un lote ubicado en las instalaciones
de la EEA INTA Cerro Azul, Misiones, en el período
comprendido entre el mes de septiembre de 2010 y abril
de 2011. El suelo de la parcela presentó las siguientes características
químicas y físicas: nitrógeno total 0,40%, fósforo
extractable (P2O5) 30 ppm, potasio intercambiable 0,94
meq/100 g, materia orgánica 5%, CIC total 30 meq/100 g,
pH agua (1:2,25) 6,11, arena 50%, limo 20%, arcilla 50%
y densidad aparente 1,2 Kg/m3 (esta última se registró
utilizando metodología para suelos pedregosos). Como
material vegetal se utilizaron 10 clones de yerba dulce
seleccionados por sus características agronómicas de un
huerto semillero policlonal implantado en el año 2006. La
selección se realizó a partir de la variabilidad que presentaron
los clones durante 4 años con respecto a morfología y
duración del ciclo vegetativo y reproductivo. Cada material
genético contaba con 18 plantas, dando una totalidad de
180 plantas en el ensayo. Los plantines fueron obtenidos
a través de propagación agámica (estacas) en condiciones
de invernáculo. Estos plantines, que tenían una altura promedio
de 15 cm y un mínimo de 5 raíces, fueron plantados
en el mes de marzo de 2010 en una parcela de 9,2 metros
de longitud por 6 metros de ancho, en secano. El marco de
plantación elegido fue de 0,4 m entre plantas y 0,5 m entre
surcos: este espaciamiento facilitó los trabajos culturales y
el registro de datos (Carneiro 1990).
Para la plantación se utilizó la siguiente metodología: el
suelo fue rastreado y se marcaron los surcos con azada, la
plantación se realizó en forma manual efectuándose posteriormente
un riego a la parcela. Cada clon con sus respectivos
18 plantines se plantaron en 3 parcelas conteniendo
6 plantas cada una. Cada grupo (6 plantas) se distribuyó
al azar en el terreno. Las borduras se implantaron de igual
manera que las parcelas, utilizando únicamente el clon denominado
T1-STE21.
Se fertilizaron con 15-15-15 (nitrógeno, fósforo y potasio)
al inicio del ciclo (septiembre) a razón 20 gramos por
planta, colocando el fertilizante a 10 cm de la planta. El
desmalezado mecánico se hizo con azada y para el control
sanitario de larvas cortadoras (Argyrotaenia sphaleropa) se
utilizó el producto químico de marca comercial Galgotrin,
conteniendo el principio activo denominado cipermetrina al
25%, a una dosis de 10 ml.L-1.
Los tratamientos consistieron en 10 clones de yerba
dulce designados como: T1-STE21, T2-STK1, T3-STK3,
T4-STK5, T5-STK6, T6-STK9, T7-STK10, T8-STK11, T9-
STK12 y T10-STK13.
El trabajo se inició el 1.º de septiembre de 2010, cuando
se realizó una poda de uniformización a la totalidad de
las plantas, cortando los tallos primarios a nivel del suelo
con tijera de podar. Posteriormente, cuando se observaron
los primeros rebrotes, se comenzó a registrar los datos en
planillas confeccionadas para tal fin. A medida que los brotes
se diferenciaban en tallos primarios se escogieron al
azar tres de ellos, los cuales se identificaron con cintas de
color amarillo, rojo y azul (colores que se encontraban en
las planillas de toma de datos), cada una de estas fueron
atadas en la base de los tallos, con la finalidad de hacer el
seguimiento a los mismos durante todo el ciclo de la planta.
A continuación se describen las metodologías utilizadas
para registrar los datos de las variables morfológicas y fenológicas
seleccionadas:
- Número total de hojas expandidas: se contaron las
hojas de los tallos primarios y secundarios que se encontraban
marcados con las cintas de colores. Al final
de cada conteo semanal se procedió a marcar con
pincel y pintura de tela color blanco las últimas hojas
expandidas, tanto de los tallos primarios como de los
secundarios. En la siguiente toma de datos se realizó
el conteo de las nuevas hojas desarrolladas por encima
de dichas marcas.
- Número de tallos primarios: se realizó el conteo de
todos los tallos primarios (tallos provenientes del cuello
o corona de la planta).
- Número de tallos secundarios/tallo primario: se
contabilizaron únicamente los tallos secundarios que
se desarrollaron en las axilas de las hojas de los tallos
primarios que poseían las cintas en su base.
- Número de entrenudos/tallo: Se contabilizaron, únicamente,
los entrenudos de los tallos principales que
poseían las cintas en su base.
- Altura en cm: se utilizó para ello un metro, se midió desde
la base de la planta hasta el ápice del tallo más alto.
- Peso de 1000 semillas oscuras (en gramos): para
cuantificar esta variable se procedió primeramente a
la cosecha de semillas; para ello se utilizó una bolsa
de polietileno negro de 10 litros de capacidad. La parte
superior de la planta se introdujo en una bolsa e inclinada
a 45 grados con respecto al suelo, se realizó un
movimiento violento con el propósito de desprender las
semillas maduras de la planta, quedando dentro de la
bolsa. Luego, las semillas cosechadas se volcaron en
recipientes de un litro de capacidad con su identificación
correspondiente. Después de la cosecha, en el laboratorio,
se procedió a separar las semillas claras de
las oscuras y estas últimas se pesaron en una balanza
de precisión.
Al no existir una metodología para registrar los datos fenológicos
basándose en el tiempo térmico para yerba dulce,
se propuso el siguiente método: se utilizó la fórmula de
constante térmica Método Residual, la cual utiliza la sumatoria
de la temperatura media en ºC (grados centígrados)
menos la temperatura base en ºC establecida para el cultivo
(Σ T media - T base). Las temperaturas medias se obtuvieron
del Boletín Agro-meteorológico de la EEA Cerro Azul,
Misiones, y la temperatura base seleccionada fue 10 ºC, ya
que a partir de esta, la planta de yerba dulce reanuda su
actividad (Mizukami et al., 1983).
Las variables seleccionadas para ser estudiadas fueron
las siguientes:
- Tiempo térmico etapa vegetativa: se determinó el
tiempo térmico en grados día acumulados desde el inicio
de brotación hasta el fin de producción de hojas.
- Tiempo térmico botón floral (inicio etapa reproductiva): se determinó el tiempo térmico en grados día
acumulados desde el inicio de brotación, hasta la aparición
del primer botón floral.
- Tiempo térmico en botón floral: se determinó el
tiempo térmico en grados día acumulados desde inicio
del botón floral hasta la finalización de este.
- Tiempo térmico en fase flor abierta: se determinó
el tiempo térmico en grados día acumulados desde la
aparición de las primeras flores abiertas hasta que no
se observaron más flores en dicho estado.
- Tiempo térmico en fase de fructificación: se determinó
el tiempo térmico en grados día acumulados
desde el inicio de aparición de frutos hasta el final de
fructificación.
- Tiempo térmico etapa reproductiva: se determinó el
tiempo térmico en grados día acumulados desde el inicio
de botón floral hasta fin de fructificación.
Diseño experimental
El diseño experimental utilizado fue el completamente
aleatorizado, con tres repeticiones por cada tratamiento
establecido.
Los resultados obtenidos de las variables fenológicas
y morfológicas fueron sujetos a un análisis de varianza
(ANOVA), con un posterior test de comparación múltiple
(Duncan) a un nivel de significancia del 5%, excepto para la
variable peso de 1000 semillas oscuras, la cual solamente
registró una sola repetición por cada tratamiento. Todos los
análisis fueron realizados con el programa InfoStat versión
2011 (Di Rienzo et al., 2011).
RESULTADOS
Variables morfológicas
Analizando las variables morfológicas se observó que
los mayores valores obtenidos para el número total de
hojas expandidas se registraron en los clones T3-STK3
y T4-STK5, presentando valores por encima de las 1186
hojas por planta, encontrándose diferencias significativas
entre estos y los clones T10-STK13 y T8-STK11 que no
superaron las 757 hojas expandidas por planta (tabla 1).
También se halló que para la variable número de tallos
primarios, los valores de las medias se encontraron entre
1,56 y 3,2 tallos/pl no difiriendo significativamente ninguno
de los clones (tabla 1). Sin embargo, se registraron diferencias
estadísticamente significativas en el número de
tallos secundarios/tallo, presentando los mayores valores
medios los clones T2-STK1 y T3-STK3 (superiores a 67
tallos secundarios/tallo).
Los mayores valores obtenidos para el número de entrenudos/
tallo se observaron en los clones T4-STK5, T2-STK1,
T3-STK3 y T1-STE21 (medias superiores a 34 entrenudos/
tallo). No se encontraron diferencias significativas entre los
clones citados anteriormente, pero sí se detectaron entre
estos y los restantes. Para la variable altura de planta en
cm, los valores de las medias de los clones estudiados se
encontraron entre 93,28 cm y 127,8 cm (el 70% de estos superaron
los 100 cm; tabla 1). También se observó la existencia
de diferencias significativas entre los clones T1-STE21,
T3-STK3, T8-STK11 y T9-STK12 y los restantes.
Del registro del peso de 1000 semillas oscuras surge que
el 40% de los clones presentaron valores superiores a los
0,4 gramos (T1-STE21, T9-STK12, T5-STK6 y T8-STK11)
encontrándose el mayor peso en el clon T1-STE21. El
restante 60% mostró valores inferiores a los 0,36 gramos
(tabla 1). Al no existir repeticiones para el registro de esta
variable no se afirma que existan diferencias significativas
para los datos obtenidos.
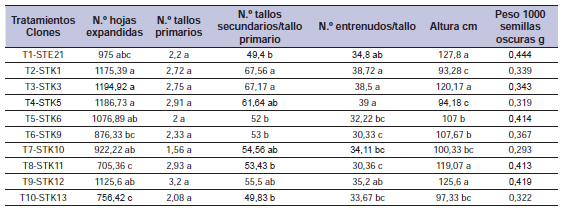
Tabla 1. Valores medios de las variables morfológicas: número de hojas expandidas/planta, número de tallos primarios/planta, número de
tallos secundarios/tallo primario, número de entrenudos/tallo, altura de planta en cm y peso de 1000 semillas oscuras.
Letras distintas indican diferencias significativas entre tratamientos para una misma variable de acuerdo con el test de Duncan (p<0,05).

Variables fenológicas
En la figura 1 se aprecia que no existen diferencias significativas
para la variable tiempo térmico acumulado hasta
el fin de la etapa vegetativa. También se puede observar
que los clones T9-STK12, T1-STE21, T2-STK3, T4-STK5
y T5-STK6 requieren valores por encima de 1800 grados
día para completar esta etapa. En contraposición a estos
se encuentran el 50% de los clones (T2-STK1, T6-STK9,
T7-STK10, T8-STK11 y T10-STK12) los cuales requirieron
valores por debajo de los 1800 grados día para completar
dicha etapa.
Igualmente que para la variable descripta anteriormente,
el clon T9-STK12 es el que requiere los mayores valores
de tiempo térmico para el inicio de la etapa reproductiva
(aparición del botón floral), demandando 1596 grados días.

Figura 1. Valores medios de las variables fenológicas (tiempo térmico etapa vegetativa, tiempo térmico hasta inicio etapa reproductiva)
expresados en grados día. Letras distintas indican diferencias significativas entre tratamientos para una misma variable de acuerdo con
el test de Duncan (p<0,05).
Para esta variable se detectaron diferencias significativas entre el clon T9-STK12 y los clones T10-STK13, T6-STK9, T2-STK1 y T1-STE21 (figura 1). Este último es el que presenta mayor precocidad para el inicio de la etapa estudiada (857 grados día). En la figura 2 se puede apreciar el comportamiento de los clones en la etapa reproductiva (medido en tiempo térmico) y, dentro de esta, sus correspondientes fases (botón floral, flor abierta y fructificación). Con respecto al tiempo térmico necesario para completar la etapa reproductiva, el mayor requerimiento se observó en el clon T1-STE21 (1664 grados día), el cual difirió significativamente del 80% de los clones estudiados (T2-STK1, T3-STK3, T5-STK6, T6-STK9, T7-STK10, T8-STK11, T9-STK12 y T10-STK13), los que mostraron requerimientos menores a 1400 grados día. También se observó que, para finalizar la fase de botón floral, nuevamente el clon T1-STE21 demandó la mayor acumulación de tiempo térmico (957 grados día), difiriendo significativamente de los demás clones. Los clones que acumularon menor tiempo térmico fueron el T7-STK10 y T9-STK12, registrando valores por debajo de 400 grados día para completar la fase. El tiempo térmico necesario para completar la fase flor abierta en los diferentes clones se encontró entre 600 y 1700 grados día (figura 2). El máximo valor se registró en el clon T8-STK11 (1609 grados día), este clon difirió significativamente de los clones que demandan menos de 1300 grados día para finalizar la fase (T2-STK1, T3- STK3, T4-STK5, T5-STK6, T6-STK9, T7-STK10, T9-STK12 y T10-STK13). Con respecto al tiempo térmico necesario para finalizar la fase de fructificación, el mayor requerimiento se observó en el clon T1-STE21 (1254 grados día), difiriendo significativamente de los demás clones.
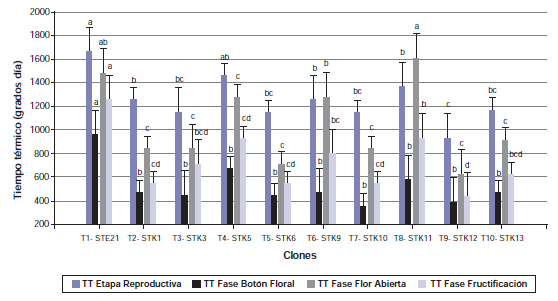
Figura 2. Valores medios del tiempo térmico de la etapa reproductiva y sus respectivas fases (tiempo térmico fase botón floral, tiempo
térmico fase flor abierta y tiempo térmico fase fructificación) expresados en grados día. letras distintas indican diferencias significativas
entre tratamientos para una misma variable de acuerdo con el test de Duncan (p<0,05).
DISCUSIÓN
Variables morfológicas
En lo que respecta a las variables morfológicas estudiadas,
los resultados obtenidos para el número de tallos
primarios concuerdan con lo reportado para la variedad
Iguazú CTM, la cual registró de 1 a 5 tallos primarios en
el primer ciclo luego de una única poda de uniformización,
clasificándose como variedad de mediana cantidad (INASE
2005). Sin embargo, Molero (1984) menciona datos preliminares
de 40 tipos de yerba dulce mostrando valores promedio
de 10,3 tallos/planta, los cuales son muy superiores
a lo obtenido en los clones estudiados. Contrariamente con
lo reportado en la variable anterior, la variedad Iguazú CTM
supera ampliamente a los clones en el número de tallos secundarios, ya que presenta entre 80 a 150, clasificándose
como variedad muy ramificada (INASE 2005).
Existen pocos trabajos publicados que reporten características
morfológicas de yerba dulce. Sin embargo, Molero
(1984) registró en su investigación 12 variables morfológicas
en una colección de esta especie. Una de dichas variables
fue el número de entrenudos en el tallo, para esta
variable obtuvo un promedio de 18,9 (entrenudos) valor
inferior a lo alcanzado por todos los clones en esta investigación.
Otros investigadores como Casaccia y Álvarez
(2006) presentan en su informe algunas características de
la variedad clonal IAN/VC-142 (EIRETE) la cual posee un
porte alto pudiendo alcanzar 120 cm de altura, valor similar
a los clones con mayores medias registrados en este trabajo.
Sin embargo, la descripción morfológica de la variedad
Iguazú CTM muestra tallos primarios erectos de 40-70 cm
de longitud (INASE 2005).
El peso de 1000 semillas es uno de los componentes de
calidad utilizados en yerba dulce junto con la pureza, la viabilidad
y la germinación. Randi y Felippe, (1980) obtuvieron
los mayores porcentajes de germinación al utilizar semillas
más pesadas. Los datos obtenidos del peso de 1000
semillas de los 10 clones superaron a los encontrados en
la variedad DULCINEA 777 la cual registró 0,24 gramos
(INASE 2005).
Variables fenológicas
Los clones no poseen grandes diferencias en tiempo térmico
para finalizar la etapa vegetativa. Sin embargo, estas
diferencias se aprecian en la etapa reproductiva, la cual
muestra una gran variabilidad entre los materiales genéticos
estudiados (clones).
Dentro de la etapa reproductiva las fases establecidas
tienen gran relevancia. Conocer el tiempo térmico de la
fase botón floral nos permite organizar la cosecha de hojas
(la cual se realiza en forma manual durante varios días).
Esta se efectúa mientras las plantas se encuentran con botones
florales (Casaccia y Álvarez, 2006).
Conocer el tiempo térmico requerido para el inicio de
la apertura de flores y finalización de la floración (fase de
flor abierta), nos permite planificar cruzamientos entre clones
que requieran similares cantidades de tiempo térmico
acumulado, maximizando la probabilidad de polinización
cruzada (Carneiro, 1990). En este trabajo de investigación
los clones que evidenciaron mayor probabilidad de cruzamientos
(cultivados a campo) son aquellos que requirieron
mayor tiempo térmico para finalizar la fase de flor abierta.
Utilizando este criterio de clasificación, los clones más aptos
son el T8-STK11 y T1-STE21.
La fase de fructificación también presenta su importancia,
ya que conocer el desarrollo de esta, permite un mejor
manejo de la cosecha de semillas en los huertos semilleros.
Los clones estudiados, en general, presentaron un
comportamiento similar para esta variable, exceptuando el
clon T9-STK12, cuyo requerimiento en tiempo térmico es
inferior a todos los demás clones, y el clon T1-STE21 cuyo
requerimiento en tiempo térmico es muy superior a los demás
materiales estudiados.
CONCLUSIONES
Los datos obtenidos para las variables estudiadas son muy importantes ya que no se tenía un registro detallado del comportamiento de estos 10 clones de yerba dulce. Se encontraron diferencias morfológicas entre algunos de los clones para las variables número de hojas expandidas, número de tallos secundarios, número de entrenudos y altura de planta en cm. Sin embargo no se registraron diferencias para el número de tallos primarios. Las 2 primeras variables son de gran importancia a la hora de realizar la cosecha comercial de la yerba dulce, ya que una planta con mayor número tallos secundarios, también posee un mayor número de hojas. No obstante, el número de entrenudos y la altura de la planta son parámetros a tener en cuenta cuando se realiza la propagación por estacas. Una planta con mayor altura y mayor número de entrenudos, proporcionará un mayor coeficiente de multiplicación (número de estacas obtenidas por cada planta madre utilizada). El clon T1-STE21, seguido del T4-STK5, son los que más favorecerían el trabajo de cosecha de hojas, ya que presentan la fase de botón floral más extendida. Los clones T9-STK12, T1-STE21 y T3-STK3 son los que poseen mejor perfil para ser cruzados. Estos pueden ser utilizados en futuros huertos semilleros porque requieren tiempos térmicos compatibles en fase de flor abierta, de esta forma se puede producir la polinización natural realizada por insectos. Los registros de las variables fenológicas no fueron comparadas con otros trabajos ya que no se encontraron registros detallados de investigaciones anteriores en la especie.
BIBLIOGRAFÍA
1. BELLO, M. 1988. Consideraciones metodológicas para estudios fenológicos en árboles templados de coníferas. Ciencia Forestal 14, 89-109.
2. BONDAREV, N.I.; SUKHANOVA , M.A.; RESHETNYA, O.V.; NOSOV, A.M. 2003. Steviol Glycoside Content in Different Organs of Stevia rebaudiana and Its Dynamics during Ontogeny. Biología Plantarum 47 (2), 261-264.
3. CARDELLO, H.; SILVA, M.; DAMASIO, M. 1999. Tempo-intensidade dos estímulos doce e amargo de extracto de folhas de stévia em doçura equivalente a sacarose. Ciência Tecnologia Alimento 19 (2), 163-169.
4. CARNEIRO, J.W. 1990. Stevia produçao de sementes. Universidade Estadual de Maringá. Maringá 65p.
5. CASACCIA, J.; ÁLVAREZ, E. 2006. Recomendaciones técnicas para una producción sustentable de Ka´a He´e (Stevia rebaudiana Bertoni) en el Paraguay Caacupe Ministerio de Agricultura y Ganadería, Dirección de Investigación Instituto Agronómico Nacional Agrícola. Manual técnico 8, 51.
6. DI RIENZO, J.A.; CASANOVES, F.; BALZARINI, M.G.; GONZALEZ, L.; TABLADA, M.; ROBLEDO, C.W. InfoStat versión 2011. Grupo InfoStat, FCA, Universidad Nacional de Córdoba, Argentina.
7. FAKHRUL, R.; NORRIZAH, J.; JAAPAR , S.; NOOR ANILIZAWATIMA, S. 2014. The Effect of Potassium Concentrations on the Growth and Development of Stevia rebaudiana (Bertoni) and Production of Stevioside and Rebaudioside A. American-Eurasian Journal of Sustainable Agriculture 8 (2), 42-51.
8. GUEDES, T.; ROSSI, R.; MARTINS , A.; JANEIRO, V.; CARNEIRO , J. 2014. Applying regression models with skew-normal errors to the height of bedding plants of Stevia rebaudiana (Bert) Bertoni. Acta Scientiarum-Technology 36 (3), 463-468.
9. IBRAHIM, M.; RODENBURG, D.; ALVES, K.; FRONCZEK, F.; McCHESNEY, J.; WU, C.; NETTLES, B.; VENKATARAMAN, S.; JASSCH, F. 2014. Minor diterpene glycosides from the leaves of stevia rebaudiana. Journal of Natural Products 77 (5), 1231-1235.
10. INASE. INSTITUTO NACIONAL DE SEMILLAS 2005. Descripción morfológica fenológica y sanitaria del cultivar. Denominación del cultivar Iguazú ctm y dulcinea para dulcinea. Folio 10-26. (http://www.inase.gov.ar. Verificado: 01 de julio de 2014).
11. JAIN, P.; KACHHWAHA, S.; KOTHARI, S. 2012. Optimization of micronutrients for the improvement of in vitro plant regeneration of Stevia rebaudiana (Bert.) Bertoni. Indian Journal of Biotechnology 11 (4), 486-490.
12. KRYVENKI, M.; DOMÍNGUEZ, M.; GUERRERO, D. 2007. Evaluación de reguladores de crecimiento en el enraizamiento de estacas de yerba dulce. Instituto Nacional de Tecnología Agropecuaria Informe Técnico 93, 15 p.
13. LORENZO, C.; SERRANO-DÍAZ, J.; PLAZA, M.; QUINTANILLA , C.; ALONSO, G. 2014. Fast methodology of analysing major steviol glycosides from Stevia rebaudiana leaves. Food Chemistry 157, 518-523.
14. LV, X.; KUANG, P.; YUAN, Q.; LIANG, H.; ZHENG, G. 2014. Preparative separation of steviol glycosides from Stevia rebaudiana bertoni by macroporous resin and preparative HPLC. Acta Chromatographica 26 (1), 123-135.
15. MELIS, M.S.; ROCHA, S.T.; AUGUSTO, A. 2009. Steviol effect, a glycoside of Stevia rebaudiana, on glucosa clearance in rats. Brazilian Journal of Biology 69 (2), 371-374.
16. MIDMORE, D.J.; RANK, A.H. 2002. A new rural industry -Steviato replace imported chemical sweeteners. A report for the Rural Industries Research and Development Corporation 50p.
17. MIZUKAMI, H.; SHIIBA, K.; SATOSHI, I.; OHASHI, H. 1983. Effect of temperature on growth and stevioside formation of Stevia rebaudiana Bertoni. Shoyakugaku Zasshi 37 (2), 175-179.
18. MOLERO, J. F. 1984. El ka’a he’e, Stevia rebaudiana (Bertoni) Bertoni, Análisis bibliográfico y anotaciones hortícolas. Ministerio de Agricultura y Ganadería. Proyecto de intensificación de cultivos en fincas pequeñas. USAID-CREDICOOP. Asunción, Paraguay. Publicación Miscelánea 11, 75p.
19. NOWER, A. 2014. In Vitro Propagation and Synthetic Seeds Production: An Efficient Methods for Stevia rebaudiana Bertoni. Sugar Tech Journal 16 (1), 100-108.
20. PRAKASH, I.; DUBOIS, G.E.; CLOS, J.F.; WILKENS, K.L.; FOSDICK, L.E. 2008. Development of rebiana, a natural, non-caloric sweetener. Food and Chemical. Toxicology 46, 75-82.
21. RAZAK, U.; ONG, C.; YU, T.; LAU, L. 2014. In vitro micropropagation of Stevia rebaudiana Bertoni in Malaysia. Brazilian Archives Biology and technology 57 (1), 23-28.
22. ROJAS MONTOYA, S.W. 2009. Stevia edulcorante orgánico del siglo xxi. Universidad Nacional Agraria La Molina. Lima Perú. 391p.
23. RANDI, Á.M.; FELIPPE, G.M. 1980. Detecção de esteviosídeo e substâncias giberelínicas nos aquênios de Stevia rebaudiana; efeito de esteviosídeo em germinação. Revista de Brasileira Botânica 3, 55-58.
24. SAGAKUCHI, M.; TATASUIKO , K. 1982. As pesquisas japonesas com Stevia rabaudiana (Bert.) Bertoni e o esteviosideo. Ciencia e Cultura 34 (2), 235-248.
25. SHOCK, C. 1982. Experimental Cultivation of Stevia Rebaudiana B. in California. University of California Agronomy Progress Report. N.º 122. (http://ucce.ucdavis.edu/files/repositoryfiles/ca3609p4-61878.pdf.: Verificado 07 de julio de 2014).
26. SINGH, P.; DWIVEDI, P. 2013. Efficient micropropagation protocols of regeneration of Stevia rebaudiana Bertoni, an anti-diabetic herb. Vegetos 26 (1), 318-323.
27. SOJEARTO, D.D.; COMPADRE, C.M.; MEDON, P.J.; KAMATH, S.K.; KINGHORN, A.D. 1983. Potential Sweetening Agents of plants origin. Economic Botany 37, 71-79.
28. VAZQUEZ-BAXCAJAY, L.; ROBLEDO-PAZ, A.; MURATALLA LUA, A. Y CONDE-MARTINEZ, V. 2014. Micropropagación de Stevia rebaudiana Bertoni y detección de steviósidos. Bioagro 26 (1), 49-56.