Introducción
El ALPPS (associating liver partition and portal vein occlusion for staged hepatectomy) es un procedi miento que ha representado un gran avance en la ciru gía hepatobiliopancreática 1,2.
La cirugía sigue siendo la única opción curati va para tumores malignos hepáticos. No es infrecuente que se requieran grandes resecciones hepáticas a fin de lograr unos márgenes tumorales libres. Para ello resulta fundamental mantener un volumen y futuro remanen te hepático (FRH) adecuados, ya que la insuficiencia he pática posoperatoria (IHP) es una de las principales cau sas de morbimortalidad tras resecciones extensas3,4. Clásicamente se establecía como necesario mantener al menos dos segmentos anatómicos contiguos, repre sentando un FRH mínimo del 20-25%4,5 y del 40% en ca sos de hepatopatía. El ALPPS rompió este paradigma4,5.
Material y métodos
Búsqueda de publicaciones en Pubmed em pleando el término “ALPPS” y búsqueda en racimos, se leccionándolos por su relevancia e influencia histórica en la técnica.
Técnicas de regeneración hepática previas a ALPPS
En las últimas décadas se desarrollaron dos técnicas para inducir hipertrofia del FRH: la oclusión portal (OP) y la hepatectomía en dos tiempos (HDT)6, si bien ambas suelen asociarse.
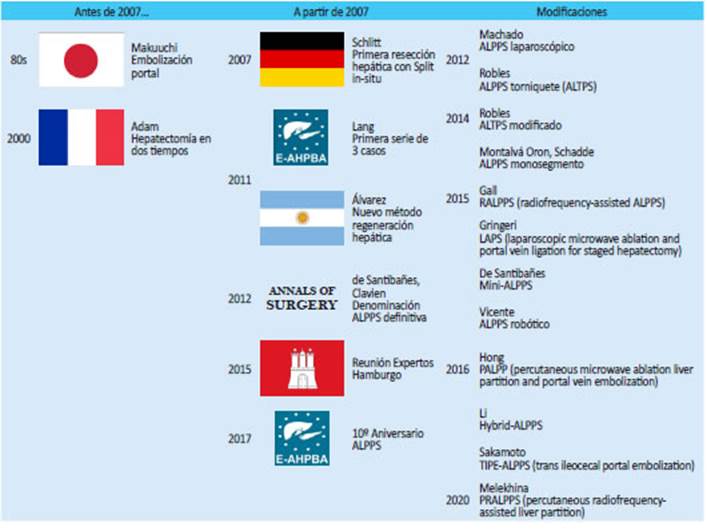
La OP puede realizarse por embolización (EP) o ligadura (LP). La EP es actualmente la técnica de refe rencia (gold standard). Makuuchi7 en los años 80 intro dujo este nuevo concepto: embolizar la porta derecha para inducir la hipertrofia del lóbulo hepático izquierdo, permitiendo la exéresis de tumores de gran tamaño o múltiples de forma segura. Sin embargo, la hipertrofia del FRH no siempre es suficiente, lo que da lugar a una IHP, y en algunos pacientes la enfermedad progresa tras la EP4,8. Hasta el 40% de los pacientes no son candida tos a cirugía por estos motivos4,9.
La HDT fue descripta por Adam y col.10 en el año 2000. Se utilizó para tratamiento de la enfermedad bilobar por metástasis hepáticas de carcinoma colo rrectal (MHCCR) inicialmente irresecable. En un primer tiempo se reseca el mayor número posible de metásta sis; tras un período de hipertrofia del FRH y quimiotera pia sistémica, se puede proceder a un segundo tiempo con intención curativa. La morbilidad alcanza el 49-59% y la mortalidad oscila entre 6,4 y 8,8%4. Aproximada mente el 25% de los pacientes no consiguen completar la resección11.
Primeros procedimientos de ligadura portal y parti ción hepática
En 2007, Hans Schlitt realizó por primera vez la técnica que posteriormente se conocería como ALPPS en una paciente con colangiocarcinoma hiliar Bismuth de tipo IV. La primera comunicación fue una serie de tres casos presentada por Lang en el 9º congreso de la E-AHPBA (European-African Hepato-Pancreato-Biliary Association) en Ciudad del Cabo, Sudáfrica, en 2011, que creó gran expectación y controversia12.
Ya en 2011, Álvarez y col.13 publicaron una nue va técnica de regeneración hepática llevada a cabo en una paciente con cáncer de colon izquierdo y metás tasis hepáticas inicialmente irresecables; se practicó la hemicolectomía izquierda, exéresis de metástasis del hígado izquierdo y partición hepática in situ con liga dura portal derecha. Realizaron también la ligadura de vía biliar derecha, gesto que posteriormente se ha se ñalado que puede aumentar la fuga biliar14. Describie ron un aumento del FRH > 40% al 6º día posoperatorio, completando la hepatectomía derecha al 7º día, y la paciente pudo ser dada de alta 11 días después.
Fue en 2012 cuando Schnitzbauer y col.5 pu blicaron una revisión retrospectiva de 25 casos tratados entre 2007 y 2011, mayoritariamente con MHCCR.
La técnica inicial consta de dos tiempos: en el primero, se practica la ligadura portal derecha y di visión in situ del parénquima a lo largo del ligamento falciforme, cubriendo el hígado derecho con una bolsa de plástico para evitar adherencias. Tras un intervalo medio de 9 días (rango 5-28 días) en el que se obtiene una hipertrofia aproximada del 75% del lóbulo hepático izquierdo, se realiza una volumetría. En el segundo, se completa la trisectorectomía derecha (Fig. 1).
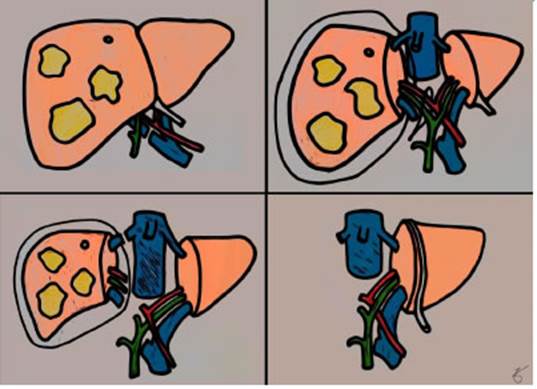
Figura 1 Técnica ALPPS descripta inicial mente. Superior izquierda (1ª fase): tumoraciones hepáticas princi palmente localizadas en hemi hígado derecho. Ligadura portal derecha. Superior derecha (1ª fase): Split in situ, cobertura de hígado dere cho en bolsa plástica, referencia de hilio derecho. Inferior izquierda (2ª fase): liga dura de hilio hepático derecho y vena suprahepática derecha. Inferior derecha (2ª fase): resul tado final con FRH hipertrofiado.
El 64% presentaron complicaciones; de las 50 complicaciones descriptas, 22 (44%) fueron Clavien- Dindo grados III-IV. La mortalidad fue del 12%.
La técnica fue inicialmente denominada “hepa tectomía en 2 etapas con LP derecha y división in situ”, pero fue rebautizada por de Santibañes y Clavien en 201215 con el acrónimo ALPPS (Tabla 1).
Expansión y registro internacional
La técnica generó gran interés16, y se creó un registro internacional en 2012 que ha reclutado más de 1200 casos17. Ha contribuido a controlar los resultados, mejorar la selección de pacientes y estudiar las compli caciones y sus posibles soluciones.
El primer informe publicado con datos extraí dos del registro recogía 202 pacientes hasta enero de 201418. Al año y dos años, la supervivencia global (SG) fue del 73% y 59% y la supervivencia libre de enferme dad (SLE) fue del 60% y 42%, respectivamente, con una supervivencia media de 24 meses. La mortalidad a 90 días fue del 9%. Los factores predictivos de complica ciones graves fueron: tumores hepáticos primarios, edad > 60 años, necesidad de transfusión intraopera toria y tiempo quirúrgico > 5 horas. Los peores resulta dos correspondían a pacientes con cáncer de vesícula y colangiocarcinoma18, probablemente relacionado con la alta tasa de complicaciones biliares4.
El registro también ha permitido analizar las indicaciones de ALPPS19. Se evaluaron los pacientes in cluidos entre 2012 y 2017, considerando que una ratio entre FRH y peso corporal ≥ 0,5% en hígados sanos y ≥ 0,8% en hígados enfermos resultaría potencialmente resecable en un solo tiempo y, por tanto, una hepatec tomía derecha podría haberles evitado ese riesgo adi cional. Concluyó que hasta un tercio de los pacientes in tervenidos de ALPPS no cumplían criterios. Este artículo ha reabierto un debate que surgió desde los inicios, ya que muchos autores consideran que el ALPPS ha gene rado una “moda” que ha aumentado su uso indebido y debe entenderse como otra opción para tener en cuen ta dentro de las posibilidades de las que dispone todo cirujano20.
Modificaciones de la técnica original
Desde la descripción inicial del ALPPS se han publicado variaciones técnicas:
▪▪ALPPS mínimamente invasivo (MIS). En 2012, Machado y col.21 realizaron el primer ALPPS laparoscópico, y Vicen te y col.22 publicaron en 2016 el primer ALPPS robótico. La revisión sistemática de Melandro y col.23 incluyó veintisiete pacientes intervenidos en alguna de las etapas por esta vía; el 15,4% presentaron complica ciones grado III y no hubo mortalidad. En la revisión de Michal y col.24 se compararon 46 pacientes MIS-ALPPS frente a 1088 por vía abierta. Los parámetros operatorios (tiempo y pérdida sanguínea) no mostra ron diferencias; el grupo abierto presentó más comor bilidades de base, mayor número de hepatectomías derechas extendidas, de complicaciones graves y mor talidad; en conclusión, por el momento, la evidencia es limitada.
▪▪ALPPS torniquete (ALTPS). Descripto por Robles y col.25 en 2012, consiste en la LP con colocación de un torniquete sobre la línea de transección, acelerando la hipertrofia y consiguiendo una regeneración eficaz, con índices de morbimortalidad aceptables26.
▪▪ALTPS modificado27. Ideado para tumores perihiliares en los que prima la técnica “non-touch”. Se evita la ligadura de la porta realizando una EP derecha en el 4º día posoperatorio.
▪▪ALPPS monosegmento. En 2015, Montalvá Oron y col.28 y Schadde y col.6 publicaron series de ALPPS monosegmento en 8 y 12 pacientes, respectivamen te. En la primera serie, la morbilidad alcanzó el 50%, la mortalidad el 25% y la recurrencia de enfermedad fue 100%, con una mediana de SLE de 155 días28. En la segunda, no hubo fallecidos y la morbilidad grado IIIa fue del 33,3%, con una recurrencia de la enfermedad del 50% a 14 meses de seguimiento6.
▪▪RALPP (radiofrequency-assisted ALPPS). La opción pu blicada por Gall y col.29 en 2015 es la realización de un ALPPS por abordaje laparoscópico mediante el uso de radiofrecuencia (RFA), produciendo una línea de necrosis a lo largo de la futura línea de transección. Esta técnica interrumpe el flujo sanguíneo desde el FRH hacia el hemihígado enfermo mientras induce la hipertrofia del FRH sin una división física del parén quima.
▪▪LAPS (laparoscopic microwave ablation and portal vein ligation for staged hepatectomy). Referida por Gringeri y col.30 en 2015; es similar a la RFA, pero uti liza las microondas para la partición.
▪▪Mini-ALPPS. Descripto por de Santibañes y col.1 en 2016. Se propone que la embolización portal intraope ratoria y la transección parcial del parénquima (hasta la vena suprahepática media) en comparación con la partición completa (hasta la vena cava inferior) mini mizan el impacto de la primera etapa y favorecen la recuperación. Los pacientes no presentaron complica ciones graves y desarrollaron un FRH adecuado4.
▪▪PALPP (percutaneous microwave ablation liver parti tion and portal vein embolization). De Hong y col.31, en 2016, realizan una técnica percutánea con microon das para el split (partición).
▪▪Hybrid-ALPPS32: descripto por Li y col.32 en 2016, para turmores con infiltración tumoral de la porta derecha cuando no es posible su ligadura. Realiza una técni ca “non-touch” con split in-situ mediante abordaje anterior y EP derecha por radiología intervencionista (pudiendo acceder a través de la vena ileocólica), sin manipular el ligamento hepatoduodenal ni el hemihí gado derecho; se completa la segunda fase, aconse jando resecar la bifurcación portal.
▪▪TIPE-ALPPS (trans ileocecal portal embolization): téc nica descripta por Sakamoto y col.33, en 2016. En la primera fase se practica la EP accediendo a través de la vena ileocecal, sin manipular el ligamento hepato duodenal y practicando una partición parcial a lo largo de la línea de Rex-Cantlie.
▪▪PRALPPS (percutaneous radiofrequency-assisted li ver partition): técnica descripta en el estudio casos-control de Melekhina y col.34 en 2020, en pacientes con colangiocarcinoma perihilar. En la primera fase se practica EP y ablación por RFA ecoguiada a lo largo del margen lateral de la vena suprahepática (VSH) bajo anestesia general. La ablación térmica incluía aproxi madamente el 50% del futuro plano de transección, manteniendo una distancia mínima de 2 cm de la pla ca hiliar para evitar lesionarla.
Dada la gran cantidad de términos surgió la ne cesidad, expresada por Linecker y col.2, de emplear una terminología de consenso: Rescue-ALPPS (ALPPS rea lizado por una hipertrofia inadecuada tras EP), ALPPS laparoscópico (empleo de laparoscopia en alguna eta pa), EP-ALPPS (uso de EP como parte de la primera eta pa), ALPPS parcial (en caso de transección incompleta: ALTPS, RALPP y LAPS) o ALPPS monosegmento.
Reuniones de consenso
1ª Reunión de Expertos de Hamburgo
La primera reunión de expertos en ALPPS se celebró en 2015 en Hamburgo16. Se emitieron ocho re comendaciones:
▪▪Resulta crucial el conocimiento de la anatomía hepá tica, además de preservar el flujo arterial y el drenaje venoso del hígado “deportalizado”, evitándose toda manipulación innecesaria del hilio hepático.
▪▪No se puede recomendar ninguna técnica de transec ción como superior al resto.
▪▪El colangiograma puede favorecer la identificación del árbol biliar y posibles fugas. El “marcado” de las estructuras anatómicas puede facilitar la segunda fase.
▪▪La primera volumetría debería realizarse a los 8-10 días y repetir semanalmente durante 4 semanas si no se alcanza un FRH suficiente.
▪▪La principal indicación son MHCCR, alertándose de su uso en carcinoma hepatocelular (CHC) y colangiocar cinoma por la elevada morbimortalidad.
▪▪El ALPPS es una opción viable en casos de FRH peque ño o enfermedad bilobar, con menores tasas de aban dono que EP/HDT. Se abre la posibilidad del “rescue- ALPPS” en esos casos.
▪▪Se debe posponer la segunda fase en caso de MELD > 10. La edad > 60 años se asocia a peores resulta dos, aconsejándose mayores intervalos entre las dos fases.
▪▪En MHCCR, el ALPPS debería realizarse tras neoadyu vancia. La progresión es contraindicación de ALPPS. En caso de tumor sincrónico hepático y colorrectal, la estrategia inversa puede ser una buena opción. Se alerta acerca de realizar procedimientos en hígado y colon de forma simultánea.
Reunión de expertos ‘‘10º aniversario de ALPPS’’
Con la necesidad de seguir estableciendo indi caciones claras, selección de pacientes y estandariza ción de la técnica quirúrgica, se celebró durante el 12º Congreso de la E-AHPBA (Mainz, Alemania, 2017) una nueva reunión de expertos35. Entre los múltiples aspec tos valorados, destacan:
▪▪Las modificaciones técnicas que minimizan la exten sión del primer procedimiento se asocian a una mayor seguridad
▪▪El grado de hipertrofia del futuro remanente hepáti co en hígados cirróticos/fibróticos, parece ser inferior que en aquellos no cirróticos
▪▪Las tasas de resección son superiores con ALPPS fren te a la HDT, con morbilidad y mortalidad perioperato rias similares
▪▪ALPPS es eficaz incluso tras fallo de la embolización portal.
Situación actual del ALPPS
Esta cirugía ha demostrado ofrecer una oportu nidad de curación a pacientes que, de inicio, no tienen opción quirúrgica11,15,23,36. En comparación con la HDT, el metanálisis de Moris y col.11 demostró que 90,9% de los pacientes operados mediante ALPPS logran la resección completa, comparados con 74,6% interveni dos mediante HDT. En relación con la SG y SLE, algunos estudios no hallaban diferencias entre ambas técnicas11,37,38. Sin embargo, los resultados del LIGRO trial39,40 en pacientes con MHCCR han demostrado la superioridad del ALPPS frente a HDT, con mejor tasa de resección y supervivencia, como se verá posteriormente.
La morbimortalidad de la técnica es motivo de preocupación. Con el objetivo de predecir la mortali dad a 90 días, Linecher y col.41 validaron dos modelos de riesgo, y, recientemente, Raptis y col.42 establecieron los resultados de referencia (“benchmarks”) del ALPPS.
No hay datos que demuestren que el crecimien to de volumen vaya en paralelo a la función hepática43. La mayoría de muertes por IHP aparecen tras la segunda fase. Surge así el dilema de cuál puede ser el momento óptimo de realizar la segunda intervención. La reunión de Hamburgo determinó unos valores mínimos para pro ceder con la segunda fase de FRH > 30% o una ratio FRH/ peso corporal (FRH/PC) > 0,5% y, según la calidad del hígado, un FRH > 40% o FRH/PC > 0,8%4,16. Se aconseja realizar la primera tomografía computarizada (TC) a los 8-10 días tras completar la primera cirugía y se puede re petir semanalmente durante 4 semanas en caso de FRH insuficiente44. Las pruebas funcionales, entre ellas gam magrafía o verde de indocianina, deben convertirse en rutinarias antes de completar la segunda fase del ALPPS. Pueden resultar especialmente útiles en pacientes con un FRH borderline para decidir el mejor momento para la intervención y prevenir la IHP. Serenari y col.45 realizaron una centellografía HIDA (ácido iminodiacético) incluyen do técnica de SPECT previa a la segunda fase del ALPPS y desarrollaron el índice HIBA-i con el que se mide la proporción de radionúclido acumulado en el FRH. En su artículo, ninguno de los pacientes con un valor de corte del 15% o superior desarrolló IHP.
Los resultados obtenidos difieren en depen dencia de la patología intervenida:
MHCCR
Las MHCCR son la principal indicación de ALPPS18,39,46-53. Se han descripto como factor indepen diente predictor de menores tasas de complicaciones graves, con una morbilidad mayor (Clavien-Dindo IIIa o superior) del 36%. La SG a 1 y 2 años es del 76% y 62%, respectivamente, con una SLE del 59% y 41%18. El LIGRO trial39 es un ensayo clínico aleatorizado (ECA) multicéntrico con aleatorización 1:1 ALPPS:HDT de 97 pacientes con MHCCR. En los resultados emitidos por Sandström y col.39, la tasa de resección fue del 92% en el grupo ALPPS frente al 57% de la HDT (p < 0,0001). El ALPPS se asoció a mayor hipertrofia del FRH (ALPPS: 92% vs. HDT: 57%, p < 0,0001). No hubo diferencias sig nificativas en cuanto a complicaciones mayores (≥ IIIa) (ALPPS: 43% vs. HDT: 43%, p = 1) o mortalidad a 90 días (ALPPS: 9,1% vs. HDT: 10,7%, p = 0,64). Los tiempos en tre la primera y segunda etapa resultaron superiores en HDT (ALPPS: 11±11 vs. HDT: 43±15 días, p < 0,0001). La mediana de supervivencia descripta por Hasselgren y col.40 fue de 46 meses en el grupo ALPPS frente a 26 meses de HDT (p = 0,028).
CHC
Los hígados con CHC parecen presentar menor velocidad e hipertrofia del FRH (40-47% frente a 76- 138%)54-56, correlacionándose con el grado de fibrosis. La mortalidad oscila entre 9%56 y 31%54, por lo cual se acon seja el ALPPS en pacientes con bajos grados de fibrosis y un mayor intervalo entre las dos fases que permita una hipertrofia suficiente9. En estos pacientes, la transec ción parcial parece no inducir una hipertrofia suficiente, en contraste con la transección completa (17,5 mL/día frente a 31,2 mL/día, p = 0,022)56. En comparación con otras técnicas, el ALPPS ha presentado una mejor SG y SLE frente a la quimioembolización transarterial (TACE, por sus siglas en inglés)57, además de una mayor tasa de resección frente a EP58.
Colangiocarcinoma
Los pacientes intervenidos por colangiocarci noma presentan una elevada morbimortalidad. La SG descripta frente a quimioterapia paliativa59 es superior con el ALPPS, alcanzando a 1, 2 y 3 años el 82,4%, 70,5% y 39,6% frente a 51,2%, 21,4% y 11,3% (p < 0,01). Este beneficio no se aprecia en aquellos pacientes con IHP o colangiocarcinoma intrahepático multifocal. La morbili dad grave alcanza el 6,1% tras la primera fase, el 41,4% tras la segunda fase, y la mortalidad el 21,2%.
Sobre el colangiocarcinoma perihiliar, los re sultados inicialmente descriptos alcanzaban una mor talidad del 40%60 al 48% a 90 días y una SG de 6 meses61,62. Se ha descripto el uso de partial-TIPE-ALPPS63 y PRALPPS34 para estos tumores. Sin embargo, Olthof y col.62 informaron los resultados de casos de colangio carcinoma perihiliar incluidos en el registro ALPPS; la mortalidad a 90 días fue del 48% con una SG media de 6 meses. En comparación con hepatectomías mayores, el ALPPS logró una hipertrofia similar del FRH, con mayor mortalidad y menor SG. Por ello, desaconsejan el ALPPS en colangiocarcinoma perihilar y aconsejan la EP para incrementar el remanente hepático.
ALPPS en pediatría
La primera indicación de ALPPS en pediatría fue comunicada en 2014 por Chan y col.64. Posterior mente, en 2015, la serie de 5 pacientes de Wiederkehr y col.65, no presentó complicaciones graves o muertes.
Conclusiones
El ALPPS es un procedimiento que ha generado gran interés a pesar de una importante morbimortali dad. Su análisis ha permitido una mejor selección de pacientes, definir el momento de la segunda cirugía y mejorar las técnicas quirúrgicas, lo que ha logrado tasas de morbimortalidad aceptables en comparación con las resecciones hepáticas estándar. Las modificaciones téc nicas, que en su mayoría minimizan la extensión del pri mer procedimiento, se asocian con mejoras significati vas en la seguridad, al tiempo que se conserva una alta tasa de resección curativa. La segunda etapa debe re trasarse o abandonarse en caso de compromiso clínico, complicaciones o FRH insuficiente. Los datos recientes confirman tasas de resección más altas en ALPPS que con procedimientos clásicos. Si bien el ALPPS es un con cepto establecido, varias preguntas siguen sin respues ta, principalmente en cuanto a resultados oncológicos a largo plazo. El ALPPS no reemplaza otras técnicas, sino que forma parte del arsenal terapéutico.











 texto en
texto en