Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Ciencia y Tecnología
versión On-line ISSN 1851-7587
Rev. cienc. tecnol. no.32 Posadas dic. 2019
Optimización de las condiciones de cultivo para la producción de una Poligalacturonasa Microbiana
Optimization of culture conditions for the production of a Microbial Polygalacturonase
Silvana A. Maidana1*; Alicia A. Mieres2; Emilce R. Zubreski1; María A. Martos1
1- Facultad de Ciencias Exactas, Químicas y Naturales, Universidad Nacional de Misiones. Félix de Azara 1552, (3300) Posadas, Misiones, Argentina.
2- Facultad de Ciencias y Tecnología. Universidad Nacional de Itapúa. María Auxiliadora, Encarnación, Paraguay.
* E-mail: silvana.a.maidana@gmail.com
Resumen
El objetivo del presente trabajo fue evaluar el efecto de las condiciones de cultivo sobre la producción de una Poligalacturonasa (PGasa) por Wickerhamomyces anomalus. Las fermentaciones se realizaron en frascos agitados, en un medio sintético, variando las condiciones de cultivo (temperatura, pH y velocidad de agitación). Se aplicó inicialmente un diseño factorial 23 y posteriormente la metodología de superficie de respuesta. Se evaluó la capacidad macerante del extracto enzimático sobre un tejido vegetal. El pH y la temperatura influyeron significativamente en la producción de la enzima PGasa, mientras que la influencia de la velocidad de agitación fue no significativa. Los mayores títulos se obtuvieron a 30° C y pH de 5,1; con un valor máximo de actividad PGasa de 18,84 UE/mL. El extracto enzimático fue capaz de macerar tejidos de pimiento morrón. Se obtuvieron extractos enzimáticos con elevada actividad PGasa, en las condiciones seleccionadas, de interés en tecnología de los alimentos.
Palabras clave: Poligalacturonasa; Wickerhamomyces anomalus; Diseño factorial; Diseño de Doehlert; Optimización.
Abstract
The objective of the present research was to evaluate the effect of the cultivation conditions on the production of a polygalacturonase (PGase) by Wickerhamomyces anomalus. Fermentations were carried out in agitated flasks, in a synthetic medium, varying culture conditions (temperature, pH and agitation). A 23 factorial design was initially applied and then response surface methodology. The macerating capacity of the enzymatic extract on a vegetal tissue was evaluated. PH and temperature significantly influenced the production of PGase enzyme, while the influence of the stirring rate was not significant. The highest titles were obtained at 30°C and pH of 5.1; with a maximum PGase activity of 18.84 EU / mL. The enzymatic extract was able to macerate bell pepper tissues. Enzymatic extracts with high PGase activity were obtained, under selected conditions, of interest in food technology.
Keywords: Polygalacturonase; Wickerhamomyces anomalus; Factorial design; Doehlert desing, Optimization.
Introducción
Las enzimas son ampliamente utilizadas en la industria de alimentos ya que catalizan diversas reacciones que resultan en mayores rendimientos y mejor calidad del producto fnal. En la industria de procesamiento de frutas y vegetales las más importantes son las enzimas pécticas o pectinasas [1]. Estas enzimas son las responsables de la degradación de las sustancias pécticas presentes en la laminilla media y en la pared celular primaria de las plantas superiores. Según su modo de acción se clasifican en: poli-galacturonasas (PGasas), pectinesterasas (PE), pectinliasas (PL) y pectatoliasas (PAL). Las PGasas pueden ser del tipo
endo-PGasas (EC 3.2.1.15) and exo-PGasas (EC 3.2.167), las cuales hidrolizan los enlaces glicosídicos α-(1,4) internos y externos de las moléculas de ácido galacturónico, respectivamente [2; 3].
Un tipo de PGasas, denominadas protopectinasas (PPasas), hidrolizan de forma restringida la protopectina presente en los tejidos vegetales, liberando pectina soluble, con la consiguiente separación de las células sin producir mayores daños, proceso denominado maceración [4]. En el proceso de maceración, los tejidos organizados de los vegetales, se transforman en una suspensión de células intactas, lo que les permite mantener sus propiedades nutritivas. El proceso de maceración es empleado en la W. anomalus, levadura aislada en la Facultad de Cien-[6]. La producción de enzimas a partir de las levaduras cias. Exactas Químicas y Naturales, UNaM (Wa cepa 110, tienen ventajas comparadas con los hongos flamentosos, cepario del Laboratorio de Microbiología de Alimentos son unicelulares, su crecimiento es relativamente simple y Biotecnología "Dr. Fernando O. Benassi", FCEQyN, en medios de cultivo económicos, y además a muchas de UNaM) [11]. ellas se las considera como microorganismos GRAS (Generalmente Reconocidos como Seguros). Otra ventaja de Medio de cultivos las levaduras es que sólo producen PGasas a diferencia de
los hongos, que originan una compleja mezcla de enzimas a)Medio de propagación (g/L): extracto de levadura
pécticas [7]. (Sigma), 5; Triptona (Difico), 5; Glucosa (Britania), 10;
La producción de enzimas microbianas, y los meca- Agar (Britania), 15; pH 5,0.
nismos que controlan su síntesis y secreción, están bajo la b)Medio de producción: glucosa (Britania), 10 g/L;
infuencia de diversos factores, tales como el pH del medio, pectina (Parafarm), 5 g/L; (NH4)2SO4, 3 g/L; KH2PO4, 1
temperatura de incubación, velocidad de agitación, natura- g/L; MgSO4, 0,5 g/L; CaCl2, 0,1 g/L; solución de vitaminas
leza y cantidad de la fuente de carbono y energía, etc. Estos (1000 ×), 1 mL/L; solución de aminoácidos (100 ×), 10
factores deben ser estudiados a fn de optimizar el creci- mL/L; solución de microelementos (1000 ×), 1 mL/L; pH
miento adecuado del microorganismo y la producción de la 5,0 [13].
enzima de interés[8]. Los diseños experimentales basados Solución (1000 ×) de vitaminas (Sigma) (µg/L): biotina,
en estadísticas son aproximaciones muy eficientes que 2; pantotenato de Ca, 400; ácido fólico, 2; inositol, 2000;
pueden llevarse a cabo con un gran número de variables niacina, 400; ácido p-aminobenzoico, 200; piridoxina, 400;
simultáneamente y además, se puede estimar la interacción ribofavina, 200; tiamina, 400.
entre variablesmejorando los rendimientos del proceso [9]. Solución (100 ×) de aminoácidos (Sigma) (mg/L):
En Argentina y en Paraguay, la producción y utiliza- histidina, 10; metionina, 20 y triptófano, 20.
ción de enzimas en la industria de alimentos es una tarea Solución de microelementos 1000 × (µg/L):
pendiente, considerando que actualmente, la mayor parte CuSO4·5H2O, 40; FeCl3·6 H2O; 200; MnSO4·H2O, 400;
de las enzimas utilizadas en la industria de alimentos son NaMoO4·2H2O, 200; ZnSO4·7H2O, 400.
importadas. El presente trabajo podrá contribuir a incenti- Todos los componentes del medio fueron autoclavados
var la producción de enzimas microbianas para aplicarlas (121º C, 15 min), excepto las vitaminas que se esterilizaron
al sector alimentario [10]. por separado mediante fltración a través de un papel de
Wickerhamomyces anomalus, es una levadura con fltro celulósico (0,22 μm, Sartorius). actividad pectinolítica, autóctona de la provincia de
Misiones, Argentina, aislada a partir de cáscaras de Producción de la enzima poligalacturonasa (PG) cítricos e identificada por métodos moleculares en el
Instituto Nacional de Tecnología Agropecuaria (INTA), Inóculo: A partir de cultivos jóvenes (24 h) de la levadura Centro Regional Mendoza, San Juan [11]. Esta levadura, desarrollada en estrías de medio de mantenimiento, se efec-al crecer en un medio compuesto por glucosa como fuente tuaron diluciones en agua destilada hasta una DO620 de 0,96. de carbono y energía y pectina de citrus como inductor, Fermentación: Se inocularon frascos Erlenmeyers de produce extractos enzimáticos con actividad, endo-PGasa, 500 mL que contenían 95 mL del medio de producción fundamentalmente. Esta enzima también posee actividad (MP) con 5 mL del inóculo. Los mismos se incubaron PPasa, capaz de macerar tejidos vegetales[12]. a 30° C en una incubadora con agitación orbital (MRC,
El objetivo del presente trabajo fue evaluar la infuen- TOU-50N 25 mm de excentricidad)a 180 rpm, durante cia de factores físicos y químicos sobre el proceso de 16 h. Finalizada la etapa de fermentación, el cultivo se producción de PGasa por W. anomalus, a escala frascos centrifugó, para remover las células de levaduras y el so-agitados, mediante diseños factoriales y luego optimizar brenadante libre de células, al que se le denominó extracto la producción enzimática mediante la metodología de enzimático (EE), se mantuvo a -18º C, hasta su utilización. superficie de respuesta.
Diseño factorial
Las fermentaciones se realizaron variando las condiciones de cultivo (temperatura, pH y agitación), mediante la aplicación de un diseño factorial 23. Estos factores se analizaron en dos niveles: alto (+1) y bajo (-1). Las variables codificadas y las respectivas variables reales, se presentan en la Tabla 1. Basado en el diseño factorial, se confeccionó una matriz con 8 experimentos (Tabla 2). Las experiencias se realizaron en un orden aleatorio, con tres repeticiones y los resultados se presentan como valores medios. El análisis de los datos obtenidos se llevó a cabo con el programa estadístico Statgraphics Centurión X V.
Los cultivos se llevaron a cabo según se describió anteriormente y se incubaron bajo las condiciones determinadas según el diseño experimental planteado, durante 16 h. Se midió la actividad PGasa de los sobrenadantes por determinación de los grupos reductores liberados con el método de Somogyi-Nelson, usando AG como referencia [4].
Tabla 1: Valores reales y codificados de los factores según el diseño factorial 23.
| Factor | Código | Niveles del factor | |
| Alto (+1) | Bajo (-1) | ||
| Temperatura (º C) | A | 50 | 30 |
| pH | B | 6 | 3 |
| Agitación (rpm) | C | 250 | 150 |
Tabla 2: Diseño a niveles alto y bajo para cada factor.
| tc | A | B | C | Exp |
| 1 | 30 | 3 | 150 | 1 |
| a | 50 | 3 | 150 | 2 |
| b | 30 | 6 | 150 | 3 |
| ab | 50 | 6 | 150 | 4 |
| c | 30 | 3 | 250 | 5 |
| ac | 50 | 3 | 250 | 6 |
| bc | 30 | 6 | 250 | 7 |
| abc | 50 | 6 | 250 | 8 |
| A: Temperatura (º C); B: pH; C: Agitación (rpm) | ||||
Diseño experimental de Doehlert
Se aplicó la metodología de superficie de respuesta, utilizando el diseño experimental de Doehlert, para optimizar las condiciones de cultivo para la producción de PGasa por Wa cepa 110 [14], Se realizaron un total de nueve experiencias que estudiaron el efecto de dos variables independientes a cinco niveles cada una, con tres repeticiones en el punto central [15].Los factores estudiados fueron temperatura (30º C- 50º C) y pH (3-6). Los valores reales y codificados de las variables independientes de acuerdo al diseño experimental, se presentan en la Tabla 3.
Las fermentaciones se realizaron según se describió anteriormente. Las experiencias se realizaron por triplicado y se tomaron para los cálculos valores promedios. Las curvas de superficie de respuesta se obtuvieron a través del programa estadístico Statgraphics Centurión XV.
Tabla 3: Valores codificados y reales utilizados en el diseño experimental de Doehlert.
| Experiencia | Valores codificados | Valores reales | ||
| Temperatura | pH | Temperatura (º C) | pH | |
| 1 | 1 | 0 | 50 | 4,5 |
| 2 | 0,5 | -0,866 | 45 | 3 |
| 3 | -0,5 | -0,866 | 35 | 3 |
| 4 | -1 | 0 | 30 | 4,5 |
| 5 | -0,5 | 0,866 | 35 | 6 |
| 6 | 0,5 | 0,866 | 45 | 6 |
| 7 | 0 | 0 | 40 | 4,5 |
| 8 | 0 | 0 | 40 | 4,5 |
| 9 | 0 | 0 | 40 | 4,5 |
| Aplicación del extracto enzimático | ||||
Se evaluó la capacidad macerante del EE de Wa cepa 110 sobre tejidos vegetales de pimiento morrón (Capsicum annuum L.). Para ello los frutos de morrón fueron lavados y cortados en cubos de aproximadamente 5 mm de cada lado. El proceso de maceración se llevó a cabo en frascos Erlenmeyers de 125 mL, los que contenían 15mL del EE y 35 mL de bufer acetato de sodio/ácido acético (BAc., 0,2 M, pH 4,5). Los frascos se incubaron a 180 rpm, en una incubadora con agitación orbital, durante 3,5 h, a 40º C. Las experiencias se realizaron por triplicado. El pH y la temperatura seleccionados para el proceso de maceración se encuentran dentro del rango de estabilidad de la enzima [5]. Una vez cumplido el tiempo de maceración correspondiente, el contenido total de cada frasco se fltró a través de malla de 20 mesh. El fltrado se recolectó en tubos cónicos graduados de 10 mL. La suspensión de células simples liberadas fue sedimentada a 5º C, durante 4 h [12] y luego secadas en estufa a 45º C hasta peso constante. La pérdida de coherencia de los tejidos y el peso de las células libresse utilizaron como indicadores de la actividad macerante [16]. La observación de células libres se efectuó mediante un microscopio Olympus, modelo CH-2, con un aumento de 400 ×. Los blancos del proceso de maceración se realizaron con la enzima inactivada. El rendimiento del proceso de maceración se expresó como porcentaje de células simples liberadas respecto al peso seco del tejido original (% p/p).
Resultados y Discusión
En la Tabla 4 se presenta el Análisis de Varianza para la producción de PGasa por Wa cepa 110 mediante el diseño factorial 23.
Tabla 4: Análisis de Varianza para la producción de PG por Wa cepa 110mediante el diseño factorial 23.
| Fuente | Suma de Cuadrados | Gl | Cuadrado Medio | Razón-F | Valor-P |
| A:Temperatura | 1139,08 | 1 | 1139,08 | 3722,3 | 0,0000 |
| B:pH | 18,7884 | 1 | 18,7884 | 61,40 | 0,0043 |
| C:Agitación | 0,26645 | 1 | 0,26645 | 0,87 | 0,4196 |
| AB | 19,7192 | 1 | 19,7192 | 64,44 | 0,0040 |
| Error total | 0,91805 | 3 | 0,30602 | ||
| Total (corr.) | 1178,77 | 7 |
En la Figura 1 se presenta el Diagrama de Pareto y en la Figura 2 el gráfico de los Efectos Principales.
| 1=1 + | ||||
| A: Temperatura | ||||
| AB B:pH | 1 | 1 | ||
| C: Agitación | íl | |||
| C | ) | 20 40 60 Efecto estandarizado | 80 | |
Figura 1: Diagrama de Pareto para la producción de PG por Wa cepa 110.
Figura 2: Gráfica de los efectos Principales para la producción de PG por Wa cepa 110
La Tabla de ANOVA (Tabla 4) muestra que la temperatura, el pH y la interacción entre éstos, influyeron significativamente en la producción de la enzima, siendo el valor de P menor a 0,05, para un nivel de confanza del 95,0%. El R2 estadístico (99,92%) indicó que el modelo presentó un buen ajuste a los datos experimentales.
El pH infuyó de manera positiva sobre la producción de la enzima, mientras que la temperatura lo hizo de manera negativa, al igual que la interacción entre ambos factores. La velocidad de agitación no influyó sobre la misma variable de respuesta (Fig. 1). El aumento de temperatura mostró una marcada disminución en la producción de la enzima (Fig. 2).
La producción de PGasa por Wa cepa 110 en las distintas experiencias realizadas según el diseño experimental de Doehlert (Tabla 3) se convirtieron en una ecuación po-linomial de segundo orden que se presenta a continuación:
En dicha ecuación, la temperatura (T) y el pH, representan los valores codificados. La ecuación presentó un muy buen ajuste a los datos experimentales (R2= 0,99).
Según la ecuación 1, se puede puntualizar que las dos variables independientes tuvieron un efecto lineal signif-cativo positivo (pH) y negativo (T). La temperatura fue la variable lineal más importante que afectó la producción de PG, ya que posee el mayor coeficiente de regresión. Ambos factores tuvieron efectos cuadráticos negativos (pH) y positivos (T), indicando la existencia de un máximo de producción para la temperatura y un mínimo para el pH.
En la Figura 3 se presenta la superficie de respuesta para la producción de PG en función de las dos variables independientes.
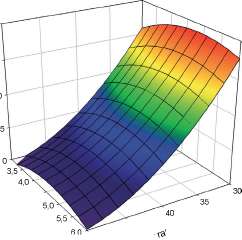
Figura 3: Superficie de respuesta mostrando el efecto de la temperatura y el pH sobre la producción de PG por W. anómalus.
La Figura 3 muestra que la mayor producción de la enzima se obtuvo a temperaturas bajas y pH en el rango de 5 a 6.
La ecuación 1 arrojó un valor máximo de producción de PG de 18,84 UE/mL a 30° C y pH 5,1.Esta temperatura de 30º C coincide con el valor más bajo ensayado, por lo tanto es posible suponer que la misma no se corresponde con la temperatura óptima para la producción de la enzima. Sin embargo se seleccionó esta temperatura mínima, a los efectos de evitar costos adicionales en el proceso, debido a la necesidad de refrigerar el cultivo en el biorreactor, en las épocas de elevadas temperaturas en la región.
Moyo y col. (2003) [17] determinaron que los efectos de la temperatura y el pH fueron los factores más significativos en la producción de enzimas con actividad pectinolítica de Kluyveromyces wickerhamii. Las condiciones óptimas estimadas fueron pH 5,0 y temperatura a 32º C. Otros autores informaron que la temperatura de fermentación ejerció un efecto significativo sobre la producción de PG por Bacillussubtilis, obteniéndose elevados rendimientos entre 30-35º C [18].
En la Figura 4 se muestra el tejido de pimiento morrón, luego del proceso de maceración con el EE de Wa cepa 110. En la Figura 5 se muestran microfotografías (400 ×) de las células liberadas del tejido vegetal, luego del tratamiento enzimático.

Figura 4: Tejidos de pimiento morrón macerados con el extracto enzi-mático (A). Blanco con la enzima inactivada (B).
Transcurridas 3,5 h de incubación se observó ablandamiento del tejido vegetal (Fig. 4 A). Los controles realizados con la enzima inactivada mostraron que el efecto de la maceración fue causado principalmente por la actividad PGasa presente en el extracto enzimático y no por efectos mecánicos productos de la agitación (shear) (Fig. 4 B).
El examen microscópico de los productos macerados mostró células simples liberadas y agregados celulares (Fig. 5 A) no se observó lisis de la pared celular. El rendimiento del proceso de maceración resultó del 98,02% (% p/p).
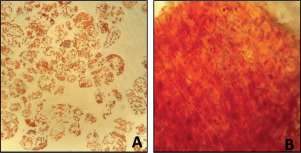
Figura 5: Microfotografías (400 ×) de células de tejidos de pimiento morrón macerados con el extracto enzimático de Wa cepa 110 (A), blanco con la enzima inactivada (B).
La actividad de la enzima producida por Wa cepa 110se centra particularmente en la laminilla media (protopectina) que une entre sí a las células del tejido y no degrada celulosa, debido a lo cual, las células no se lisaron [11].
Conclusión
El pH y la temperatura infuyeron significativamente en la producción de la enzima PGasa por Wa cepa 110, mientras que la infuencia de la velocidad de agitación fue no significativa. Los mayores títulos se obtuvieron a 30° C y pH 5,1; con un valor máximo de producción de la enzima
(en el rango evaluado) de 18,84 UE/mL. Teniendo en cuenta las elevadas temperaturas imperantes en la región, durante los meses de verano, esta temperatura de 30º C permitiría realizar los cultivos a escala biorreactor sin la necesidad de refrigeración, evitando de esta manera costos adicionales al proceso.
El extracto enzimático de Wa cepa 110, fue capaz de macerar tejidos de morrón, observándose ablandamiento del tejido y células simple liberadas, sin evidenciarse ruptura celular, luego de 3,5 h de incubación.
Bibliografía
1. Tapre, A. R. y Jain, R. K. Pectinases: Enzymes for fruit pro-cessing industry. International Food Research Journal, 21(2): p. 447-453. 2014. [ Links ]
2. Tari, C.; Gögus, N. y Tokatli, F. Optimization of biomass, pellet size and polygalacturonase production by Aspergillus sojae ATCC 20235 using response surface methodolo-gy. Enzyme and Microbial Technology, 40(5): p. 1108-1116. 2007.
3. Paudel, Y. P.; Lin, C.; Shen, Z. y Qin, W. Characterization of pectin depolymerising exo polygalacturonase by Ba-cillus sp. HD2 isolated from the gut of Apis mellifera L. Microbiology Discovery, 3 (2): 1-8. 2015.
4. Ferreyra, O. A.; Cavalitto, S. F. ; Hours, R. A. y Ertola, R. J. Infuence of trace elements on enzyme production: Protopectina-se expression by a Geotrichum klebahnii strain. Enzy-me and Microbial Technology.31(4): p. 498-504. 2002.
5. Martos, M. A.; Butiuk, A. P.; Rojas, N. L. y Hours, R. A. Purifi-cation and characterization of a polygalacturonase produced by Wickerhamomyces anomalus. Brazilian Archives of Biology and Technology, 57(4): p. 587-594. 2014b.
6. Malvessi, E. y Da Silveira, M. M. Infuence of medium compo-sition and pH on the production of polygalacturonases by Aspergillus oryzae. Brazilian Archives of Biology and Technology, 47(5): p. 693-702. 2004.
7. Da Silva, G. E.; De Fátima Borges, M.; Medina, C.; Hilsdorf Piccoli, R. y Freitas Schwan, R. Pectinolytic enzymes secreted by yeasts from tropical fruits. FEMS Yeast Research, 5(9): p. 859-865. 2005.
8. Barragán, J. C. A.; Zerpa, S. A. I.; Castillo, M. L. S.; Haro, M. R.; Alarcón, W. N. y Gasco, F. O. Efecto de la temperatura y pH sobre la actividad y estabilidad de pectinasas producidas por Bacillus spp. Revista Científica de la Facultad de Ciencias Biológicas. 34(1): p. 33-41. 2014.
9. Díaz, A.; Flórez, J. y Cotes, A. M. Optimización de un medio de cultivo para la producción de la levadura Pichia onychis (Lv027). Revista Colombiana de Biotecnolo-gía.VII(1): p. 51-58. 2005.
10. Yubero, F. Relevamiento del uso de enzimas en la industria paraguaya y su aplicación en la producción de alimentos para animales. Compendio de Ciencias Veterinarias, 6(1): p. 31-34. 2016
11. Martos, M. A.; Zubreski, E. R.; Combina, M.; Garro, O. A. y Hours, R. A. Isolation of a yeast strain able to produce a po-lygalacturonase with maceration activity of cassava roots. Food Science and Technology (Campinas), 33(2): p. 332-338. 2013a.
12. Martos, M. A.; Zubreski, E. R.; Garro, O. a. y Hours, R. A. Pro-duction of Pectinolytic Enzymes by the Yeast Wickerha-nomyces anomalus Isolated from Citrus Fruits Peels. Biotechnology research international, p. 1-7. 2013b.
13. Martos, M. A.; Butiuk, A. P.; Rojas, N. L. y Hours, R. A. Batch culture of Wickerhamomyces anomalus in a lab scale bioreactor for poligalacturonase production. Revista Colombiana de Biotecnologia, 16(2): p. 68-73. 2014ª.
14. Doehlert, D. H. Uniform Shell Designs. Journal of the Royal Statistical Society.19(3): p. 231-239. 1970.
15. Butiuk, A. P.; Adachi, O. y Hours, R. A. Yerba mate as a novel inducer for fungal chlorogenate hydrolase production. Biocatalysis and Agricultural Biotechnology.4(3): p. 327-334. 2015.
16. Schwan, R. F.; Cooper, R. M. y Wheals, A. E. Endopolygalac-turonase secretion by Kluyveromyces marxianus and other cocoa pulp-degrading yeasts. Enzyme and Mi-crobial Technology, 21(4): p. 234-244. 1997.
17. Moyo, S.; Gashe, B. A.; Collison, E. K. y Mpuchane, S. Optimi-sing growth conditions for the pectinolytic activity of Kluyveromyces wickerhamii by using response surface methodology. International Journal of Food Microbio-logy, 85(1-2): p. 87-100. 2003.
18. Uzuner, S. y Cekmecelioglu, D. Enhanced pectinase produc-tion by optimizing fermentation conditions of Bacillus subtilis growing on hazelnut shell hydrolyzate. Journal of Molecular Catalysis B: Enzymatic, 113: p. 62-67. 2015.
Recibido: 08/01/2018. Aprobado: 14/02/2019.














