En diciembre de 2019 surgieron casos de neumonías causadas por patógenos desconocidos en la ciudad de Wuhan, provincia de Hubei, China. En enero 2020, se identifica un nuevo ARN beta-coronavirus, posteriormente fue nombrado como síndrome coronavirus respiratorio agudo grave 2 (SARS-CoV-2), agente etiológico de la enfermedad denominada COVID-19. La OMS declara la enfermedad por SARS-CoV-2 como una emergencia de salud pública mundial y el 12 de marzo declara la situación de pandemia1.
La mortalidad varía según la región. Se estima la misma entre 1 al 20% dependiendo de las características del huésped2. Al inicio, se consideraba que afectaba es pecialmente a mayores de 65 años, con comorbilidades como diabetes mellitus (DBT), hipertensión arterial (HTA) e inmunocomprometidos. En el estudio de Huangy col.1 se sugiere que los hombres mayores con comorbilidades crónicas son más vulnerables a COVID-19 grave1. Los estudios sugieren que existen diferencias entre hombres y mujeres en la respuesta inmunitaria a la infección por COVID-19. Las mujeres, en comparación con los hombres, son menos susceptibles a las infecciones virales basadas en una inmunidad innata diferente, hormonas esteroides y factores relacionados con los cromosomas sexuales. Los genes reguladores inmunitarios codificados por el cromosoma X en el género femenino provocan niveles de carga viral más bajos y menos inflamación que en el hombre, mientras que las células T CD4+ son más altas con una mejor respuesta inmune. Adicionalmente, las mujeres generalmente producen niveles más altos de anticuerpos que permanecen en la circulación por más tiempo3.
Aún es materia de estudio como afecta la COVID-19 a pacientes con enfermedades autoinmunes del tejido conectivo (EATC), con o sin tratamiento inmunosupresor y que característica adopta la respuesta inmunitaria al virus en estos pacientes4,5. Murtas y col. encontraron que la enfermedad autoinmune es un factor de riesgo para COVID-196. No se encontró diferencia en las manifesta ciones clínicas de COVID-19 entre pacientes con EATC y población general, incluyendo media de días de estadía en el hospital, porcentaje de requerimiento de ventilación mecánica, hallazgos en las radiologías de tórax y tasa de letalidad1,7. Por otra parte, la evidencia de alteraciones de la coagulación en algunos casos de COVID-19 puede implicar consideraciones adicionales para la atención clínica de los pacientes con COVID-19 que tienen EATC con presencia de anticuerpos antifosfolípidos, incluido el anticoagulante lúpico, el cual se considera un factor de riesgo de trombosis arterial y venosa. Aunque los estudios aún no han confirmado un riesgo elevado de trombosis entre el subconjunto de pacientes con COVID-19 con anticuerpos antifosfolípidos, la coagulación anormal sugiere que los que poseen ambos factores de riesgo, pueden requerir un seguimiento más estricto debido a la posibilidad de generar eventos trombóticos8,9.
Otros estudios mostraron que existiría un mayor ries go de infección por SARS-CoV-2 en quienes recibieron fármacos inmunosupresores biológicos (b-DMARD). Los usuarios de rituximab podrían tener una mayor tasa de infección por SARS-CoV-2 que la población general6,8,9. Si bien se observó que las respuestas específicas de las células T son importantes para eliminar la infección, la respuesta de anticuerpos sigue siendo crucial para neutra lizar el virus10. En general, la inmunosupresión se asocia con un mayor riesgo de infección grave por SARS-CoV-2, por lo tanto, podrían tener también un curso más grave en aquellos pacientes con EATC. Sin embargo, podría haber un posible efecto protector o inclusive terapéutico de ciertas terapias inmunomoduladoras11. Entre otros se mencionan prednisona (40 mg/día), antipalúdicos, colchi cina, inhibidores de JAK quinasas y antagonistas de IL -6 o IL-112. El uso de esteroides es controversial, ya que su uso crónico se asoció a peor pronóstico, sin embargo el uso en etapa aguda puede mejorar la supervivencia13. En el ensayo RECOVERY se mostró que la dexameta sona en dosis bajas (6 mg/día) durante 10 días reduce la mortalidad en pacientes ventilados en un 35% y en los que recibieron oxígeno en un 20%14.
Se ha demostrado que los adultos inmunodeprimidos producen anticuerpos contra la infección por SARS-CoV-2 de forma eficaz, aunque un poco más tarde en compara ción con los controles inmunocompetentes. Sin embargo, hay datos emergentes indicando que las respuestas de anticuerpos a la infección por SARS-CoV-2 pueden ser de corta duración, con una disminución de los niveles séricos a los 3 meses15.
La respuesta inmune al SARS-CoV-2 se caracteriza por un fuerte incremento de los anticuerpos anti SARS-CoV-2 luego de la segunda o de la tercera semana a partir del inicio de la enfermedad. Long y col. informa que las respuestas de IgM alcanzan su punto máximo durante la primera semana después de la infección y antes del cambio de clase a IgG (17-19 días)16. Otros autores mencionan que tanto la IgM como la IgG suelen aumentar concomitantemente y detectarse apartir de los 10 días de la aparición de los síntomas. Estos autores no proporcionan información sobre el tiempo que permanece dosable la IgG17.
La seroconversión IgG se produce luego de los 14 días del inicio de los síntomas, los Ac. generados tienen una adecuada especificidad y sensibilidad18,19.
En estudios previos es controvertido el vínculo entre la gravedad de la infección y la respuesta de anticuerpos10,19; sin embargo, como concepto general, se asume que a mayor gravedad los niveles de anticuerpos serán supe riores. En cuanto a la seroconversión no se ha llegado a un acuerdo en cuanto a que varíen los diferentes grupos etarios20. Las pruebas de detección de anticuerpos espe cíficos para el virus SARS-CoVIgG e IgM han mostrado resultados falsos positivos en pacientes con EATC como lupus eritematoso sistémico (LES), síndrome de Sjögren, esclerosis sistémica, enfermedad mixta del tejido conecti vo y artritis reumatoide (AR)21. Se ha informado reacción cruzada de estos Ac. con los de hepatitis A IgG, con el factor reumatoideo y con los Ac. anti ds-DNA, por lo que deben interpretarse de acuerdo al contexto clínico de cada paciente22.
En nuestro medio existen muy pocos datos sobre prevalencia, incidencia, características clínicas, curso evolutivo y respuesta inmunitaria humoral de esta infec ción en EATC.
El objetivo de este estudio fue describir las carac terísticas clínicas de la COVID-19 en una cohorte con EATC, además de evaluar la prevalencia de anticuerpos de tipo IgG contra la proteína spike (S) SARS-CoV-2 (SARS-CoV-2 anti S) en pacientes con y sin EATC que cursaron COVID-19.
Materiales y métodos
Población de estudio: se consideraron como criterios de in clusión edad mayor a 18 años, de ambos sexos, con EATC que hayan cursado infección por SARS-CoV-2 y con un tiempo no menor a 20 días desde el inicio de los síntomas para la toma de muestra. Se consideró caso clínico de CO VID-19 a la definición brindada por el Ministerio de Salud de la Nación. Los pacientes podían tener confirmación por técnica de PCR mediante hisopado nasofaríngeo o contacto epidemiológico estrecho con un caso confirmado y síntomas compatibles. Se realizó también dosaje de anticuerpos IgG anti-proteína S de SARS-CoV-2 a un grupo poblacional sin EATC con antecedentes de COVID-19. Todos los pacientes firmaron consentimiento informado, la negativa para la firma se consideró criterio de exclusión.
Toma de muestra, almacenamiento y procesamien to: los pacientes concurrieron con un ayuno de 4 horas. Se realizó punción venosa periférica extrayendo 8 ml de sangre entera, se fraccionó el suero en alícuotas y se al macenó a -20 °C hasta el procesamiento del mismo. Las variables de interés fueron la edad, sexo, tipo de EATC y actividad al momento de la infección, tratamiento inmuno supresor, prevalencia de uso y dosis de esteroides, signos y síntomas de COVID-19, necesidad o no de internación, duración del cuadro viral, diagnóstico (antecedente de PCR positiva o epidemiológico), días desde el primer signo o sín toma de COVID-19 y la toma de muestra para anticuerpos, y niveles de anticuerpos SARS-CoV-2anti spike (S).
La cuantificación de anticuerpos IgG dirigidos contra la proteína S de SARS- CoV-2 se realizó mediante test de ELI SA (COVID AR IgG, Laboratorio Lemos SRL. Con desarrollo CONICET, Argentina)
Luego de validar el ensayo con los valores de absorban cia obtenidos tanto del control negativo como del positivo se procedió a calcular la reactividad de las muestras en estudio. Se consideraron negativas a las muestras con un valor de DO 450 nm inferior a 0.237 y positivas a las que tuvieron un valor de DO 450nm superior a 0.28923.
Los datos cualitativos se describen como porcentaje, los datos cuantitativos como media y desvío estándar o mediana y rango intercuartílico(RIC) de acuerdo a la distribución de la variable. Se utilizó chi cuadrado para la evaluar diferencias en variables discretas y test de student o Mann-Whitney para variables continuas, según corresponda. Para las variables que se asociaron de forma independiente con la variable de resultado dicotómica se realizó un análisis de regresión logística binaria. Se consideró significativa un valor alfa de 5% o menor. Se utilizó IBM SPSS versión 19.
Los datos fueron procesados y presentados de tal mane ra que resultase imposible la identificación de los pacientes participantes. El estudio fue aprobado por el Comité de Ética del Hospital de Clínicas José de San Martín de la Ciudad Autónoma de Buenos Aires.
Resultados
Se evaluaron 53 pacientes con EATC, 46 con infección demostrada por técnica de PCR (87%). La mayoría mu jeres (81%) y edad media de 48 ± 14 años. La zona de residencia predominante fue el área metropolitana de Buenos Aires (34/53, el 64.2%) que comprende la Ciudad Autónoma de Buenos Aires y las localidades linderas de la Provincia de Buenos Aires.
Se describieron 61 casos de enfermedades auto inmunes considerando las superposiciones en los 53 pacientes de la muestra. En orden de frecuencia fueron: AR (22/61), LES (17/61), esclerodermia sistémica (7/61), vasculitis primarias (7/61), enfermedad de Still del adulto (7/61), artritis psoriásica (2/61), síndrome antifosfolípido (2/61), síndrome antisintetasa (1/61) y artritis idiopática juvenil (1/61).
Las comorbilidades más frecuentes fueron hiper tensión arterial (21%) y diabetes mellitus no insulino-requiriente (13%). Otras fueron hipotiroidismo (9%), dislipidemia (6%), insuficiencia renal crónica (4%), osteoporosis (2%), amiloidosis (2%), epilepsia (2%), tumores (2%) y asma bronquial (2%). El tabaquismo estuvo presente en el 8% de los pacientes y 9% se clasificaron como ex tabaquistas.
Con respecto a la medicación habitual, 17/53 (32%) utilizaban b-DMARD, siendo los inhibidores del TNF alfa (9/17), rituximab (3/17), abatacept (3/17) y tocilizumab (2/17) los más utilizados. Una paciente, en tratamiento con adalimumab, lo había suspendido por decisión propia al inicio de la epidemia. Durante la infección viral, la mitad (8/16) continuaron con el b-DMARD (5 con anti TNF alfa, 2 con rituximab y 1 con abatacept) y el resto lo suspendió hasta la resolución del cuadro.
Más de la mitad utilizaban esteroides (30/53, 56.6%), la mediana de dosis diaria fue de 8 (RIC 6) mg, y 16 tomaban hidroxicloroquina (30%). El inmunosupresor sintético más frecuente fue el metotrexato (22/53, 41.5%) con una dosis promedio semanal de 15 ± 5.5 mg.
La Figura 1 describe los signos y síntomas durante la infección.
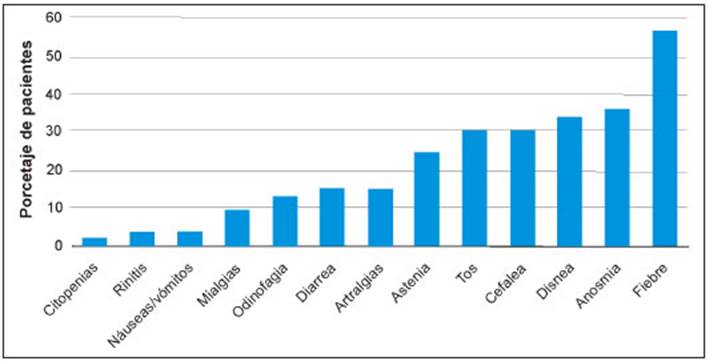
Fig. 1 Signos y síntomas de infección por SARS CoV2 en 53 pacientes con enfermedad autoinmune del tejido conectivo
Del total de pacientes, 30/53 (56.6%) cursaron la in fección de manera ambulatoria y 23/53 (43.4%) debieron ser ingresados en centros de salud, de los cuales solo 5 (9.4%) requirieron internación en sala de cuidados intensivos y uno de ellos necesitó asistencia respiratoria mecánica. Durante la internación se indicó dexametasona en 11/23, tocilizumab en 1/23, plasma de convalecientes en 3/23 y antibióticos en 12/23.
La mayor proporción de los hospitalizados padecían LES 6/23, seguido por vasculitis 5/23, esclerodermia 5/23, AR 4/23, artritis psoriásica 2/23 y enfermedad de Still del adulto 1/23.
Se registraron 3 muertes: un paciente de 81 años con vasculitis asociada a ANCA, diabetes e insuficiencia renal crónica en diálisis; uno de 53 años con LES y síndrome antifosfolípido y uno de 61 años con esclerodermia aso ciada a cáncer de cuello de útero estadio IV-B.
Los que utilizaban una dosis diaria de meprednisona mayor o igual a 10 mg mostraron una tendencia a requerir más internaciones (8/12) que los que no utilizaban este roides o que recibían una dosis estable y menor a 10 mg diarios (15/41, p = 0.064).
En la evaluación de variables que predisponen a nece sidad de internación se encontró que la edad [OR 1.094 (IC95% 1.008-1.187), p = 0.032] fue la única variable que se asoció a internación de manera independiente.
Se determinó la presencia de SARS-CoV-2 anti S en 23/53 (43.4%) pacientes, 15/23 tuvieron niveles detecta bles de anticuerpos y en 8/23 el resultado fue negativo.
El tiempo de duración del cuadro clínico por COVID-19 mostró una tendencia a ser mayor en los pacientes que desarrollaron anticuerpos que en aquellos que no los desarrollaron (14 ± 8 vs 9 ± 3 días, p = 0.07).
El tiempo transcurrido desde la infección clínica y la toma de muestra de suero para detección de SARS-CoV-2 anti S fue de 66 ± 33 días (69 ± 38 días en el grupo con anticuerpos positivos y 60.5 ± 24 en el grupo con anticuerpos negativos, p = 0.01).
Entre los 17 pacientes con b-DMARD, 3 usaban rituxi mab, dos de ellos fueron testeados y ambos desarrollaron anticuerpos. Dos usaban tocilizumab al momento de la infección y solo 1 desarrolló anticuerpos.
De los 15 pacientes con anticuerpos positivos, 7 requi rieron internación durante la COVID-19, en contraste con los 8 pacientes con anticuerpos negativos donde solo 1 requirió internación durante el cuadro infeccioso.
La prevalencia de signos y síntomas en cada grupo se representan en el Tabla 1.
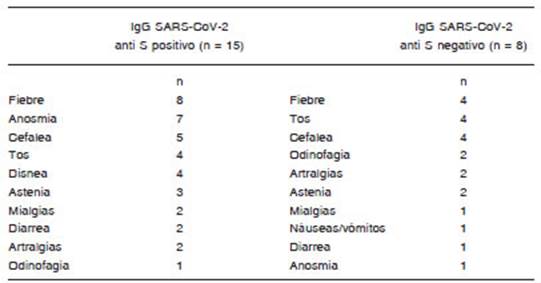
Tabla 1 Pacientes con enfermedades autoinmunes del tejido conectivo. Signos y síntomas en orden decreciente de prevalencia
Por otro lado, se incluyeron 23 pacientes que cur saron la infección viral, 19/23 confirmados por PCR, que no tenían EATC para investigar los niveles de anticuerpos IgG anti-SARS-CoV-2. En 12/23 se detec taron anticuerpos.
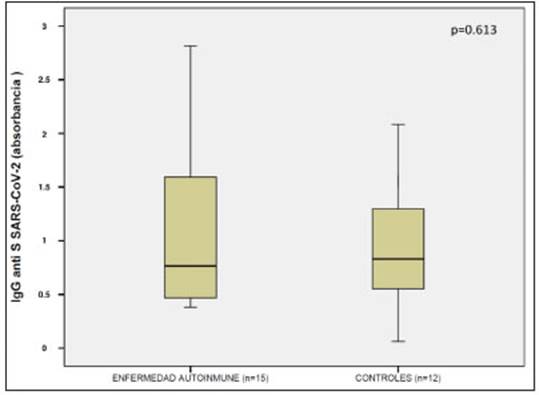
Entre este grupo y los pacientes con EATC hubo diferencias significativas, respectivamente, en la edad (35 ± 9 vs 48 ± 14 años, p < 0.0001), en el género (34.8 vs 81% eran del sexo femenino, p < 0.001), el tiempo desde la infección hasta la toma de la muestra para anticuerpos (73 ± 39 vs 66 ± 33 días, p = 0.01) y la necesidad de internación (2/23 vs. 23/53, p = 0.032). Por el contrario, no hubo diferencias significativas entre ambos grupos en la duración de la enfermedad COVID-19 (12 ± 8 vs 13 ± 7 días), ni en los niveles de Ac IgG anti-SARS-CoV-2 [0.77 (RIC = 1.47) vs 0.83 (RIC = 0.99)] (Fig. 2).
Discusión
En nuestra serie de pacientes con EATC, el síntoma prin cipal fue la fiebre. Fiebre, disnea, anosmia, tos y astenia acumularon el 80% de la sintomatología.
La mitad usaba esteroides a dosis bajas y un tercio utilizaba b-DMARD, sin embargo, no pareció influir en la evolución de la enfermedad viral. En nuestra serie, el 43.4% requirió hospitalización, un porcentaje similar al comunicado por otros autores23. Al igual que en la cohorte citada, las principales enfermedades fueron LES y vasculitis primarias. La edad avanzada fue una variable relacionada con la necesidad de internación. Hubo mayor prevalencia de internados en el grupo que utilizaba esteroides a dosis de 10 mg diarios o mayores, aunque no alcanzó un nivel estadístico de significancia.
Pocos necesitaron del ingreso a unidad de cuidados intensivos (9.4%). El porcentaje de fallecidos fue de 5.6%, ligeramente menor a lo informado en otras series13.
Según nuestro conocimiento, este es el primer estu dio que evalúa la prevalencia de anticuerpos IgG anti S SARS-CoV-2 en una población de pacientes con EATC en la República Argentina.
Se detectaron anticuerpos en concentraciones signi ficativas en el 62% de los pacientes luego de la recupe ración de COVID-19.
Mayor cantidad de pacientes en el grupo con anti cuerpos habían requerido internación durante el curso de la infección viral, asumiendo que tuvieron un cuadro clínico más grave, aunque no fue significativo desde el punto de vista estadístico. No hubo diferencias entre ambos subgrupos con respecto a la edad, la duración de la enfermedad, la dosis de esteroides o uso de in munosupresores.
En la población sin EATC la prevalencia de anticuerpos fue de 52.1%.
El estudio no fue diseñado para comparar entre ambos grupos y la distribución de variables no fue similar, con diferencias significativas como la mayor prevalencia de sexo femenino en los pacientes con EATC y mayor edad media. Sin embargo, los valores de anticuerpos en suero fueron similares en ambos grupos.
Tal como sugiere nuestro estudio, los pacientes con EATC desarrollarían una respuesta inmune humoral con tra SARS-CoV-2 similar a la población general, a pesar del compromiso del sistema inmunitario por las distintas enfermedades de base y los fármacos inmunomodulado res utilizados en el tratamiento.
Debido a algunas de las limitaciones de nuestro estu dio como la poca cantidad de pacientes y la evaluación transversal sin seguimiento, desconocemos si estos anticuerpos persisten en el tiempo. Creemos necesario realizar estudios con mayor número de casos y segui miento clínico y serológico.