Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Archivos argentinos de pediatría
Print version ISSN 0325-0075
Arch. argent. pediatr. vol.108 no.6 Buenos Aires Nov./Dec. 2010
ARTÍCULO ESPECIAL
Pediatría basada en la evidencia. Estudios de diagnóstico (2ª parte)
Evidence-based pediatrics. Diagnostic tests (2nd part)
Dra. Graciela Demirdjiana
a. Docencia e Investigación. Hospital Nacional de Pediatría"Prof. Dr. Juan P. Garrahan."
Correspondencia: Dra. Graciela
Demirdjian:
gdemir@intramed.net
Conflicto de intereses:
Ninguno que declarar.
Recibido: 4-7-10
Aceptado: 28-7-10
RESUMEN
El proceso diagnóstico es complejo y ejercitarlo
exige experiencia e instrumentos adecuados. El
avance tecnológico ha multiplicado el número
de pruebas diagnósticas disponibles, aunque son
pocas las herramientas clínicas bien diseñadas,
validadas y útiles. En este artículo describimos
el proceso de construcción de reglas de predicción
clínica y el uso de curvas ROC para la selección
del valor límite óptimo para una prueba
con resultado numérico.
Palabras clave: Medicina basada en la evidencia; Diagnóstico; Pronóstico; Curva ROC; Reglas de predicción clínica.
SUMMARY
Diagnosis is a complex process, demanding
experience and proper instruments. Technology
has advanced rapidly, increasing the number
of available diagnostic tests. However, few
well designed and validated useful clinical tools
exist. This article summarizes the development
process for clinical prediction rules and the use
of ROC curves to select the best cutoff point for
tests with continuous results.
Key words: Evidence-based medicine; Diagnosis; Prognosis; ROC curve; Clinical prediction rules.
INTRODUCCIÓN
En la primera parte de este artículo,
publicada en la Sección de Pediatría
basada en la evidencia, iniciamos
el análisis crítico de los estudios de validación
de pruebas diagnósticas1 según
las Guías del JAMA2 y utilizamos,
como ejemplo, un artículo sobre gases
capilares y arteriales para el diagnóstico
de hiperoxemia en neonatos.3 En
esta segunda parte abordaremos dos
temas conexos algo más complejos:
las curvas ROC y las reglas de predicción
clínica.
CURVAS ROC
Nuestro análisis crítico del artículo
sobre diagnóstico de hiperoxemia en
neonatos había considerado la capacidad
operativa de la prueba tomando
sus resultados en formato dicotómico.
Esto presupone que la prueba sólo
puede ofrecer un resultado cualitativo
(positivo-negativo), o bien que los resultados
se expresan en una escala numérica
continua, pero se conoce cuál
es el valor límite para discriminar entre
enfermos y sanos (el punto de corte
o "cut-off point"). Seleccionar un punto
de corte óptimo puede parecer sencillo,
pero en realidad involucra una serie
de consideraciones acerca de cómo
se utilizará la prueba diagnóstica.
Para empezar, recordemos que la
sensibilidad y especificidad sirven
principalmente para elegir la prueba
a utilizar:
• Las pruebas más sensibles se utilizan para tamizaje (screening), al inicio del proceso diagnóstico, para descartar enfermedad, o cuando la oportunidad perdida de tratamiento presupone un gran riesgo.
• Las pruebas más específicas se utilizan para confirmación, al final del proceso diagnóstico, y para enfermedades cuyo tratamiento innecesario puede ser peligroso.
Cuando el resultado del estudio diagnóstico se expresa en una escala numérica continua, es necesario decidir a partir de qué valor de la prueba se considerará al sujeto como enfermo. Aquí ocurre algo interesante: modificar el punto de corte altera la capacidad operativa de la prueba:
• Si corremos el punto de corte hacia valores menos patológicos, ganamos en sensibilidad (incluimos más casos como enfermos), pero perdemos en especificidad (muchos de estos casos pueden ser falsos positivos).
• Si lo movemos hacia valores más patológicos, ganamos en especificidad (tendremos menos falsos positivos), pero perderemos sensibilidad (es posible que algunos enfermos escapen al diagnóstico).
Para entender esto con más claridad volvamos a nuestro artículo y observemos en la Tabla 1 (Cuadro 2 en la publicación original3) cómo se modifica la capacidad operativa (medida por la razón de probabilidad o "likelihood ratio" que relaciona los verdaderos y falsos positivos y negativos) utilizando distintos puntos de corte de PcapO2. (Como repaso de los conceptos del artículo anterior se pueden reconstruir con estos datos las tablas de 2 x 2 y calcular las medidas operativas para cada punto de corte).
Tabla 1. Rendimiento diagnóstico del gas capilar contra el arterial para distintos valores límite (puntos de corte)3
La elección del valor límite (punto de corte) óptimo de una prueba con resultado numérico
implica balancear estas dos alternativas para
maximizar la capacidad operativa del método
(máxima sensibilidad y especificidad) y minimizar
los errores "negociando" entre verdaderos
positivos (sensibilidad) y falsos positivos (1 - especificidad).
Para este proceso se utiliza un gráfico
denominado curva ROC (Receiver Operating
Characteristic) o curva de respuesta relativa.4 Estas
curvas son diagramas de correlación donde se
relacionan la sensibilidad en las ordenadas contra
la especificidad en las abscisas para los diferentes
puntos de corte de un método. La principal utilidad
de la curva es asistir en la toma de decisión
acerca de cuál es el valor límite óptimo, que es
aquél que más se acerca al extremo superior izquierdo
del gráfico: máxima sensibilidad y especificidad,
o máxima tasa de verdaderos positivos
(TVP) con un mínimo de falsos positivos (TFP).
En la Figura 1 (reproducida de nuestro artículo
de gases capilares) se presenta esta curva ROC
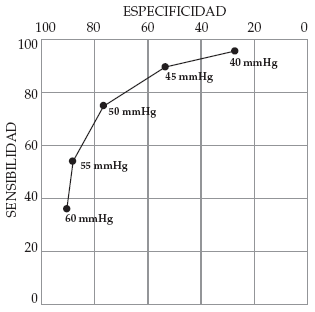
para los distintos puntos de corte de PO2 capilar para el diagnóstico de hiperoxemia. Observe que:
• en el eje Y se representa la sensibilidad (TVP) de manera creciente de 0 a 100%;
• en el eje X se grafica la especificidad (1 - TFP) en forma decreciente de 100 a 0% (también podría mostrarse en escala creciente de 0 a 100% pero como 1 - especificidad);
• a medida que aumenta la sensibilidad, la especificidad disminuye y viceversa;
• el valor de PcapO2 de 50 mmHg es el punto que tiene mayor TVP y menor TFP (el que se ubica más cercano al ángulo superior izquierdo de la curva).
Figura 1. Curva ROC para distintos valores límite (puntos de corte) del gas capilar contra el arterial3
Cuando se elabora una curva ROC por medio
de un programa informático estadístico, éste informa
un valor para el área bajo la curva. El área
total del gráfico es igual a 1; los valores posibles
del área comprendida bajo la curva ROC oscilan
entre 0 y 1. Esta medida es proporcional a la capacidad
diagnóstica, de tal manera que cuanto mejor
sea el desempeño de la prueba el área será mayor
(más cercana a 1). Estas curvas y áreas bajo la curva
permiten no sólo comparar puntos de corte de
un método determinado sino también comparar
el desempeño de dos o más métodos diagnósticos
diferentes.
Como cierre, es importante destacar que este
punto de corte es óptimo para el uso amplio de
la prueba en todo el espectro de aplicaciones. Sin
embargo, es perfectamente lícito utilizar un punto
de corte diferente si se apunta a un uso particular
de la prueba diagnóstica que requiera optimizar
la sensibilidad (rastreo o screening), o bien maximizar
la especificidad (confirmación diagnóstica).
También es posible calcular el desempeño diagnóstico
para distintas categorías o intervalos de
valores de la prueba en lugar de utilizar un único
punto de corte.5
Reglas de predicción clínica
El proceso diagnóstico es complejo y requiere
una justa combinación de experiencia clínica
y exámenes complementarios. El avance tecnológico
ha permitido el desarrollo de innumerables
prueba diagnósticas que van desde las muy
simples hasta las sumamente sofisticadas; pero
el campo de los instrumentos diagnósticos clínicos
está aún relativamente virgen. Interpretar los
resultados de las pruebas diagnósticas suele parecer
bastante sencillo: basta conocer los valores
normales de laboratorio o adquirir la habilidad visual
requerida para los estudios de imágenes, sin
olvidar el aspecto que analizamos en nuestro artículo
previo respecto de la capacidad operativa de la prueba (su sensibilidad, especificidad y valores
predictivos). En cambio, los signos y síntomas clínicos
requieren otro enfoque. Primeramente, es
necesario tener la destreza para detectarlos, ya
sea mediante un examen físico apropiado o una
anamnesis dirigida pero exhaustiva (habilidad
que luchamos por conseguir durante nuestros primeros
años de formación de postgrado…). Luego,
corresponde ponderar su impacto sobre nuestros
diagnósticos presuntivos, ya que las formas de
presentación son sumamente variables y todos los
signos clínicos no "pesan" lo mismo. Este último
proceso suele ser el más "artesanal" de la medicina;
tanto es así, que se va perfeccionando a lo largo
de los años, es difícil de explicitar de manera
precisa para poder transmitirlo a los más jóvenes,
y se lo acaba expresando con el término "ojo clínico",
que denota nuestra total incapacidad para
estandarizarlo o sistematizarlo.
Por suerte, la Estadística puede brindar un
aporte valioso en este campo. Así como el desarrollo
tecnológico mejoró la calidad de las pruebas
diagnósticas disponibles, haciéndolas más
fáciles de aplicar, menos invasivas y menos subjetivas,
el crecimiento de los métodos estadísticos
multivariados gracias a la informática permite la
construcción de instrumentos estandarizados y
confiables de diagnóstico o pronóstico, procedimiento
que está al alcance de cualquier investigador
clínico que disponga del número suficiente
de pacientes y asesoramiento estadístico. Estas
herramientas, denominadas "reglas de predicción
clínica" ("clinical prediction rules", "decision
rules"), proveen un abordaje estructurado para
diagnosticar una enfermedad o estimar el riesgo
de un evento, y si se elaboran con la metodología
adecuada, tienen la doble capacidad de ponderar
la contribución individual de cada signo y poder
ser aplicadas de manera eficaz para la toma de decisiones
diagnóstica o terapéutica por profesionales
con menor experiencia.
Metodología para la construcción
de reglas de predicción clínica
Cuando utilizamos una prueba diagnóstica lo
hacemos porque tenemos evidencia previa de que
los pacientes con prueba positiva o con determinados
valores tienen mayor probabilidad de estar
enfermos; esta evidencia proviene de los estudios
de validación de pruebas diagnósticas como las
que analizamos en nuestro artículo anterior. Lo
mismo ocurre con los síntomas y signos clínicos
que, como ya vimos, también pueden ser considerados
pruebas diagnósticas. Ahora bien: todos los signos, síntomas o estudios complementarios no
repercuten del mismo modo sobre nuestro diagnóstico;
la integración de toda esta información
(a menudo contradictoria, excepto en casos floridos)
suele ser asistemática, basada en nuestra
experiencia previa y muy artesanal. Sin embargo,
podemos aplicar conceptos ya analizados en
esta serie para mostrar cómo el desarrollo y uso
de reglas de predicción clínica puede sistematizar
nuestro proceso diagnóstico o pronóstico, haciéndolo
más explícito y eficiente.
Para entrar en este tema es interesante describir
las distintas etapas en la investigación del valor
diagnóstico de un signo clínico o un examen
complementario.6 De manera similar a lo que ocurre
en el estudio de nuevos fármacos, el desarrollo
de pruebas diagnósticas atraviesa cuatro fases
sucesivas:7
• Fase I: El primer paso es explorar si el resultado de la prueba es diferente entre pacientes con enfermedad conocida y sujetos sanos. Esto es básico, ya que si la prueba falla en distinguir sanos de enfermos, la investigación se detiene ahí.
• Fase II: El segundo paso es averiguar si los pacientes con determinados resultados de la prueba tienen mayor probabilidad de estar enfermos. En esta etapa también se utilizan sujetos de los extremos del espectro de enfermedad (sanos y enfermos conocidos), para aumentar la evidencia que avale que la prueba es promisoria.
• Fase III: La tercera etapa intenta establecer si la prueba distingue entre enfermos y sanos entre sujetos sospechados de tener la enfermedad.
Aquí lo que se pretende es ver si la prueba es útil en la situación clínica real en la que se aplica para hacer diagnóstico en la gama "gris" del espectro de enfermedad, no ya para distinguir entre pacientes claramente enfermos o sanos. Esta es la fase de los estudios de validación que analizamos en nuestro artículo anterior, donde los resultados de la prueba se comparan contra los del estándar de referencia (el "gold standard") en un grupo de individuos de un espectro apropiado de la enfermedad.
• Fase IV: Finalmente, para decidir si vale la pena aplicar la prueba diagnóstica se necesita demostrar que su uso tiene algún impacto sobre la evolución de la enfermedad. Aquí, la prueba se analiza como una intervención diagnóstica, por lo que el diseño óptimo para verificar su eficacia es un ensayo clínico controlado y aleatorizado en el que se analice si el grupo al que se aplicó la prueba tiene mejores resultados de salud (es decir: si el diagnóstico más temprano o más eficaz contribuyó a mejorar el pronóstico de la enfermedad).
Ahora supongamos que queremos desarrollar
un instrumento de diagnóstico o pronóstico utilizando
un conjunto de signos clínicos y estudios
complementarios, o sea una regla de predicción
clínica. Nuestra línea de investigación incluiría
básicamente 2 etapas:8-11
1. Etapa de derivación
La primera tarea sería seleccionar de una lista
exhaustiva de potenciales predictores (extraídos
de la bibliografía y la propia experiencia) aquellos
asociados con mayor probabilidad de un
determinado diagnóstico o pronóstico de la enfermedad:
esta es la etapa de derivación de nuestra
regla (equivalente a las fases I y II). Ya hemos
visto antes cómo se estudian los factores de riesgo:
utilizando idealmente una cohorte de sujetos
(la denominada "muestra de derivación" o "training
set"), podríamos identificar aquellos signos
o factores asociados a la enfermedad; esto significa
que sus medidas de efecto en el análisis bivariado,
riesgo relativo (RR) u odds ratio (OR), son
mayores de 1 con intervalos de confianza (IC) que
no contienen el 1. Para controlar posibles sesgos
de confusión o interacciones entre ellos, es conveniente
incluir aquellos con diferencias significativas
o límite (p< 0,10) en un análisis multivariado;
este análisis nos proveerá la magnitud del efecto
ajustada por todos los confundidores (o "covariables")
incluidos en el modelo, expresada por
el OR o RR "ajustados" que constituyen una medida
del "peso independiente" de cada factor para
el diagnóstico o pronóstico de interés. Con esta
información, estamos en condiciones de armar
nuestra regla de predicción o "score", otorgando
a cada factor seleccionado como significativo un
puntaje que sea proporcional a su medida de efecto
ajustada (su peso independiente).
2. Etapa de validación
Una vez creado el "score" (y antes de utilizarlo
para la toma de decisiones) debemos corroborar
que, de verdad, mide lo que queremos que mida,
es decir "validarlo". Esta es la etapa de validación
(similar a la fase III de estudios de validación de
métodos diagnósticos analizada en nuestro número
anterior). Aquí el objetivo es verificar la
capacidad operativa de la prueba (el puntaje o
score creado) frente a algún estándar de referencia
que nos proporcione la mejor certeza diagnóstica
posible. Este "gold standard" puede ser un solo
método diagnóstico o una combinación o secuencia de pruebas valoradas en conjunto como una única prueba. Para el diseño de esta etapa caben
todas las consideraciones de validez interna ya
comentadas en nuestro artículo anterior: utilizar
un diseño transversal, independiente y en lo posible
con enmascarmiento ("ciego"), y un espectro
de pacientes amplio y parecido al del futuro ámbito de aplicación del score. Un aspecto insoslayable
de estos estudios es que deben realizarse
sobre una nueva muestra de sujetos (la "muestra
de validación" o "testing set"), que sustente la
validez externa del instrumento (que es aplicable
y eficaz en otros subconjuntos de sujetos similares
a aquellos de los que se derivó). En esta etapa
se evalúan la calibración del instrumento (la
concordancia entre la probabilidad estimada del
evento y la observada realmente) y su discriminación
(la relación entre aciertos y errores evidenciable
por el área bajo la curva ROC). Para la
aplicación del puntaje, se puede elegir un único
punto de corte (balanceado mediante una curva
ROC o bien con máxima sensibilidad, ya que estos
instrumentos se utilizan habitualmente como
screening); alternativamente, se pueden establecer
categorías de puntajes que representen alto o bajo
riesgo del evento. Los resultados analizados
en esta fase serán las medidas de capacidad operativa
para cada punto de corte o cada categoría
de puntajes: sensibilidad (S), especificidad (E),
valores predictivos (VP) y razones de probabilidad
(likelihood ratios, LR) positivos y negativos
con sus respectivos IC 95%. Si nuestro puntaje
predice o diagnostica bien, quedará así validado
y, en líneas generales, podría ser utilizado en poblaciones
similares.
Veamos un ejemplo:
En un artículo publicado en Critical Care Medicine en 1988,12 Pollack y col. comunican la derivación
y validación del conocido Pediatric Risk of
Mortality (PRISM) que es una escala o puntaje para
pronosticar riesgo de muerte en terapia intensiva
pediátrica. Hasta ese momento, el riesgo de
muerte en este tipo de pacientes se estimaba con
el Physiologic Stability Index (PSI) elaborado mediante
un consenso de expertos, que valoraba 34
variables fisiológicas. Para intentar reducir este
gran número de factores requeridos para estimar
el pronóstico, los autores estudiaron una cohorte
multicéntrica que abarcó nueve unidades de cuidados
intensivos (UCI) pediátricas, utilizando la
mitad de los datos para la derivación ("estimation
set") y la otra mitad para la validación ("validation
set"). Para la creación del PRISM score se utilizó un método multivariado (regresión logística) que
seleccionó las 14 variables que componen el instrumento.Éste fue sometido a un proceso de validación
que mostró una predicción muy similar
a la del PSI (observable en la curva ROC, con un área bajo la curva de 0,92).
Utilidad de las reglas de predicción clínica
Los puntajes clínicos (scores) bien diseñados
y validados tienen un gran valor en el proceso
diagnóstico o la estimación del pronóstico, facilitando
la elección de un determinado manejo terapéutico
o la información al paciente sobre el curso
de su enfermedad. Constituyen así herramientas
valiosas para apoyar la toma de decisiones diagnósticas
o terapéuticas por profesionales de diverso
grado de experiencia, ya que habitualmente
requieren la medición de unas pocas variables
sencillas de obtener (a veces marcadores o subrogantes
de otras más difíciles de medir, como el color
de la piel en el puntaje de Apgar).
Por otra parte, su revalidación en distintos ámbitos amplía su validez externa, sustentando
su aplicabilidad a poblaciones similares, aunque
algo diferentes de aquella en la cual se crearon.
(El puntaje PRISM, por ejemplo, fue revalidado
en una UCI pediátrica en India,13 mostrando un
menor desempeño (área bajo la curva ROC de
0,80) atribuible a diferencias poblacionales y de
recursos).
Las escalas cuantitativas adecuadamente validadas
sirven, además, para estandarizar la clasificación
de enfermedades, categorizar con precisión
grupos de riesgo o gravedad o mostrar variaciones
evolutivas (como los puntajes de APACHE o
de Glasgow). Todas estas utilidades tienen aplicación
no sólo en el ámbito asistencial, sino también
en el campo de la investigación clínica.
El uso de reglas de decisión puede influir sobre
el manejo clínico mejorando los resultados de
salud de los pacientes, la calidad de la atención o
su costo-efectividad. La valoración de este impacto
implica considerar el uso de la regla como una
intervención (fase IV mencionada anteriormente)
y evaluar su eficacia mediante diseños experimentales
(ensayos aleatorizados) o cuasi-experimentales
(antes-después).14
La estimación de riesgo por medio de reglas
de predicción repercute también sobre la organización
y gestión de servicios de salud; puede utilizarse
para la asignación racional de recursos y
permite la evaluación comparativa de la calidad
de atención entre distintos centros o diferentes períodos
de un mismo centro (como el Clinical Risk
Index for Babies o CRIB score, útil para comparar mortalidad y performance entre unidades de cuidados
intensivos neonatales).
Finalmente, para que estos beneficios puedan
observarse, es necesario que la regla sea simple,
objetiva, válida y útil para que sea incorporada a
la práctica. Conocer las bases metodológicas de su
desarrollo y revalidarlas en el ámbito de la propia
tarea pueden promover la utilización de reglas de
predicción por parte de los profesionales de la salud.
Los instrumentos de diagnóstico adecuadamente
diseñados y validados son escasos en la
bibliografía pediátrica. La disponibilidad de métodos
estadísticos para la selección y ajuste de
variables hacen del desarrollo de reglas de predicción
un campo interesante de investigación,
que espero haber promovido entre los pediatras
con este artículo.
1. Demirdjian G, berlín V, Rowensztein H. Pediatría basada en la evidencia. Estudios de diagnóstico (1ª Parte). Arch Argent Pediatr 2009;107(6):527-535. [ Links ]
2. Jaeschke R, Guyatt GH, Sackett DL. Guía para usuarios de la literatura médica. Cómo utilizar un artículo sobre un examen diagnóstico. JAMA 1994;271: 389-392 y 703-707. [ Links ]
3. Hinojosa-Pérez JO, Treviño báez JD. Utilidad de la gasometría capilar para detector hiperoxemia en el recién nacido grave. Bol Med Hosp Infant Mex 1999;56(2):93-96. [ Links ]
4. Altman DG, bland LM. Diagnostic tests 3: receiver operating characteristic plot. BMJ 1994;309:188. [ Links ]
5. Irwig L, bossuyt P, Glasziou P, Gatsonis C, et al. Designing studies to ensure that estimates of test accuracy are transferable. BMJ 2002;324:669-671. [ Links ]
6. Ferrero F. Reglas de predicción clínica. Arch Argent Pediatr 2010;108(1):6-7. [ Links ]
7. Sackett DL, Haynes Rb. Evidence base of clinical diagnosis. The architecture of diagnostic research. BMJ 2002;324: 539-541. [ Links ]
8. Wasson JH, Sox HC, Neff RK, Goldman L. Clinical prediction rules: application and methodological standards. N Engl J Med 1985;313:793-799. [ Links ]
9. Laupacis A, Sekar N, Stiell IG. Clinical prediction rules. A review and suggested modifications of methodological standards. JAMA 1997;277:488-494. [ Links ]
10. Moons KGM, Royston P, Vergouwe Y, Grobbee DE, et al. Prognosis and prognostic research: what, why and how? BMJ 2009;339:b375. [ Links ]
11. Wade A. Derivation versus validation. Arch Dis Child 2000; 83:459-460. [ Links ]
12. Pollack MM, Ruttimann UE, Getson PR. Pediatric Risk of Mortality (PRISM) Score. Crit Care Med 1988;16:1110-1116. [ Links ]
13. Thukral A, Lodha R, Irshad M, Arora NK. Performance of Pediatric Risk of Mortality (PRISM), Pediatric Index of Mortality (PIM), and PIM2 in a pediatric intensive care unit in a developing country. Pediatr Crit Care Med 2006;7:356-361. [ Links ]
14. Reilly bM, Evans AT. Translating clinical research into clinical practice: impact of using prediction rules to make decisions. Ann Intern Med 2006;144:201-209. [ Links ]