INTRODUCCIÓN
La pandemia causada por el coronavirus de tipo 2 del síndrome respiratorio agudo grave (SARS-CoV-2, por su sigla en inglés) tuvo un impacto sin precedentes en la sociedad y en los sistemas de salud. La atención del cáncer se ha visto profundamente afectada como consecuencia de las barreras que surgieron en el proceso asistencial.
Diferentes publicaciones sugieren que, en los niños que reciben terapia contra el cáncer, la infección por SARS-CoV-2 suele ser asintomática, leve o moderada, y que no parecen tener mayor riesgo de infección grave en comparación con la población pediátrica general.1-5
El Registro Oncopediátrico Hospitalario Argentino del Instituto Nacional del Cáncer informó 417 casos confirmados en el período del 23 de abril de 2020 al 24 de abril de 2021 en pacientes con patología oncohematológica. De ellos, el 45 % fue asintomático.6
La evidencia disponible abona la necesidad de priorizar una atención global del cáncer pediátrico y la continuidad del tratamiento oncológico, en forma efectiva y segura. Las instituciones de todo el mundo han implementado nuevas políticas para brindar atención adecuada a esta población.1
Varias guías recomiendan el cribado de los pacientes en tratamiento con quimioterapia para permitir la identificación temprana y el aislamiento de los pacientes asintomáticos.7-10 Hasta el momento, se dispone de poca información con respecto a la continuidad o la modificación del tratamiento quimioterápico en los niños asintomáticos con prueba positiva.11
En el Hospital Garrahan, una de las estrategias implementadas fue la incorporación de un programa de cribado para detectar al paciente con enfermedad por el coronavirus del 2019 (COVID-19, por su sigla en inglés) asintomática previa a la internación para recibir los ciclos de quimioterapias o tratamiento hematológico parenteral. Los objetivos de este trabajo fueron conocer la portación asintomática de SARS-CoV-2 en niños oncológicos y/o en sus cuidadores al hospitalizarse para realizar quimioterapia, y describir el impacto en la continuación del tratamiento en aquellos con prueba detectable o con síntomas compatibles con SARS-CoV-2 durante la internación.
POBLACIÓN Y MÉTODOS
Se realizó un estudio observacional y prospectivo durante el período comprendido entre el 20 de julio de 2020 y el 30 de abril de 2021.
Se incluyeron los pacientes con enfermedad oncohematológica que ingresaron a realizar quimioterapia programada o tratamiento hematológico parenteral desde el área ambulatoria y a sus cuidadores.
Se realizó una prueba de detección microbiológica de SARS-CoV-2 por reacción en cadena de la polimerasa con transcripción inversa (RT-PCR) en los pacientes y en sus cuidadores.
Se excluyeron del estudio aquellos pacientes que se internaban para realizar el tratamiento y contaban con una prueba no detectable dentro de las 72 horas previas, y aquellas díadas con alta epidemiológica luego de una infección por SARS- CoV-2 dentro de los 3 meses del diagnóstico.
La enfermedad oncohematológica de base de los pacientes se clasificó según la tercera edición de la Clasificación Internacional de Enfermedades Oncológicas de la Organización Mundial de la Salud y la Clasificación Internacional de Cáncer Pediátrico. Se agruparon en las categorías: 1) leucemias y linfomas, 2) tumores sólidos, 3) tumores del sistema nervioso central (SNC), y 4) enfermedad hematológica.
Las variables consideradas fueron edad, sexo, agrupación diagnóstica, diagnóstico, resultado de la prueba de detección de SARS- CoV-2 del paciente y su cuidador, suspensión o modificación de la quimioterapia por la presencia de síntomas clínicos incluidos en los criterios de caso sospechoso con prueba de SARS-CoV-2 detectable y no detectable, y suspensión o modificación de la quimioterapia en pacientes asintomáticos con prueba detectable.
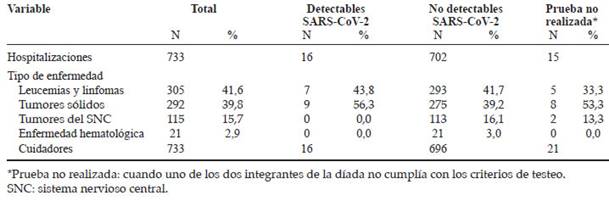
Tabla 1: Resultados de la prueba de detección de SARS-CoV-2 de los pacientes evaluados en cada hospitalización, características de la enfermedad de base y resultados de las pruebas de los cuidadores
Los síntomas clínicos que se registraron fueron aquellos que se incluyen en los criterios de caso sospechoso según el Ministerio de Salud de la Nación.12
El estudio fue aprobado por el Comité Revisor de Investigación y el Comité de Ética de la institución.
Análisis estadístico
Para el análisis descriptivo de las variables continuas, se usaron como medidas de resumen media y mediana, según correspondiera a la distribución de los datos. Las variables categóricas se midieron en valor absoluto y porcentual. Para el análisis, se utilizó el programa estadístico Epi Info versión 7.2.4®.
RESULTADOS
Se registraron un total de 865 hospitalizaciones de pacientes para realizar tratamiento programado y el mismo número de cuidadores. Cumplieron criterios de inclusión 733 hospitalizaciones en 241 pacientes que recibieron entre 1 y 15 ciclos de quimioterapia (mediana: 3).
De estos 241 pacientes, 128 eran varones (53 %) y la mediana de edad fue de 91 meses (rango 1-210). En la Tabla 1 se presentan los resultados.
De las 733 pruebas realizadas en los pacientes hospitalizados, 16 presentaron prueba positiva para SARS-CoV-2. La tasa de positividad fue del 2,2 % (intervalo de confianza del 95 % [IC95%]: 1,35-3,52). Todos los casos confirmados permanecieron asintomáticos durante toda la hospitalización y completaron su quimioterapia.
Con respecto a las pruebas de los cuidadores, la tasa de positividad fue del 2,2 % (IC95%: 1,35 3,52). Se encontró positividad simultánea para SARS-CoV-2 en 8 diadas paciente-cuidador.
Se observaron síntomas clínicos compatibles con caso sospechoso en el 7,8 % de los pacientes. Los síntomas más frecuentes se describen en la Tabla 2.
Se continuó la administración de la quimioterapia programada en el 77 % de los pacientes hospitalizados que presentaron síntomas compatibles. Todos ellos presentaban prueba para SARS-CoV-2 no detectable y permanecieron dentro de la unidad de administración de quimioterapia prolongada durante la evolución de los síntomas.
El tratamiento programado se suspendió en el 23 % de los pacientes que presentaron síntomas compatibles con infección por SARS-CoV-2.
DISCUSIÓN
La atención médica adecuada en oncología pediátrica depende de una evaluación y diagnósticos oportunos, la derivación a centros de alta complejidad, la interacción de equipos multidisciplinarios, la terapia multimodal coordinada y el acceso a centros de atención. Todos estos factores se han visto afectados por la pandemia.
Múltiples estrategias2 se han implementado en todo el mundo para minimizar el riesgo de infección por SARS-CoV-2 en los niños con cáncer sin reducir la eficacia de los tratamientos oncológicos.
Los pacientes asintomáticos son una fuente potencial de infección. Varias publicaciones7-10 coinciden en que el cribado mediante pruebas por RT-PCR para SARS-CoV-2 permite una detección temprana y eficaz para reducir la transmisión viral.
Los datos sobre la prevalencia del SARS- CoV-2 en niños con cáncer son limitados y no hay evidencia suficiente respecto a la continuidad o la modificación del tratamiento quimioterápico programado en los niños asintomáticos con prueba positiva.
En nuestro estudio, se observó que fue baja la portación asintomática de SARS-CoV-2 en los niños con cáncer y en sus cuidadores.
Boulad y cols.,4 analizaron los resultados de la detección de casos positivos para SARS- CoV-2 en 3 cohortes de individuos. Describen una cohorte de pacientes de oncología pediátrica, asintomáticos, a los que se les realizó una prueba RT-PCR para SARS-CoV-2 previa a quimioterapia o a procedimiento de sedación, con una tasa de positividad del 2,5 %. Este resultado es concordante con el obtenido en nuestro estudio. Describen, también, otra cohorte donde incluyeron a los cuidadores de estos pacientes; en esta, la tasa de positividad fue del 14,7 %. Este valor es muy superior al observado en nuestro estudio.
Encontramos positividad simultánea de SARS- CoV-2 en 8 díadas. Siete pacientes tenían prueba negativa a pesar de la exposición cercana de sus cuidadores positivos. La infección por SARS- CoV-2 no reconocida en cuidadores asintomáticos es una consideración importante para el control de infecciones.
En Italia, durante el pico de la pandemia, varios centros de hematología-oncología pediátrica adoptaron como estrategia el cribado para SARS-CoV-2 antes de iniciar la quimioterapia.
Cesaro S. y cols.,13 encontraron que la prevalencia de prueba positiva en pacientes pediátricos que acudían al hospital para recibir quimioterapia era alrededor del 3 %, un resultado levemente más alto que el reportado en nuestro informe. Describen, además, que la medida adoptada para estos pacientes fue posponer la quimioterapia hasta que dos pruebas fueran negativas. La precaución referida por Cesaro y cols.,13 está en consonancia con la poca evidencia sobre el impacto en la morbimortalidad en los niños con cáncer al momento de la publicación.
Tanto Bisogno y cols.,14 como Ferrari y cols.15 sugieren que puede no ser necesario modificar o postergar los tratamientos contra el cáncer en los pacientes pediátricos.
En nuestra población, a diferencia de lo descrito por Cesaro y cols.,13 y en concordancia con Bisogno y cols.,14 y Ferrari y cols.,15 los casos confirmados de SARS-CoV-2 completaron su quimioterapia sin presentar complicaciones clínicas. Todos ellos permanecieron asintomáticos durante la hospitalización y fueron trasladados a un área destinada a la internación de casos positivos. Los pacientes que presentaron síntomas clínicos compatibles con caso sospechoso contaban con una prueba no detectable y la suspensión de su tratamiento se debió a criterios clínicos no asociados a SARS-CoV-2.
La limitación de este estudio es el pequeño número de pacientes asintomáticos positivos para dar una recomendación definitiva en cuanto a la continuidad del tratamiento oncológico. Se requieren estudios prospectivos multicéntricos para conocer mejor los efectos de la COVID-19 en la población pediátrica de hematología-oncología.