Introducción
Los defectos congénitos de la glicosilación (CDG) son un grupo heterogéneo de trastornos genéticos mayoritariamente de herencia autosómica y recesiva. Se deben a defectos en la síntesis de glicanos (monosacáridos y oligosacáridos) y en la unión de éstos a proteínas y lípidos.
Jaeken describió por primera vez en 1980 (1) un caso de CDG inicialmente denominada CDG tipo Ia, que a partir de la nueva nomenclatura propuesta en 2009, corresponde a PMM2-CDG (2).
Los CDG de las proteínas se clasifican en defectos en la N-glicosilación y en la O-glicosilación, según el tipo de unión afectado. Las proteínas son glicosiladas enzimáticamente. Esta modificación covalente se da en ciertos residuos aminoacídicos, en diferentes compartimentos celulares; la mayoría de estos ocurre en el citoplasma, retículo endoplasmático y aparato de Golgi. Estos glicanos son responsables de importantes funciones de las proteínas, entre ellas estabilidad, plegamiento y vida media. Normalmente, gran parte de las proteínas humanas están glicosiladas, lo que explica la gran variedad de signos y síntomas clínicos observados en los CDG (3).
Al día de hoy se han descripto más de 130 tipos de CDG. Se estima que la incidencia global de portadores, de al menos una variante conocida, es de 1/10 000 en población europea y afroamericana, habiéndose encontrado una incidencia de hasta 1/20 000 para la forma más frecuente (la tipo Ia o PMM2-CDG) en reportes de población europea (4).
Estas afecciones generalmente se presentan con manifestaciones multisistémicas; en la mayoría de los casos se observan alteraciones neurológicas y retrasos del desarrollo. Por esto, el diagnóstico de CDG requiere un elevado índice de sospecha clínica (4).
La elevada incidencia informada de este grupo de afecciones y la ausencia de datos a nivel nacional junto a la complejidad diagnóstica que trae aparejada este tipo de pacientes hizo que, desde el Laboratorio de Pesquisa Neonatal (LPN), se viera como esencial la implementación de una técnica que permitiera orientar y confirmar el diagnóstico para CDG, al menos para aquellas formas más frecuentes.
Con ese objetivo, en el año 2017 el LPN incorporó el isoelectroenfoque (IEF) de transferrina. Si bien éste es un método no automatizado y que requiere mucho tiempo, es utilizado como screening para orientar el diagnóstico presuntivo de CDG. Esta técnica permite la detección de defectos en la N-glicosilación de proteínas e identifica dos patrones: CDG tipo I y tipo II.
La PMM2-CDG es la forma más frecuente de CDG y es causada por variantes patogénicas del gen de la fosfomanomutasa 2 (PMM2), que produce una deficiencia de dicha enzima, la cual cataliza la conversión de manosa- 6-fosfato en manosa-1-fosfato, en el segundo paso de la síntesis de guanosina difosfato-manosa (GDP) en el citoplasma. Dicho gen se localiza en el cromosoma 16q13 y tiene 8 exones que codifican para una proteína de 246 aminoácidos.
En mayo de 2018 el área de biología molecular del LPN comenzó a realizar la secuenciación del gen PMM2 en aquellas muestras que presentaban un perfil de CDG tipo I en el IEF.
En el presente trabajo se expone el proceso que realizó el LPN para la definición bioquímica y genética de los CDG.
Materiales y Métodos
Entre noviembre de 2017 y diciembre de 2018 el LPN recibió muestras de suero provenientes de pacientes con clínica sugestiva de CDG. Estas muestras se utilizaron para la realización del presente trabajo y en todos los casos se trabajó siguiendo las pautas recomendadas en la Declaración de Helsinki.
Cada muestra de suero fue incubada con FeCl3 y NaHCO3 durante 1 h a temperatura ambiente; posteriormente se incubó 15 minutos a 4 ºC y, una vez transcurrido este tiempo, las muestras fueron diluidas al décimo con H2O y conservadas a -20 ºC hasta el momento de su análisis.
El IEF se realizó en gel ultrafino de acrilamida/bisacrilamida utilizando anfolitos de rango de pH 5-7, en un equipo PowerPack Universal de Bio-Rad - California, EE.UU.
Luego de realizada la corrida electroforética, se reveló con anticuerpos anti-transferrina (DAKO) y posterior tinción con Coomasie Blue (5).
Para el estudio del gen PMM2 se realizó la extracción del ADN genómico en muestras en papel de filtro Whatman 903 con Investigator kit de Quiagen y secuenciación en un equipo ABI 310 de Applied Biosystems - California, EE.UU. Los resultados encontrados fueron comparados con la base de datos Ensembl y HGMD.
Resultados
Entre noviembre de 2017 y diciembre de 2018 se procesaron 47 muestras por IEF, 26 correspondían a pacientes del sexo femenino y 21 a pacientes masculinos, no consanguíneos, de edades comprendidas entre los dos meses y los 13 años de vida. Las manifestaciones clínicas que presentaban los pacientes fueron muy amplias; las más frecuentes fueron los retrasos del desarrollo (28%), hipotonía (15%) y ataxia (15%).
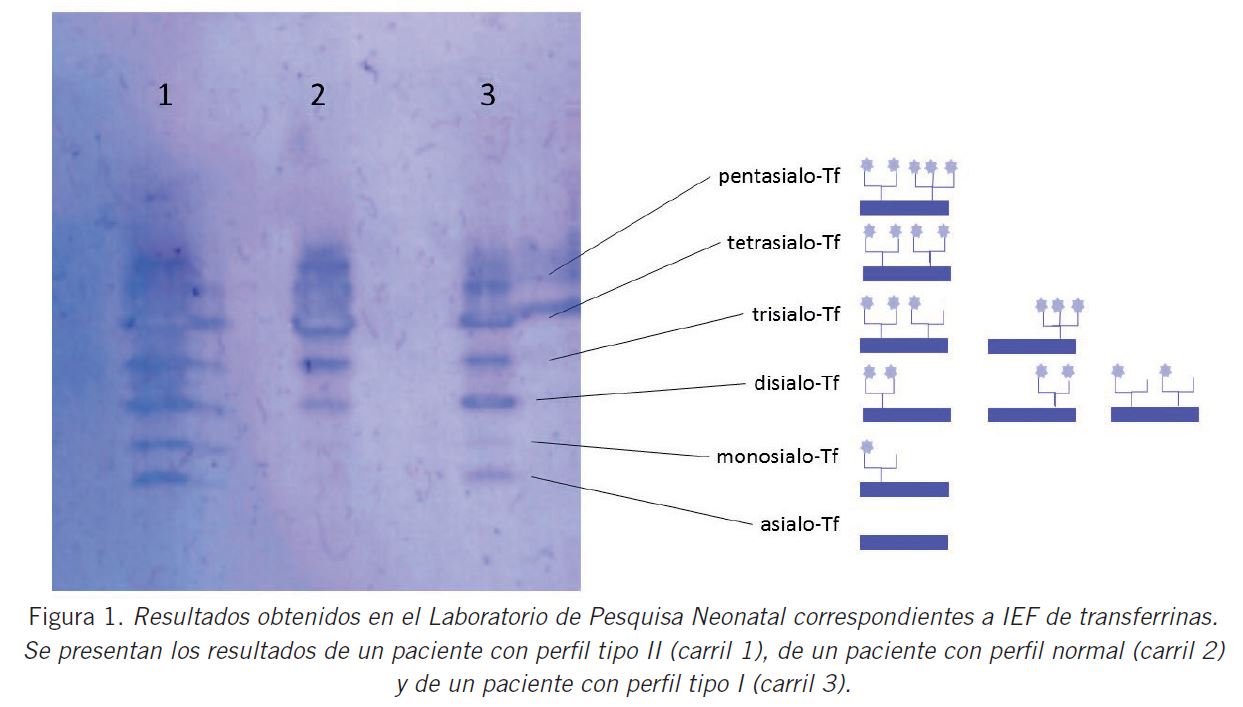
Se encontraron 4 perfiles compatibles con CDG tipo I y 2 perfiles compatibles con CDG tipo II. En la Figura 1 se pueden observar los resultados obtenidos en el LPN para los perfiles típicos de CDG tipo I, II o normal.
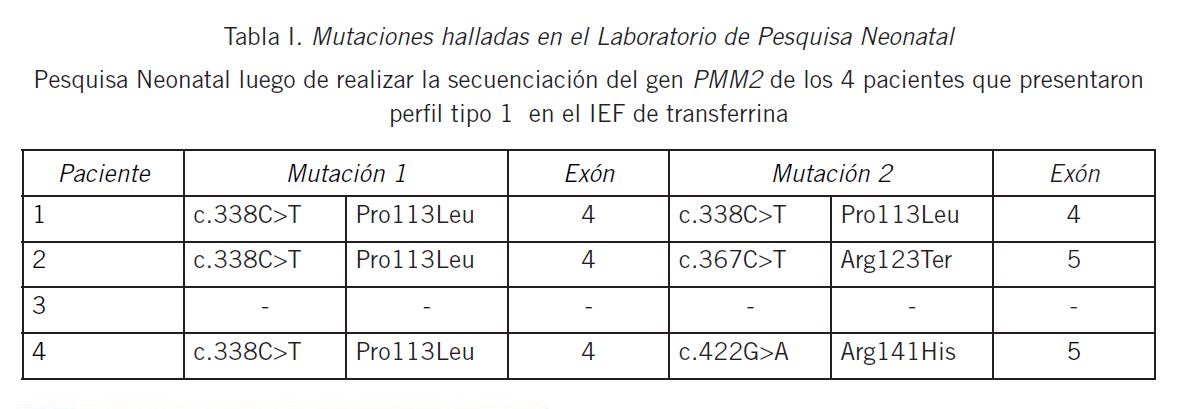
Se realizó la secuenciación del gen PMM2 a las 4 muestras con perfil tipo I encontrándose, en 3 de éstas, mutaciones patogénicas conocidas en ambos alelos (Tabla I). En el caso de homocigosis (Pro113Leu) las únicas manifestaciones clínicas observadas fueron retrasos del desarrollo, mientras que los otros dos casos caracterizados presentaban, además, hipotonía.
Discusión y Conclusiones
Actualmente no se dispone de un test que permita realizar un screening de todos los tipos de CDG, pero se estima que el IEF de transferrina sérica permite detectar hasta un 50% de los casos (6).
La deficiencia en la N-glicosilación determina la ausencia o disminución de ácido siálico unido a las proteínas, lo que produce cambios en la carga de la transferrina sérica. El IEF permite separar isoformas de transferrina a partir de esta deficiencia y de la alteración en la carga de esta molécula. Si bien es una técnica cualitativa y hoy en día han surgido nuevas metodologías que permiten una identificación más sensible de las isoformas (electroforesis capilar, HPLC, espectrometría de masa), el IEF sigue siendo una técnica útil como primer screening (7) (8) (9).
Los perfiles que se obtienen con esta técnica pueden ser de dos tipos: un perfil tipo I que se caracteriza por el aumento de las bandas correspondientes a di y asialotransferrina y una disminución de tetrasialotransferrina, y un perfil tipo II que se caracteriza por el aumento de tri, di, mono y asialotransferrina (Fig. 1).
En un principio los CDG fueron clasificados por los patrones de isoformas de transferrinas encontrados por IEF; los patrones tipo I fueron relacionados con trastornos en el citoplasma y retículo endoplasmático, mientras que el tipo II se asoció a defectos en el aparato de Golgi.
En 2009 la nomenclatura se adaptó a los hallazgos moleculares de estas enfermedades.
Estas afecciones generalmente se presentan con manifestaciones multisistémicas. Las más comunes son: retrasos del desarrollo, hipotonía, síntomas neurológicos, hepatopatía y coagulopatía, enfermedades oculares, cutáneas y cardíacas, así como dismorfias faciales. En la mayoría de los casos se observan alteraciones neurológicas y retrasos del desarrollo (4).
Por lo antes expuesto, el diagnóstico de CDG requiere un elevado índice de sospecha clínica y es imprescindible la incorporación de una herramienta que oriente en el diagnóstico.
En todos los casos se hace necesario cotejar los resultados con los datos clínicos del paciente y descartar posibles falsos positivos, como ser galactosemia, trastornos hepáticos, algunas infecciones y algunas variantes de transferrina no patológicas. Del mismo modo, un resultado negativo o perfil normal no asegura la ausencia de un CDG debido a que hay casos, incluso de PMM2- CDG, con perfil normal. Se requieren siempre estudios complementarios (10).
Desde la incorporación del IEF de transferrina en este laboratorio, ha sido posible orientar en el diagnóstico en un 12% de los casos sospechosos clínicamente. De aquellos con perfil tipo I, un 75% pudo ser confirmado con el estudio molecular del gen PMM2.
Se estima que la alta tasa de casos positivos detectados se debe a que los pacientes derivados al LPN tuvieron una anamnesis detallada y una sospecha clínica acertada.
La población uruguaya tiene sus orígenes ancestrales predominantemente en población mediterránea (España, Italia), sin embargo el estudio molecular del gen PMM2 mostró que todos los pacientes presentaban la mutación Pro113Leu, incluso un caso en que se encontró en forma homocigota. Si bien esta mutación no es la más frecuentemente hallada, ha sido descripta en la población europea (Francia, Alemania, Holanda, Bélgica, España) (11) (12). Estudios realizados informaron que esta mutación (Pro113Leu) afectaría la zona de interacción de cada subunidad de la proteína, comprometiendo entonces la dimerización normal de la PMM2 (12).
La mutación Arg141His, conocida como la más frecuente en la población caucásica (73% de pacientes con CDG tipo I) y la más frecuente en la población de España e incluso en la Argentina, país que tiene una población similar a la de Uruguay en cuanto a origen genético, fue encontrada solo en un caso, y en heterocigosis (13) (14) (15).
La muestra que presentó perfil tipo I en el IEF, en la que no se encontraron mutaciones con el método utilizado, debería ser objeto de posteriores estudios con el fin de descartar otras posibles mutaciones que causen CDG tipo I como MPI-CDG (antes CDG Ib). De acuerdo a esto, el médico tratante evaluaría la situación del paciente y realizaría otros estudios complementarios como determinar el perfil de transferrina por otras técnicas como espectrometría de masas y/o secuenciación completa del gen (WES).
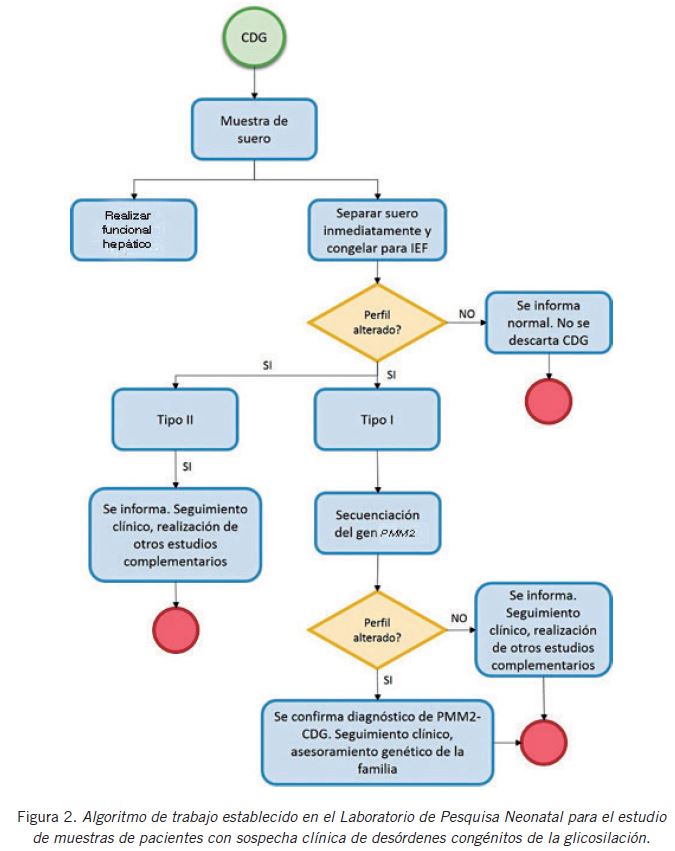
En conclusión, a partir de los resultados obtenidos, basados en la experiencia descripta en la bibliografía y optimizando los recursos disponibles en el LPN, se estableció un algoritmo de trabajo (Fig. 2).
De los resultados presentados se concluye que la incorporación del IEF de transferrina y la secuenciación del gen PMM2 impactaron positivamente, ya que permitieron establecer diagnósticos de certeza.
La confirmación de los tres casos con PMM2-CDG posibilitó realizar un adecuado asesoramiento genético a la familia y una evaluación del pronóstico.
Agradecimientos
Los autores agradecen al Prof. Iván Martinez-Dunker, a la Prof. Carla Asteggiano y al Prof. Jaak Jaeken, quienes permitieron iniciar el presente trabajo, ayudando con las metodologías instaladas en el laboratorio. También agradecen a los médicos que colaboraron en aunar esfuerzos para tener un mejor conocimiento de los CDG en Uruguay.
Fuentes de financiación
El presente trabajo fue realizado sin la utilización de una financiación específica.












 uBio
uBio