Introducción
Las últimas investigaciones arqueológicas desarrolladas en el Gran Chaco argentino permitieron aportar conocimientos sobre distintos aspectos de la forma de vida de las sociedades originarias que allí habitaron (e. g. Santini, 2009; Lamenza et al., 2015, 2018, 2019). Aun así, estos avances fueron generando nuevos interrogantes que requieren volver sobre el registro y examinar nuevas vías de análisis e interpretación. De esta manera, comenzamos a indagar sobre el tiempo de ocupación de los sitios y cuáles son las vías de evidencia posibles de analizar, en función de los materiales arqueológicos característicos de la región chaqueña. Producto del relevamiento exhaustivo de la bibliografía sobre la biología de las especies representadas en el registro zooarqueológico regional, encontramos que el pez Hoplosternum littorale (cascarudo, tamuatá, cascadura, curito, entre otros, según el país) presenta cambios morfológicos relacionados con las variaciones ambientales. Por ello, a los fines de explorar su potencial para estimar el momento del año en que ha sido explotado el recurso, en este trabajo nos proponemos sintetizar los conocimientos sobre la biología de la especie, con énfasis en sus variaciones morfológicas. Esto nos permitirá establecer sus vinculaciones con la variación estacional, proponer un modelo que permita generar expectativas arqueológicas y testear su validez aplicándolo al caso concreto de un sitio arqueológico del Chaco húmedo argentino.
Distribución y ciclo vital de Hoplosternum littorale
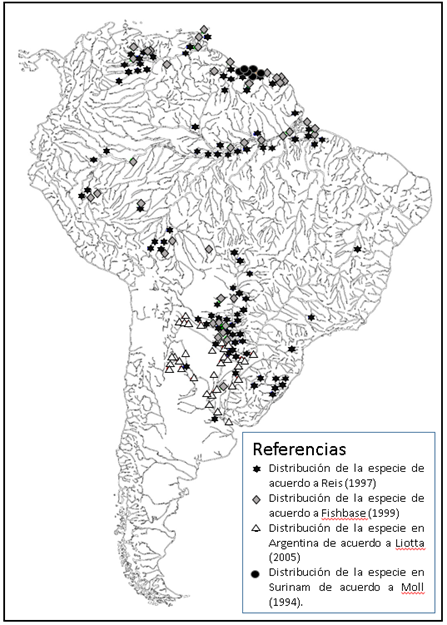
H. littorale es un Siluriformes que se encuentra ampliamente distribuido en el Neotrópico (Hostache y Mol, 1998). Específicamente en América del Sur, al este de los Andes (Reis, 1997), desde Venezuela hasta Argentina (Farías Díaz, 2010). En Argentina, habita en las cuencas de los ríos Paraguay, Bermejo, Paraná y Uruguay (Hostache y Mol, 1998; Vallone, 2015) (Fig. 1).
La especie ha desarrollado características morfológicas, fisiológicas y de comportamiento en adaptación a un ambiente hipóxico (Kramer y Graham, 1976; Luquet et al., 1989; Mol, 1993 y bibliografía allí citada). En general, el comienzo de la temporada de lluvias (el cual varía entre las diferentes regiones del área de distribución de la especie) coincide con el inicio del periodo reproductivo. (Winemiller, 1987; Luquet et al., 1989; Hostache y Mol, 1998; Lasso y Sánchez-Duarte, 2011, entre otros). En el transcurso del periodo reproductivo, los individuos maduros presentan dimorfismo sexual marcado (Winemiller, 1987; Luquet et al., 1989; Hostache y Mol, 1998; Reis, 1998; Lasso y Sánchez-Duarte, 2011, entre otros que han registrado las modificaciones). Las espinas pectorales de los machos sufren un drástico alargamiento (Reis 1998) y sus extremos libres se inflexionan hacia arriba, formando un gancho en ángulo recto (Reis, 1998; Casciotta et al., 2005; Almirón et al., 2008; Vallone, 2015). Durante el ciclo de reproducción, las hembras maduras mantienen sus espinas pectorales lisas, con una morfología recta a semicurva. Desovan hasta 14 veces a lo largo del período y cada puesta puede alcanzar los 9000 huevos y el estadio de huevo presenta una duración de hasta tres días (Hostache y Mol, 1998). Las larvas pueden criarse en agua estancada (Luquet et al., 1989) y desarrollan las espinas pectorales a los 17 días luego de la eclosión. El estadio juvenil es considerado a partir de los 29 días de edad a una temperatura de 26°C ± 2°C (Ramnarine, 1994), encontrándose en regiones marginales poco profundas entre exuberante vegetación acuática. De acuerdo con Winemiller (1987) y Hostache y Mol (1998), durante el periodo no reproductivo no han sido recolectados individuos machos con espinas pectorales modificadas, lo cual permite aseverar que dicha estructura se agranda durante la recirculación gonadal y vuelve a las proporciones normales después de la estación reproductiva. A diferencia de lo que ocurre con los machos adultos, de acuerdo con Winemiller (1987), es posible encontrar individuos inmaduros aproximadamente un mes después de haber finalizado el periodo reproductivo. En los rangos de tamaño menores, la rama dorsal de la espina pectoral es dentada y la morfología de los dientes es deprimida, de perfil triangular, con una punta por base y, en su mayoría, perpendiculares. A medida que incrementan su tamaño, el dentado es reabsorbido progresivamente y en los estadios adultos no queda vestigio de su presencia original (Vallone, 2015). De esta manera, los individuos en estadios avanzados del desarrollo presentan espinas pectorales rectas a semicurvas y lisas.
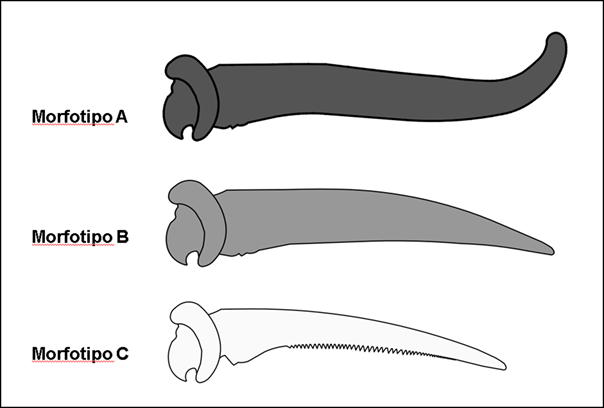
Por lo tanto, y a partir de la vasta información que sintetizamos para la especie H. littorale, pueden establecerse los siguientes tipos morfológicos de espinas pectorales:
Variación morfológica y ciclo anual
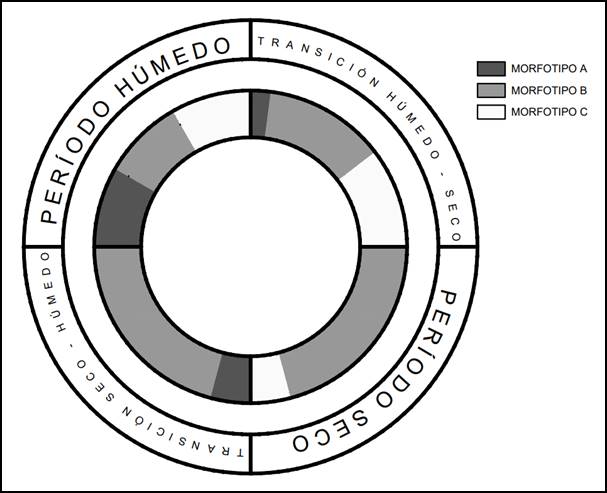
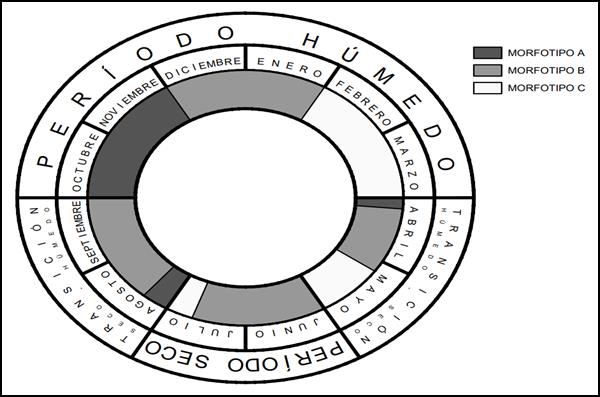
Integrando la información del apartado anterior podemos resumir que a lo largo del ciclo anual sería esperable encontrar distintas combinaciones de las morfologías de las espinas pectorales de H. littorale (Fig. 3). Durante los meses de lluvia, dentro del área de distribución de la especie, esperamos encontrar machos maduros con espinas pectorales modificadas a modo de gancho (morfotipo A), hembras maduras con espinas pectorales rectas a semicurvas (morfotipo B) y juveniles con diferentes grados de desarrollo de denticulaciones en sus espinas pectorales (ya que el estadio de huevo es breve con respecto a otros estadios y los individuos desarrollan las espinas pectorales tempranamente, morfotipo C). Hacia fines del periodo húmedo y comienzo del periodo de sequías, las probabilidades de encontrar individuos machos con espinas pectorales modificadas serán escasas y aumentarán las probabilidades de encontrar machos y hembras con espinas pectorales rectas a semicurvas (morfotipo B) e individuos inmaduros con espinas pectorales dentadas en distintos grados de desarrollo (morfotipo C). En el periodo de sequías propiamente dicho, se espera encontrar una predominancia de adultos hembras y machos sin modificaciones (morfotipo B) y, posiblemente, algunos individuos juveniles, principalmente aquellos de estadios avanzados de desarrollo (espinas pectorales de dentado reducido, morfotipo C). Hacia fines del periodo seco y comienzo del periodo húmedo, continuaría la predominancia de adultos sin modificaciones (morfotipo B). Dado que se aproxima la temporada de reproducción, es posible encontrar algunos individuos machos con espinas pectorales modificadas (morfotipo A). Consideramos que en este periodo no es probable hallar individuos juveniles (morfotipo C).
Caso de aplicación. Sitio Sotelo I (SChaSmar 1.1)
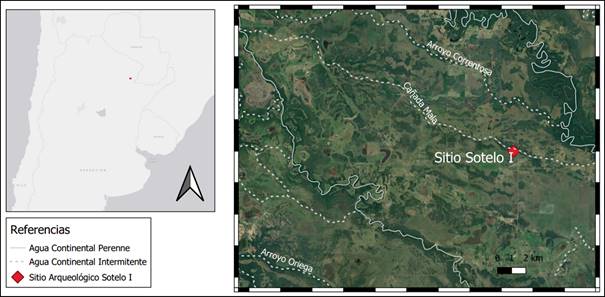
El sitio arqueológico Sotelo I (26º 47’31.9” LS y 59º 03’31.9” LO) (Fig. 4) se encuentra sobre un albardón fluvial de 350 m2, ubicado a 70 m del riacho Malá, un curso temporario rodeado de bañados estacionales. En términos ecológicos, se encuentra dentro de la subregión de esteros, cañadas y selvas de ribera del Chaco húmedo argentino (sensu Morello y Adámoli, 1968). Esta subregión está caracterizada por la presencia de condiciones estacionales marcadas debido a variaciones en los regímenes de las precipitaciones (Burkart et al., 1999). El periodo de lluvias tiene lugar en la estación cálida, entre octubre y abril; mientras que el periodo seco ocurre en el invierno, entre junio y agosto, en el que también se presentan algunas heladas (Ginzburg y Adámoli, 2005). La excavación arqueológica del sitio cubrió una superficie de 24 m2 y se estableció la antigüedad en 1690±90 años 14C AP (LP-1917, sobre colágeno del hueso de Myocastor coypus, según Santini, 2009). Sobre la base de estimaciones de tamaño, marcas de corte, formatizaciones y ausencia de determinadas unidades anatómicas, se ha propuesto el origen antrópico de los materiales faunísticos del sitio Sotelo I. Para este sitio, se estableció una ocupación por parte de sociedades cazadoras, recolectoras y pescadoras (Santini, 2009) características del componente alfarero Pantanal Chaco (Lamenza et al., 2019). En investigaciones previas se relevaron y analizaron 5798 restos óseos faunísticos y 1855 valvas de moluscos (Santini, 2009; Santini et al., 2011). En el sitio se observa un predominio del roedor caviomorfo Myocastor coypus (ca. 76,1 % de los restos óseos y ca. 57,65 % del conjunto arqueofaunístico) y gran cantidad de moluscos gastrópodos (el 24,23 % de los restos faunísticos, de los cuales el 99 % corresponden a Pomacea canaliculata chaquensis1). Los recursos ictícolas son complementarios, correspondiendo al 8,39 % de los restos óseos. A partir de la presencia dominante de Myocastor coypus, Santini (2009) menciona la posible preferencia de captura durante o inmediatamente después de la estación de lluvias. Se refuerza esta propuesta con el patrón de explotación inferido para Pomacea canaliculata, el cual presenta mayor disponibilidad durante los meses lluviosos e hiberna durante los meses de invierno. Se ha descartado la acumulación natural de estos gastrópodos mediante estimaciones de tamaño que arrojaron la selección intencional de los ejemplares más grandes. A partir de esto, se ha propuesto que el sitio fue ocupado durante el periodo de grandes lluvias o momentos inmediatamente posteriores (Santini, 2009). Esta información sienta las bases para poner a prueba la utilidad de H. littorale como estimador de momento de ocupación.
Análisis del registro ictioarqueológico
Dados los objetivos propuestos en la presente comunicación se procedió a la revisión de los restos esqueletales de peces (NISP = 608) con énfasis en el reconocimiento de los morfotipos de las espinas pectorales de H. littorale. La identificación de elementos a nivel anatómico y taxonómico fue realizada por comparación con colecciones de referencia de la Facultad de Ciencias Naturales y Museo (UNLP) y de la Fundación de Historia Natural Félix de Azara, con la colaboración del Lic. Sergio Bogan. Aquellos especímenes que no pudieron ser incluidos dentro de niveles taxonómicos de mayor resolución fueron referidos a categorías más generales (clase, orden, familia). Cabe aclarar que debido a que la reevaluación de los materiales no fue hecha por los mismos investigadores que hicieron el análisis original, pueden darse diferencias en el nivel de determinación debido al adiestramiento del investigador, a las diferencias en la formación, al mejoramiento de las colecciones de referencia, así como a la posible mayor fragmentación por el manejo de los materiales o técnicas de conservación (factores tréficos, véase discusión en Mengoni Goñalons, 1988). En esta oportunidad, no nos detendremos en las diferencias entre un análisis y otro, tal y como se realizó para el reanálisis del conjunto arqueofaunístico de otro sitio arqueológico, El Cachapé Potrero IVB (e. g. Zarza et al., 2019).
Para la cuantificación, se tuvieron en cuenta los cálculos referentes a la abundancia taxonómica en forma de NISP (number of identified specimens per-taxón) y MNI (minimum number of individuals), siguiendo a Mengoni Goñalons (1988) y sus versiones porcentuales (NISP % y MNI %).
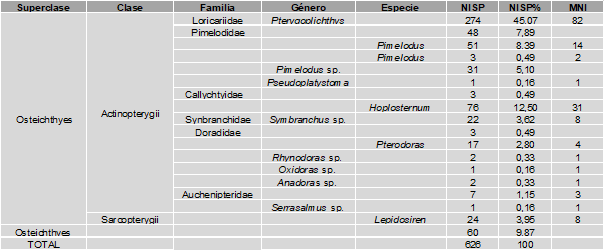
En la Tabla 1 se detalla la abundancia taxonómica de la ictiofauna del sitio. Como resultado de este reanálisis se identificaron 13 taxones no traslapados a nivel de familia, género y especie (siguiendo la terminología de Grayson, 1991). Se registra una representación importante de Pterigoplichthys sp. (sinónimo senior de Liposarcus), seguido por H. littorale y por representantes de Pimelodidae, que incluye los restos asignados a Pimelodus sp. y a las especies P. albicans y P. maculatus. En menor proporción se encuentran restos del dipnoo Lepidosiren paradoxa y le siguen, en proporciones similares, Symbranchus sp. y Pterodoras granulosus. Representantes de las familias Auchenipteridae, Callichthyidae y Doradidae, y los restos de los géneros Anadoras, Rynodoras, Oxydoras, Serrasalmus y Pseudoplatystoma son los menos representados. Los restos referidos como Osteichthyes incluye principalmente vértebras (98,3 %) y restos fragmentarios de huesos dérmicos craneanos.
Dentro del conjunto identificado como H. littorale, el 78,95 % de los restos fueron espinas pectorales mientras que el 21,05 % corresponde al elemento cleitro. Las causas de la baja representación de otras unidades anatómicas podría deberse a varios factores no necesariamente excluyentes: a) una preservación diferencial mediada por su menor densidad ósea en relación a las espinas pectorales (Butler y Chatters, 1994; Musali et al., 2003, Musali y Pérez Jimeno, 2016); b) los métodos de preparación de los alimentos como son la producción de harina de pescado que derivaría en la destrucción de la región axial, principalmente vértebras (Arenas, 2003), o al ahumado de las presas permitiendo diferir su consumo en ocasiones en que se necesita consumirlas fuera del campamento base; c) manejo de las colecciones que puede producir una mayor fragmentación del material con la consecuente pérdida de caracteres diagnósticos que aumenta el número de piezas indeterminadas (INDET), mientras que las espinas pectorales y dorsales tienen un mayor grado de determinación taxonómica, tanto por sus caracteres como por su mejor preservación.
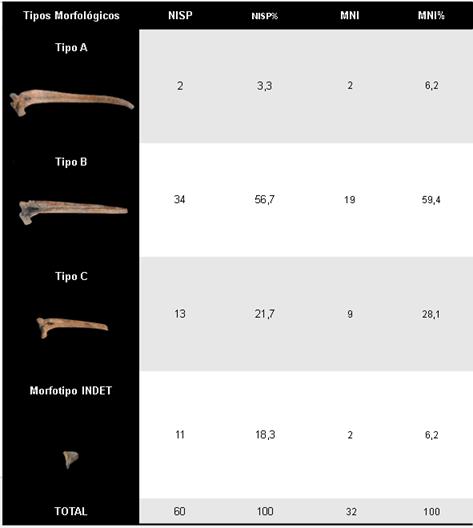
El 81,66 % de las espinas pectorales clasificadas como H. littorale (NISP: 49) pudieron ser asignadas a uno de los tres morfotipos. El 3,3 % corresponde a espinas pectorales de machos adultos en periodo reproductivo (tipo morfológico A), el 56,7 % corresponden a espinas pectorales de adultos sin diferenciación sexual (tipo morfológico B) y el 21,7 % fue clasificado como espinas pectorales de juveniles (tipo morfológico C). Las del tipo C presentan una alta diversidad de grados de desarrollo del dentado. El 18,3 % fue clasificado como morfotipo INDET debido a que se ha perdido la porción diagnóstica. El MNI correspondiente a machos en época reproductiva es de dos individuos, mientras que para machos fuera del periodo reproductivo o hembras MNI= 19 y el de juveniles MNI= 9 (Tabla 2). Para el grupo de espinas de morfotipos indeterminado, el MNI= 2 luego de estimar las posibles correspondencias con los otros morfotipos (Tabla 2). Si bien los valores de MNI % varían levemente en relación con el NISP %, siguen la misma tendencia.
Integración de la información y discusión
El potencial analítico e interpretativo de los restos de peces ha sido ampliamente abordado en las investigaciones arqueológicas (e. g. Acosta et al., 2007; Pérez Jimeno, 2009; Santini, 2009; Musali, 2010; Santini, 2012; Musali et al., 2013; Sartori, 2015; Barboza, 2016; Musali y Pérez Jimeno, 2016; Bastourre y Apolinaire, 2017, entre muchos otros). Sin embargo, un aspecto de escaso desarrollo está relacionado con su potencial para abordar la estacionalidad de explotación de recursos en sitios arqueológicos. En particular, el estudio de los periodos de captura a partir del registro ictiofaunístico presenta algunas ventajas, pues está relacionado con la fisiología y etología de los peces (Svoboda, 2013) y permite obtener información valiosa para profundizar sobre los contextos de las ocupaciones humanas (Béares y Zangrando, 2016 y la bibliografía allí citada). Por lo tanto, consideramos que los estudios ictioarqueológicos con una perspectiva ecológica nos permiten conocer más acerca del ambiente, el uso del espacio y la explotación de recursos que implementaron las sociedades del pasado.
En esta oportunidad, vemos que la información obtenida a través de la identificación y cuantificación de los morfotipos de espinas pectorales de H. littorale es congruente con las interpretaciones previas que se realizaron sobre la ocupación del sitio arqueológico seleccionado para probar el modelo. Las proporciones de los morfotipos de Sotelo 1 (Fig. 5), dan cuenta que la pesca comenzó en el periodo de lluvias, con mayor probabilidad hacia fines del periodo reproductivo de la especie. Es decir, hacia el final del periodo húmedo e inicio del de sequía (escasa presencia del morfotipo A y proporciones similares de los morfotipos B y C, véase Fig. 3). Sin embargo, hay que tener en cuenta que una proporción considerable de espinas (NISP %= 18,3) no pudieron asignarse a un morfotipo. En este sentido, entendemos que el morfotipo A podría estar subrepresentado debido a que la zona diagnóstica para su determinación es la más propensa a perderse por fragmentación. En ese caso, deberíamos pensar que los eventos de captura comenzaron en pleno período húmedo.
De todos modos, consideramos que las proporciones se ajustan al modelo, teniendo en cuenta las variaciones estacionales en los cuerpos de agua y la disponibilidad de los recursos. Se destaca que la captura de estos especímenes debió haber sido difícil en aguas profundas y de gran extensión. Mientras que los cuerpos de agua en reducción -proceso que en la región comienza a inicios de la estación seca en el otoño- permiten la agregación de los peces, que se traduce en una mejor identificación de estos para aplicar una pesca mediante redes (Arenas, 2003)2. Cabe destacar que este método de captura (dependiendo del tamaño de la malla) favorece la obtención de presas de pequeño tamaño y con distinto grado de desarrollo como pueden ser los casos de Anadoras sp. y H. littorale. También pudieron haber sido obtenidos individuos de estadios tempranos de Rhinodoras sp. y Oxydoras sp. mediante la misma técnica, aunque la sistematización del registro arqueológico de estas especies en diferentes estadios del desarrollo es un estudio que se encuentra en curso. Los individuos de H. littorale que alcanzan la etapa juvenil presentan una longitud total de 24,1 mm mientras que la longitud estándar media de las hembras maduras es de 106,3 mm y la de machos maduros es de 119,9 mm (estos últimos pueden alcanzar una longitud total de 266 mm; Winemiller, 1987; Orfinger, 2015). En este sentido, la gran representación de juveniles en el sitio analizado estaría de acuerdo con tamaños de malla relativamente pequeños.
Además, teniendo en cuenta la baja proporción de peces en el sitio Sotelo I, proponemos que la captura de individuos de H. littorale pudo haber sido parte de un evento temprano/primeros eventos de pesca de la temporada. Esta inferencia se basa en la información etnobiológica (Tola y Medrano, 2014) y casos arqueológicos de la región (del Papa y Lamenza, 2019), ya que se espera una predominancia de la pesca sobre otras actividades extractivas durante la estación seca (Tola y Medrano, 2014).
Conclusiones
Las proporciones de los morfotipos de Sotelo 1 (Fig. 5) dan cuenta de que la pesca comenzó en el período de lluvias, con mayor probabilidad hacia fines del periodo reproductivo de la especie. Es decir, el momento de transición entre el final del periodo húmedo e inicio del de sequía de los meses de abril y mayo (escasa presencia del morfotipo A y proporciones similares de los morfotipos B y C, véanse Figs. 3 y 5). La captura de los peces debió haber sido difícil en aguas profundas y de gran extensión, mientras que en los cuerpos de agua someros -proceso que en la región comienza a inicios de la estación seca en el otoño- permiten la agregación de los peces, que se traduce en una mejor identificación de estos para aplicar una pesca mediante redes. Este método de captura favorece la obtención de presas de pequeño tamaño y con distinto grado de desarrollo como sería el caso de H. littorale. La mayor representación de ejemplares juveniles en el sitio concuerda con tamaños de malla relativamente pequeños. Teniendo en cuenta la baja proporción de peces en el sitio Sotelo I, proponemos que la captura de individuos de H. littorale fue parte de un evento temprano o de los primeros eventos de pesca de la temporada.
En esta oportunidad aportamos información precisa sobre cómo las variaciones morfológicas de H. littorale pueden contribuir a los estudios sobre las estrategias de movilidad de las sociedades prehispánicas. Sin embargo, reconocemos el carácter tentativo y preliminar del modelo con algunas limitaciones propias del conocimiento sobre la biología de la especie y otras del registro arqueológico al que se quiera interpretar. Si bien se ha determinado que en individuos adultos el dentado es totalmente reabsorbido sin quedar ningún vestigio de su presencia, no hay información precisa sobre el momento en que se reabsorben totalmente. Actualmente, se están realizando estudios actualísticos que consisten en analizar especímenes recolectados en diferentes meses del año. De esta forma, podremos aumentar la resolución de la variación morfológica de las espinas y estimar el momento del ciclo vital en el que los dientes se reabsorben totalmente. Otra de las limitaciones tiene que ver con que la región diagnóstica para determinar al macho en periodo reproductivo es la más propensa a perderse por fragmentación del material. Por tal motivo, han comenzado a realizarse estudios de morfometría geométrica para explorar si existen variaciones en la región proximal de la espina pectoral que también permita su identificación.
Finalmente, señalamos que este modelo brinda información sobre el periodo de mínima ocupación del sitio y que puede ser aplicado a otros registros con presencia de H. littorale. En este sentido, hay que destacar la amplia distribución de la especie y la necesidad de poner a prueba el modelo en otras regiones. La integración de estos resultados con otras líneas de evidencia contribuirá a esclarecer la estrategia de ocupación del espacio y permitirá identificar con mayor precisión la estabilidad de los asentamientos.