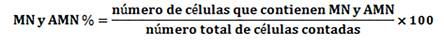Introducción
Clorpirifos es un insecticida organofosforado, clasificado entre los productos de clase II (moderadamente peligroso). Según la nomenclatura IUPAC su nombre es 0,0- dietil 0-(3,5,6-tricloro-2-piridil fosforotioato) y su fórmula empírica es C9H11Cl3NO3PS 19 . Al combinarse con la acetilcolinesterasa inhibe su acción enzimática, por lo cual la acetil colina no se libera del sitio receptor y el mensaje del impulso continúa pasando en las terminales nerviosas del insecto 3.
Es empleado como insecticida en cultivos de granos, algodón, frutas, nueces y hortalizas, así como en césped y plantas ornamentales. También está registrado para su uso directo en varias especies animales (caballos, ovejas, perros y otros). El clorpirifos actúa sobre las plagas principalmente como un veneno de contacto 9.
En seres humanos y animales, el clorpirifos puede introducirse por vía digestiva, pulmonar y cutánea. La exposición por poco tiempo a niveles bajos (miligramos) puede causar mareo, fatiga, secreción nasal, lagrimeo, salivación, náusea, molestia intestinal, sudor y cambios en el ritmo cardíaco. A niveles más altos, la exposición oral de corta duración puede provocar parálisis, convulsiones, desmayos y muerte.
Semanas después de la desaparición de los síntomas originales, puede causar debilidad muscular. Otras consecuencias incluyen cambios de conducta o hábitos de sueño, trastornos de humor y efectos en el sistema nervioso, así como en los músculos de las extremidades 4.
Este insecticida se dispersa en el aire y en aguas superficiales, acumulándose en diferentes organismos acuáticos, especialmente en los peces, que son vulnerables a los efectos perjudiciales del compuesto.
En teleósteos, las investigaciones sobre las consecuencias provocadas por exposición a pesticidas adquieren gran relevancia ya que los resultados obtenidos se pueden emplear para predecir probables mecanismos de toxicidad en seres humanos. Además, los peces han demostrado ser modelos experimentales útiles para la evaluación del estado de los ecosistemas acuáticos expuestos a la contaminación ambiental 8.
El objetivo del presente trabajo fue evaluar la genotoxicidad del clorpirifos en Prochilodus linneatus (Pisces, Prochilodontidae) a través de la frecuencia de micronúcleos (MN) y de alteraciones de la morfología nuclear (AMN) en eritrocitos de sangre periférica, después de una exposición crónica al insecticida.
Material y Métodos
Animales. Ejemplares juveniles de P. linneatus con 18,2 ± 3,2 g y 11 ± 1,8 cm (media ± DE, n = 36), fueron proporcionados por el Instituto de Ictiología del Nordeste (INICNE, Corrientes, Argentina). Antes de las pruebas de toxicidad, los especímenes fueron aclimatados a las condiciones de laboratorio por un lapso de 15 días, permaneciendo en tanques de 300 litros de agua declorinada a 20ºC, pH 7.0 y un fotoperíodo ajustado de 12 h de oscuridad y 12 h de luz. Durante esta etapa los especímenes fueron alimentados cada 48 h y se efectuaron controles periódicos de su estado sanitario.
Producto químico. Se empleó clorpirifos (0,0-dietil 0-[3,5,6-tricloro-2-piridil fosforotioato]) en su forma pura (99,9%), Sigma Aldrich Nº CAS 2921-88-2.
Experimento de exposición in vivo. Los peces se dividieron en dos grupos: control (C= mantenidos en agua de pozo artesiano) y tratados con clorpirifos (T1 = 10 μg/l; T2= 30 μg/l y T3 = 90 μg/l). Se efectuaron tres réplicas por grupo (3 individuos por pecera). Las peceras poseían 10 litros de capacidad para el bienestar de los peces y el mejor equilibrio de los acuarios (se empleó el cálculo de un litro de agua por cada centímetro de pez). Para la elección de las dosis se tomaron como referencia los valores establecidos en los niveles guía para la calidad de agua potable: 30 µg/l (Organización Mundial de la Salud, OMS) y 90 µg/l (Decreto 831/1993 reglamentario de la Ley
24.051 sobre régimen de desechos peligrosos, República Argentina). De esta manera el ensayo contempló las dos dosis referenciadas y una tercera de menor concentración.
Sacrificio. Los animales permanecieron en los acuarios durante un lapso de 7 días. Este periodo es inferior al tiempo necesario para la degradación del insecticida en agua, estimado en 29 días en condiciones controladas del laboratorio. Culminada la etapa de exposición, los ejemplares fueron sacrificados con sobredosis de clorhidrato de lidocaína. Para el ensayo de micronúcleos las muestras de sangre se obtuvieron del pez por punción de la vena caudal, utilizando una jeringa heparinizada.
Ensayo de micronúcleos. Inmediatamente después de la extracción de sangre, se colocó una gota sobre un portaobjeto para la realización de los frotis. Éstos se fijaron en etanol durante 10 min y se dejaron secar al aire a temperatura ambiente; luego se tiñeron con Giemsa al 5% en tampón Sörenson (pH 6,9) durante 20 minutos. Se examinaron un total de 2000 eritrocitos de cada individuo. Las microfotografías fueron tomadas con microscopio Olympus BX41 provista de cámara digital Motic 9.0. En las muestras analizadas se determinó la cantidad de micronúcleos (MN) y el número de alteraciones
morfológicas nucleares (AMN). Los criterios para la identificación de MN y AMN fue- ron los establecidos para los test de micronúcleos en peces 7. Las frecuencias de MN y AMN se obtuvieron según el siguiente cálculo:
Análisis estadísticos: los cálculos incluyeron media aritmética y desvío estándar, efectuándose asimismo el test t de Student. Se realizó además, un análisis de la variancia (ANOVA) con un nivel de significancia del 5%.
Resultados y Discusión
Se analizaron 36 ejemplares de P. linneatus. En cada uno de ellos se examinaron 2.000 eritrocitos, resultando un total de 72.000 células contadas. Se observaron células con MN, muescas, lobulaciones, evaginaciones, núcleos en forma de ocho, núcleos segmentados y núcleos con vacuola (Figura 1).
Las frecuencias de MN y AMN para los diferentes grupos fueron: control = 0,13%; T1 = 0,29%, T2 = 0,37% y T3 = 0,88% (Tabla 1). El análisis estadístico reveló que hubo diferencias significativas entre las dosis 10 µg/l y 90 µg/l (p<0,005) y entre las dosis 30 µg/l y 90 µg/l (p<0,005), mientras las dosis 10 µg/l y 30 µg/l no mostraron diferencias entre ambas, ni tampoco con el grupo control (Figura 2).
No se encontraron trabajos que emplearan clorpirifos en su formulación pura. Con relación al efecto genotóxico de formulaciones comerciales a base de clorpirifos en pe- ces, existen estudios realizados en especímenes de agua dulce. Experiencias en ejempla- res de Channa punctatus expuestos a las concentraciones de 203, 406 y 609 µg/l de clorpirifos (Tricel) revelaron que la concentración más baja del tratamiento indujo en eritrocitos una frecuencia de MN a las 24 h de 0,070%, viéndose aumentado significativamente a 0,875% después de 96 h de exposición.
Una tendencia similar se observó para la segunda concentración, en la cual la frecuencia de MN de 0,134% en 24 h aumentó a 0,964% después de 96 h. Sin embargo, en la concentración más alta, la inducción de MN fue menor comparada con los demás tratamientos 1.
Especímenes de Channa punctatus se utilizaron en ensayos crónicos (35 días), empleando dosis de 203, 102 y 68 µg/l del pesticida; el análisis mostró que el clorpirifos de grado técnico (Tricel) es genotóxico para los peces, incluso a una concentración 68
µg/l, siendo ello indicativo de los potenciales peligros del plaguicida para los organismos acuáticos 2.
De igual manera, los peces de agua dulce de la especie Channa punctatus expuestos a las concentraciones de 10, 5, 2,5 y 1 µ/l de clorpirifos evidenciaron después de 25 días una mayor frecuencia de eritrocitos con MN y anomalías nucleares en comparación con los individuos controles.
La frecuencia de micronúcleos y anomalías nucleares en los eritrocitos periféricos aumentó progresivamente con el incremento del período de exposición y/o concentración del insecticida 14. Otros estudios realizados con ejemplares de Cirrhinus mrigala expuestos durante 35 días a las dosis de 0,02, 0,04 y 0,08 mg/l de clorpirifos, revelaron que todos los grupos tratados tuvieron una mayor frecuencia de eritrocitos con MN y anomalías nucleares, en comparación con el control.
El incremento en la frecuencia de MN fue dependiente de la dosis empleada y de la duración del tratamiento. A lo largo del período experimental, la inducción de MN y su frecuencia fueron significativamente mayores en la dosis de 0,08 mg/l en comparación con los tratamientos de 0,02, 0,04 y control 5.
Ensayos efectuados con una formulación comercial (Pyrinex) a base de clorpirifos en Poecilia reticulata por un período de 96 h y a las concentraciones de 0; 0,005; 0,01; 0,015; 0,020 y 0,025 mg/l revelaron la aparición de micronúcleos y otras anormalidades nucleares en todos los tratamientos y controles, siendo su frecuencia dependiente de la concentración de clorpirifos y de la temperatura, registrándose mayores alteraciones (MN y AMN) en coincidencia con la mayor temperatura (30°C) y concentración (0,025 mg/l) 21 .
Por otro lado, se realizaron ensayos de laboratorio con ejemplares marinos. Así, Chanos chanos puestos en contacto con clorpirifos a la dosis de 1,38; 2,15; 4,53; 9,27 y 18,79 µg/l mostraron una respuesta clastogénica (formación de micronúcleos) al aumentar las concentraciones de pesticidas 18.
Del mismo modo, en Oreochromis mossambicus sometidos a la acción del insecticida durante 48 h a las concentraciones de 0,0001; 0,0002; 0,0003; 0,001 y 0,01 ppm se observó un aumento en la frecuencia de MN en los individuos tratados en comparación con los del grupo control, siendo esta especie considerada muy resistente, por lo tanto cualquier efecto de los pesticidas indicaría un impacto mayor en otras especies susceptibles 17.
La detección del impacto de xenobióticos es de gran importancia para la evaluación de la citotoxicidad de los mismos, ya que el potencial genotóxico suele estar implicado en toxicidades carcinógenas y reproductivas como un factor de riesgo primario. Las pruebas de genética toxicológica son útiles ya que permiten describir la capacidad de diferentes compuestos para dañar la información genética celular y para inducir mutaciones 10.
Los glóbulos rojos son un valioso modelo in vitro para evaluar la citotoxicidad de diferentes moléculas naturales o sintéticas, y orgánicas o inorgánicas mediante medidas de daño celular 10. El test de MN es una prueba muy utilizada como marcador de efecto genotóxico de diferentes contaminantes en los estudios de monitoreo biológico para evaluar su potencial citogenotóxico a campo y en condiciones de laboratorio. La aparición de micronúcleos en una célula indica la presencia de aberraciones cromosómicas durante la mitosis 11.
Por otro lado, las anormalidades morfológicas nucleares han sido observadas en eritrocitos cómo consecuencia de contaminantes ambientales y químicos con acciones citotóxicas y mutagénicas. Los mecanismos de su formación no han sido totalmente explicados. Sin embargo, son considerados como indicadores de daño genotóxico, completando así los resultados de los conteos de micronúcleos en ensayos de rutina 12.
Una probable explicación sobre el daño en el material genético de P. linneatus puede deberse al potencial del clorpirifos para ocasionar anomalías inmunológicas, daño tisular y producción de especies reactivas de oxígeno (EROs), además de la consecuente inducción de estrés oxidativo 13.
Todos los organismos están expuestos a EROs, los cuales pueden ocasionar daño en el ADN, sin embargo en condiciones normales existe un eficiente sistema de enzimas detoxificantes y de reparación de ADN que mantienen el equilibrio de la oxidoreducción 6. Por otro lado, cuando la concentración de las especies reactivas de oxígeno está crónicamente aumentada, se produce estrés oxidativo, perturbando así el metabolismo celular, su regulación y sus constituyentes 16 .
Los organofosforados como el clorpirifos, pueden producir estrés oxidativo a través de varios mecanismos, así como ruptura de las señales neuronales y endocrinas, ocasionando un incremento en el influjo intracelular de Ca2, desencadenando la activación de enzimas proteolíticas, y la generación de radicales libres.
Si bien, el Eros regula varios procesos biológicos mediante vías de transducción, niveles altos y/o sostenidos de estas sustancias desencadenan estrés oxidativos que podrían causar daño severo al ADN, proteínas y lípidos, generando disfunciones y culminando en la muerte celular 15, 20.
En conclusión, los resultados obtenidos permiten deducir que el clorpirifos puro a la dosis de 90 μg/l genera la aparición de alteraciones en el núcleo de eritrocitos de P. linneatus, lo cual podría indicar su potencial efecto nocivo para el medio ambiente.
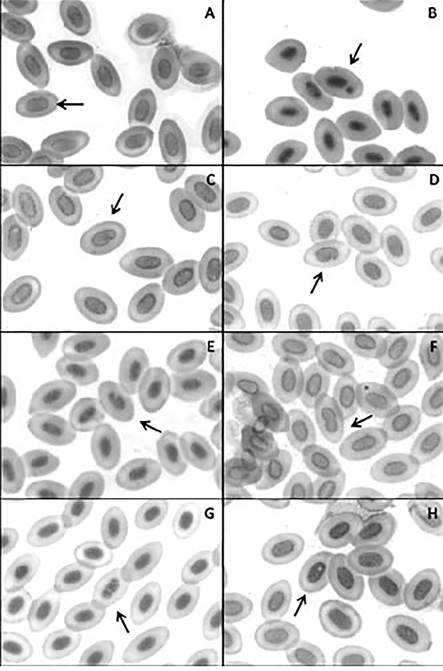
Figura 1 Fotomicrografía de frotis sanguíneos de P. linneatus, a: eri- trocitos con núcleos normales; b: micronúcleo; c: muesca; d: lobula- cion; e: evaginación, f: forma de ocho; g: segmentado; h: vacuolas.
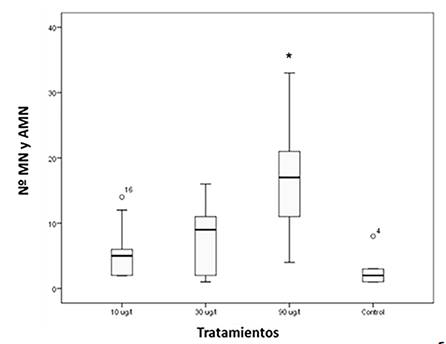
Figura 2 Box plot mostrando el número de micronucleos (MN) y anormalidades morfológicas nucleares (AMN) en los diferentes tratamientos en P. linneatus después del periodo de exposición (7 días). Se observan diferencias significativas en la dosis de 90 µg/l (*p<0,05).
Tabla 1 Porcentaje de eritrocitos con morfología nuclear normal y alterada según tratamientos. MN: número de micronucleos, AMN: anormalidades morfológicas nucleares.
| concentracion del clorpirifos en agua | % de eritrocitos sin MN y AMN | % de eritrocitos con MN y AMN |
|---|---|---|
| no contiene (control) | 99,87 | 0,13 |
| 10 µg/l (T1) | 99,71 | 0,29 |
| 30 µg/l (T2) | 99,63 | 0,37 |
| 90 µg/l (T3) | 99,12 | 0,88 |