I. INTRODUCCIÓN
La enfermedad de Alzheimer (EA), la causa más frecuente de demencia, es una enfermedad neurodegenerativa progresiva caracterizada por la pérdida de habilidades funcionales, de comportamiento y cognitivas, que principalmente afecta a la población de adultos mayores. El trastorno lentamente progresa con pérdida de las habilidades funcionales y finalmente a una completa dependencia [1].
La Depresión Mayor (DM), trastorno de salud mental de alta prevalencia a nivel mundial, es una enfermedad neurocognitiva que se caracteriza por depresión persistente y pérdida de interés. La DM es una condición incapacitante, que puede conducir al suicidio [2].
Las neuroimágenes funcionales de medicina nuclear con Tomografía Computada de Fotón Único (SPECT) proveen información valiosa en el diagnóstico de EA y DM. En ambas patologías se describe una alteración en el flujo cerebral regional (rCBF) [3] que puede verificarse mediante imágenes SPECT luego de administrar a los pacientes el radiofármaco 99mTc-etilcisteinato dimérico (99mTcECD). En el caso de EA, las imágenes SPECT arrojan luz sobre los procesos patológicos subyacentes, muchos años antes de la aparición de los síntomas clínicos [4]. En el caso de la DM, las imágenes SPECT aportan datos objetivos al diagnóstico psiquiátrico que principalmente está basado en relatos del paciente y entrevistas clínicas [5].
Existen pautas y recomendaciones consensuadas referentes a la indicación, preparación, realización, interpretación e informe de los SPECT con 99mTc-ECD [6]. Entre las recomendaciones para realizar los estudios SPECT cerebrales se destaca la necesidad de usar el colimador de mayor resolución disponible, el menor radio de rotación posible y adquirir el estudio entre los 30 minutos y las 6 horas de administrado el RF. En la mayor parte de los Servicios de Medicina Nuclear (SMN) de nuestro país el colimador de mayor resolución posible es el de propósitos generales (LEAP), que por sus dimensiones es compatible con un radio de rotación de 25 cm. Asimismo, por cuestiones prácticas es frecuente que las imágenes SPECT cerebrales se tomen al paciente lo más pronto posible luego de haber administrado el RF. Es posible que, aún operando dentro de los parámetros recomendados por las sistemáticas, los estudios SPECT cerebrales que se realizan en los centros de salud locales no arrojen resultados con valor diagnóstico.
SIMIND Montecarlo (MC) [7] fue diseñado para simular adquisición de imágenes en una cámara gamma, permitiendo modelar distintos parámetros de operación del equipo. Se ha verificado la validez de SIMIND MC para simular distintos modelos de cámaras gamma [8,9], en particular el modelo Picker Prism 2000XP [10,11] que es objeto de estudio en este trabajo.
El objetivo del trabajo es simular los SPECT cerebrales que se adquieren en una cámara gamma Picker Prism 2000XP tanto en escenarios recomendados por las sistemáticas así como en condiciones de trabajo frecuentes en los centros de salud locales y evaluar cómo la elección de los parámetros de afecta la detección de EA y DM en las imágenes de cerebro resultantes. Las simulaciones realizadas verificaron que con la cámara gamma configurada las lesiones patognomónicas de la EA y la DM sólo pueden ser visualizadas si se utilizan colimadores de alta resolución, distancias paciente/ detector de 16 cm y tiempos de espera post-administración de 45 minutos.
II. MÉTODOS
Programa SIMIND MC
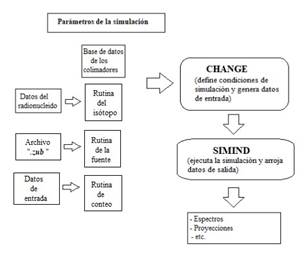
El programa SIMIND MC se basa en el uso de números pseudoaleatorios de distribución uniforme para simular el proceso de transporte de radiación. En este trabajo se simulará el transporte de fotones emitidos a partir de una fuente radiactiva de 99mTc con una distribución de actividad simulada en un fantoma antropomórfico en su camino hacia el cristal de centelleo de la cámara gamma. El código SIMIND MC consiste de dos programas principales: 1) CHANGE que permite definir las condiciones de simulación y además genera los datos de entrada al sistema, que luego se van a guardar en un archivo de extensión .smc y 2) SIMIND que lee los archivos de entrada y los ejecuta. La simulación se lleva a cabo en SIMIND y devuelve los resultados calculados como espectros, imágenes en formato interfile, mapa de densidades, etc. En la Fig. 1 se esquematiza la entrada y salida de archivos usados y creados por SIMIND.
Fantoma Zubal
Los fantomas antropomórficos voxelizados consisten en un arreglo 3-D de voxeles que modelan la anatomía humana. En la Fig. 2 se muestran cortes transversales a distintas alturas del fantoma de cabeza Zubal [12], que se eligió como modelo del paciente en el presente trabajo.
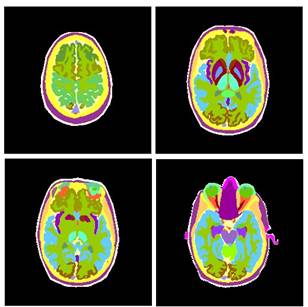
FIG. 2: Cortes transversales a distintas alturas del fantoma antropomórfico de cabeza desarrollado por Zubal et al.
Los criterios que se utilizaron para recrear el patrón de la distribución del radiofármaco (RF) en el fantoma antropomórfico son los siguientes:
Para el escenario que corresponde a un paciente normal se asignó una concentración relativa(CR) de actividad con preponderancia en la sustancia gris y en los núcleos de la base, respetando una relación 4:1 con la sustancia blanca [13], que es la que muestran estos territorios en estudios de cerebros normales.
Para simular la distribución del RF que corresponde a las enfermedades del SNC (EA y DM)se asignó un valor de CR menor (umbral con carácter diagnóstico) a las regiones específicas donde esas patologías muestran hipoflujo sanguíneo (hipoflujo en región frontal en DM [5] y en regiones temporo- parietales en EA [14]).
Para simular la distribución del RF a distintos tiempos post-administración se asignaron dis-tintos valores de CR en el pool sanguíneo (cuanto menos tiempo se espera luego de inyectar el RF, mayor es la CR del RF en el pool sanguíneo) [15].
En la Tabla 1 se muestran los valores CR para cada región anatómica en los distintos escenarios simulados.
Simulación de la cámara gamma
Una vez definido el archivo simu.zub (que contiene los datos de la distribución de la actividad del fantoma) se realizó la simulación de una imagen SPECT con el programa SIMIND MC utilizando las especificaciones de adquisición de la cámara gamma Picker Prism 2000XP (que es el equipo más empleado actualmente en nuestro país). Los parámetros técnicos de la cámara se cargaron en el programa CHANGE y se guardaron en el archivo simu.smc.
Los escenarios simulados se correspondieron con parámetros operacionales óptimos (colimador de alta resolución -LEHR- y distancia detector/ paciente de 16 cm -que es posible de alcanzar en equipos especialmente diseñados para realizar este tipo de estudio-) y con parámetros operacionales que son más frecuentes en los centros de salud de nuestro país (colimador de propósitos generales -LEAP- y distancia detector/ paciente de 25 cm).
III. RESULTADOS
Influencia del colimador y de la distancia detector-centro de rotación en la calidad de la imagen
En la Fig. 3 se muestran cortes transversales de SPECT cerebrales obtenidos por simulación de cerebros normales (A) y cerebros patológicos (B y C) a distintas distancias detector/ centro de rotación y utilizando distintos colimadores. Las imágenes marcadas con un asterisco (3.2 y 3.4) fueron adquiridas en lo que podría considerarse condiciones ideales, al mínimo de distancia del detector, con el colimador de mayor resolución y a un tiempo de espera óptimo de 45 minutos. En estas imágenes se visualizan claramente los defectos bilaterales configurados en la simulación: hipocaptación biparietal en el caso de la EA e hipocaptación en ambos lóbulos frontales en el caso de la DM. La bilateralidad de las hipocaptaciones es fundamental para hacer el diagnóstico correcto en ambas patologías.
Las imágenes 3.3 y 3.5 corresponden a la adquisición con un colimador LEHR, pero se aleja el detector a 25 cm del centro. En estas condiciones de adquisición prácticamente no se logran percibir los defectos configurados en la simulación. La falta de bilateralidad de las zonas hipocaptantes no permiten una presunción diagnóstica correcta.

FIG. 3: Imágenes SPECT simuladas de un cerebro normal (A), con lesiones compatibles con la enfermedad de Alzheimer (B) y Depresión Mayor (C) a distintas distancias detector/centro de rotación y con colimadores de distinta resolución. El asterisco marca las imágenes que fueron simuladas en las condiciones óptimas.
Una situación similar a la anterior se plantea en las imágenes 3.7 y 3.9, que fueron adquiridas a la distancia óptima de 16 cm, pero con un colimador LEAP, el más común en nuestro medio. El defecto que intenta detectarse es siempre el mismo. En estos escenarios se observa una mínima hipoactividad en las regiones donde se configuró la hipocaptación. Más aún, la falta de bilateralidad de las lesiones impide establecer un diagnóstico correcto.
Por último, las imágenes 3.8 y 3.10 fueron adquiridas en las peores condiciones. Con un colimador LEAP y a una distancia de 25 cm del centro de rotación. En estos escenarios el defecto simulado no se observa impidiendo establecer una sospecha fundada de alguna patología específica. El colimador LEAP, si bien detecta más eventos (por su alta sensibilidad) lo hace a costa de una menor resolución, (no los distribuye bien) y el patrón se desdibuja.
Influencia del tiempo de espera post-administración en la calidad de la imagen
En la Fig. 4 se muestran cortes transversales de SPECT cerebrales obtenidos por simulación de cerebros normales (A) y cerebros patológicos (B y C) a distintos tiempos post- administración del RF. En todos los casos las imágenes fueron simuladas utilizando un colimador LEHR y una distancia detector-centro de rotación de 16 cm, es decir, en óptimas condiciones. Las imágenes 4.2 y 4.3 se corresponden con la adquisición óptima (45 minutos post-administración). Las imágenes inferiores (4.4 - 4.6) son tanto la normal como la patológica simuladas con un incremento de la actividad en el pool sanguíneo debida a la obtención muy temprana del estudio. Es notorio cómo la presencia excesiva del RF en el pool sanguíneo impide el diagnóstico de la alteración que se configuró en la simulación.
IV. CONCLUSIONES
Las sistemáticas para la adquisición de SPECT cerebrales recomiendan adquirir la imagen al menos 30 minutos luego de la administración del 99mTc-ECD, utilizando colimadores de la mejor resolución posible y minimizando la distancia entre el detector y el paciente. Sin embargo, la implementación de estas recomendaciones en los SMN locales es difícil debido principalmente a cuestiones económicas y prácticas. Estas situaciones conllevan al detrimento de la calidad de las imágenes obtenidas y disminuyen su capacidad diagnóstica.