INTRODUCCIÓN
La hipertensión arterial (HTA) y las apneas e hipopneas obstructivas del sueño (AOS) son patologías de alta prevalencia frecuentemente relacionadas, fundamentalmente en pacientes con HTA resistente. 1,2,3
La HTA afecta al 36% de la población adulta. Su falta de control o tratamiento conduce a enfermedad cardiovascular, insuficiencia cardíaca, infarto agudo de miocardio, insuficiencia renal y accidente cerebrovascular después de años de exposición. 4
La AOS es un problema sanitario emergente, que afecta a más del 15% de los varones y más del 10% de las mujeres en la población general adulta, 5 y se asocia a morbimortalidad atribuible a accidentes de tránsito, laborales, domésticos y al desarrollo de complicaciones cardiovasculares y cerebrovasculares. 6,7
Se ha documentado que, en pacientes con apneas del sueño, se producen episodios de hipercapnia e hipoxemia secundarios al desarrollo de los eventos respiratorios. Estos fenómenos generan activación del sistema nervioso simpático con posterior aumento de la liberación de catecolaminas séricas y, como consecuencia, elevación de la frecuencia cardíaca y la presión arterial (PA) por mecanismo de vasoconstricción reflejo. 8 Otros desencadenantes son el efecto proinflamatorio, el aumento del estrés oxidativo y el aumento de la rigidez vascular. 9
La gravedad evaluada mediante el índice de apneas-hipopneas (IAH) se acompaña de cambios en los parámetros cardiovasculares, principalmente oscilaciones de la PA y frecuencia cardíaca. 10,11,12 Uno de los sistemas de regulación cardiovascular que se ve afectado durante AOS es el barorreflejo. Esto produciría una alteración de la activación quimiorrefleja secundaria a la hipoxia intermitente, lo que contribuye al aumento agudo y crónico de la PA. 13,14,15 Se ha observado que tan solo dos semanas de hipoxia intermitente nocturna en pacientes sin patología asociada podría incrementar la PA sistólica y diastólica hasta 8 mmHg y 5 mmHg respectivamente. 15,16
Datos de nuestro país describen que aproximadamente el 50% de los individuos con AOS son hipertensos 17,18 y el 44% de los hipertensos derivados a una consulta cardiológica especializada tuvieron apneas del sueño moderada a grave y fueron candidatos a tratamiento con dispositivos de presión positiva continua en las vías aéreas (CPAP). 19
Hay una relación dosis-efecto entre HTA y la gravedad de la AOS, habiéndose descripto que, por cada evento/h de incremento en el IAH, aumenta en 1% la posibilidad de desarrollo de HTA. 16,20,21,22
La HTA oculta se subestima en los pacientes con AOS y el monitoreo ambulatorio de presión arterial de 24 h (MAPA) frecuentemente la pone de manifiesto (del 42% al 80% de los casos). 16,22,23,24
Múltiples estudios demuestran que los individuos con AOS moderada-grave (IAH >15 eventos/h) presentan más probabilidades de ser hipertensos que individuos de similar edad y peso corporal, pero sin AOS. 16 En el Wisconsin Sleep Cohort Study, los sujetos normotensos con AOS moderada-grave triplicaron el riesgo de desarrollar HTA durante el seguimiento a 4 años en comparación con pacientes sin AOS. 16 Además, se ha observado que, cuanto mayor es la gravedad de la AOS, se requiere un mayor número y dosis de fármacos antihipertensivos para lograr el mismo control de la PA que los pacientes con AOS menos grave. 16
El tratamiento con CPAP ha demostrado beneficio antihipertensivo constante aunque modesto, con una amplia variación en la respuesta de un paciente a otro, y se observa mayor beneficio en la AOS grave, niveles de presión arterial más altos y según la adherencia al uso del dispositivo. 16,20 Si bien la mejoría en las cifras de PA oscila en el rango de -2 mmHg, pequeños ensayos de intervención sugieren que con el uso crónico del CPAP se reduce la actividad sostenida del sistema simpático, mejora la función barorrefleja y el estado proinflamatorio, por lo que disminuye así el riesgo cardiovascular. 13,16,20
Por otra parte, en los pacientes con HTA resistente, los niveles de aldosterona se correlacionan con la gravedad de la AOS y el bloqueo de esta reduce su gravedad. 16 Se ha afirmado que la AOS podría aumentar la secreción de esta hormona y que este podría llegar a ser uno de los mecanismos involucrados en el aumento de la PA. 25 En un estudio prospectivo de 114 pacientes con HTA resistente, se observó que los pacientes con riesgo elevado de AOS mediante cuestionario de Berlín presentaron mayor excreción urinaria de aldosterona de 24 h. 20
Se han planteado dos posibilidades: que la AOS estimule la liberación de aldosterona o que el exceso de aldosterona empeore la AOS preexistente, aunque la falta de un efecto constante del CPAP en los niveles de aldosterona en varios estudios parece un argumento en contra. 20 Sin embargo, datos clínicos documentan el efecto opuesto, es decir; el exceso de aldosterona empeora la gravedad de AOS, ya que la espironolactona (droga que bloquea el efecto de la aldosterona) disminuye la gravedad de AOS moderada-grave 21,27,28. En este sentido, algunos autores han propuesto, al fenómeno de redistribución caudorostral de fluidos, como mecanismo que vincula la génesis de las apneas del sueño en pacientes con HTA, lo que incrementa la colapsabilidad de la vía aérea superior. 26
Por lo expuesto, existe una relación entre aldosterona plasmática y AOS, y el mayor cuerpo de evidencia científica al respecto se ha obtenido de poblaciones con HTA resistente. En consecuencia, el objetivo del presente estudio es evaluar los niveles de aldosterona en pacientes con sospecha de HTA y riesgo de AOS derivados a un centro especializado antes de recibir tratamientos farmacológicos y su relación con la gravedad del AOS.
MATERIAL Y MÉTODOS
Estudio prospectivo, observacional y descriptivo en pacientes adultos con sospecha de HTA y AOS sin tratamiento al momento de la consulta.
La población estudiada debía cumplir con los siguientes criterios para ser incluidos: pacientes mayores de 18 años evaluados en el Centro de Hipertensión Arterial del Hospital Británico de Buenos Aires entre los meses de enero y octubre del año 2017 con sospecha de HTA sin tratamiento al momento de inclusión.
Se realizó sistemáticamente un registro MAPA de 24 h para confirmar el diagnóstico de HTA y se realizó un registro nocturno de poligrafía respiratoria domiciliaria.
En el laboratorio de rutina, se incluyó una medición de aldosterona plasmática, actividad de renina plasmática y su relación/cociente.
La aldosterona y renina se midieron desde una extracción basal matinal con el individuo en ayunas, en reposo por al menos 30 min y en decúbito. Las muestras sanguíneas fueron procesadas in situ por radioinmunoanálisis.
Los criterios de exclusión fueron diagnóstico previo conocido de hiperaldosteronismo primario, tratamiento farmacológico antihipertensivo, contraindicación para realizar un MAPA, requerimiento de tratamiento farmacológico urgente, diabetes no controlada, enfermedad pulmonar obstructiva crónica conocida de grado moderado a grave, tratamiento previo con CPAP, diagnóstico de insuficiencia cardíaca aguda o crónica, insuficiencia renal grado moderado a grave, imposibilidad o intolerancia a la realización de la poligrafía respiratoria, patología tiroidea no controlada, supresión completa de la actividad de renina plasmática.
La medición de la PA en consultorio se realizó según guías nacionales e internacionales, 29,30 con un tensiómetro automático (OMRON 7220), en tres oportunidades separadas por 2 min entre cada una, descartando la primera y considerando el promedio entre las dos últimas.
El MAPA fue realizado con un equipo Spacelabs Ultralite (modelo 90217, SpaceLabs, Redmond, WA). Las tomas de PA fueron programadas cada 15 min durante el día (8:00 a. m. a 11:00 p. m.) y cada 30 min durante la noche (11:00 p. m. a 8:00 a. m.), luego ajustado al diario del paciente. Se definieron como normotensión cifras de PA diurna y nocturna menores o iguales a 135/85 mmHg y 120/70 mmHg, respectivamente. El MAPA y el registro de poligrafía respiratoria se realizaron en noches sucesivas.
La poligrafía respiratoria fue realizada con un polígrafo Apnea Link Plus™ (ResMed. Australia) con cinco canales y tres señales básicas, oximetría de pulso, flujo por cánula nasal y esfuerzo torácico, (dispositivos de nivel III de la American Academy of Sleep Medicine). 31 Solo se aceptaron como válidos aquellos registros con un tiempo total de registro en el análisis manual >240 min (>4 h). Se definió apnea como reducción del flujo aéreo en más del 80% del basal ≥10 s y las hipopneas se consideraron como una reducción del flujo aéreo del 50% ≥10 s asociadas a desaturaciones ≥3%. El IAH se calculó como el número de apneas/hipopneas por hora de evaluación válida (TTR) y se expresa en eventos por hora (ev/h). 32 Los pacientes se clasificaron como NO AOS (IAH <5 ev/h), AOS de grado leve (IAH ≥5,1 y menos de 15 ev/h) y AOS moderada-grave (IAH ≥15 ev/h).
Según los resultados obtenidos en los estudios, los pacientes se clasificaron en 6 categorías:
Normotensos sin AOS (No HTA GI) con IAH <5 ev/h.
Normotensos con AOS leve (No HTA GII) con IAH entre 5,1 y 15 ev/h.
Normotensos con AOS moderada-grave (No HTA GIII) con IAH >15 ev/h.
Hipertensos sin AOS (HTA GI) con IAH <5 ev/h.
Hipertensos con AOS leve (HTA GII) con IAH entre 5,1 y 15 ev/h.
Hipertensos con AOS moderada-grave (HTA GII) con IAH >15 ev/h.
Análisis estadístico
Los resultados se presentaron como porcentajes en las variables categóricas o media y desviación estándar en las numéricas. Las variables con distribución normal se expresan como medias y desviación estándar, y las variables sin distribución normal se muestran como medias y percentilos (25%-75%). Para comparar diferencias se utilizaron pruebas de comparaciones múltiples de Fisher, Kruskall Wallis y Dums. Una vez obtenidas las variables de predicción, se calculó el valor de p para la evaluación de significación estadística. Se consideró una p <0,05 para determinar significación estadística. Para el análisis estadístico se utilizó Graph Pad Prism-7.04™ software.
RESULTADOS
Se incluyeron 109 pacientes con la siguiente distribución: 16 pacientes No HTA GI, 15 pacientes No HTA GII, 9 pacientes No HTA GIII, 26 pacientes HTAGI, 19 pacientes HTAGII y 24 HTAGIII.
En los pacientes No HTA GI observamos menor perímetro de cintura y circunferencia de cuello que los No HTA GII y GIII (p <0.05). No se observaron diferencias significativas entre edad e índice de masa corporal (IMC) Tabla 1A.
Tabla 1 A. Variables de la población no hipertensa
| No HTA | No HTA GI (n 16) | No HTA GII (n 15) | No HTA GIII (n 9) |
|---|---|---|---|
| Hombres (%) | 31 | 33,3 | 77,7 |
| Edad (años) | 50,9 ± 12,4 | 48,5 ± 15,8 | 57,3 ± 14,7 |
| Perímetro cintura (cm) | 89,7 ± 12 | 99,7 ± 17,3 | 108,6 ± 14,4 * |
| Perímetro de cuello (cm) | 35,8 ± 3,1 | 39,6 ± 4,4 | 40,8 ± 3,8 ** |
| IMC (kg/m2) | 27,6 ± 5,5 | 32,4 ± 5,8 | 32,4 ± 7,6 |
| Tabaquistas (%) | 6,2%, n: 1 | 20%, n: 3 | 11,1%, n:1 |
| Diabéticos (%) | 6,2%, n: 1 | 6,6%, n: 1 | 11,1%, n:1 |
| Dislipémicos (%) | 31,2%, n: 5 | 60%, n: 9 | 100%, n: 9 |
| Score ACC/AHA | 4,5 | 7 | 8,6 |
* p < 0,05 entre No HTA GI y No HTA GIII ** p < 0,05 para No HTA GI respecto de No HTA GII y GIII Score ACC/AHA: Riesgo de eventos cardiovasculares a 10 años según la calculadora de American College of Cardiology/American HeartAssociation. IMC: índice de masa corporal.
En grupo de pacientes con HTA hubo predominio de tabaquistas, diabéticos (tratamiento con hipoglucemiantes orales y/o insulina) y dislipemia (tratamiento con hipolipemiantes orales y/o; colesterol total, LDL o triglicéridos mayor al valor de referencia). Existieron además diferencias significativa en; edad, perímetro de cintura, circunferencia de cuello e IMC (p <0.05), siendo mayor en el grupo con AOS moderada-severa (Tabla 1B).
Tabla 1 B. Variables de la población con HTA
| HTA | HTAGI (n 26) | HTAGII (n 19) | HTAGIII (n 24) |
|---|---|---|---|
| Hombres (%) | 42 | 68,4 | 66,6 |
| Edad (años) | 44,4 ± 12,5 | 49,3 ± 12,61 | 56±9,6* |
| Perímetro cintura (cm) | 89,4 ± 13,5 | 105,1 ± 9,9 | 105,5 ± 13,3 ** |
| Perímetro de cuello (cm) | 36,9 ± 4,4 | 41,6 ± 3,2 | 41,4 ± 3,5 ** |
| IMC (kg/m2) | 27,6 ± 6,7 | 32,2 ± 5,8 | 32,9 ± 7,3 ** |
| Tabaquistas (%) | 23,1%, n: 6 | 52,6%, n: 10 | 41,6%, n: 10 |
| Diabéticos (%) | 3,8%, n: 1 | 36,8%, n: 7 | 29,2%, n: 7 |
| Dislipémicos (%) | 19,2%, n: 5 | 44,4%, n: 8 | 33,3%, n: 8 |
| Score de ACC/AHA | 4,9 | 10 | 10,2 |
* p < 0.05 entre HTA GI y HTA GIII ** p < 0.05 para HTA GI respecto de HTA GII y HTA GIII Score ACC/AHA: riesgo de eventos cardiovasculares a 10 años según la calculadora de American College of Cardiology/American HeartAssociation. IMC: índice de masa corporal.
El riesgo cardiovascular global evaluado mediante la calculadora propuesta por ACC/AHA mostró que el riesgo es más elevado en los grupos de No HTA GII y III en comparación con los No HTA GI, al igual que en los HTA GI versus HTA GII y GIII (Tablas 1 A y B), sin embargo, este incremento no resultó estadísticamente significativo.
En cuanto a la PA se hallaron diferencias significativas en la PA sistólica diurna entre los grupos HTA GI y G III, con aumento en los valores de MAPA en IAH >15 ev/h (Tabla 2).
Tabla 2 Valores de presión arterial en consultorio y en el monitoreo ambulatorio de 24 h
| Sin hipertensión arterial | HTA | |||||
|---|---|---|---|---|---|---|
| No HTA GI (n: 16) | No HTA GII (n: 15) | No HTA GI III (n: 9) | HTA GI (n: 26) | HTA GII (n: 19) | HTAGIII (n: 24) | |
| PA sistólica consultorio | 122 ± 14 | 119 ± 13,6 | 121 ± 13,5 | 135 ±17 | 140,3 ± 17,7 | 140,8 ± 18 |
| PA diastólica consultorio | 80 ± 7 | 77 ± 8 | 78 ± 10 | 90±11 | 91,3 ± 11 | 92 ± 11 |
| MAPA sistólico diurno | 118 ± 7 | 119 ± 10 | 120,7 ± 10,5 | 136 ± 12 | 139,8 ± 17,4 | 140 ± 17,5 |
| MAPA diastólico diurno | 74 ± 6 | 74 ± 7 | 77 ± 7 | 88 ± 8 | 87 ± 10,6 | 87,2 ± 10,6 |
| MAPA sistólico nocturno | 106 ± 9 | 104 ± 7 | 106 ± 7,5 | 123 ± 12 | 127 ± 14,7 | 128±1 |
| MAPA diastólico diurno | 64 ± 5 | 60,5 ± 5,5 | 62,8 ± 4,7 | 76 ± 7 | 76,6 ± 8,9 | 77,2 ± 9 |
En los resultados obtenidos de la extracción de sangre, fue posible observar un aumento escalonado en los valores de ácido úrico y lípidos en pacientes sin HTA, dependiente de la gravedad del AOS por IAH con diferencias estadísticamente significativas. El mismo patrón se observa en los pacientes con HTA, pero la diferencia no fue significativa. En cuanto a la glucemia en ayunas en el grupo con HTA fue más elevada basalmente que los no HTA y su aumento fue escalonado (p <0,05, Tabla 3).
Tabla 3 Datos de laboratorio
| Categorías | Sin HTA | HTA | ||||
|---|---|---|---|---|---|---|
| Grupos | No HTA GI (n: 16) | No HTA GII (n: 15) | No HTA GIII (n: 9) | HTA G1 (n: 26) | HTA GII (n: 19) | HTA GIII (n: 24) |
| Ácido úrico (mg/dL) | 5±1* | 5,6±1 | 6±1* | 5 ± 1 | 5,6 ± 1,2 | 5,6 ± 1,2 |
| Glucosa (mg/dL) | 89 ± 18 | 93 ± 11 | 95,5 ± 14 | 91 ± 8,5** | 100,6 ± 30,2** | 101 ± 30,5** |
| Hb1Ac (%) | 5,5 ± 0,3 | 5,5 ± 0,6 | 5,7 ± 0,66 | 5,4 ± 0,25 | 5,9 ± 1,6 | 5,9 ± 1,6 |
| Triglicéridos (mg/dL) | 91 ± 33 | 129,5 ± 55 | 127,2 ± 51 | 140 ± 106 | 142 ± 105 | 151,8 ± 73,6 |
| Colesterol total (mg/dL) | 173 ± 30** | 201 ± 35** | 201 ± 30** | 190 ± 42 | 194 ± 38 | 196 ± 38 |
| Creatinina (mg/dL) | 0,8 ± 0,1 | 0,8 ± 0,1 | 0,85 ± 0,12 | 0,8 ± 0,1 | 0,9 ± 0,13 | 0,9 ± 0,12 |
| Aldosterona (pg/mL) | 120 ± 88 | 132,4 ± 98,3 | 138,4 ± 98,4 | 128 ± 61,2 | 130 ± 76 | 133 ± 76 |
| Renina (ngA1/mL/h) | 1,9 ± 0,9 | 1,7 ± 1,3 | 1,4 ± 0,5 | 2,2 ± 1,5 | 1,8 ± 1,0 | 1,4 ± 0,8 |
| Relación aldosterona/renina | 8,7 ± 5,7 | 9 ± 5,1 | 12,7 ± 7,9 | 2,3 ±1,4 | 10,3 ± 7 | 11 ± 6,5 |
* p < 0,05 entre dos grupos y ** p < 0,05 para No HTA GI respecto de GII y GIII.
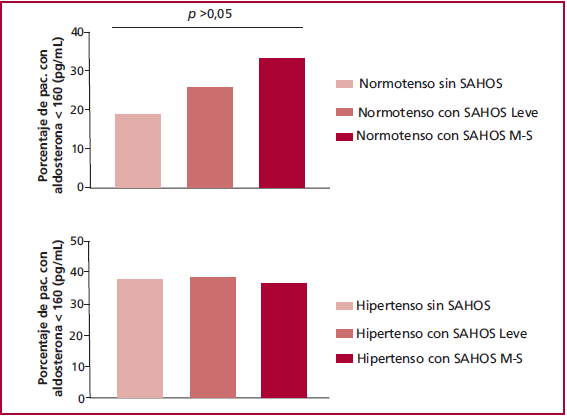
En la Figura 1, se observa que los pacientes con AOS presentaron un incremento progresivo (aunque no significativo), con mayores niveles basales matinales de aldosterona plasmática, independientemente que fuesen o no hipertensos. Adicionalmente, encontramos un incremento escalonado y proporcional, a medida que aumenta la gravedad de la AOS por IAH, en el grupo de pacientes normotensos (p <0,05). Este patrón no se observó en el grupo de pacientes con HTA, en los cuales el nivel de aldosterona plasmática mostró una tendencia ligeramente creciente según la gravedad del AOS, pero sin diferencias estadísticamente significativas (Figura 2).
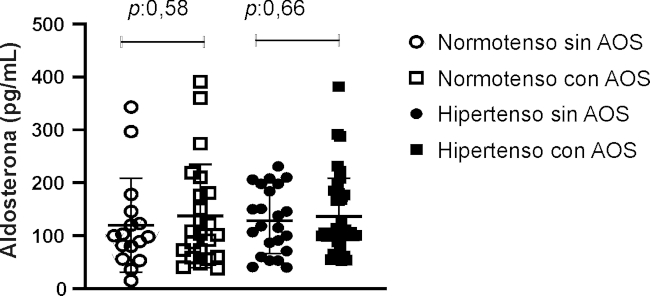
Fig. 1 Valores medios de aldosterona plasmática en relación al diagnóstico de HTA e IAH >5 ev/h en la poligrafía respiratoria. El valor basal medio de aldosterona fue mayor en hipertensos (139,1 ± 88,6 vs. 127,4 ± 83,3).
Los niveles de renina y su relación/cociente aldosterona renina fueron evaluados con el fin de descartar pacientes con hiperaldosteronismo primario (Tabla 3). Los valores de renina no mostraron ninguna diferencia significativa entre los grupos, mientras que la relación o cociente aldosterona renina mostró un aumento gradual y creciente entre los grupos, pero sin diferencias significativas.
DISCUSIÓN
La HTA y AOS están relacionados y ambos aumentan la morbimortalidad, por ello es relevante comprender la interacción entre ambas patologías.
Este estudio sugiere que la AOS se podría vincular a modificaciones en los valores de aldosterona independientemente de la HTA.
Llamativamente, se observó un incremento escalonado entre AOS y los valores de aldosterona en no hipertensos (p <0,05), mientras que en el grupo HTA se observó una tendencia creciente, pero sin diferencias estadísticamente significativas. Esto podría deberse a dos posibles motivos; el primero podría ser estadístico, ya que, para lograr significancia estadística, el tamaño de la muestra requerido con esos valores sería de 266 pacientes con un poder zeta de 1,96; y el segundo podría ser que los valores de aldosterona basales en pacientes hipertensos podrían deberse a una vía fisiopatogénica diferente.
Los estudios que analizan el papel de la aldosterona en AOS, en general, fueron llevados a cabo en pacientes con HTA grave o HTA resistente, o bien, en poblaciones de hipertensos tratados con fármacos (incluso antialdosterónicos) que podrían afectar la interpretación. 16,20
Los resultados de factores independientes de riesgo cardiovascular, como perímetro de cintura, circunferencia de cuello, IMC y valores de perfil glucémico y lipídico en el laboratorio, posiblemente se reflejen en conjunto mediante el Score ACC/AHA y nos lleven a la conclusión de que los pacientes hipertensos con AOS presentan un riesgo cardiovascular más elevado. 19,33
Entre los hipertensos se observó una discreta elevación, tanto entre los valores de PA de consultorio como en el MAPA diurno y nocturno, a medida que aumenta la gravedad por IAH. Valores de PA por MAPA consistentes con criterios diagnósticos de HTA se asociaron a valores de aldosterona superiores al hallado en el grupo No HTA.
El patrón de ascenso del valor de aldosterona plasmática mostró una tendencia proporcional y escalonada en normotensos dependiente de la gravedad de la AOS y alcanzó significación estadística. De esta manera, hallamos que la aldosterona se eleva con pendiente gradual en el grupo normotensión, atribuible a un fenómeno biológico dosis-respuesta, posiblemente como consecuencia del incremento del IAH y del grado de hipoxemia nocturna.
En nuestra población, el porcentaje de pacientes con aldosterona basal > 160 ng/mL fue del 35% con IAH > 15 ev/h versus el 40% en el grupo HTA. En sintonía con la hipótesis del grupo de Birmingham, es posible que exista en los pacientes con AOS un importante papel de la aldosterona y la retención hidrosalina con desplazamiento de fluido desde los tejidos al cuello se relacione con la gravedad por IAH. 20 Nosotros no realizamos mediciones fisiológicas acerca del fenómeno de movimiento de líquidos en estos pacientes y esto, de alguna manera, representa una limitación para nuestro estudio.
Adicionalmente, las fortalezas del presente análisis radican en la definición de HTA utilizando una lectura sistemática de MAPA, así como una técnica estandarizada para los estudios de sueño por expertos en medicina del sueño 17,19 y al hecho de que incluimos pacientes sin tratamiento (näive) al momento de la evaluación, de los cuales se tiene menor información. Estudios con mayor número de sujetos son necesarios para confirmar nuestros hallazgos, que deben ser vistos como generadores de hipótesis. El escaso tamaño de muestra puede generar un error beta de significación que deberá ser saldado con la continuación de este y otros estudios en la misma línea.
Finalmente, nuestros resultados muestran un aumento proporcional de los valores de aldosterona, glucemia y riesgo cardiovascular a medida que aumenta la gravedad de la apnea del sueño.