Los pacientes con diagnóstico de Tetralogía de Fallot (TF) que requieren una intervención precoz son aquellos dependientes de prostaglandinas o con cianosis grave debido a la disminución del flujo pulmonar, ya sea por una anatomía desfavorable del tracto de salida del ventrículo derecho (TSVD) o de las arterias pulmonares. El manejo de estos pacientes con factores de riesgo asociados (bajo peso, prematurez, edad <3 meses, anatomía desfavorable de arterias pulmonares, distribución coronaria anómala y condiciones preoperatorias críticas) continúa generando debate. Los procedimientos paliativos posibles incluyen la apertura quirúrgica del TSVD, la anastomosis sistémico pulmonar, la valvuloplastia pulmonar, o la colocación de un stent en el ductus arterial persistente o en el TSVD. La cirugía reparadora temprana en estos pacientes puede ser realizada con éxito, pero a pesar de sus múltiples ventajas, se asocia a mayor cantidad de complicaciones en el postoperatorio y posteriores reintervenciones. 1,2,3,4
El objetivo de este trabajo es presentar el manejo de un paciente con diagnóstico de TF, con múltiples factores de riesgo y operado con éxito sin complicaciones en el Hospital Interzonal Especializado Materno Infantil de Mar del Plata, Buenos Aires, Argentina.
Se trata de un paciente que nació de 32 semanas de gestación, con un peso de 1460 gramos y con cariotipo con trisomía 21, por cesárea de urgencia debido a los hallazgos de un ecocardiograma Doppler fetal patológico, con diagnóstico de comunicación interventricular (CIV) grande (localización anterior), estenosis pulmonar infundibular y valvular (Z score valvular -4), ramas pulmonares confluentes y de buen calibre, cabalgamiento de la aorta, comunicación interauricular (CIA) chica y ductus arterial persistente. Debido a la anatomía cardíaca desfavorable se indicó goteo continuo de prostaglandinas con el objetivo de mantener permeable el ductus arterial.
A los 20 días de vida presentó sepsis con bacteriemia a Escherichia Coli, asociada a un síndrome de distrés respiratorio severo. Luego de 7 días del tratamiento de su sepsis, se detectó una vegetación en la aurícula derecha de 7×7 mm, y se asumió el cuadro como endocarditis infecciosa por Escherichia Coli, por lo que se prolongó el tratamiento antibiótico 4 semanas, con un ecocardiograma de control sin vegetación. Luego de su salida de la unidad de terapia intensiva neonatal, y habiendo cumplido 58 días de asistencia ventilatoria mecánica, permaneció con requerimiento de oxígeno por displasia bronquio pulmonar. Como comorbilidades agregó diarrea crónica por enteropatía perdedora de proteína, por lo que se alimentó con leches hidrolizadas con requerimiento de nutrición parenteral (68 días totales). En el laboratorio presentaba hipoproteinemia con hipogamaglobulinemia e hipoalbuminemia.
Debido a los múltiples factores de riesgo descritos (TF ductus dependiente, prematurez, bajo peso, síndrome de distrés respiratorio e hipoproteinemia) y una vez resuelta la endocarditis infecciosa, la alternativa de colocar un stent en el TSVD impresionaba la opción más segura para postergar la cirugía reparadora y poder realizarla en las mejores condiciones clínicas posibles.
Implante del stent
Se ingresó por punción de vena femoral derecha, y se colocó un introductor de 6 French. Se observó un tracto de salida de 15mm de largo con una marcada estrechez dinámica en la sístole que se generaba a 4mm del plano valvular pulmonar. Se decidió colocar un stent coronario de 4×16 de cromo cobalto. Se progresó el stent tomando el plano valvular y el TSVD. Se insufló el balón lográndose un diámetro estable del infundíbulo de 4mm. En la angiografía posterior se observó buen flujo a través del mismo, con insuficiencia valvular pulmonar grave por haber sido la válvula colapsada con el stent.
Tras el procedimiento, el paciente fue trasladado a la sala de neonatología con saturación arterial de oxígeno entre 93-95%; se suspendieron las prostaglandinas y se constató el cierre del ductus arterial a las 48hs post procedimiento, descendiendo la saturación a 90 %. El paciente permaneció internado en la sala de pediatría para recuperación nutricional.
A los 7 meses de vida, presentaba saturación arterial de oxígeno de 85% con requerimiento de 0,5 litros de oxígeno por cánula nasal. El examen físico mostraba desnutrición crónica (peso 3,4 kg), precordio activo, signo de Dressler positivo, soplo sistólico en foco pulmonar 3-4/6. En el ecocardiograma: CIV grande de localización subaórtica, stent en TSVD que generaba un gradiente de 55 mmHg, hipertrofia del ventrículo derecho, ramas pulmonares confluentes y de buen calibre, cabalgamiento de la aorta y CIA chica. Se decidió su reparación quirúrgica.
Procedimiento quirúrgico
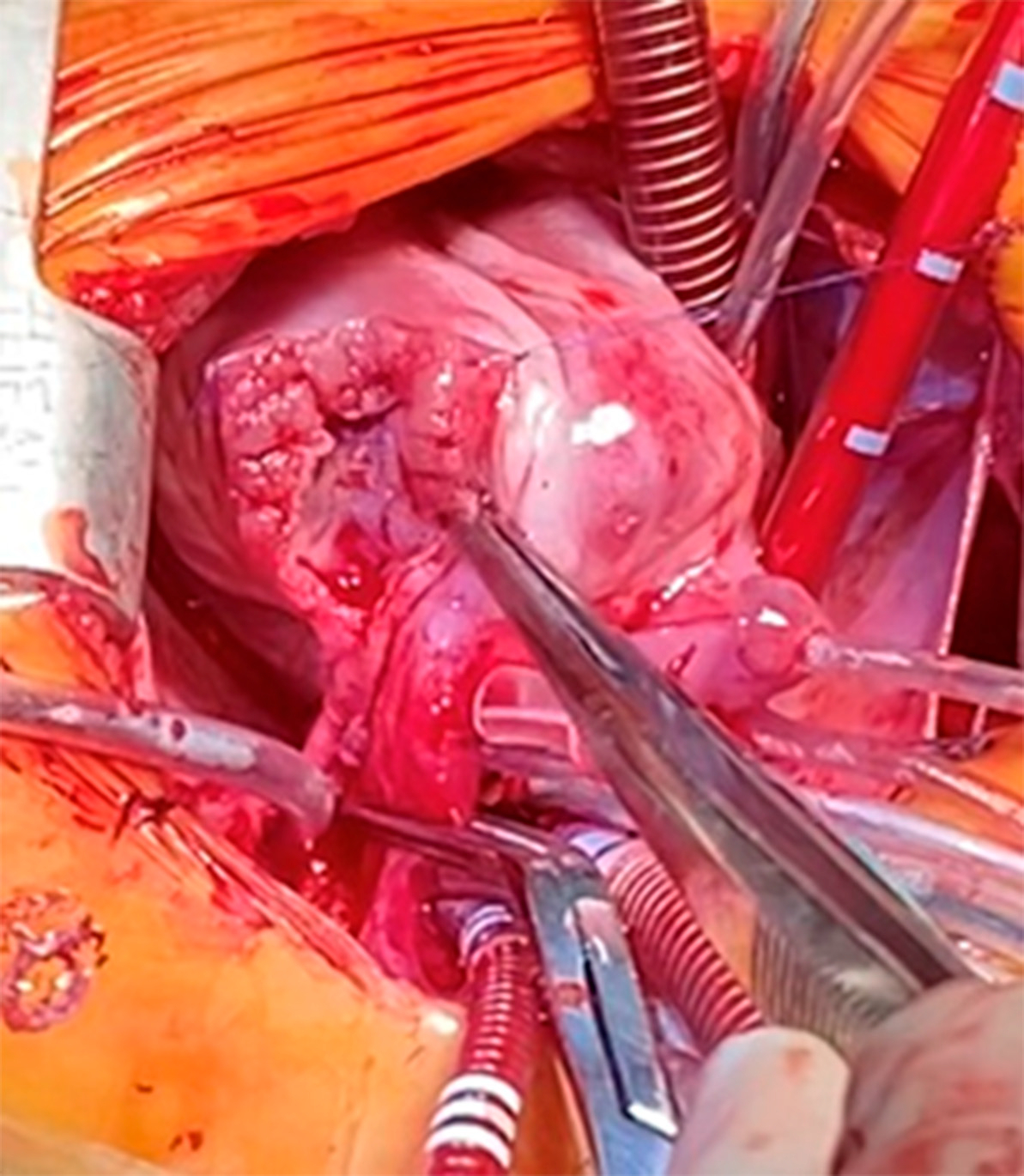
Se realizó por esternotomía mediana. Se reservó parche para plástica de la arteria pulmonar y se heparinizó al paciente. Se realizó canulación de las venas cavas superior e inferior y la aorta, se descendió la temperatura a 28 °C, se clampeó la aorta, se infundió cardioplejía de manera anterógrada y se colocó cánula de venteo de cavidades izquierdas. Se abrió el tronco de la arteria pulmonar a nivel del anillo y se extendió la incisión hasta la bifurcación de las ramas pulmonares (Figura 1). Se observó el stent a nivel de la válvula pulmonar y del TSVD, adherido a la pared posterior; se lo resecó por completo sin complicaciones (Figura 2). Se realizó resección infundibular por hipertrofia del ventrículo derecho y se cerró la CIV grande con parche de politetrafluoretileno de 0.6mm. Se suturó una válvula monocúspide de pericardio autólogo sobre el anillo pulmonar y parche transanular desde la ventriculotomía hasta la bifurcación de las ramas pulmonares. Se purgó aire de las cavidades izquierdas y se desclampeó la aorta luego de 61 min. El paciente recuperó ritmo sinusal. Con el paciente a 36,5 °C se desasistió de la circulación extracorpórea luego de 100 min y se decanuló.
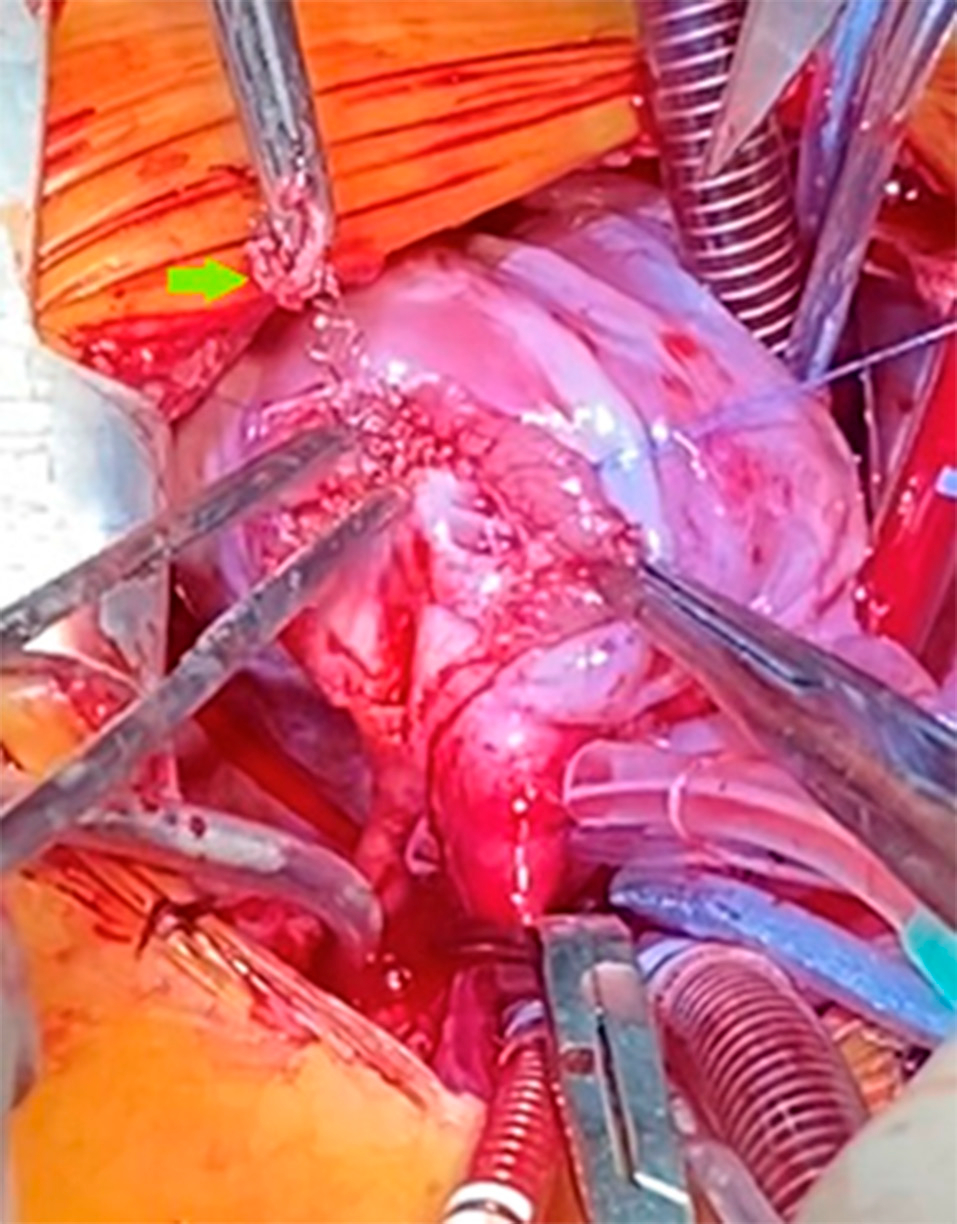
Fig. 1 Se comienza a extraer el stent (flecha verde) a través de la ventriculotomía donde se puede ver la adherencia a la pared posterior del tracto de salida del ventrículo derecho
El paciente cursó el postoperatorio inmediato con requerimiento de bajas dosis de inotrópicos. Fue extubado a las 48hs del postoperatorio, y se mantuvo con oxígeno por cánula nasal debido a su displasia broncopulmonar. Al 5° día postquirúrgico fue trasladado a un área de menor complejidad donde permaneció internado para recuperación nutricional. El ecocardiograma al mes de la cirugía mostró CIV cerrada, sin CIV residual, CIA cerrada, estenosis pulmonar leve, insuficiencia pulmonar leve a moderada, ramas pulmonares confluentes de buen calibre.
La TF se caracteriza por presentar una CIV grande de localización subaórtica, estenosis pulmonar, hipertrofia del ventrículo derecho y cabalgamiento aórtico. La cirugía en estos pacientes con ramas pulmonares confluentes y de buen calibre, habitualmente permite la reparación en forma primaria sin complicaciones y con excelentes resultados. Aquellos pacientes que son dependientes de prostaglandinas son cianóticos graves por hipoflujo pulmonar anterógrado severo, por lo que requieren una intervención temprana. En los pacientes con comorbilidades asociadas, la cirugía reparadora primaria puede ser realizada con éxito con baja mortalidad, pero se asocia a más complicaciones en el postoperatorio y reintervenciones.1,2,3,4 El procedimiento paliativo más frecuente es la anastomosis sistémico pulmonar, pero realizada en pacientes prematuros, con bajo peso o hipoplasia de ramas pulmonares, se asocia a mayor índice de complicaciones, como estenosis de la arteria pulmonar.5 En estos pacientes, la colocación de un stent en el TSVD es una alternativa como puente a la cirugía reparadora. 6 La cirugía reparadora de los pacientes con diagnóstico de TF con stent en el TSVD puede realizarse sin complicaciones. El stent se puede retirar en su totalidad en hasta un 95 % de los pacientes, requiriendo mayor tiempo de circulación extracorpórea. 6
En pacientes prematuros con bajo peso y comorbilidades asociadas, la colocación de stent en el TSVD resulta en una mejoría de la cianosis, no altera la anatomía de las ramas pulmonares y permite resolver las comorbilidades no cardíacas para poder realizar la cirugía reparadora sin complicaciones.