Introducción
La enfermedad de Hansen es una infección granulomatosa crónica producida por el Mycobacterium leprae y lepromatosis. La presentación clínica depende del estado inmunológico del individuo y de la evolución de la enfermedad. Afecta principalmente piel, sistema nervioso periférico, mucosa de vías respiratorias superiores y otras áreas, dependiendo de la forma clínica. Los bacilos producen lesiones cutáneas polimorfas anestésicas con gran tropismo a los nervios periféricos y afectación de estos, y ocasionan daño neurológico irreversible, que puede llevar a complicaciones como neuropatía periférica no traumática, alteraciones estéticas e incapacidades, lo que es estigmatizante para los pacientes por el rechazo social.1,2
Ciertamente, ha habido un mayor énfasis en el desarrollo de herramientas para una mejor detección de la infección y el diagnóstico precoz mediante la visualización de los bacilos y la biopsia cutánea; además, la enfermedad presenta resultados positivos en avances con la poliquimioterapia, con mejoría a medida que pasan los años.3,4
El espectro clínico patológico de la enfermedad de Hansen va desde un polo localizado paucibacilar denominado TT (Hansen tuberculoide), hasta un polo lepromatoso denominado LL. También existen las formas borderline (BT, BB, BL) y una forma indeterminada o de inicio (LI). Tradicionalmente se asocia a las formas paucibacilares de la enfermedad con una adecuada respuesta de inmunidad innata o celular frente a las bacterias (TH1), y a las formas multibacilares con una inadecuada respuesta celular que no limita la enfermedad, que origina estimulación de la respuesta TH2 o adquirida con formación de anticuerpos que no eliminan la micobacteria.3
Basados en esta premisa, las acciones de profilaxis de esta patología han sido dirigidas principalmente a la búsqueda de una vacuna o inmunoterapia que proteja frente a la enfermedad o module la forma clínica hacia una forma paucibacilar.4
Se ha estudiado la utilización de la vacuna Bacilo Calmette-Guerin (BCG) frente a la enfermedad de Hansen; se evaluó la protección conferida tras la inmunización aseverando que estimula la inmunidad mediada por células frente a M. leprae.3,4Dadas las similitudes en la composición antigénica entre los patógenos M. tuberculosis (Mtb) y M. leprae, la vacuna BCG inicialmente fue utilizada como agente inmunoestimulador inespecífico y de inmunidad cruzada entre micobacterias. Existen antígenos de reacción cruzada entre M. leprae y la vacuna BCG que confieren factor de protección contra el Hansen, por aumento de la respuesta TH1 celular con liberación de factor de necrosis tumoral.5,6
Los efectos de la vacuna BCG sobre la aparición y las manifestaciones clínicas de Hansen dependen de la respuesta inmune inducida por BCG en el contexto de la capacidad inmune individual con respecto a M. leprae y la respuesta a la vacuna BCG.6
En el ensayo Karimui de vacunación con BCG contra el Hansen se evaluó el efecto de la vacuna sobre la incidencia y forma clínica de Hansen. Sus resultados pueden reflejar los efectos de la vacuna BCG en el Hansen, además de la prevención de la infección, y pueden incluir cambios en la historia natural de la infección por M. leprae en sujetos infectados antes y después de la vacunación con BCG.7
Convit, en 1992, realizó un estudio en una población que recibió la vacuna BCG. Planteó repetidas pruebas de contacto con lepromina (inyección directa de aproximadamente 10 millones de bacilos leprosos muertos) y vacunas repetidas con BCG en aquellos que dieron negativos. Sus hallazgos mostraron que el riesgo de contraer el Hansen era más bajo en los contactos con dos o más cicatrices de la vacuna BCG. Concluyó que confiere alto grado de protección frente a la enfermedad de Hansen.4
En 1993, Convit evaluó la presencia de cicatrices de la vacuna BCG y la respuesta a la lepromina. Una o más cicatrices se asociaron con una eficacia protectora del 56%. Hubo una tendencia de protección con cuatro o más cicatrices de la vacuna BCG, pero esto no fue estadísticamente significativo. No hubo pruebas de que la eficacia de la vacuna variara con la edad o según si el contacto vivía o no en el mismo hogar. El efecto protector fue significativamente mayor entre los hombres y para el Hansen multibacilar.5
Debido a la imposibilidad de cultivar el Mycobacterium leprae in vitro y a los resultados de la inmunoterapia contra la enfermedad de Hansen en distintas poblaciones, no se ha podido recomendar una práctica consensual de inmunoprofilaxis para la enfermedad. En efecto, el diagnóstico precoz y el tratamiento de los contactos con la inmunización con BCG en zonas endémicas siguen siendo estrategias importantes adoptadas en Brasil, pero el uso de la vacuna no se ha ampliado en todas las poblaciones.6
Kleinnijenhuis y cols., en el 2014, publican los efectos de la vacunación con BCG en respuestas HeterologoTH1/ TH17 e inmunidad innata entrenada de larga duración. Demostraron que la vacunación con BCG en voluntarios sanos induce la reprogramación epigenética de monocitos, lo que lleva a una producción incrementada de citocinas en respuesta a patógenos no relacionados hasta 3 meses después de la vacunación. Este fenómeno fue llamado “inmunidad entrenada”. Evaluaron si la BCG fue capaz de inducir efectos de larga duración tanto en la inmunidad entrenada como en la respuesta inmunitaria heteróloga T helper 1 (TH1) y TH17 un año después de la vacunación. En resumen, la BCG indujo cambios en el sistema inmune asociados con una respuesta inespecífica a las infecciones de inmunidad entrenada innata como a las respuestas heterólogas TH1 / TH17.8
Gillis, en el mismo año, investigó la inmunidad inducida por la vacuna rBCG30 y protección cruzada contra M. leprae. Demostró que ambas aumentan al potenciar el antígeno 85B de M. tuberculosis 30-Kilodalton.9
Se evaluó la vacuna rBCG30 demostrada para inducir protección superior a la de BCG contra M. tuberculosis y M. bovis en modelos animales. La vacuna rBCG30 sobreexpresa el antígeno 85B de proteína secretora mayor de M. tuberculosis, que es homólogo en un 85% con el de M. leprae (r30ML). Los ratones se inmunizaron por vía intradérmica con BCG o rBCG30 y se estimularon 2,5 meses más tarde mediante la inyección de M. leprae viables. Tanto la vacuna BCG como rBCG30 indujeron una protección significativa contra el desafío de M. leprae; rBCG30 indujo significativamente mayor protección que la vacuna de BCG. Además, indujo protección mejorada contra M. tuberculosis y una protección cruzada contra M. leprae comparable o potencialmente superior a la inducida por BCG, y la potenciación de rBCG30 con antígeno 85B potenció aún más la respuesta inmunitaria y la eficacia protectora.9
Más tarde, en 2017, Marques evaluó el impacto de la respuesta inmune frente a M. leprae en pacientes con Hansen multibacilar (MB). Se detectaron células T CD4 + que reconocen epítopos específicos de M. leprae. Este resultado refuerza la hipótesis de que la exposición continua de pacientes MB a M. leprae in vivo reguló la respuesta inmune celular específica contra el patógeno. Además, sugiere que la vacunación con BCG del paciente MB induce la activación de clones de células T, probablemente a través de "inmunidad entrenada". Reconoce antígenos específicos de M. leprae no compartidos con BCG como mecanismo de protección adicional, además del refuerzo esperado en la inmunidad mediada por células por homólogos de la BCG de antígenos de M. leprae. 10
Debido a los resultados controvertidos de la literatura con respecto al papel de la vacuna BCG como profilaxis o inmunomodulador en Hansen, nos propusimos realizar este trabajo para determinar si hay correlación del tamaño de la cicatriz de la vacuna BCG ubicada en la región deltoidea del brazo derecho y la severidad o forma de presentación clínica de la enfermedad de Hansen.
Objetivo general
Determinar la relación del tamaño de la cicatriz de la vacuna BCG y la severidad clínica de los pacientes con enfermedad de Hansen en el servicio de Dermatología del Instituto de Biomedicina Dr. Jacinto Convit del Hospital Vargas de Caracas, Venezuela.
Objetivos específicos
Establecer el tamaño de la cicatriz de la vacuna BCG en pacientes con diagnóstico de enfermedad de Hansen
Identificar la forma clínica de Hansen en los pacientes y su relación con el tamaño de la cicatriz de la vacuna BCG
Categorizar la severidad de la enfermedad de Hansen en los pacientes bajo estudio y su relación con el tamaño de la cicatriz de la BCG
Materiales y Métodos
Tipo de estudio:
Se realizó un estudio descriptivo transversal en pacientes con diagnóstico de enfermedad de Hansen en la consulta externa del Servicio Central de Hansen, Instituto de Biomedicina Dr. Jacinto Convit.
Población:
Pacientes con Enfermedad de Hansen multibacilar diagnosticados en el Instituto de Biomedicina Dr. Jacinto Convit entre el año 2008 y 2018.
Muestra:
150 pacientes. Dicha muestra demostró ser significativa ya que correspondió al 39% de los nuevos diagnósticos realizados en dicho período en la Institución.
Criterios de inclusión
Pacientes con diagnóstico clínico, bacteriológico y por biopsia de enfermedad de Hansen
Pacientes con antecedentes de vacunación con BCG en la infancia, previamente al diagnóstico de Hansen
Pacientes con registro en la historia clínica del tamaño de la cicatriz de BCG
Criterios de exclusión
Pacientes oncológicos
Pacientes con sepsis
Pacientes con tuberculosis
Pacientes inmunosuprimidos
Pacientes con cicatriz de viruela
Pacientes en tto. con inmunoterapia
Pacientes sin antecedente de vacunación por BCG
Historias de pacientes que no registraban el tamaño de la cicatriz de la vacuna BCG
Métodos
Se procedió a realizar la revisión de las historias clínicas de los pacientes con diagnóstico de Hansen en el Instituto de Biomedicina entre el año 2008 y 2018. De manera aleatoria, fueron seleccionadas 150 historias que cumplían con los criterios de inclusión antes mencionados. En dichas historias se investigaron las siguientes variables:
Operacionalización de las variables
Variables cuantitativas: edad (años), tamaño de la cicatriz (mm), duración del tratamiento (meses).
Variables cualitativas: sexo (masculino, femenino), Presencia de cicatriz de BCG (sí, no), forma clínica de Hansen (LI, TT, BT, BB, BL, LL), tratamiento (sí, no), fenómeno reaccional (reversión, Eritema nodoso, eritema polimorfo).
Se procedió además a realizar el cálculo de la severidad de la enfermedad, mediante escala elaborada por los investigadores, siguiendo los siguientes parámetros: escala del 1 al 8 según el grado de severidad, siendo el 1 la más leve y el 8, la más severa.
Formula de severidad:
Forma clínica de la enfermedad
LI 1 punto
TT 2 puntos
BT 3 puntos
BB 4 puntos
BL 5 puntos
LL 6 puntos
Se adicionó un punto a los pacientes que requirieron más de 1 año de tratamiento (+1pto), así como a aquellos pacientes que presentaron fenómenos reaccionales (+1pto), por considerarse formas más severas de la enfermedad.
Estos datos fueron registrados a través de un instrumento de recolección de datos en formato Excel y se procedió a la elaboración de tablas descriptivas y de correlación, calculando promedios, rangos y porcentajes. Como prueba estadística se empleó el chi cuadrado.
Resultados

Tabla III: Distribución de la muestra por tamaño de la cicatriz de BCG. Instituto de Biomedicina Dr. Jacinto Convit

Tabla IV: Distribución de la muestra por forma clínica de la Enfermedad de Hansen. Instituto de Biomedicina Dr. Jacinto Convit

Tabla V: Distribución de la muestra por duración del tratamiento. Instituto de Biomedicina Dr. Jacinto Convit

Tabla VI: Distribución de la muestra por severidad de la enfermedad. Instituto de Biomedicina Dr. Jacinto Convit

Tabla VII: Relación del tamaño de la cicatriz con la forma clínica de la enfermedad. Instituto de Biomedicina Dr. Jacinto Convit
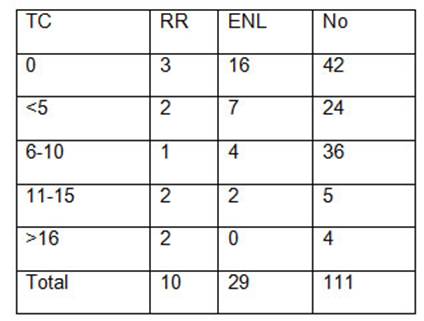
Tabla VIII: Relación del tamaño de la cicatriz con la presencia de fenómenos reaccionales. Instituto de Biomedicina Dr. Jacinto Convit

Tabla IX: Relación del tamaño de la cicatriz con la severidad de la enfermedad. Instituto de Biomedicina Dr. Jacinto Convit
Además, se evidenció que en cuanto a fenómenos reaccionales el 26% correspondieron a reversión y el 74%, a eritema nodoso.
Discusión
La enfermedad de Hansen es una enfermedad granulomatosa crónica infectocontagiosa, causada por Mycobacterium leprae y lepromatosis. El período de incubación de la enfermedad puede ser de cinco años o más y la aparición de la sintomatología puede tardar hasta 20 años. Afecta principalmente los nervios periféricos, la piel y mucosas. Puede atacar otros órganos internos y las manifestaciones clínicas e histológicas son muy variables, dependiendo de la inmunidad celular o innata del individuo frente a M. leprae.11,12
Los datos reportados por la OMS para el 2015 a nivel mundial, de 138 países, fueron de 176.176 casos, con una incidencia de 211.973. Brasil, India e Indonesia fueron los países que reportaron aproximadamente el 81% del total de los casos. En Venezuela, los primeros casos reportados de la enfermedad datan del año 1627; a partir de entonces nuevos casos fueron señalados en los estados Sucre, Yaracuy, Zulia, Mérida y Trujillo. Actualmente, hay enfermedad de Hansen en todo el país, con mayor prevalencia en los estados Guárico y Apure.13,14
La muestra estuvo representada principalmente por población joven (edad promedio 23 años), del género masculino (un 60%) y la forma de presentación de la enfermedad más frecuente fue la multibacilar (88%). Estos datos de la muestra se ajustan a la epidemiología mundial de la enfermedad. En cuanto a la presentación clínica, el 33% de los pacientes eran LL y solo el 2%, TT. En la enfermedad de Hansen se reporta un déficit en la inmunidad innata específica frente al bacilo, lo cual se refleja, desde el punto de vista epidemiológico, en formas de presentación a predominio multibacilar y en especial, LL y BL.12
Además, el 41% de la muestra no presentaba cicatriz de BCG, a pesar de haber recibido la vacuna. La BCG es una vacuna que busca estimular la respuesta inmune frente al Mycobacterium tuberculoso mediante un inóculo conformado por M bovis. Se ha propuesto que puede conferir inmunidad cruzada frente a otras micobacterias, entre ellas la M leprae. 15
La ausencia de cicatriz de la vacuna BCG en un porcentaje importante de la población multibacilar puede estar asociada a un déficit en el sistema inmune para el reconocimiento y eliminación de la micobacteria (por esto, después de la vacuna no se forma la cicatriz). Este factor además se ha asociado a mayor riesgo de contraer la enfermedad; por ello, se propone la revacunación con BCG en poblaciones endémicas, en especial en aquellas personas sin cicatriz de BCG. Convit propuso la vacunación consecutiva con BCG, la cual se asociaba con menor riesgo de contraer la enfermedad o padecer formas menos severas .4,16
En este estudio, un 29% de los pacientes ameritaron más de un año de tratamiento para ser dados de alta. Dicho fenómeno ocurre y ya ha sido reportado por nosotros, debido a la persistencia de bacterias sólidas en biopsias tras un año de tratamiento. En estos pacientes se requirió más de 1 año de poliquimioterapia para eliminar los bacilos sólidos de biopsias y linfas para considerarse libres de la enfermedad. El fenómeno de persistencia bacteriana no ha sido considerado en estudios previos como un factor asociado a mayor severidad de la enfermedad.
En ese mismo sentido, al elaborar una escala de severidad en pacientes con Hansen intentamos considerar este fenómeno, así como la presencia de reacciones, como un agravante en el curso de la enfermedad. Teniendo en cuenta que el 26% de los pacientes presentaron fenómenos reaccionales de reversión y el 74%, eritema nodoso, los valores se corresponden con los reportados previamente para la enfermedad.
Es evidente, entonces, al aplicar la escala de severidad a nuestros pacientes, que el 42% tenía una severidad moderada, y solo un 24,7%, una afectación severa producto de la enfermedad. A pesar de que la mayoría de los pacientes eran multibacilares, BB, BL y LL, sólo un pequeño número coincidió con persistencia bacteriana y fenómenos reaccionales al momento de realizar la valoración.
Dadas las consideraciones anteriores, cuando correlacionamos el tamaño de la cicatriz de la vacuna BCG con la forma de presentación de la enfermedad, hemos evidenciado diferencias estadísticamente significativas que demuestran que los pacientes con LL tienden a tener ausencia de cicatriz, a diferencia de los pacientes BT y LI que tienen un tamaño mayor de la cicatriz (más de 6 mm). Al analizar el gráfico, observamos una tendencia a menor tamaño de la cicatriz de la vacuna BCG en formas más multibacilares de la enfermedad, coincidiendo ello con un mayor tamaño de la cicatriz en formas paucibacilares BT y LI.
En efecto, se demuestra el factor de protección de la vacuna BCG frente a formas severas de la enfermedad. Dicho fenómeno puede explicarse con dos hipótesis: una estimulación de respuesta inmune innata tras el uso de BCG que confiere inmunidad cruzada frente a micobacterias o un aumento de la inmunidad innata, previo a la vacuna, en pacientes que responden adecuadamente a BCG, lo cual se extrapola a una mejor respuesta inmune frente a micobacterias en general.
También observamos, con valores estadísticamente significativos, un mayor porcentaje de fenómenos reaccionales tipo II (ENL) en pacientes con ausencia de cicatriz de BCG, demostrando que en ellos existe un predominio de la respuesta TH2 sobre la TH1, interfiriendo en la forma como reaccionan frente a la enfermedad.
A pesar de que existe tendencia a presentar formas menos severas de Hansen en pacientes con mayor tamaño de cicatriz de la vacuna BCG, dichos resultados no fueron estadísticamente significativos. Este hecho se corresponde con las investigaciones de Convit, quien concluyó que, a pesar de que la vacuna BCG muestra una tendencia protectora frente a la enfermedad, no se pudo demostrar una asociación estadísticamente significativa.
En el presente estudio, proponemos fortalecer la evidencia de que la vacunación con BCG y la revacunación hasta obtener una cicatriz de la vacuna BCG positiva pueden constituir un factor protector frente a la enfermedad de Hansen y que debe ser recomendado como práctica en poblaciones endémicas.
Conclusión
En el presente estudio, proponemos las siguientes conclusiones:
Existe una relación inversa entre el tamaño de la cicatriz de la vacuna BCG y la severidad de la enfermedad de Hansen
La utilización de la vacuna de BCG produce una respuesta TH1, que puede proteger de manera inespecífica frente a formas multibacilares de Hansen
Los fenómenos de reversión se asocian a mayor tamaño de la cicatriz, así como el eritema nodoso leproso a su ausencia
La vacunación y revacunación con la vacuna BCG puede conferir protección frente a la enfermedad de Hansen, evitando las formas clínicas más severas, por lo que debería ser recomendada en la práctica médica diaria.
Agradecimiento
A los profesores por su apoyo incondicional, personas que nos han transmitido sus conocimientos y dedicación para un mejor crecimiento profesional.


















