Introducción
La cantidad de trasplantes pulmonares ha ido en aumento en el mundo, observándose en los últimos años una estabilización. Dicho aumento se ha producido a expensas de los trasplantes bilaterales que son mayoritarios, siendo los unilaterales proporcionalmente menores año tras año. Europa ha reducido la cantidad de trasplantes en forma relativa con aumentos proporcionales de los trasplantes realizados en América del Norte pero sobre todo en otras localizaciones1.
En Argentina, la cantidad de trasplantes ha variado anualmente en los últimos 10 años (2010-2019), con un promedio de 37 trasplantes anuales (Figura 1). El 87% de los mismos son realizados en 2 centros.
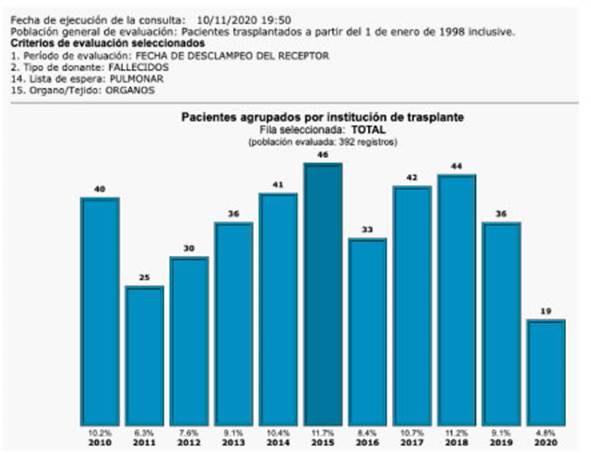
Fig. 1 Variación anual de trasplantes pulmonares en Argentina. Datos Sintra http://sintra.incucai.gov.ar/ Nótese la caída de los trasplantes durante el 2020, coincidente con la pandemia Covid 19.
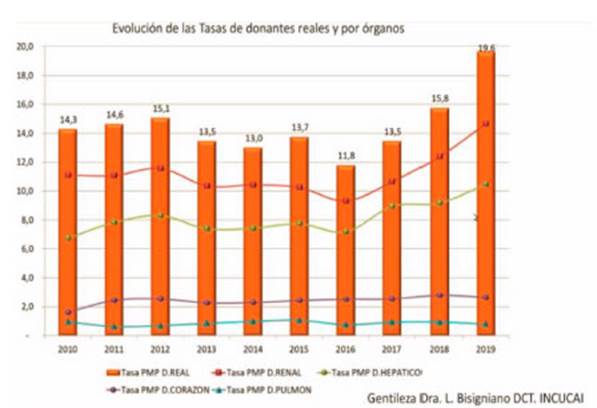
Existe una menor tasa de utilización de órganos para pulmón y corazón respecto a hígado y riñón que se ha elevado en los últimos años. Ésta está cerca del 1 por millón (específica por órgano pulmón), para una tasa de 19,6 por millón en 2019 para el resto de los órganos (Figura 2).
En el resto del mundo la tasa de conversión de donantes en general a donantes de pulmón es va riable: con máximos cercanos al 60% en países como Austria y Canadá, y mínimos del 17% en países como España y Reino Unido2. En EE.UU la tasa es del 18,5% para pulmón, mientras que es del 67% para riñón3. En Argentina, ha aumentado del 6,2% en el período 2011-2015, al 10,6% entre 2016-20184 coincidiendo este aumento con la visibilización mediática y judicial que hubo en el país con la modifi cación de la ley de trasplante5.
La disparidad descrita hace años entre los ingresos en lista de espera y la cantidad de trasplantes efectuados genera un aumento de muertes en lista de espera6. En los registros del Sintra, desde 2010 hasta 11/2020, 407 pacientes de la lista pulmonar y 44 de la cardio-pulmonar fueron excluidos por fa llecimiento. En el mismo período, 281 pacientes fueron incluidos en la lista pulmonar mientras que 4 en la cardiopulmonar. Solamente 402 pacientes fueron trasplantados en el mismo período*.
Los problemas planteados son: la escasez de donantes pulmonares, el aumento de los pacientes en lista de espera y el aumento de las muertes en lista de espera. Existen varias estrategias para resolver estos problemas. Trataremos de dividirlas en grupos temáticos para hacer más fácil su comprensión.
Estrategias
Existen estrategias enfocadas en la promoción del trasplante pulmonar. Básicamente apuntan a con cientizar a la población del problema y tienen como objetivo aumentar la donación global de órganos. Se requiere de la propaganda estatal a través de programas específicos. Países como España han logrado tasas de 34 donantes por millón de habitantes (DPMH)7. En el ámbito local, provincias como Corrientes han logrado tasas elevadas de 25 DPMH en 20158.
En 2005 en Argentina, a través de la ley 26.066, se estableció la figura del Donante Presunto9. Años después, en el 2018 a través de la Ley 27.4475, se consolidó la confirmación de dicha figura, con un aumento generalizado de las tasas de donación, probablemente causadas por la visibilidad que tuvo la problemática de la donación de órganos durante el tratamiento de dicha ley. En forma indirecta, esto genera un aumento de la donación global, afectando positivamente a los donantes pulmonares. Este tipo de estrategias deben ser transversales y continuas en el tiempo para lograr efectos positivos.
Las estrategias basadas en la procuración tienen como fundamento la optimización de los poten ciales donantes de modo que puedan ser elegibles por los grupos de trasplante. Todas apelan a una estrategia ventilatoria protectora y requieren de un adecuado manejo del donante como un paciente crítico10. Los aspectos de mejora están dados en el cuidado desde el aspecto kinésico respiratorio. Su objetivo es la mejoría de las presiones parciales de oxígeno (PaFiO2) ofrecidas. El promedio de aceptación para el período 2009-2013 fue de 430 mmHg8. Es de destacar que a pesar de las múltiples publicaciones internacionales que ponen el límite de aceptabilidad más bajo11-19, en Argentina los niveles de exigencia de los grupos son más altos.
La mejora se ve favorecida por el uso de guías de manejo clínico. El INCUCAI ha logrado el consenso y difusión de las mismas. No obstante, en una encuesta anónima de 39-items publicada recientemente20, dirigida a los profesionales registrados en la Sociedad Argentina de Terapia Intensiva, se observaron algunos inconvenientes. El porcentaje de respuesta fue bajo: 736 respuestas (cercano al 10%); 61% médicos; 21% enfermeros y 18% kinesiólogos. Llama la atención que sólo un 71% de los respondedores reconocieron a un potencial donante. Pero alarma aún más que sólo el 18% tenía un protocolo de man tenimiento de los donantes en su centro de atención.
La experiencia en este aspecto es prometedora. En un trabajo recientemente publicado de un protocolo realizado en el ámbito de la Ciudad de Buenos Aires, entre 4/2017 y 3/2018, kinesiólogos respiratorios estuvieron a cargo de la optimización de los donantes21. Los potenciales donantes incluidos tenían entre 18 y 65 años, eran donantes ideales de pulmón o con no más de un criterio marginal; se excluía a pacientes con alteraciones radiográficas, secreciones purulentas o evidencias de broncoaspiración y antecedentes de paro cardio respiratorio. Se instauró un protocolo de ventilación mecánica y cuidados respiratorios, con la presencia de un kinesiólogo respiratorio en el lugar, sistema cerrado de aspiración, aplicación de fisioterapia respiratoria. El test de apnea se efectuó con válvula de presión positiva al final de la espiración (PEEP) para evitar la pérdida de reclutamiento alveolar y se efectuaron maniobras de reclutamiento. Se logró un aumento de los pulmones procurados con la totalidad de aceptación de los mismos con valores estadísticamente significativos.
Las estrategias basadas en la distribución de los donantes tienen su origen en el Lung Allocation Score (LAS) de EE.UU del año 2005 corregida en 2010. Son estrategias enfocadas en la optimización del uso de los órganos ya procurados. Así se busca lograr cambios en la distribución de dichos órganos a favor de los pacientes con más riesgo a morir en lista de espera. Las consecuencias del uso de esta estrategia fueron la reducción de las muertes en lista de espera y la realización de más trasplantes22. En Argentina desde el año 2010, se comenzó a priorizar la distribución de los donantes en base a la mor talidad del receptor, tanto por la situación clínica (requerimiento de ARM, ECMO o VNI, o utilización de drogas vasoactivas, entre otras) como la mortalidad aumentada inherente a su diagnóstico (fibrosis pulmonar idiopática o quística)23. La realización de trasplantes uni-pulmonares también genera un impacto al duplicar el donante a favor de dos receptores. La detección de anomalías unilaterales puede evitar perder todo el bloque pulmonar, utilizando pulmones, por ejemplo, con neumonías contralatera les o traumas; aunque esta estrategia implica mayor riesgo para el receptor y no siempre es posible de utilizar en todas las patologías (como ser bronquiectasias, fibrosis quística pulmonar, etc.)24.
El siguiente escalón de mejora abarca a la selección de los donantes. Los equipos de trasplante son los que finalmente toman las decisiones en este punto. Los criterios ideales de selección de los donantes pulmonares fueron descritos hace más de 20 años25. Sin embargo, incluso antes de su establecimiento, se comenzaron a describir experiencias de grupos que comenzaron a utilizar donantes subóptimos con el objetivo de aumentar la cantidad de donantes26. En forma paralela, los grupos comenzaron a describir aumentos en las tasa de disfunción primaria de injerto (DPI). En el caso particular de los trasplantes bilaterales, la consecuencia directa es el aumento en mortalidad temprana aunque por otro lado, ob servaron que la funcionalidad a mediano plazo no se veía afectada27.
Los criterios a flexibilizar en la selección pueden ser discordantes en relación a las consecuencias. En el caso de la edad, algunos trabajos no muestran diferencias28. Otros mostraron aumento de las tasas de síndrome de bronquiolitis obliterante, disminución de la supervivencia global, aumento de la frecuencia de DPI y hasta consecuencias no tan directas ni correctamente evaluadas como mayor susceptibilidad a desarrollar cáncer de pulmón en los receptores, presencia de enfisema subclínico con reducción en la función pulmonar y menor reserva funcional. Contrariamente algunos grupos describieron disminución de la frecuencia de DPI justificándose por una menor inmunogenicidad de los órganos más añosos29-31.
Cuando observamos los registros de trasplante pulmonar de la ISHLT, vemos que en los últimos años los grupos redujeron la edad promedio de sus donantes con una media de 36 años al 2019.(1) El análisis multivariable arroja que por encima de los 55 años existe correlación estadísticamente significativa de aumento de la mortalidad a 10 años de los receptores. Al discriminar las regiones del trasplante, observamos que en América del Sur, las edades de los donantes son más bajas. Mientras que el 58,3% de los donantes en el mundo pertenecen al grupo etario 18-49 años, ese porcentaje aumenta al 84,4% para los donantes en la región de Sudamérica es decir los donantes son más jóvenes en la región32.
La evaluación de la radiografía de tórax del potencial donante implica variabilidad interobservador. Afortunadamente en Argentina cada vez más centros disponen de radiografía digital, permitiendo el envío de imágenes, evitando interpretaciones inadecuadas. Puede evaluarse la presencia de edema bilateral, contusiones, atelectasias y demás alteraciones. Muchos grupos informaron la presencia de radiografías patológicas en la selección de sus donantes (23-61%)33. Finalmente, la radiografía de tórax parece ser más que un factor de descarte, una variable a corregir.
La gasometría es quizás la variable más importante en la toma de decisiones. Asimismo, es la que tiene mayor posibilidad de cambio. Muchos trabajos referían hace tiempo, que el límite de 300 mmHg parecía ser muy estricto11-19. A pesar de esto advirtieron precozmente el aumento en la mortalidad tem prana y los casos de DPI. Hay que considerar que la gasometría no distingue lateralidad de la patología. Es por eso que algunos grupos utilizan la medición intraoperatoria de la misma. Ante una gasometría no adecuada el equipo de trasplante debe enfocarse en la optimización del donante, a través de una comunicación fluida con procurador. Un adecuado control hemodinámico, a través del uso correcto de drogas y un eficiente manejo hídrico con medición de diuresis y presión venosa central, sumado a trabajos kinésicos respiratorios que incluyen la adecuada ventilación y reclutamiento alveolar, pueden lograr mejoras en los valores de gasometría. En la práctica, esta variable es la más exigente dentro de los grupos de trasplante local. En Argentina, los donantes utilizados en el periodo 2009-13 registraron una PaFiO2 promedio de 430 mmHg3 según datos de INCUCAI. En el mismo periodo en nuestro cen tro, registramos una PaFiO2 de 505 mmHg (valor corregido y optimizado) para los órganos aceptados e implantados8.
El tabaquismo es una variable, muchas veces, difícil de obtener en nuestro medio. El límite establecido es de 20 pack/year. No pareciera haber diferencias clínicas en cuanto a la evolución de los pacientes34.
Una variable a considerar desde el punto de vista local es el tiempo de isquemia, siendo aceptable con tiempos menores a las 6 horas34. La falta de logística nacional con ciudades con inadecuada comu nicación terrestre, aeropuertos cerrados en horarios nocturnos y la falta de transporte aéreo a través de helicóptero (ideal para distancias menores a los 400 km.), hacen que sea una variable de peso para todos los grupos de trasplante.
Se ha tratado de objetivar a través de puntaje la presencia de criterios de elegibilidad35. Sin embargo, esto es difícil convirtiéndose estas experiencias en no reproducibles por distintos grupos. Se requiere de una selección artesanal en donde el objetivo sea no sumar factores de riesgo, evaluando al donante en relación al receptor.
Finalizando, existen estrategias que llamaremos de nuevas tecnologías. Incluyen múltiples inter venciones descritas en la literatura mundial que pueden tener inconvenientes operativos al momento de extrapolarlas a la práctica local. Hace más de 15 años se reportó el primer trasplante pulmonar con un donante inicialmente descartado pero reacondicionado a través de la perfusión normotérmica ex-vivo de la solución de Steen (EVLP, ex-vivo lung perfusion)36. En dicho reporte, se informa el aumento de una PaFiO2 inicial de 97 mmHG a una final de 390, haciéndolo apto para el implante. Años después comienzan a publicarse los resultados con grupo control de los trasplantes de órganos acondicionados37. Este trabajo compara 20 pacientes trasplantados con órganos sometidos a EVLP contra 116 trasplantes en el grupo control. Los aumentos de las PaFiO2 reportados fueron de 335 mm Hg a 414 y 443 mm Hg en 1 h y 4 h, respectivamente (P < 0.001). Llamativamente los investigadores observaron una reducción en la frecuencia de DPI sin significancia estadística (DPI 72 h. 15% EVLP vs. 30% control (P = 0.11)). Tampoco encontraron significancias estadísticas en mortalidad a 30 días, complicaciones bronquiales, duración de la ventilación mecánica y estancia en terapia intensiva (UTI) y hospitalaria.
Luego de años de su uso en el mundo, vemos que es una estrategia que logra un aumento del 20% aproximadamente en la cantidad de trasplantes realizados en el grupo donde se implementa, requi riendo mucha logística y habitualmente una participación público-privada por los elevados costos que acarrea (costo incremental de USD 45.000 en EEUU)38. La costo efectividad de la práctica fue evaluada en países con sistema público de salud como el Reino Unido, observando un aumento en años de vida estimado en 0,040, a su vez que un aumento en los años de vida ajustados por calidad (QALY) de 0,045. No obstante el costo incremental por QALY ganado fue estimado en £90.00039. Teniendo en cuenta esos costos y el bajo PBI per cápita de nuestro país, esta tecnología parece superar la capacidad de pago para nuestro país. En resumen, es una herramienta útil como estrategia final habiendo realizado previamente intervenciones con mayor costo-efectividad.
Otra nueva estrategia es la del uso de donantes en asistolia. Presenta sus inicios en España en el año 200240, terminando a finales de 2009 con 29 trasplantes. Los resultados publicados fueron aceptables en cuanto a supervivencia a mediano y a largo plazo e incidencia de síndrome de bronquiolitis obliterante (SBO), aunque reportaron altos índices de falla primaria de órgano y mortalidad temprana (30d:17%)41.
Un metaanálisis evalúa 6 trabajos importantes publicados del tema42. Allí no se observa aumento significativo de la mortalidad al año, ni diferencias en cuanto a DPI y rechazo agudo celular. En otros 2 estudios que utilizaron donantes en asistolia no controlados se observó tasas relativamente elevadas de DPI, SBO y mortalidad alejada. La conclusión del metaanálisis es que el uso de donante en asistolia tendría un potencial de impacto favorable en la reducción de las listas de espera. El uso de estos donantes es discordante con frecuencias que varían entre 25-40% para grupos de Londres, Australia y Países Bajos, respectivamente. No obstante, las cifras para EE.UU no superan el 2%42. Existe, sin embargo, consenso en que los donantes deben ser controlados. Un ensayo utilizó pulmones recuperados de donan tes no controlados: a todos se le efectuaba tomografía computada (TC), realizando luego recuperación a través de EVLP. Luego de 29 meses y 502 potenciales donantes menores a 66 años, ningún pulmón pudo ser trasplantado debiendo finalizarse el protocolo43. De modo que si bien la estrategia de donantes en asistolia en interesante hay que tener cuidado con las extrapolaciones a nuestro medio. Se requiere de un sólido sistema prehospitalario, con tiempos de atención menores a 8 minutos, muy difícil de apli car en la mayoría de nuestras jurisdicciones. Los tiempos de isquemia total deben ser menores a 300 minutos y los tiempos de isquemia caliente (tiempo entre la interrupción de la circulación del órgano donado hasta la perfusión con la solución hipotérmica de preservación) entre 30 y 120 minutos. Estos valores presentados en la mayoría de las experiencias son igualmente difíciles de conseguir en nuestro medio. Secundariamente, el uso de sistemas de circulación extracorpórea en los centros donde ocurre la procuración es de difícil implementación en el país. Asimismo, actualmente EVLP no está disponible para su uso clínico en Argentina.
No hay dudas de que los resultados muestran que no hay diferencias entre los grupos; parece fac tible y seguro; aunque debe realizarse siempre con donantes en paro cardíaco controlados. En nuestra opinión creemos que otras intervenciones son más necesarias en nuestro contexto.
Conclusión
Todas las estrategias son útiles en diferentes niveles. A saber:
Las estrategias de promoción son necesarias, continuas y transversales a todo el proceso, no exclusivo al pulmón. Las de procuración son necesarias, implican una mejora continua en la calidad de atención médica en general, con una valoración adecuada del RRHH participante. Impresiona ser muy costo-efectiva en nuestro contexto. Las de distribución ya se emplean, deben ser constantemente evaluadas para ajustar cambios y han generado mejoras en el acceso al trasplante. Finalmente, las de selección involucran mejoras a expensas de mayores costos a veces con consecuencias negativas, por lo que deben ser evaluadas caso a caso.
Existen finalmente las estrategias consideradas en esta publicación como de alto costo, que son la EVLP y el uso de los donantes en asistolia. El uso de EVLP es efectivo, aunque no impresiona ser una intervención costo-efectiva en nuestro medio debiendo emplearse otras estrategias previamente. La utilización de donantes a corazón parado (NHBD) es efectiva aunque requiere de una inversión en un sistema logístico que no parece ser viable por el momento en Argentina