Introducción
Los problemas vinculados al exceso de peso constituyen uno de los principales desafíos para la salud pública del siglo XXI. La Organización Mundial de la Salud (OMS) calcula un billón de personas alre dedor del mundo padece sobrepeso y la prevalencia de obesidad en países occidentales supera el 20%, con una inquietante tendencia incremental1.
La obesidad en adultos es uno de los factores determinantes que explican el crecimiento de la morbilidad y mortalidad cardiovascular y se estima que causa más de 4 millones de muertes al año en el mundo2.
La última Encuesta Nacional de Factores de Riesgo (ENFR) del 2019 muestra un alarmante aumento sostenido respecto sus ediciones anteriores, registrando un 33,7% de sobrepeso y un 32.4% de obesi dad en la población adulta de Argentina2,3. Por lo tanto, y según datos oficiales, más de la mitad de la población de Argentina (66,1%) tiene exceso de peso en algún grado2.
La Segunda Encuesta Nacional de Nutrición y Salud (ENNyS-2) obtuvo valores de sobrepeso en la población adulta del 34% con mayor prevalencia de sobrepeso en los varones (37,5%) con respecto a las mujeres (31,1%). Además, expuso que el grupo de menor nivel educativo tuvo una prevalencia de obesidad 1,4 veces mayor que el segmento educativo más alto (39,8% vs 28,3%)4.
Obesidad y función pulmonar
En la obesidad, las propiedades mecánicas de los pulmones y la pared torácica se alteran por los depósitos de grasa en el mediastino y en la cavidad abdominal, que resultan en una disminución de la distensi bilidad toracopulmonar. Las presiones intraabdominal y pleural aumentan, por lo cual el movimiento hacia abajo del diafragma y el retroceso de la pared torácica hacia afuera se restringen alterando el patrón respiratorio y condicionando una reducción del volumen de reserva espiratorio (VRE) y la capa cidad residual funcional (CRF). Los volúmenes pulmonares estáticos como la capacidad pulmonar total (CPT) y el volumen residual (VR), pueden encontrarse levemente disminuidos, al igual que medidas dinámicas de función pulmonar como el volumen espiratorio forzado en el primer segundo (VEF1) y la capacidad vital forzada (CVF). El volumen corriente también es menor en pacientes con obesidad, aunque el aumento de la frecuencia respiratoria compensa el patrón de respiración superficial. La distribución de la grasa a predominio abdominal (androide) es un factor de riesgo de disminución del VEF1 y CVF independiente del IMC5.
La reducción de los volúmenes pulmonares, el aumento del volumen sanguíneo pulmonar y colapso alveolar por cierre de la pequeña vía aérea contribuyen a la disminución de la distensibilidad pulmonar, que según las revisiones sería el principal causante de la diminución de la distensibilidad del aparato respiratorio en estos pacientes6,7.
Las presiones bucales máximas (presión inspiratoria [Pimax] y espiratoria máxima [Pemax]) son en general normales, pero pueden encontrarse disminuidas en la obesidad grave. Un comportamiento similar suele observarse en la resistencia de los músculos respiratorios, que se ve alterada en la obe sidad extrema8.
Como consecuencia de estas anomalías el trabajo ventilatorio se incrementa, de manera que en los pacientes con obesidad mórbida (índice de masa corporal [IMC] > 40 kg/m2) el consumo de oxígeno en reposo (VO2) puede alcanzar hasta el 16% de la VO2 total, mientras que no excede el 3-5% en no obesos9,10.
Por otra parte, en los pacientes con obesidad existen anomalías del control de la ventilación que fa vorecen la retención de dióxido de carbono (CO2) durante el sueño e inclusive durante la vigilia, como ocurre en la hipoventilación alveolar central de pacientes con obesidad8,10.
Otras dos entidades, la Enfermedad Pulmonar Obstructiva Crónica (EPOC) y las Apneas Obstructi vas del Sueño (AOS), frecuentemente presentes en obesos, pueden agravar la hipoventilación alveolar diurna y nocturna
Diferentes estudios han detectado la existencia de una asociación entre el índice de masa corporal (IMC) basal y el posterior desarrollo de asma, concluyendo que la obesidad es la principal comorbilidad asociada a esta enfermedad11,12.
La asociación de asma y obesidad son consideradas un fenotipo particular, con características clínicas, biológicas y funcionales propias13,14.
Al igual que la obesidad, la EPOC incrementa el trabajo ventilatorio, modifica la mecánica respi ratoria y disminuye la eficiencia de los músculos respiratorios. La coexistencia de ambas condiciones contribuye a la hipercapnia. Adicionalmente, la coexistencia de estas anormalidades con apneas del sueño ha sido denominada por algunos autores como: “triple O” (Obstructive, Obstruction, Obesity), con mayor riesgo de requerir soporte ventilatorio ante injurias variadas15.
Puntos clave
- La obesidad condiciona una disminución en la distensibilidad del sistema respiratorio, un descenso de volúmenes pulmonares, una afectación de la permeabilidad de la vía aérea superior y de la capa cidad de oxigenación y depuración de la CO2.
- La coexistencia de enfermedades pulmonares crónicas puede agravar las alteraciones vinculadas a la obesidad y viceversa.
Evaluación básica de la función pulmonar en el paciente con obesidad
La espirometría es una técnica sencilla, no invasiva y de bajo costo, que permite una aproximación rápida al conocimiento de la función pulmonar. Sus alteraciones se han correlacionado con complica ciones postoperatorias en casos de cirugía bariátrica (CB) y no bariátrica en pacientes con obesidad y comorbilidades16-18. Es la técnica básica que se recomienda en el paciente obeso para la evaluación del riesgo según la magnitud de la limitación funcional10, 19. Los pacientes evaluados para cirugía (aún asintomáticos), deben tener un estudio espirométrico aceptable y reproducible en los últimos 3 meses con una adecuada interpretación clínica20-22.
Cualquier alteración de las pruebas funcionales debe ser interpretada por un neumonólogo y recibir el tratamiento acorde al diagnóstico final (según la normativa vigente actualizada para la mejor prác tica clínica) antes de ser aceptado para cirugía, fundamentalmente en CB21, 23, 24. Todos los hallazgos y tratamientos instituidos deben ser adecuadamente consignados en la historia clínica.
Los volúmenes pulmonares y la difusión de monóxido de carbono (DLCO) no forman parte de la evaluación rutinaria de los candidatos a CB, aunque en casos seleccionados podrá recurrirse a este tipo de estudios según criterio del médico especialista cuando la espirometría no ofrezca información concluyente (tabaquistas, antecedentes de resección pulmonar, coexistencia con enfermedades ocupa cionales, EPOC con VEF1 < 50%, fibrosis pulmonar, compromiso funcional severo por otra causa, etc.).
En circunstancias específicas, dependiendo del criterio del médico especialista que evalúe el caso, puede ser necesario incluso adicionar otras pruebas tales como presiones bucales máximas, espirometría sentado-acostado o un test de ejercicio cardio-pulmonar con consumo de oxígeno.
La determinación de gases en sangre arterial (punción arterial y estado ácido-base) no forma parte de la rutina en la evaluación preoperatoria del paciente obeso. Sin embargo, se sugieren contemplar en las condiciones detalladas en la Tabla 1.
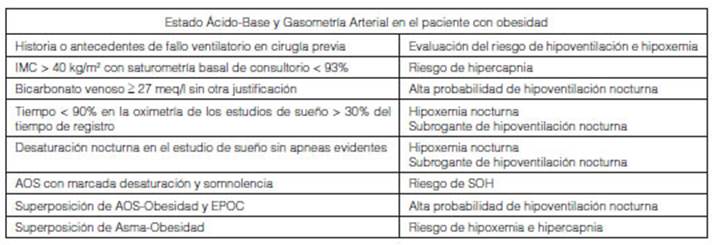
Tabla 1 Indicaciones para la realización de gases en sangre arterial en pacientes con obesidad durante la evaluación preoperatoria
La identificación de hipercapnia en vigilia constituye un indicador de la presencia del Síndrome de obesidad e hipoventilación (SOH); definido como la combinación de obesidad (IMC > 30 kg/m2) e hiper capnia diurna (PaCO2 > 45 mmHg) en ausencia de causas concurrentes10,25. Esta es una condición de alto riesgo que no representa una contraindicación absoluta para la CB per se, pero obliga a un manejo cuidadoso, considerando el soporte ventilatorio no invasivo en el perioperatorio ya que la mitad de los casos de SOH se diagnostican durante un episodio de fracaso ventilatorio26-28.
Las características clínicas que deberían hacer sospechar SOH son; la obesidad severa, disnea, nicturia, edema de las extremidades inferiores, somnolencia diurna excesiva, fatiga, ronquidos de alta intensidad, apneas presenciadas, así como una oximetría de pulso (SpO2) < 92% durante la vigilia y / o hipoxemia
significativa durante el sueño (SpO2 < 90%). Valores elevados de bicarbonato sérico (HCO3-) venoso hacen sospechar hipoventilación y SOH. Ante el hallazgo de ≥ 27 mmol/l se sugiere una determinación de gases arteriales para verificar el valor de PaCO225.
Puntos clave
- Es prudente que los pacientes con obesidad evaluados para procedimientos quirúrgicos con anestesia general realicen una espirometría aceptable y reproducible en los últimos 3 meses con una adecuada interpretación clínica.
- Toda alteración funcional debe recibir el tratamiento acorde con el diagnóstico etiológico, antes de cualquier cirugía electiva.
- Otras pruebas funcionales no se consideran de rutina, aunque son auxiliares del diagnóstico cuando los patrones espirométricos son anormales o existe sospecha clínica de enfermedades que comprometen la función pulmonar.
- La pesquisa de SOH se recomienda a través de la sospecha clínica y valores gasométricos.
Trastornos respiratorios del sueño en pacientes con obesidad
La AOS es un problema de salud pública por su elevada prevalencia y por el aumento de la morbi-mortalidad que ocasiona29,30. Su prevalencia en la población general oscila entre el 9% y el 38%31-33, situándose cerca del 28% en América Latina34, haciendo necesarias estrategias prácticas para casi un billón de afectados en el mundo35.
En población quirúrgica, la AOS es significativamente más prevalentes que en la población general y 6 de cada 10 pacientes candidatos a cirugía bariátrica tienen apneas del sueño definida por un IAH > 10 ev/h29,31,36,37.
Akram Khan y cols, en Pittsburgh, llevaron adelante el estudio LABS-2 (evaluación de adultos can didatos a cirugía bariátrica) y en 693 pacientes con polisomnografia (PSG) preoperatoria hallando una prevalencia de IAH > 5 ev/h del 80,7%38.
El diagnóstico de AOS se confirma convencionalmente mediante una PSG, aunque se acepta como válido el diagnóstico mediante una poligrafía respiratoria (PR) en poblaciones con probabilidad clínica moderada o alta32,39.
Casi la mitad de los pacientes con AOS en evaluación para CB reúnen criterios para tratamiento con presión positiva en las vías aéreas (CPAP)40-42 debido a la severidad del trastorno y a las comorbilidades con las que se asocia38.
Los pacientes con AOS tienen riesgo de complicaciones respiratorias y cardiovasculares en relación a cirugías que requieren anestesia general, sedación y/o analgesia, en forma directamente proporcional a la severidad por IAH y al grado de hipoxemia37,43,44. Los factores que pueden contribuir al aumento del riesgo operatorio en obesos se detallan en la Tabla 2. Dos metaanálisis y una revisión sistemática de 63 publicaciones basadas en 413 576 pacientes con AOS y 8 557 044 controles, confirmaron una mayor incidencia de desaturaciones de oxígeno en el postoperatorio, eventos cardíacos e insuficiencia respiratoria en presencia de apneas del sueño45. Estas complicaciones incluyen: hipoxia, hipercapnia, neumonía, atelectasias, broncoespasmo, dificultad respiratoria aguda, edema pulmonar y la necesidad de ventilación no invasiva y/o intubación45,46.

Tabla 2 Indicaciones para la realización de gases en sangre arterial en pacientes con obesidad durante la evaluación preoperatoria
En pacientes con elevada sospecha clínica de apneas del sueño y que deban ser sometidos a cirugías electivas, existen recomendaciones para la realización de un estudio de sueño que confirme el diagnóstico, determine el grado de severidad y la necesidad de tratamiento con CPAP u otras terapias específicas37,38. Si no fuese posible un estudio de sueño (cirugía no electiva) los pacientes con diagnóstico clínico presuntivo deben ser manejados con las mismas precauciones postoperatorias que los pacientes con AOS confirmado39,44.
Un aspecto relevante del problema es que, a pesar de conocerse esta asociación, frecuentemente numerosos pacientes candidatos en programas de cirugía bariátrica no son diagnosticados ni reciben tratamiento antes de la cirugía43,47,48.
Debido a la magnitud del problema, se han diseñado cuestionarios y modelos de predicción de AOS con la intención de priorizar los pacientes para una prueba de sueño que confirmará el diagnóstico39,49.
El cuestionario de Berlín49, ampliamente usado en la población general como método tamiz, supone alto riesgo con IMC > 30 kg/m2 y por ello muestra escasa utilidad práctica en CB, donde los candidatos tendrán riesgo elevado de padecer apneas del sueño (> 30% de probabilidad estadística de padecer un IAH > 10 ev/h por hora).
Las unidades que trabajan con pacientes candidatos a CB utilizan mediciones antropométricas. Las más estudiadas como factores de riesgo para AOS serían: el IMC, la circunferencia del cuello y el diámetro de cintura50. Borsini y Cols., en 81 pacientes candidatos a CB no hallaron correlación entre el índice de cintura-cadera (ICC) y diámetro sagital (DS) con la probabilidad de AOS, atribuible a la elevada prevalencia de IAH > 15 ev/h (55% de los obesos)51.
El cuestionario STOP-BANG (CSB) descripto por Chung, fue validado para el cribado de AOS en población quirúrgica. Consta de 8 preguntas, con una sensibilidad del 93 al 100% y una especificidad del 43%52,53. Borsini et al., estudiaron la utilidad de CSB con PR y demostraron que la mejor relación sensibilidad (S) y especificidad (E) para la identificación de AOS se obtuvo con tres componentes de STOP en cualquier combinación posible (S: 52,9%; E: 60.0%) o dos componentes de BANG (S: 79,0% - E: 43,7%). Cinco componentes CSB (cualquier combinación) alcanzaron sensibilidad de 60,7% y es pecificidad de 65%46,53, área bajo la curca ROC de 0,7654,55 permitiendo priorizar individuos de riesgo.
Sin embargo, la metodología empleada para el diagnóstico o el tipo de población pueden modificar la predicción del cuestionario, como lo han propuesto Silva56, usando PSG domiciliaria, quien comunico que el desempeño de CSB difiere del trabajo de validación original o Glazer notificando limitada eficacia de predicción de CSB y Berlín, utilizando PSG en obesos candidatos a cirugía bariátrica57,58. En esa misma línea también se han descripto diferencias del desempeño según el género, remarcando mejor predicción de los cuestionarios en las mujeres59.
En un metaanálisis, Ramachandran y Josephs compararon instrumentos multiparamétricos para identificar pacientes con apneas del sueño, concluyendo que Berlín y CSB fueron más eficaces60. Abris hami y cols., arriban a conclusiones similares, destacando que es posible que el uso concomitante de más de una herramienta de predicción mejore los resultados61.
Independientemente de la predicción previa a la realización de un estudio de sueño, las guías prácticas de la Asociación Argentina de Medicina Respiratoria (AAMR) sugieren que los pacientes candidatos a CB deben ser evaluados para descartar AOS y SOH mediante una prueba objetiva (estudio de sueño)39,62.
Los candidatos deberían tener siempre una evaluación con radiografía (Rx) de tórax, espirometría y cribado estandarizado para AOS49,63,64. Valores elevados de bicarbonato venoso hacen sospechar hipo ventilación y SOH. Ante el hallazgo de ≥ 27 mmol/l se sugiere una determinación de gases arteriales para medir la PaCO25,54,65.
En el mismo sentido, las guías de la American Association of Clinical Endocrinologists (AACE), The Obesity Society (TOS) y la American Society for Metabolic & Bariatric Surgery (ASMBS) recomiendan la pesquisa de AOS mediante un estudio de sueño de adecuada calidad, en candidatos a cirugía bariá trica y el uso de CPAP en el período preoperatorio66.
En EE.UU. la tasa de indicación de CPAP es del orden del 40% de los pacientes a quienes se realizó PSG preoperatoria38,67. Datos de nuestro país han comunicado una tasa de prescripción de CPAP previo a CB de 35,8% en el 201551.
Puntos clave
- Teniendo en cuenta que la AOS es altamente prevalente en candidatos a CB, que los cuestionarios de sueño tienen poca exactitud, se recomienda realizar un estudio de sueño (PSG o PR) como parte de la evaluación prequirúrgica, y determinar la necesidad de tratamiento con CPAP u otras terapias específicas”.
Protocolo básico de actuación clínica
La CB es un tratamiento con alta eficacia para la obesidad grave, ya que reduce la mortalidad por todas las causas, mejora la expectativa de vida y la calidad de vida, impactando sobre las comorbilidades (diabetes tipo 2, hipertensión arterial, AOS, esteatosis hepática, etc.)68,69,70.
La CB se realiza como un tratamiento a largo plazo para obesidad mórbida (IMC > a 40 kg/m2) o IMC > de 35 kg/m2 en combinación con comorbilidades relacionadas. En la actualidad, se realizan alrededor de 500.000 procedimientos en todo el mundo y su número continúa creciendo71.
Una pérdida de peso de 10% o mayor puede mejorar las apneas del sueño según el IAH72,73. Estudios clínicos que evalúan la eficacia de la CB han demostrado eficacia para mejorar la sintomatología y las puntuaciones de IAH en pacientes con AOS74-76.
La evaluación de riesgo respiratorio en el marco de la evaluación del riesgo operatorio para CB debe ser mandatoria y sistemática39,45,46,66,68,77-79.
Los pacientes que padezcan insuficiencia respiratoria diurna, insuficiencia cardiaca, apneas del sueño previamente diagnosticada o bien que usen oxigeno suplementario o algún tipo de dispositivo de ventilación deberán estar en seguimiento por médicos con formación y experiencia en el manejo de la patología respiratoria, constatándose la corrección de los trastornos.
El paciente con AOS con CPAP deberá utilizar su propio dispositivo tras la intervención y esta te rapia será aplicada en el postoperatorio inmediato y en todo el periodo perioperatorio. Sin embargo, en pacientes con un nivel de cumplimiento de CPAP inadecuado o que presentan efectos secundarios deberán ser evaluados por el especialista de sueño para identificar y solucionar las causas de intolerancia.
Si el paciente acude con estudios de sueño realizados con anterioridad, estos pueden aceptarse como válidos si su vigencia es < 3 meses y han sido revisados por un especialista para verificar que cumplan criterios de reproducibilidad, aceptabilidad y calidad del informe80.
La Figura 1 sintetiza el algoritmo de manejo inicial de la evaluación del riesgo respiratorio en CB.

Figura 1 Esquema básico de evaluación del riesgo respiratorio perioperatorio en paciente con obesidad candidato para cirugía bariátrica (CB) y no bariátrica.
Puntos clave
- La evaluación de riesgo respiratorio en el marco de la evaluación del riesgo operatorio en CB debe ser mandatoria y sistemática.
- Los pacientes que padezcan insuficiencia respiratoria diurna deberán estar en seguimiento y su aptitud se decidirá de manera individualizada.
- El paciente con AOS e indicación de CPAP, deberá utilizar el tratamiento antes de la intervención en todo el periodo perioperatorio.
Manejo perioperatorio
Preoperatorio
Es recomendable identificar situaciones que podrían favorecer la aparición de complicaciones respirato rias en el perioperatorio y factores predictores de vía aérea de difícil manejo; Mallampati III/IV, obesidad mórbida, portadores de enfermedades neuromusculares, síndrome de obesidad e hipoventilación, apneas del sueño, comorbilidades cardiovasculares y otras enfermedades respiratorias crónicas que impactan en la obesidad (asma, EPOC, fibrosis pulmonar, etc.)13,14,81,82. Considerar siempre el protocolo de manejo de vía aérea dificultosa incluyendo la intubación asistida por endoscopia.
Adicionalmente, se sugerirá la cesación-tabáquica como mínimo 6 semanas antes de la cirugía y en el postoperatorio dado el mayor riesgo de retraso en la cicatrización y úlcera anastomótica78.
Cuando el diagnóstico de apneas del sueño está confirmado, se debe iniciar el tratamiento en el período preoperatorio38,83. Es importante que la AOS reciba adecuado tratamiento al menos 2-4 semanas antes de la fecha prevista de cirugía para resolver la respuesta inflamatoria y el riesgo cardio-metabólico. Esta instancia deberá ir seguida de adecuado monitoreo objetivo (monitoreo del cumplimiento y de la eficacia de la CPAP mediante tarjeta de memoria o vigilancia remota)84,85.
En el manejo preoperatorio es aconsejable la preoxigenación al 100% antes de la inducción anestésica y elegir agentes anestésicos y bloqueantes musculares (en caso de ser necesarios) fácilmente reversibles, prefiriéndose los de acción corta86,87.
Se deben maximizar los esfuerzos para controlar el riesgo de reflujo gastroesofágico y de broncoas piración7.
El diámetro traqueal se reduce con el aumento del IMC88. Debe optimizarse la permeabilidad de la vía aérea, con la posición en Trendelemburg invertido (elevar la cabeza y parte superior del tórax 20 a 30° por arriba del plano horizontal) ya que optimiza la oxigenación87,89,90. Durante la inducción anestésica de pacientes con AOS el uso de CPAP puede usarse para mantener la capacidad residual funcional y reducir el tiempo de desaturación79.
Intraoperatorio
La sociedad americana de anestesia y medicina del sueño han publicado durante el 2018 las guías de manejo intraoperatorio del paciente con AOS. El procedimiento anestésico va a estar determinado por el tipo de cirugía y las necesidades de analgesia91. En términos generales se debe seleccionar la técnica anestésica que permita minimizar o evitar el uso de depresores respiratorios de efecto prolongado.
El Propofol presenta un efecto en la permeabilidad de la vía aérea superior (VAS) dosis dependiente, con disminución del tono muscular y del diámetro anteroposterior de la VAS. El uso de capnografía durante la sedación, disminuye la incidencia de complicaciones respiratorias91.
La Dexmedetomidina es un agonista α2 cuyo efecto sobre la VAS es mínimo. Este agente induce sueño no REM sin depresión respiratoria por lo que podría valorarse en función de las comorbilidades del paciente. No obstante, no hay evidencia suficiente para sugerir su uso sistemático en pacientes con AOS. La Ketamina, antagonista del receptor N-metil-D-Aspartato, tiene un efecto favorable sobre la colapsabilidad de la VAS, siendo otra buena alternativa92.
Los pacientes con AOS son sensibles a los efectos depresores de sedantes y opiáceos, lo cual puede ser controlado por la aplicación de bajas dosis de drogas de acción corta, además de tener siempre disponibles agentes que reviertan su acción67. Los benzodiacepinas son fármacos que deben evitarse, incluso como premedicación, debido a su capacidad de inhibir el centro respiratorio, a su efecto relajante muscular y a su vida media larga. Las fasciculaciones asociadas a relajantes despolarizantes pueden aumentan el consumo de oxígeno86.
Se recomienda monitoreo continuo de la oxigenación por oximetría, e idealmente de la ventilación con capnografía, restringiendo el aporte excesivo de fluidos ya que agravan el edema en la vía aérea93.
Postoperatorio
La extubación se decidirá cuando la ventilación espontánea y la oxigenación sean adecuadas, con el paciente semisentado, controlando que los reflejos de la VAS estén conservados y efectos de bloqueantes neuromusculares revertidos79. En los pacientes con obesidad las atelectasias postoperatorias persisten durante más tiempo, por lo que debe considerarse el riesgo de hipoxemia94. Algunos estudios sugieren que el riesgo de complicaciones es mayor en varones95, > 50 años y con IMC ≥ 60 kg/m2.
El monitoreo postoperatorio debería llevarse a cabo al menos en una sala de recuperación post anesté sica con pulsioximetría continua96,97, e idealmente en unidades con mayor capacidad de monitoreo98,99,100.
En aquellos pacientes que requieren O2 suplementario debido a comorbilidades respiratorias debe monitorizarse la ventilación con capnografía o estado ácido base con gases arteriales en el postoperatorio inmediato78. Es recomendable que los pacientes adopten la posición semisentada en el postoperatorio para reducir la hipoxemia postoperatoria, la disfunción diafragmática y los eventos obstructivos101,102. Esto se fundamenta en que el decúbito supino genera mayor caída de la CRF, más hipoxemia y mayor frecuencia de apneas/hipopneas obstructivas101,102. Por otro lado, se ha documentado disfunción dia fragmática en el postoperatorio de cirugía abdominal y cirugía torácica103.
En pacientes con AOS, la administración de O2 sin CPAP mejora la oximetría, pero puede agravar la retención de CO2 y disminuir los microdespertares protectores, por lo que debe administrarse el menor flujo que mantenga una adecuada saturación y controlarse el patrón ventilatorio, el sensorio y los niveles de CO2104-106.
En el postoperatorio, la hipoventilación con hipoxemia e hipercapnia no son infrecuentes debido a efecto residual de drogas anestésicas, atelectasias y dolor, razón por la cual debe considerase la instau ración de CPAP. Cuando sea necesario, también se puede considerar adicionar oxígeno25,68,77-79. Adicio nalmente, se recomienda el uso de CPAP en los pacientes con uso previo del dispositivo o en aquellos pacientes en los que se documenten eventos obstructivos en la unidad de recuperación104,105,106.
La CPAP en el postoperatorio inmediato ha demostrado ser segura, sin incremento en la incidencia de fístulas o dehiscencias (no tiene riesgo de alterar la integridad de la anastomosis ni la circulación local peri-anastomótica)107-110. En casos de retención de CO2 se debe contemplar la implementación de VMNI25,37,68,77-79,107.
Para el control del dolor postoperatorio se pueden combinar técnicas loco-regionales (infiltración, analgesia epidural y bloqueo de nervios periféricos) con fármacos de diferente blanco terapéutico; para cetamol, antiinflamatorios no esteroideos o ketamina, intentando disminuir necesidad de opiáceos67,79,101.
La mayoría de los pacientes con AOS (80%) muestran mejoría con la pérdida de peso112,113. Estudios prospectivos describen que en al menos tres cuartas partes de los pacientes con IAH preoperatorio ≥ 15 ev/h, podría reducirse por debajo de este punto durante el seguimiento. Alrededor del 75% de los pacientes con CPAP en el preoperatorio podrían prescindir de esta terapia después de la CB113.
La pérdida de peso inducida quirúrgicamente no solo disminuye la gravedad de las apneas del sueño, sino también la gravedad del SOH. Múltiples estudios han demostrado que esta pérdida de peso mejora la gasometría arterial, la función hemodinámica y los volúmenes pulmonares25,114-117.
Por otro lado, revisiones sistemáticas muestran que el 20% de los pacientes podrían persistir con AOS moderado a severo al año de la cirugía68. Un estudio holandés en 205 pacientes sometidos a bypass gástrico, estableció que el mayor predictor de falta de remisión de las apneas del sueño fue un IAH preoperatorio ≥ 30 ev/h (OR 5.7; IC del 95%: 2.4-13.2)113. Una menor edad e índice de desaturación de oxígeno (IDO) menor, serían predictivos de mejoría después del bypass gástrico118.
La oportunidad de reevaluar la continuidad de CPAP ó VMNI mediante un nuevo estudio de sueño está determinada por; la magnitud de la pérdida de peso, la mejoría de los síntomas y la reducción de la presión terapéutica de CPAP requerida en los controles119. Por otro lado, datos recientes sugieren que alteraciones hormonales podrían estar asociadas a cambios en el IAH independientemente a la pérdida de peso. Amin y cols., describieron una asociación entre la disminución de la leptina y aumento de la orexina con una disminución del IAH entre 3 y 5 semanas del postoperatorio, independientemente de la pérdida de peso120,121.
Si bien no está claro cuál es el momento ideal, guías de manejo clínico sugieren que los pacientes con AOS deben continuar con CPAP o VMNI después de la cirugía durante al menos 3 a 6 meses68,77,79. A partir de la pérdida del 10-15% del peso corporal se deberá considerar la realización de un nuevo estu dio de sueño para determinar la necesidad de continuar la terapia y/o para el ajuste de parámetros122.
La mejoría sintomática no sería suficiente para indicar la suspensión del tratamiento de la AOS luego de la CB. Franceschini y cols., valoraron que la magnitud del cambio en el IMC y los síntomas de somnolencia (EES) son factores predictivos de suspensión de CPAP a dos años de la cirugía bariátrica50.
Antes de la decisión final de suspender la CPAP ó VMNI, se sugiere un estudio de sueño postopera torio alejado (PSG o PR)77,79,119,123,124. Se ha informado que hasta el 50-60% de los pacientes con AOS no realizan una PSG postoperatoria112,113,125.
Además, algunos trabajos alertan que una elevada proporción de pacientes con CB y disminución de peso no cumplen la terapia con CPAP a largo plazo126. Para aumentar la adherencia y adecuar las expectativas del paciente, el asesoramiento y el seguimiento del tratamiento con CPAP debe comenzar antes de la CB124,127.
En caso de AOS persistente pese a un adecuado descenso de peso, se recomiendan los lineamentos establecidos por las guías argentinas de diagnóstico y tratamiento39.
Algunos pacientes con CPAP pueden utilizar tratamientos alternativos de acuerdo a los resultados de la evaluación en el postoperatorio (dispositivos de avance mandibular, terapia posicional, etc.).
Conclusiones
La cirugía en individuos con obesidad y la CB son procedimientos a los que se arriba luego de una eva luación exhaustiva de la situación clínica y funcional, por lo que es necesaria una evaluación respirato ria que incluya un examen de la función pulmonar y de los trastornos respiratorios durante el sueño.
La tarea multidisciplinaria y el tratamiento de las anormalidades detectadas en un examen sistemá tico y ordenado pueden disminuir los riesgos peri-operatorios.
Pacientes con obesidad que requieren cirugía electiva con anestesia general deben ser evaluados me diante pruebas objetivas para confirmar o descartar la AOS. Los pacientes obesos con AOS candidatos quirúrgicos deben estar adecuadamente tratados con CPAP.














