INTRODUCCIÓN
El paludismo, o malaria, es una enfermedad potencialmente mortal causada por parásitos que se transmiten al ser humano por la picadura de mosquitos hembra infectados del género Anopheles, De las cuatro especies de Plasmodium que afectan al hombre, P. falciparum se considera la más virulenta, ya que es responsable de la mayoría de muertes y de las formas graves de la enfermedad, La PCR se ha convertido en el método de elección para estudios de diversidad genética en P. falciparum en muestras recolectadas en el campo, sobre todo por la alta sensibilidad y especificidad para amplificar marcadores genéticos, su capacidad de revelar polimorfismos de longitud y la posibilidad de usar muestras pequeñas de sangre o mosquitos sin necesidad de realizar cultivos de parásitos, los cuales pueden conducir a una selección de clones, Según el último informe mundial de la Organización Mundial de la Salud1 sobre paludismo, publicado en noviembre de 2018, se estima que en 2017 ocurrieron 219 millones de casos de malaria en todo el mundo, frente a 239 millones en 2010 y 217 millones en 2016, La cifra estimada de muertes por paludismo en 2018 fue de 435 000, número similar al del año anterior,
En América Latina, la transmisión de malaria ocurre principalmente en seis países (Brasil, Colombia, Guyana, Haití, Perú y Venezuela), y alrededor de 132 millones de personas se encuentran en riesgo de infección2,
En el caso de Perú, la malaria es endémica en algunas zonas de la costa norte y posee una distribución importante en la región amazónica; el departamento de Loreto es el más afectado, En la Amazonia peruana, la enfermedad presenta una transmisión mayormente estacional, con picos de noviembre a mayo; en el caso de la costa norte, esto ocurre de abril a junio3,4,
Aunque tanto P. vivax como P. falciparum son responsables de la transmisión de malaria en la cuenca amazónica (Perú y Brasil), aproximadamente el 77% de las infecciones se atribuyen a P. vivax, seguida de P. falciparum5.
En P. falciparum, el grado de diversidad se pudo demostrar inicialmente empleando marcadores bioquímicos en el estudio de poblaciones naturales del parásito, Posteriormente, el desarrollo de métodos moleculares basados en ADN, como la reacción en cadena de la polimerasa (PCR), permitió precisar diferencias genéticas dentro de la especie,
Hasta la fecha, las investigaciones realizadas sugieren que la diversidad genética de las poblaciones de P. falciparum varía de acuerdo con las características epidemiológicas de la región6-9, Plasmodium es un protozoo con un ciclo de vida bastante complejo, que comprende una fase asexual o esquizogonia en el hospedero humano y una breve fase sexual obligatoria en el mosquito vector,
En el humano, la infección comienza con la picadura de la hembra del género Anopheles infectada, la cual introduce las formas del parásito denominadas esporozoítos, que circulan por corto tiempo e invaden las células hepáticas para formar los esquizontes tisulares, Estos lisan los hepa-tocitos y liberan miles de merozoítos (10 000 a 30 000) que invaden los glóbulos rojos. Dentro del glóbulo rojo, los merozoítos maduran a los estadios de anillo, trofozoíto y esquizonte eritrocítico. El esquizonte maduro rompe el eritrocito y libera merozoítos, que posteriormente invadirán otros glóbulos rojos.
Algunos de estos merozoítos sufren un proceso de diferenciación en formas sexuales denominadas microgametocitos y macrogametocitos, que son los estadios infectantes para el mosquito vector. Una vez que el parásito entra al intestino medio de Anopheles, ocurre la maduración y la fertilización de gametos; esto da como resultado la formación del cigoto, el cual se convierte en una forma móvil, denominada ooquineto, que posteriormente se transforma en ooquiste. Esta última forma parasitaria contiene el producto meiótico y mitótico de un único cigoto y da lugar a los esporozoítos, que migran a las glándulas salivares del mosquito listas para infectar al humano en una nueva ingesta sanguínea10.
El objetivo de este trabajo fue describir la diversidad genética de P. falciparum a fin de conocer variantes resistentes a medicamentos y a vacunas, teniendo en cuenta que el desarrollo de medidas de control efectivas en las diferentes regiones con transmisión de la enfermedad requiere, entre otros aspectos, comprender la estructura genética de P. falciparum.
MÉTODOS
Para la revisión narrativa se hizo la búsqueda de literatura publicada, que incluyó libros, artículos científicos originales, verificando el tema, y reportes técnicos. Los documentos se consultaron entre agosto y diciembre de 2019 a través del acceso en Internet y bibliotecas del Academic Search Complete del gestor de búsquedas Medline, Science Direct, Scopus, Redalyc y Psicodoc. Se recurrió además a las bases de datos bibliográficos de la Organización Mundial de la Salud, la Organización Panamericana de la Salud y SciELO. Finalmente, se consultaron bibliografías citadas en artículos indexados.
RESULTADOS
Entre las secuencias polimórficas que han sido de utilidad como marcadores genéticos de las poblaciones de P. falciparum se encuentran los genes de las proteínas de superficie del merozoíto 1 y 2 (MSP-111,12, MSP-213,16) y el gen de la proteína rica en glutamato (GLURP)17,21.
Para MSP-1 y MSP-2 se han descrito dos tipos de polimorfismo, en secuencia y en tamaño, mientras que para GLURP sólo se ha observado polimorfismo en tamaño.
El gen MSP-1 es de copia única y está localizado en el cromosoma 922,23. Codifica uno de los antígenos más estudiados de la fase eritrocítico del parásito y se ha señalado como un potencial candidato para vacuna. La comparación de secuencias de nucleótidos de MSP-1 en diferentes clones de laboratorio ha permitido identificar 17 bloques o dominios: 7 altamente variables, 5 conservados y 5 semi-conservados. Los bloques variables (2, 4, 6, 8, 10, 14, 16) presentan dos alelos denominados MAD20 y K1 24-25; una excepción es el bloque 2, que cuenta con el alelo adicional R03325-28 (ver Figura 1). Los alelos MAD20 y K1 presentan diferentes unidades de secuencias repetidas, mientras que el alelo R033 consta de una secuencia única.
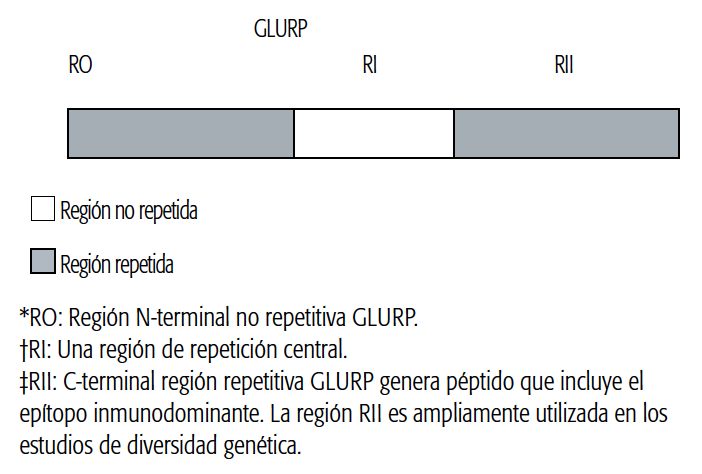
FIGURA 1 A) Representación esquemática del gen de la proteína de superficie del merozoíto 1 (MSP 1). B) Familias alélicas de diversidad genética en P. falciparum del bloque 2 del gen MSP 1.
El MSP-2 es un gen en el cromosoma 224,25' 29-31 que codifica una proteína de superficie también considerada candidata para vacuna en el tratamiento. Se puede clasificar en dos familias alélicas denominadas FC27 (FC) e IC/3D7 (IC), que derivan igualmente su nombre de las líneas de parásitos en las cuales fueron inicialmente observadas30,31.
El gen GLURP, localizado en el cromosoma 1017,22' 32-39, codifica una proteína inmunodominante rica en glutamato. Presenta una región central conservada no repetida, rodeada por dos repetidas. Una de estas regiones repetidas, denominada R II, de aproximadamente 50 pares de bases, varía entre las diferentes cepas de parásitos, por lo cual es ampliamente utilizada en los estudios de diversidad genética de P. falciparum38 (ver Figura 2).
DISCUSIÓN
En 1997 Conway, entre otros, mostró que la frecuencia de familias alélicas del gen MSP-1 difería en varios países; en el sureste de Asia y en el este africano, la familia alélica denominada Wellcome-like tuvo una frecuencia de entre 25% y 50%, pero presentó una frecuencia menor a 1% en el oeste de África y en Brasil40,41.
Asimismo, en 1991, Scherf fue uno de los que encontró grandes diferencias en la frecuencia con la que se presentaba el alelo R03342-43 del gen MSP-1 en Brasil y en Senegal (en Brasil era mucho más alta42).
En regiones con transmisión inestable, como Honduras44 y Colombia45, se ha encontrado una distribución de alelos del gen MSP-1 45-47 en la que predomina el alelo MAD-20 sobre el K-148,49. Sin embargo, en regiones de transmisión alta, como Tanzania y Senegal, esta distribución es invertida48,52.
Las secuencias polimórficas que han sido de utilidad como marcadores genéticos de las poblaciones de P. falciparum se encuentran los genes MSP-1, MSP-2 y el gen GLURP, codifican uno de los antígenos más estudiados de la fase eritrocítico del parásito y se han señalado como un potencial candidato para vacunas. Los hallazgos en las diferentes regiones estudiadas permiten concluir que la diversidad genética, la multiplicidad de infección y la dinámica en el tiempo de las infecciones por P. falciparum se ven afectadas por el grado de endemicidad de la malaria en cada país.
Sería importante realizar futuros estudios de la asociación del genotipo humano con los diferentes cuadros clínicos de la malaria, lo cual podría evaluarse investigando la variabilidad en los genes del antígeno leucocitario humano, así como la capacidad de generar interleuquinas y otros receptores involucrados en la citoadherencia del eritrocito infectado.















