Introducción
La cirugía hepática laparoscópica tuvo un lento pero continuo desarrollo. Las reservas iniciales en cuanto a este abordaje fueron progresivamente respondidas, en un paralelismo con la cirugía colorrectal. Sin embargo, dado que la cirugía hepática difiere significativamente en muchos aspectos, hubo que poner a prueba la viabilidad y utilidad de esta nueva técnica. Reich y cols. publicaron la primera resección hepática no anatómica por vía laparoscópica en 19911; Azagra y cols., en 1996, publicaron la primera resección hepática anatómica por vía laparoscópica (sectoriectomía lateral izquierda)2.
El desarrollo se incrementó gracias al aporte e intercambio generado entre los pioneros internacionales de esta técnica,3),(4 y posteriormente se llevaron a cabo reuniones de consenso entre expertos y guías: 2008 Louisville, Estados Unidos; 2014 en Morioka, Japón; 2018 en Southampton, Gran Bretaña. Fue creada la Asociación Internacional de Cirugía Hepática Laparoscópica (International Laparoscopic Liver Society - ILLS) y organizaron un primer congreso en París en 2017, luego en Tokyo en 2019, que aportaron mucho al desarrollo seguro de esta técnica5),(6),(7.
Las objeciones iniciales al abordaje laparoscópico estaban relacionadas con que los cirujanos hepáticos no tenían experiencia en laparoscopia; por ello, las primeras series fueron realizadas por cirujanos laparoscópicos no especializados en cirugía hepática. Esto fue el punto de partida para que muchos cirujanos entrenados en cirugía laparoscópica general adquirieran formación específica en cirugía hepatobiliar convencional y laparoscópica8),(9),(10.
A medida que crecía el interés por las hepatectomías mínimamente invasivas, fue necesario establecer un marco estandarizado para orientar a los cirujanos situados en lugares diferentes en la curva de aprendizaje, sobre qué resecciones iban a ser técnicamente más difíciles que otras. En 2014 fueron propuestos los criterios de Iwate. A partir de seis factores preoperatorios, estos criterios clasifican las intervenciones en cuatro niveles de dificultad, que fueron validados como una guía para los cirujanos hepatobiliares. Aplicados a las hepatectomías laparoscópicas, los criterios de Iwate fueron un indicador fiable de la dificultad quirúrgica7),(9),(10),(11.
Nuestra institución tiene una amplia experiencia en cirugía laparoscópica, la cual se inició en el año 1992 con la primera colecistectomía, e iniciamos la experiencia en cirugía hepática laparoscópica tempranamente en el año 2005. Desde entonces hubo algunos informes nacionales de centros de la Ciudad de Buenos Aires, con cohorte entre los años 2000 y 201912),(13),(14, por lo que nos pareció relevante presentar nuestra experiencia en el Hospital Privado de Comunidad de la ciudad de Mar del Plata.
El objetivo del presente estudio fue describir los resultados de una serie de pacientes con hepatectomías videolaparoscópicas.
Materiales y métodos
Se realizó un estudio observacional descriptivo y analítico de una cohorte pacientes que se sometieron a hepatectomía laparoscópica. Este estudio fue evaluado y aprobado por el Comité de Ética del hospital.
El hospital cuenta con población cautiva de Obras Sociales capitadas y Plan de Salud del Hospital, que permite asegurarnos el seguimiento de la población en la misma institución durante el postoperatorio. Además, tiene equipo de Cirugía Hepatobiliopancreática (HPB) y trasplante hepático.
Se incluyeron consecutivamente los pacientes mayores de 18 años en los que se realizó una hepatectomía laparoscópica entre enero del año 2005 y octubre de 2021. Todos ellos fueron seguidos al menos 6 meses.
La decisión de qué abordaje realizar fue individualizada según la dificultad técnica, evaluado previamente mediante los estudios por imágenes y la eco laparoscopia intraoperatoria.
La dificultad de las resecciones fue evaluada según los criterios de Iwate, que comprendía seis variables con una puntuación total que oscilaba entre 0-12 puntos. Estas variables son la localización del tumor (1-5 puntos), la extensión de la resección hepática (0-4 puntos), el tamaño del tumor menor o mayor de 3 cm (0-1 punto), la proximidad a un vaso sanguíneo importante (0-1 punto), la función hepática Child-Pugh (0-1 punto) y, por último, si la resección fue mano-asistida o híbrida (0-1 punto). El índice de dificultad 0-12 se subdividió en cuatro niveles de dificultad: bajo (0-3), intermedio (4-6), avanzado (7-9) y experto (10-12)7.
Se registraron las características de la población, las propias de los pacientes, el riesgo quirúrgico de acuerdo con la clasificación de la Sociedad Americana de Anestesiología (ASA)15, topografía, número y tamaño de las lesiones para resecar, tiempo quirúrgico, la necesidad de transfusiones y sangrado intraoperatorio, los clampeos pediculares realizados, la necesidad de conversión a cirugía abierta y los desenlaces, tanto oncológicos como el índice de resección R0, la mortalidad a los 90 días y las comorbilidades, que clasificaremos según Clavien-Dindo16.
Técnica quirúrgica
Todos los pacientes fueron discutidos previamente en ateneo multidisciplinario en donde se propusieron las opciones terapéuticas, con médicos cirujanos, especialistas en cirugía HPB y trasplante hepático, hepatólogos, oncólogos, y evaluados de manera prequirúrgica por los Servicios de Terapia Intensiva y Anestesiología.
El paciente es colocado en decúbito dorsal, la torre de laparoscopia preferentemente del lado derecho del paciente. El primer trocar se ubica cerca del ombligo (paraumbilical derecho) con técnica cerrada de neumoperitoneo (10-12 mm Hg) y, posteriormente, se colocan 3 o 4 trocares más, de 12 y 5 mm según demanda, a lo largo de la zona operatoria, todos en hemiabdomen superior. Realizamos ecografía translaparoscópica con transductor de 7,5 MH (Aloka 3500®).
Definido el tipo de resección, procedemos a la preparación de la maniobra de Pringle: en los primeros años de la cohorte, la hacíamos extracorpórea: introducimos el extremo de un lazo de tela de 3-4 mm de espesor, rodeamos el pedículo hepático, y volvemos a extraerlo. Con sus extremos unidos, los pasamos con un paso-lazada metálico a través de una de sonda K10 recortada de un largo que nos permita clampear (pinzar) desde afuera del abdomen. En los últimos años lo hemos reemplazado por un clampeo (pinzamiento) intracorpóreo con una sonda de Foley.
El clampeo pedicular es intermitente alternando clampeos y desclampeos: 15 minutos de clampeo en hígados normales, 10 minutos de clampeo en pacientes con hepatopatía crónica (cirróticos o antecedentes de quimioterapia previa), alternando con 5 minutos de desclampeo.
Luego de la exploración laparoscópica del hígado, delimitamos la o las resecciones con el bisturí monopolar. La sección parenquimatosa inicial puede ser realizada con el mismo electrocauterio o con el bisturí armónico (Ultracision®). Pasados los dos centímetros de profundidad, preferimos otro instrumento de energía sellador de vasos: Ligasure (Covidien®), Enseal (Ethicon®) o Biclamp (Medtronic®) dependiendo de la disponibilidad. Los vasos mayores de 5 mm, previa disección intraparenquimatosa, son clipados en forma selectiva con clips metálicos LT100 o LT300 o clips de polímero (Hem-O-Lok®). Las autosuturas lineales se utilizan para la sección de los pedículos vasculobiliares más grandes y para las venas suprahepáticas. No las utilizamos para la sección parenquimatosa. En las sectoriectomías laterales izquierdas preferimos la sección del pedículo de los segmentos 2 y 3 por abordaje extrafascial. En el resto de las hepatectomías anatómicas utilizamos la disección intrafascial de los pedículos correspondientes.
La hemostasia de la superficie hepática seccionada es controlada mediante coagulación bipolar, o en algunos casos con gas de Argón. Los sitios de fugas biliares detectados se cierran con suturas intracorpóreas.
Una vez finalizada la hepatectomía, la pieza es colocada en una bolsa plástica para su extracción, por lo general reutilizando alguna herida preexistente, o ampliamos alguna de los trocares o realizamos de preferencia una incisión de Pfannenstiel.
Resultados
En el período en estudio se realizaron 159 resecciones hepáticas, y de estas, 120 (75%) fueron realizadas por vía laparoscópica. La mediana de edad fue de 61 años (percentil 25 y 75 entre 51-71); 67 (55,8%) eran mujeres. Presentaron calificación ASA I y II 88 (73,3%) pacientes, y ASA III o mayor 32 (26,6%).
En las tablas 1 y 2 se describen los diagnósticos de las patologías benignas y malignas de la serie. La indicación más frecuente respondió a patología maligna: 79% (n = 95) y las metástasis de cáncer colorrectal fueron las predominantes (n = 68).
TABLA 1 Diagnósticos de las patologías benignas en la serie de 120 hepatectomías laparoscópicas
| Patologías benignas | n |
|---|---|
| Sospecha de malignidad | 16 |
| Enfermedad de Caroli | 4 |
| Quiste simple complicado | 1 |
| Abscesos hepáticos | 1 |
| Lesión indeterminada por compresión de la vía biliar | 1 |
| Atrofia secundaria (hepatolitiasis) | 1 |
| Necrosis del segmento anterior derecho | 1 |
| Total | 25 (20,8%) |
TABLA 2 Diagnósticos de las patologías malignas en la serie de 120 hepatectomías laparoscópicas
| Patologías malignas | n |
|---|---|
| Metástasis de carcinoma colorrectal | 68 |
| Hepatocarcinoma | 10 |
| Metástasis de cáncer de mama | 6 |
| Cáncer de vesícula | 5 |
| Colangiocarcinoma intrahepático | 3 |
| Metástasis de cáncer de páncreas | 1 |
| Metástasis de adenocarcinoma gástrico | 1 |
| Sarcoma indiferenciado | 1 |
| Total | 95 (79,2%) |
Fueron 103 las hepatectomías menores (45 de ellas fueron anatómicas y 58 no anatómicas) y 17 las mayores, entre las que se incluyen tres pacientes en quienes se aplicó la técnica de hepatectomía en dos tiempos o ALPPS (Associating Liver Partition and Portal vein ligation for Staged hepatectomy). Encontramos también que 34 resecciones fueron múltiples (de al menos dos segmentos).
La sectoriectomía lateral izquierda fue la resección anatómica más presente en la serie con 18 casos.
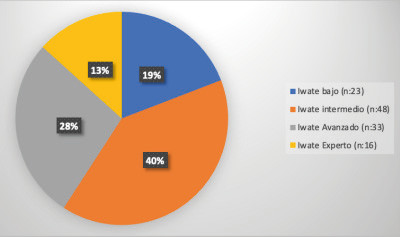
La distribución según los criterios de dificultad de Iwate se describe en la figura 1.
Se pueden observar en la tabla 3 los desenlaces y eventos intraoperatorios.
TABLA 3 Hepatectomías laparoscópicas: variables intraoperatorias, mortalidad a los 30 días, morbilidad y mortalidad, clasificadas según índice de Iwate
| Iwate (n) | 1-3 (23) | 4-6 (48) | I7-9 (33) | 10-12 (16) | Total (120) |
| Tiempo operatorio, en minutos Mediana (percentiles 25 y 75) | 150 (110-240) | 240 (160-340) | 300 (210-340) | 360 (300-420) | 280 (180-360) |
| Pérdida de sangre, en mL Mediana (percentiles 25 y 75) | 200 (100-1000) | 500 (200-1200) | 700 (400-1200) | 800 (500-2500) | 600 (200-1200) |
| Transfusiones UGR Mediana (percentiles 25 y 75) | 0 | 0 | 0 | 2 (0-4) | 0 |
| Clampeo pedicular, n (%) | 10 (43,5) | 31 (64,6) | 21 (63,6) | 13 (81,25) | 78 (65) |
| Tiempo de clampeo mediana y percentiles 25 y 75 (minutos) | 35 (20-45) | 60 (30-80) | 60 (37,7-77,5) | 55 (34,5-80) | 57,5 (30-77,5) |
| Conversión, n (%) | 1 (4,3) | 7 (14,6) | 7 (21,2) | 6 (37,5) | 21 (17,5) |
| Mortalidad a los 30 días, n (%) | 0 | 1 (2) | 0 | 2 (12,5) | 3 (2,5) |
| Morbilidad Clavien-Dindo III o IV, n (%) | 1 (4,34) | 2 (4,16) | 2 (6) | 3 (18,7) | 8 (6,6) |
| Estadía hospitalaria en días Mediana e intervalo intercuartílico (días) | 4 (3) | 4 (3) | 5 (4) | 7 (6) | 4 (4) |
UGR: unidad de glóbulos rojos.
Sesenta y siete (98%) resecciones por metástasis de cáncer colorrectal fueron R0, solo un caso fue R1. En este grupo, la recidiva local fue de 3,7% a los 5 años, la sobrevida libre de enfermedad fue de 75%, 59%, 46% al año, a los 3 y a los 5 años, respectivamente, y la sobrevida global de 93%, 79% y 69%, al año, a los 3 y a los 5 años, respectivamente.
Tuvimos una tasa de conversión del 17,5% (n = 21): 7 por complicaciones hemorrágicas, una por intolerancia al neumoperitoneo y retención de dióxido de carbono y, en los casos restantes, por dificultades técnicas o por hallar mayor número de lesiones y/o topográficamente desfavorables para la resección laparoscópica.
La conversión, de acuerdo con la complejidad según la clasificación de Iwate, fue mayor en los grupos experto y avanzado (Tabla 3). En 3 ocasiones decidimos la conversión a la técnica mano-asistida: uno de ellos para control de una hemorragia de difícil exposición, y en otros dos pacientes para mejorar la exposición y resección de lesiones grandes ubicadas en el segmento VIII.
Ocho pacientes (6,6 %), sufrieron complicaciones IIIA, IIIB o IV de la clasificación de Clavien-Dindo.
En el grupo de expertos hubo 3 complicaciones: 2 pacientes tuvieron fístula biliar, tratadas mediante drenaje percutáneo guiado por tomografía, y un paciente debió ser intervenido quirúrgicamente luego del fracaso del tratamiento mínimamente invasivo por una colección en el lecho quirúrgico.
Con respecto al grupo avanzado e intermedio, hubo dos complicaciones de tipo III o IV por cada uno de ellos.
En el grupo avanzado, un paciente presentó una complicación hemorrágica que requirió nueva operación, y otro paciente, operado por un hepatocarcinoma, cursó con insuficiencia hepática con encefalopatía luego de una hepatectomía izquierda.
En el grupo intermedio hubo un paciente con un absceso drenado percutáneo e íleo prolongado y otro con un biloma con drenaje percutáneo y complicaciones respiratorias graves debido a infecciones nosocomiales.
En el grupo de complejidad baja de Iwate, un paciente requirió un drenaje percutáneo ecoguiado por un biloma infectado.
En cuanto a la mortalidad: en un paciente con múltiples metástasis de cáncer colorrectal planeamos una hepatectomía en dos tiempos o ALPPS: hicimos el primer tiempo por vía laparoscópica y, en el segundo tiempo, decidimos la conversión por la complejidad de la resección. Hicimos sectoriectomía posterior derecha y otras recesiones no anatómicas en el hígado derecho, pero desarrolló insuficiencia hepática posoperatoria y falleció a los 25 días (small for size syndrome)17.
Los otros dos pacientes fallecidos, de 74 y 72 años, ambos con cirrosis y hepatocarcinoma del segmento 7. El primer caso fue convertido por dificultad técnica al inicio de la cirugía y desarrolló en el posoperatorio una insuficiencia hepática y renal, con requerimiento de hemodiálisis.
El otro paciente tuvo complicaciones hemorrágicas intraoperatorias que necesitaron conversión y hemostasia de una colateral de la vena suprahepática derecha. Tuvo inestabilidad hemodinámica intraoperatoria y posoperatoria, fallo orgánico múltiple y falleció a las 12 horas de la cirugía.
En los grupos de complejidad baja y avanzada, no se registró mortalidad posoperatoria (Tabla 2).
Discusión
La presente serie es una de las cohortes más largas de hepatectomías laparoscópicas, ya que comprende 120 casos, que representan el 75% del total de 150 hepatectomías en el período de estudio. Esto muestra una alta tasa de uso de la técnica. Las lesiones más frecuentemente abordadas fueron las neoplasias, y, entre ellas, las metástasis de cáncer colorrectal en 95 oportunidades (79,1%).
Esto podría deberse a que, en nuestro centro, la experiencia en cirugía general laparoscópica la iniciamos muy tempranamente en nuestra etapa de formación como cirujanos generales. Luego adquirimos experiencia específica en trasplante hepático y cirugía hepática convencional, y laparoscópica avanzada que adquirimos los médicos de planta, asociada al apoyo institucional para plasmar este proyecto en cuanto a la adquisición del equipamiento necesario y fundamentalmente a la alta motivación y convicción del equipo actuante.
A medida que adquirimos experiencia en cirugías más fáciles o segmentos más accesibles, comenzamos a realizar cirugías de los segmentos posteriores, que son más complejas. Por consiguiente, las complicaciones pueden aumentar. Esto lo demostramos al comparar la morbilidad de acuerdo con el puntaje (score) de Iwate de las hepatectomías (Tabla 2).
Es evidente que la aplicabilidad del método todavía es limitada, pero en aumento: 25% según Nguyen, similar a lo publicado en la Argentina. En una revisión multicéntrica sudamericana de la cual participamos, Juan Pekolj informó una tasa de aplicabilidad del 28,5%, siendo nuestro país el de mayor tasa de cirugía por millón de habitantes de la región (6,8 cirugías hepáticas laparoscópicas por millón de habitante), aunque lejos de las publicadas en otros países: Japón (157,8), Francia (67,3) Italia (54,6) y Estados Unidos (15,1)12),(13),(14),(18),(19.
Este lento desarrollo fue justificado por varias razones. El hígado, a diferencia de otros órganos abdominales, es un órgano voluminoso, frágil y difícil de exponer sin la ayuda de las manos como en la cirugía convencional. La sección parenquimatosa suele estar asociada a riesgo de hemorragia, como también de fístula biliar y embolismo aéreo. Los instrumentos iniciales no eran lo suficientemente seguros para realizarla.
En cuanto a las resecciones oncológicas, había muchas dudas de riesgo de diseminación, implantes en trocares, o resecciones inadecuadas, sin seguir los principios oncológicos de la cirugía convencional. Es por ello que las series iniciales tenían alta tasa de resecciones de tumores benignos (45% en la revisión de Nguyen)18),(20),(21),(22.
Gracias al aprendizaje de la técnica quirúrgica y anestésica junto al desarrollo de instrumental más eficaz y específico (instrumentos de energía para sección parenquimatosa, coagulación con gas de Argón, etc.), la cirugía hepática laparoscópica creció exponencialmente a partir del año 2000, permitiendo el abordaje de todo tipo de lesiones23),(24),(25.
Los primeros trabajos publicados acerca de patología maligna demostraron resultados similares a los de la cirugía convencional. Durante la Segunda Conferencia Internacional de Consenso de Morioka se concluyó́ que las resecciones hepáticas laparoscópicas por cáncer tuvieron similares resultados en cuanto a los márgenes tumorales obtenidos y sin diferencias en la supervivencia libre de recurrencia y global respecto de la cirugía abierta26. Maurette y cols. publicaron un trabajo comparativo entre un grupo favorable para la técnica laparoscópica comparadocon otro grupo de hepatectomía convencional, y obtuvieron resultados oncológicos similares13. En nuestra serie laparoscópica tenemos más del 89% de resecciones por cáncer, y en el 98% de los casos las resecciones fueron R0. La ecografía laparoscópica intraoperatoria fue de mucha ayuda para esto. La utilizamos en forma muy dinámica: al inicio para marcar los límites de la lesión, activamente durante la sección parenquimatosa, midiendo tanto los márgenes laterales como el profundo, el más difícil de obtener27. En los casos de tumores ubicados en el domo hepático adoptamos la técnica en diamante descripta para mejorar el porcentaje de resecciones R0 28.
En caso de no contar con el traductor laparoscópico o en caso de metástasis múltiples, podemos optar por la técnica manoasistida, utilizada con bastante frecuencia según lo publicado por Barros Schelotto y cols., y con excelentes resultados12.
Los factores de riesgo para la conversión incluyen un aumento del índice de masa corporal (IMC), el tamaño del tumor y la extensión de la resección, y también resecciones en los segmentos posterosuperiores y cirrosis29. En nuestra serie fue del 17,5% (21 pacientes).
La curva de aprendizaje sin duda es lenta. Barros Schelotto y col. informan una aplicabilidad del 23% en la etapa inicial y 44% en la tercera etapa, similar a lo reflejado por Maurette y cols. en su interesante trabajo comparativo13.
La recomendación es comenzar por los segmentos anteriores del hígado y el progreso debe ser gradual 6: segmentectomías o bisegmentectomías anatómicas; luego de haber realizado 50 cirugías laparoscópicas básicas podremos avanzar con los segmentos posteriores, hepatectomías mayores, rehepatectomías y hepatectomías en dos tiempos. En trabajos recientes que comparan resultados de hepatectomía laparoscópica versus robótica, concluyen que la curva de aprendizaje puede ser más corta en el grupo con robot, sin diferencias en el resto de las variables analizadas30),(31.
En conclusión, la hepatectomía laparoscópica en la serie aquí presentada fue una técnica factible y segura. Para su desarrollo es fundamental contar con un equipo multidisciplinario entrenado específicamente en ello, disponer de un quirófano y personal equipado y seleccionar, sobre todo inicialmente, muy bien los pacientes.











 text in
text in