INTRODUCCIÓN
El trasplante renal se ha consolidado como la terapia sustitutiva de elección para pacientes con insuficiencia renal crónica, con aumento de la sobrevida y mejoría de la calidad de vida. Estos pacientes presentan una elevada incidencia de procesos oncológicos respecto de la población general, cuya diferencia varía según la neoplasia considerada. Por otra parte, los procesos oncológicos tienden a ser más agresivos y manifestarse a edades más tempranas. El desarrollo de métodos de screening, el estudio de factores de riesgo, el ajuste de medicación inmunosupresora, la implementación de estudios complementarios sobre losefectos de la terapéutica oncológica sobre el implante son algunos de los puntos a considerar.
EPIDEMIOLOGÍA
La patología oncológica ha aumentado notablemente su incidencia en la población trasplantada renal. Este incremento ha llevado a los médicos y a los servicios de salud intervinientes en el proceso de trasplante a señalar estrategias preventivas, de diagnóstico, seguimiento y tratamiento en esta población en riesgo. Se estima que el paciente con trasplante renal padece cáncer con una frecuencia entre dos a cuatro veces mayor que su contrapartida, la población general de igual edad y sexo. Esta diferencia se acrecienta aúnmás cuando se extiende el tiempo de postrasplante y cuando es mayor la edad del receptor.1-12 Este incremento no es igual para todas las neoplasias, tal como se resume en la Tabla 1.13 Algunos tumores, como el sarcoma de Kaposi,presentan una frecuencia trescientas veces mayor respecto de la población general, mientras que otros, como el mamario o el prostático,tienen una frecuencia similar en ambas poblaciones. En algunos lugares del mundo, la patología oncológica ha desplazado a la cardiovascular como principal causa de mortalidad. En este contexto debe considerarse la evaluación de los donantes y del potencial receptor deltrasplante renal, así como las medidas diagnósticas y de seguimiento luego del mismo.
Tabla 1 Frecuencia de tumores en población trasplantada respecto de población general13SIR, Standard Incidence Ratio, refleja las veces de incremento del riesgo de neoplasia en el trasplantado renal respecto de la población general; PTLD, Post-Transpant Lynphoprolipherative disorder; LNH, Linfoma no Hodgkin
| SIR > 5 | SIR 2-5 | SIR < 2 |
|---|---|---|
| Sarcoma de Kaposi Carcinoma cutáneo no melanoma PTLD / LNH Tumores renales Tumor de pene / vulva Tumores anogenitales Tumores hepáticos Tumor de labio | Cuello uterino Tumores de tiroides Melanoma Tumor de esófago Mieloma múltiple Leucemia Tumores orofaríngeos Tumores vesicales Tumores de colon | Mama Ovario Útero Cerebro Próstata Testículo Pulmón |
Mecanismos
Si bien el tratamiento inmunosupresor en general, y en especial los anticalcineurínicos, han sido los más tempranamente implicados en el desarrollo de tumores en el postrasplante14-16, existen varias concausalidades para dicho efecto, en primer lugar, la insuficiencia renal crónica (IRC) está asociada a una mayor incidencia de neoplasias respecto de la población general.17-20Se discute si la insuficiencia renales un factor de riesgoper se, si este fenómeno está vinculado con determinadas neoplasias asociadas con fallo renal (eg. mieloma múltiple) con tratamiento quimioterápicos de la IRC, o si bien se manifiesta un efecto directo entre la disfunción renal y la aparición del tumor.
La IRC y el cáncer están ligados bidireccionalmente y ambos pueden compartir factores de riesgo como la nefropatía por el uso de analgésicos y de ácido aristocólico. Entre los diferentes tipos de tumores observados con mayor frecuencia en la población en diálisis, se destacan los de tiroides, renales y del tracto urinario.10,20
El riesgo de cáncer seexpresa con la sigla en inglés SIR (Standardized Incidence Ratio, o relación de incidencia estandarizada) y se calcula sobre la base de los casos observados dividiendo los casos esperados. En la población con IRC no trasplantada, el valor de SIR se estima entre el 1,1-1,8.10Enel postrasplante, los tumores aumentan exponencialmente en frecuencia, tal como se expresa en la Tabla 1. Los tumores vinculados a virus oncogénicos son los que presentan mayor magnitud de aumento en incidencia en esta población. En la Tabla 2 se sintetizan los virus oncogénicos observados o sospechados de tales hasta la fecha.
Tabla 2 Virus oncogénicos y tumores postrasplante13EBV: Epstein-Barr virus; HBV: hepatitis B virus; HCV: hepatitis C virus; HPV: human papilloma virus; JCV: John Cunningham virus (variante polyoma); PTLD: post-transplant lymphoproliferative disorder; HHV: virus Herpes 8; HTLV: virus de Leucemia T humana; SV: virus simiano. (*) Asociación sospechada
| Neoplasia | Virus involucrado |
| Cervix, vulvar, vaginal, perianal | HPV 16 y 18 |
| Carcinoma hepatocellular | HBV, HCV |
| PTLD | EBV |
| Leucemia y Linfoma | HTLV 1 |
| Sarcoma de Kaposi | HHV 8 |
| Tumor de Merckel | Polioma virus de células de Merckel |
| Cancer de próstata | Polioma BK* |
| Cerebro | JCV* |
| Cerebro, huso y mesotelima | SV 40* |
La relación del cáncer con los inmunosupresores es más compleja. Los agentes deplecionantes de linfocitos, los anticalcineurínicos y los antimetabolitos han sido vinculados con un mayor riesgo de desarrollo de neoplasias de diferentes tipos, dependiendo del tipo de agente considerado.21Por el contrario, los mTOR se relacionaron con una reducción en la incidencia de tumores, en especial de piel y linfoproliferativos.22Es importante tener en cuenta que la aparición y progresión de muchos tumores, aún en pacientes no trasplantados, se debe a un escape del reconocimiento de las células malignas por parte del sistema inmune.23 El bloqueo del sistema inmune, que implica el tratamiento inmunosupresor, supone un mayor riesgode aparición y de progresión de los tumores en estos pacientes. La carga global de inmunosupresión (tratamiento de rechazo, tratamiento de inducción, tratamiento quimioterápico o inmunosupresores previos) se estima como más importante como factor oncogénico que los inmunosupresores en forma individual.
Factores del paciente (edad avanzada, sexo masculino, raza blanca), de su historia clínica (tabaquismo, tiempo de diálisis, tumores previos) y del trasplante (mismatch DR, PRA, donante de criterios expandidos), se correlacionan con un incremento de la frecuencia de aparición de tumores.21-22
Por otra parte, la diabetes se ha vinculado con un riesgo menor de presencia de tumores, aunque esto ha sido discutido, alegando que los diabéticos, al tener una sobrevida menor que la población no diabética, no tienen el mismo tiempo de seguimiento por evidenciarse mayor riesgo de mortalidad cardiovascular.24-25
¿Cómo reducir el riesgo de cáncer en el paciente trasplantado?
Este aspecto debe ser abordado en las diferentes etapas del proceso, desde el ingreso a diálisis, la incorporación en la lista de espera, el seguimiento y el trasplante en sí mismo.
Reducción del riesgo de transmisión de tumores por el donante
Si bien el riesgo de transmisión de tumores de un donante es bajo (entre 0,01 y 0,05%),26-27) la mortalidad en estos casos es elevada, dependiendo del tipo de tumor transmitido (el promedio es del 20%).26
En el caso del donante vivo, las guías internacionales sugieren screening para los tumores más frecuentes de la población general (cuello de útero, mama, próstata, colorrectal) y de la misma manera que en la población general. Sin embargo, no hay evidencia sólida que demuestre la eficacia de estas medidas para reducir la frecuencia de tumores postrasplante,28 aunque sien la minimización del riesgo de transmisión de un eventual tumor.
Debido a la escasez de donantes, el uso de donantes cadavéricos es un antecedente de neoplasia que ha sido explorado en diversos estudios. Existeinclusive un reporte de trasplantes renales cuyo órgano presentaba tumoraciones inferiores a 3 cm y que pudieron ser extirpados en la cirugía de banco.29 Los registros de Australia, Reino Unido y Estados Unidos sobre el uso de órganos de donantes, que presentaban ciertos tumores del sistema nervioso central, no han demostrado transmisión luego de más de 1500 implantes de más de 500 donantes.25,30-31 En relación alo anterior, los órganos de donantes con tumores del sistema nervioso central, limitados al mismo y de bajo grado de anaplasia, son generalmente aceptados por la mayoría de los equipos de trasplante. Algo similar ocurre con los tumores de piel no melanoma y carcinomas in situ, lo que pone en discusión el uso de órganos de estos pacientes en donantes con otro tipo de neoplasias.
Receptores con antecedentes tumorales
En pacientes con antecedentes de tumores pretrasplante, el riesgo de recurrencia es, generalmente, bajo (alrededor del 2,4% en algunas series).32Esto se debe al cribaje que se realiza en estos casos antes de aceptarlos en lista, diferenciando el tipo, extensión y localización del cáncer considerado.
Se ha reportado también menor tiempoentre la recurrencia o aparición de un segundo tumor en este grupo de pacientes cuando secompara la aparición de un primer tumor en pacientes sin antecedentes (6,6 años versus 9,9 años).32-34 Respecto del tiempo de espera, luego de ser diagnosticado, un tumor determinado varía entre tumores que no implican un tiempo fuera de la lista de espera (tumores cutáneos no melanoma, carcinoma in situ) hasta la contraindicación del trasplante (melanoma invasivo, cáncer colorrectal avanzado).35-36Actualmente,están en revisión continua y varían según la localización, extensión e histología del tumor. La disponibilidad de nuevos tratamientos también influye en la incorporación de pacientes en lista de espera que antes no eran tenidos en consideración.
Detección y tratamiento de tumores en paciente en diálisis
Al igual que en el caso de los donantes vivos, las guías recomiendan el mismo screening de tumores que para la población general del país de residencia del paciente.37-42El objetivo es evitar el trasplante en pacientes con pobre pronóstico y evitar la exacerbación del cáncer con el tratamiento inmunosupresor. Dado que, como se mencionó previamente, los pacientes en diálisis presentan mayor riesgo de desarrollo de neoplasias, un screening más frecuente y exhaustivo sería recomendable. Por otro lado, un estudio demasiado exhaustivo puede llevar a estudios secundarios con sus consecuentes costos, riesgos y retraso de la inscripción en lista.
Screening tumoral en pacientes trasplantados
De los estudios realizados en la población surge que hay evidencia suficiente sobre el beneficio del screening y diagnóstico precoz, en la población general, de tumores de mama (mediante mamografía) y colorrectales (mediante detección de sangre oculta en materia fecal).43-44) Las guías clínicas de trasplante, generalmente, concuerdan en sumar al screening recomendado en la población general, por ejemplo un examen de piel anual, dada la elevada frecuencia de tumores no melanomas ya mencionada.
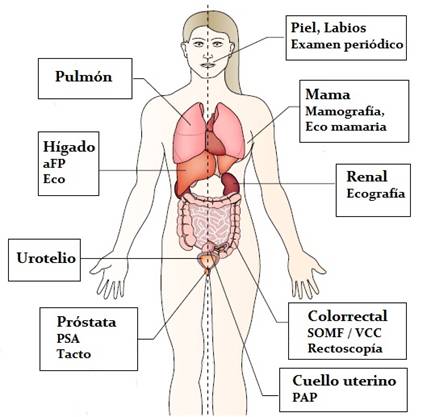
En la Argentina, la contaminación del agua de red con arsénico (hidroarsenicismo crónico endémico, HACRE) en muchas áreas de nuestro país, es un factor que potencia para el desarrollo de tumores cutáneos y, si bien no ha sido específicamente estudiado en la población trasplantada, es un factor a considerar y evitar.45El estudio de la citología cervical también ha mostrado ser de utilidad en esta población al igual que en la población general.46-47Es importante reconocer que, en la era de la medicina de precisión, se deben individualizar los estudios solicitados según el perfil de riesgo de cada paciente, por sobre una estrategia que englobe a todos los trasplantados.48En la Figura 1 se resumen las sugerencias de seguimiento anual en este grupo de pacientes.
Se debe mencionar que en el seguimiento para un eventual hepatocarcinoma se recomienda realizar estudios en aquellos pacientes de riesgo y no en todos los trasplantados.Respecto a los casos de PTLD (de su sigla en inglés Post-transplant Lymphoproliferative Disease, trastornos linfoproliferativos postrasplante), dado que algunos de ellos se relacionan con la positivización del virus de EBV (Epstein-Barr virus), se recomienda realizar cargas virales en forma periódica, en especial en la población pediátrica, teniendo siempre en mente la realización de biopsias en masas tumorales ganglionares, así como la sospecha cuando este se presenta en localizaciones atípicas (sistema nervioso central, tubo digestivo, injerto).
Conductas ante un diagnóstico de cáncer en el trasplantado renal
El enfoque del paciente trasplantado renal con neoplasias es un proceso complejo. La nefrotoxicidad de los agentes quimioterápicos, las glomerulopatías o nefropatías asociadas a tumores o al tratamiento, el riesgo de rechazo relacionado con el descenso de la inmunosupresión o con agentes terapéuticos específicos, son algunos de los tópicos a tener en cuenta en este contexto. Se ha reportado en grandes series internacionales que la población general no trasplantada diagnosticada de cáncer, presenta entre el 18 y el 25%49-51mayor frecuencia de ERC (enfermedad renal crónica) que la población general. No queda claro, como se ha mencionado previamente, si implica al tumor en sí como causa del daño renal o bien la enfermedad renal como predisponente al tumor.
El tratamiento inmunosupresor, que se realiza con la finalidad de evitar el reconocimiento del injerto como algo “no propio”, también bloquea el mecanismo que el organismo utiliza para realizar el clearance de células tumorales, por lo tanto,el consecuente aumento en la presencia de tumores en aquellos que reciben inmunosupresión en forma crónica.23Al respecto, hay consenso para reducir la inmunosupresión en estos pacientes, en especial en los casos vinculados a virus oncogénicos. Sin embargo, esto debe ser cuidadosamente contrabalanceado por el riesgo de rechazo que implica.
Excepto en los casos de PTLD, donde la reducción de la inmunosupresión se ha vinculado con hasta un 37% de remisión completa (con un costo de un 32% de incidencia de rechazo),52en el resto de los tumores sólidos no se ha demostrado que sea de utilidad el tratamiento aislado.53El riesgo global de padecer cáncer está más vinculadoa la intensidad y a la duración de la inmunosupresión que a un agente en particular. Si bien algunos agentes han sido relacionados con mayor fuerza a determinadas neoplasias (agentes antilinfocitarios con PTLD, por ejemplo) los hallazgos para cada fármaco son contradictorios. Es posible que haya diferencias entre las diversas drogas, pero estos efectos están superados ampliamente por otros factores de riesgo: sexo, tabaquismo, enfermedades subyacentes, etc.)52. Por tanto, tampoco está claro qué inmunosupresor determinar para suspender o disminuir su dosis.
Rol de los imTOR
Los inhibidores del Mammalian target of rapamycin (imTOR) han sido utilizados tanto en la prevención del rechazo agudo en pacientes trasplantados, como en algunos tipos de tumores con cierto éxito, motivo por el cual constituye estrategia considerada en este contexto. Han demostrado ser eficaces como tratamiento de Sarcoma de Kaposi, PTLDy tumores cutáneos no melanoma.54-59 En otro tipo de tumores, su utilidad es discutida, existen reportes en ambos sentidos.60-61
Nefrotoxicidad de agentes antineoplásicos
La nefrotoxicidad relacionada con la quimioterapia convencional, pero también la vinculada con los nuevos inhibidores de los checkpoints, inmunoterapia y diversos agentes utilizados actualmente en el tratamiento del cáncer, también puede vincularse con trastornos hidroelectrolíticos y de ácido-base. En la Tabla 3 se sintetizan los efectos adversos renales más frecuentemente observados de los diferentes agentes terapéuticos.62 Los fármacos favorecen el reconocimiento inmunológico de los tumores (sobre todo los inhibidores de la coinhibición), “inflamando” el tumor para que pueda así ser reconocido y atacado por el sistema inmune. Aunque, lógicamente, acarrean un elevado riesgo de rechazo, han sido utilizados con éxito en pacientes trasplantados.60
El daño renal por radiación, tanto interna como externa, aunque no en la radiación diagnóstica, suele presentarse clínicamente comonefropatía aguda o crónica, pudiendo asociarse a hipertensiónmaligna. Las lesiones histológicas renales observadas implican daño endotelial y trombosis capilar con posterior evolución hacia la fibrosis. Esto, si bien se ha observado en riñones nativos, puede presentarse también en el trasplante.63
Tabla 3 Nefrotoxicidad en tratamientos antineoplásicos. Tomado de Francisco60MAT: microangiopatía trombótica; NIA: Nefritis intersticial aguda; NTA: necrosis tubular aguda; IRA: insuficiencia renal aguda; HER 2: human epidermal growth factor receptor 2; BRAF: gen codificante de proteína B-Raf; VEGF: factor de crecimiento vascular endotelial; GEFyS: glomeruloesclerosis focal y segmentaria; HGFR: hepatocyte growth factor receptor
| Quimioterapia convencional | ||
|---|---|---|
| Agente | Lesiones renales | |
| Platino | NTA, MAT, fibrosis crónica intersticial, pérdida de sal, Sme de Fanconi, hipomagnesemia | |
| Ifosfamida | NTA, diabetes insípida nefrogénica | |
| Metotrexato | Nefropatía por cristales | |
| Premetrexed | NTA, MAT, NIA, atrofia tubular, fibrosis intersticial | |
| Gemcitabina | MAT | |
| Mitomicina | MAT | |
| Melfalán | IRA, hiponatremia | |
| Ciclofosfamida | Cistitis hemorrágica, hiponatremia | |
| Antraciclinas | Glomerulopatía colapsante, MAT, hialinosis focal, lesiones glomerulares mínimas | |
| Inhibidores EGFR | ||
| Cetuximab | IR Aguda, hipomagnesemia | |
| Panitumumab | Hipomagnesemia, alteraciones electrolíticas | |
| Erlotinib | Alteraciones electrolíticas | |
| Gefitinib | Alteraciones electrolíticas | |
| Bevacizumab | HTA, proteinuria, MAT | |
| Afibercept | HTA, proteinuria, MAT | |
| Axitinib | HTA, proteinuria, MAT | |
| Sunitinib | HTA, proteinuria, MAT | |
| Sorafenib | HTA, proteinuria, MAT | |
| Pazopanib | HTA, proteinuria, MAT | |
| Vandetanib | HTA, proteinuria, IRA, Litiasis renal, hidroelectrolítica | |
| Ipilimumab (CLA4) | Lesiones glomerulares mínimas, nefropatía lupus-like, NIAg | |
| Nivolimumab (PD1) | NIA, HTA, proteinuria, hipofosfatemia | |
| Pembrolizumab (PD1) | NIA | |
| Atezolizumab (PDL1) | NIA | |
| Avelumab (PDL1) | NIA | |
| Durbalumab | NIA | |
| Tratamientos diana | ||
| Inhibidor HER 2 | Trastuzumab | HTA |
| Inhibidor BRAF | Vemurafamib | NTA, Proteinuria, GEFyS, Fanconi, hiponatremia, hipocalcemia |
| Dabrafenib | NIA granulomatosa, IRA, Hipofosfatemia | |
| Inhibidor MEK | Trametinib | IRA, hipofosfatemia, Quistes renales |
| Inhibidor HGFR | Crizotinib | |
| Inhibidores del Proteosoma | Bortezomib Carfilzomib | MAT MAT, NTA, Lisis Tumoral |
| Inhibidores de Tirosin Kinasa | Imatinib | IRA, hipofosfatemia |
| Anti IL6 | Siltuximab | Hipercalcemia, hiperuricemia |
Como parte de la inmunoterapia, una de las nuevas modalidades terapéuticas es el uso de células T CAR (Chimeric Antigen Receptor). Esta terapia requiere extraer sangre de los pacientes y separar los linfocitos T, que son modificados genéticamente para producir receptores en sus superficies, llamados receptores de antígenos quiméricos (CAR). Estos receptores sintéticos permiten estos que los linfocitos reconozcan y se unan a un antígeno tumoral, en este caso. Luego se multiplican en forma artificial para, finalmente, ser infundidas, luego de una linfodepleción, mediante quimioterapia. De esta forma, estas células atacan selectivamente a las células que expresen el antígeno para el que fueron diseñadas.Este tratamiento no está exento de efectos secundarios serios, tales como el síndrome de liberación de citocinas o el síndrome de lisis tumoral.64 El síndrome de lisis tumoral también se ha reportado en linfomas no Hodgkin, leucemias agudas linfocíticas, linfoblásticas o mieloides, y, menos frecuentemente, en leucemias crónicas, mieloma y tumores sólidos. Se relaciona,además, con la aparición de complicaciones hidroelectrolíticas: hiperuricemia, hiperfosfatemia, hipocalcemia e hiperkalemia.
Finalmente, el seguimiento oncológico y la respuesta al tratamiento,por lo general, implica la repetición de estudios por imágenes, que muchas veces requieren de la administración de contraste endovenoso. La dosis acumulativa de contraste yodado,en procedimientos repetidos, aumenta el riesgo de lesión renal.65-66 De hecho, en las GuíasKDIGO se recomiendademorar la reexposición en pacientes con cáncer que han presentado lesión renal.67 Independientemente de la elevación de los valores de urea y creatinina, hay datos que evidencian injuria renal sin variación en la función, también conocida como alteración de la reserva funcional renal, por lo cual no puede descartarse el daño renal subclínico sin aumento de la creatinina.68 Se han postulado biomarcadores de injuria renal, tales como el inhibidor tisular de metaloproteinasa 2 o la proteína de fijación al factor de crecimiento insulino símil 7 (IGFBP-7).68
CONCLUSIONES
El cáncer es una causa frecuente de morbimortalidad en la población trasplantada renal, estimándose un incremento de dos a tres veces en promedio con la frecuencia de tumores, que se presenta a edades más tempranas y con histología más agresiva que en la población general. La prolongación de la vida de estos pacientes y el aumento del tiempo de seguimiento,es cada vez más frecuente frente a la presentación de primeros, segundos y terceros tumores, en relación a individuos no trasplantados. Los virus oncogénicos, la alteración de la inmunovigilancia relacionada a la inmunosupresión, la insuficiencia renal per se, los agentes quimioterápicos, que condiciones el daño renal, son algunos de los factores que relacionan ambas patologías. El seguimiento de este grupo de pacientes es complejo, y requiere ser más específico según el paciente y el tumor diagnosticado, al punto de que en muchos lugares del mundo se encuentra en desarrollo la subespecialidad de onconefrología.
Existen bases de datos mundialmente conocidas que registran los diferentes tipos de tumores y su evolución en la población general (Surveillance, Epidemiology and End Results Program, SEER);69de tumores en poblaciones en diálisis o trasplantada (ANZ DATA, base de datos de Australia y Nueva Zelanda, entre otros regisros);70 oespecíficamente en trasplantados (IPTTR, Israel Penn Transplant Tumor Registry),71 así como la transmisión de tumores desde donantes (NOTIFY Library),72 entre otras muy conocidas. Desde la Comisión de Trasplante Renal, de la Sociedad Argentina de Trasplante, creímos importante crear un registro interactivo de tumores en trasplante de órganos sólidos que represente lo observado en nuestra población. Tal registro, entendimos, debería ser nutrido por los especialistas que trabajamos en trasplante y, a su vez, los datos deberían poder ser consultados por quienes así lo deseen. De tal forma creamos el Registro Argentino de Tumores en Trasplante de Órganos Sólidos, para el cual se intentó lograr una carga de datos sencilla, al tiempo que involucre una cantidad significativa de datos, pasible luego de ser analizados. Invitamos a todos los médicos del país que trabajen en unidades de trasplante a participar del registro, ingresando aquellos tumores diagnosticados, o bien que hayan fallecido por causa tumoral en el corriente año.73
Conflicto de intereses: Los autores declaran no poseer ningún interés comercial o asociativo que presente un conflicto de intereses con el trabajo presentado.