Introducción
El lupus eritematoso sistémico (LES) es una enfermedad crónica, inflamatoria y autoinmune que presenta un extenso espectro de signos, síntomas y manifestaciones de laboratorio.
Las anormalidades hematológicas incluyen: anemia, trombocitopenia y leucopenia; esta última, a su vez, puede ser por neutropenia, linfopenia, o ambas.
La neutropenia es un hallazgo de laboratorio que puede apreciarse en varias enfermedades. Su aparición en el LES es relativamente infrecuente, pero de relevancia clínica. Puede ser causada por la enfermedad per se o ser secundaria al tratamiento instaurado; esto último es lo más frecuente.
Cuando se trata de una manifestación del LES, puede deberse a la disminución de la producción de neutrófilos en la médula ósea, o al secuestro y destrucción periférica de los mismos mediante opsonización por autoanticuerpos.
Los objetivos de este trabajo fueron conocer la prevalencia de neutropenia al diagnóstico de LES, evaluar su relación tanto con las manifestaciones clínicas o de laboratorio puntuales relacionadas con el LES, como con mayor actividad, daño, infección o muerte.
También fue determinar la prevalencia de la neutropenia al diagnóstico de LES en nuestro centro y, secundariamente, conocer su correlación con otras variables de la patología y pesquisar si se relaciona con una mayor probabilidad de infecciones.
Materiales y métodos
Se obtuvieron datos demográficos, clínicos y de laboratorio de historias clínicas electrónicas de una cohorte de lupus del Sanatorio Güemes (Ciudad Autónoma de Buenos Aires, Argentina) al momento del diagnóstico de la patología, desde enero de 2010 a diciembre de 2020. Se incluyeron sujetos con diagnóstico de LES mediante los criterios Systemic Lupus International Collaborating Clinics (SLICC 2012). Se excluyeron pacientes con diagnóstico de lupus cutáneo crónico como única manifestación, aquellos con dudoso diagnóstico de LES vs enfermedad mixta del tejido conectivo vs síndrome de superposición, y pacientes con diagnóstico de LES, pero de quienes no se disponía del hemograma al momento del diagnóstico.
Se consignaron los datos en una hoja de cálculo. Se dividieron en dos grupos: con neutropenia (definida como recuento absoluto <1.500/mm3) y sin neutropenia. Dentro del primero, se incluyó un subgrupo de neutropenia severa definida como un recuento absoluto de neutrófilos<500/mm3. De acuerdo con el Systemic Lupus Erythematosus Disease Activity Index 2k (SLEDAI-2k), se definió leucopenia como recuento <3.000/mm3 y plaquetopenia como un recuento <100.000/mm3.
Se realizó un análisis multivariado para evaluar la presencia de correlación entre: neutropenia y las manifestaciones clínicas, los dominios de afectación del LES, la actividad según SLEDAI-2k, el daño acumulado al diagnóstico por SDI (Systemic Lupus International Collaborating Clinics/American College of Rheumatology - SLICC/ ACR - Damage Index), los autoanticuerpos hallados y la presencia de síndromes de Sjögren y antifosfolipídico, las infecciones y muerte.
Para el análisis se utilizó el software EpiInfo© v7.2 del CDC. Para la estadística descriptiva se empleó media +/- desvío estándar o mediana +/- rangos intercuartilos según distribución. T-Test, U de Mann-Whitney, X2, según correspondiera. Se consideró como estadísticamente una p≤0,05.
Resultados
Se incluyeron 70 pacientes, 59 (84%) mujeres, la edad media al diagnóstico de LES fue de 38,6 años (DS 18-72).
Del total, 24 pacientes (34%) presentaron leucopenia, 30 (42,8%) linfopenia y 12 (17%) neutropenia. La misma fue severa en dos (2,8%).
Se observó plaquetopenia en ambos grupos, en un total de seis pacientes (8,5%): dos (16,67%) en los neutropénicos y cuatro (6,90%) en el resto.
Dentro de los pacientes con leucopenia (n=24) se detectó: neutropenia en 12 (50%), linfopenia en 10 (41%) y neutropenia severa en dos (8,3%).
Dentro del grupo con neutropenia (n=12), se halló infección por virus de Epstein-Barr (VEB) (IgM +) en uno. A tres de los restantes 12 pacientes se les realizó el panel viral (VEB, CMV, parvovirus B19, Coxsackie), con resultado negativo. Se realizó PAMO/BMO en un solo paciente, que fue normal.
Solamente dos de los 12 pacientes neutropénicos presentaron infección concomitante, siendo ambas sepsis a foco urinario por E. coli multisensible, una en el grupo de neutropenia severa. Ambas fueron tratadas satisfactoriamente.
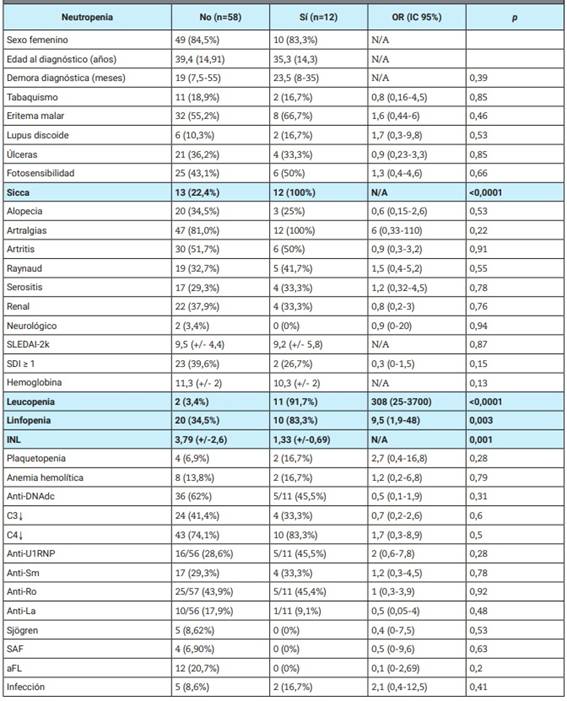
Los dos pacientes con neutropenia severa recibieron factor de crecimiento de colonias de granulocitos y monocitos (GM-GSF), sin presentar eventos adversos. Ninguno de los 12 pacientes con neutropenia falleció al momento del diagnóstico de LES (Tabla 1).
Discusión
La neutropenia en patologías autoinmunes puede tener causas diversas aún no del todo conocidas. Ante su hallazgo debe considerarse un abanico de posibilidades: que sea una manifestación de la enfermedad basal del paciente, que presente superposición con otra enfermedad que pueda provocarla, o bien que la neutropenia se trate de un efecto adverso propio del tratamiento que el paciente reciba1,9.
La neutropenia inmune se clasifica en primaria o secundaria en base a si existe una enfermedad autoinmune subyacente, o si se trata de un hallazgo aislado en el laboratorio2.
La prevalencia de neutropenia en lupus se estima en un 20-40%. En este trabajo se encontró una prevalencia levemente menor a la reportada; sin embargo, aquí solamente se ha considerado la prevalencia de neutropenia al diagnóstico de lupus y no durante la evolución de la patología.
Existen varias teorías acerca de su origen, si bien se cree que la base fisiopatológica sería por autoanticuerpos antineutrófilos13,14,16,17,20. Los mecanismos posibles son: la inhibición de precursores granulocíticos en la médula ósea, la opsonización y fagocitosis, la marginalización de pool vascular, el secuestro esplénico, la destrucción periférica, o la apoptosis de neutrófilos maduros circulantes1,17,18.
La inhibición de precursores medulares estaría dada por un mecanismo autoinmune, dado que se observaron depósitos de IgG en mielocitos y promielocitos de pacientes lúpicos con neutropenia3,4. Asimismo, in vitro, se detectó que los linfocitos T de pacientes lúpicos inhiben la formación de unidades formadoras de colonias de la médula ósea1,4.
Las trampas extracelulares de neutrófilos (neutrophil extracellular traps, NETs) son estructuras derivadas de la muerte de neutrófilos a través de un proceso singular distinto de la necrosis o la apoptosis. Cuando un estímulo antigénico propio o externo se une a receptores en la membrana de los neutrófilos, se activa una cascada que determina la liberación de radicales que causan oxidación y peroxidación, provocando la fragmentación de la membrana nuclear y la liberación de histonas, gránulos y antígenos proteicos a la matriz extracelular, los cuales son reconocidos y fagocitados por los macrófagos. Luego estos son presentados a los linfocitos B, que sintetizan anticuerpos contra estos autoantígenos perpetuando la inflamación17. En los pacientes con LES, la NETosis puede desencadenar la actividad de la enfermedad, y la disminución de la depuración de estos NETs puede perpetuarla25-28.
En cuanto a la opsonización, existe una relación inversa entre el recuento de neutrófilos y la habilidad del suero del paciente de opsonizar granulocitos para su reconocimiento y destrucción por monocitos. En un estudio se observó una relación directa entre la IgG antimembrana del neutrófilo con la actividad opsónica y un nivel elevado de actividad del complemento5. Otro trabajo demostró una relación inversa entre el recuento de neutrófilos con la capacidad de unión de C3. Estos resultados podrían sugerir una posible activación y muerte de neutrófilos mediada por complemento y gatillada por los autoanticuerpos6,13,14.
En un estudio de 72 pacientes con LES, los anticuerpos anti-Ro/SS-A se asociaron a un menor recuento de neutrófilos. El antígeno de membrana de los neutrófilos, al cual se dirige el anti-Ro/SS-A, es una proteína de 64 kD distinta a la proteína de 60 kD contra la cual se dirige el anti-Ro/SS-A habitualmente. La reactividad cruzada se debe a que tienen similitudes en distintas regiones de la cadena peptídica. Esto significa que, por más que el paciente lúpico con neutropenia presente anticuerpos anti-Ro/SS-A, no necesariamente tendrá enfermedad de Sjögren7.
En este trabajo no se encontró una mayor positividad de anticuerpos anti-Ro/SS-A en los pacientes neutropénicos incluidos. La neutropenia al diagnóstico de LES no se asoció con síndrome de Sjögren ni con mayor positividad de anticuerpos anti-Ro/SSA ni anti-La/SSB, si bien se ha determinado que el 100% de los pacientes con neutropenia tenía síntomas Sicca.
Otro estudio halló una banda de 64 kDA en pacientes con factor reumatoideo23, pero la significancia clínica de esto se desconoce.
En 2020 se publicó un estudio retrospectivo de la cohorte franco germana Lupus BioBank of the Upper Rheim (LBBR) en el cual, en 998 pacientes con lupus, se reportó una prevalencia de neutropenia del 21%, y su asociación con trombocitopenia (OR 4,11 (2,57-10,3)), linfopenia (OR 4,41 (2,51-11,5)) y C3 disminuido (OR 1,91 (1,03-4,37)). Se trata de la cohorte más grande que describió neutropenia en LES11. En este estudio se mencionó la neutropenia a lo largo de la enfermedad y no solo al diagnóstico del LES. Es importante destacar que el punto de corte de neutrófilos considerado como neutropenia fue <1,800/mm.
En varios estudios se mencionó que el hallazgo de neutropenia se correlaciona con flares más severos del lupus y anticuerpos Anti-DNAdc. A diferencia de estos trabajos, en el presente no se encontró que nuestros pacientes neutropénicos hayan presentado un score SLEDAI-2k más alto que los demás.
Podría suponerse que la neutropenia traería aparejado un mayor riesgo de infección, pero hasta la fecha los datos son controvertidos21,22. En la cohorte LBBR no pudo relacionarse la neutropenia con un aumento a la susceptibilidad de infecciones11, mientras que un estudio prospectivo de la cohorte Coímbra señaló que los pacientes lúpicos con neutropenia tenían mayor tasa de infecciones del tracto respiratorio superior12. Un estudio mexicano comparó los desenlaces de pacientes lúpicos con manifestaciones hematológicas contra un grupo control con LES, pero sin dichas manifestaciones, y halló una mortalidad intrahospitalaria mayor (16,5% vs 4,8%; p<0,001)24. Si bien hemos hallado el doble de prevalencia de infección en los pacientes neutropénicos, esta diferencia no demostró mayor mortalidad ni logró significancia estadística.
El tratamiento de la neutropenia asociada a LES se basa en el abordaje de la patología de base, y eventualmente con el uso de estimulantes de colonias de granulocitos. Su uso se ha correlacionado con reactivación hematológica y del sistema nervioso central8, por lo que deberían emplearse con cuidado y monitoreo estrecho en pacientes selectos considerando potenciales riesgos y beneficios19. Generalmente se indican cuando la neutropenia es severa y se sospecha infección concomitante10. En este trabajo no se encontró asociación entre la presencia de depleción neutrofílica con un mayor número de infecciones al diagnóstico de LES, ni que las mismas fueran más severas que en los pacientes no neutropénicos.
Se ha observado correlación estadística entre neutropenia al diagnóstico de LES y linfopenia, pero no con otros parámetros de actividad del LES, ni con puntaje mayor del SLEDAI-2k, sin poder imputar una implicancia clínica a la primera.
El índice neutrófilo linfocito (INL) es un marcador de laboratorio que puede obtenerse fácilmente del hemograma. Varias son las publicaciones que mencionan que un INL ≥3 se correlaciona con inflamación, tanto en el lupus29 como en otras enfermedades inflamatorias, infecciones y cáncer. En este trabajo se observó, con significancia estadística, que al diagnóstico de LES el grupo neutropénico tenía un INL menor que su contraparte, que promedió un valor por encima de 3. Esto podría suponer que, en nuestra cohorte, el grupo con recuento normal de neutrófilos presentaría un estado inflamatorio mayor que los neutropénicos. Sin embargo, este grupo no presentó datos de mayor inflamación: SLEDAI-2k más elevado, mayor porcentaje de hipocomplementemia, índice de daño, o mayor porcentaje de compromiso de ciertos órganos o sistemas.
Se describe que el uso de GM-GSF se asoció con flares de LES19, los cuales se usaron de forma prudente. En nuestra cohorte, solamente dos pacientes recibieron GM-GSF, sin presentar eventos adversos.
Dentro de las limitaciones de este trabajo, se menciona el número de pacientes incluidos y que, por tratarse de un estudio transversal, se desconoce su evolución a lo largo del tiempo.
Deberían realizarse estudios prospectivos con un mayor número de pacientes para evaluar si la neutropenia al diagnóstico de LES tiene alguna significancia clínica en la evolución de estas personas.
Conclusiones
Nuestro estudio demostró una prevalencia de neutropenia ligeramente inferior a la descripta en la bibliografía. La presencia de neutropenia se ha correlacionado con mayor prevalencia de síntomas Sicca, pero sin mayor prevalencia de anticuerpos anti-Ro/SS-A ni La/SS-B, ni con el cumplimiento de criterios diagnósticos para enfermedad de Sjögren. Además, la neutropenia se asoció a mayor leucopenia y linfopenia, menor índice de neutrófilos/ linfocitos, pero sin detectar peores variables clínicas al diagnóstico de LES (gravedad del LES, riesgo de infección ni muerte).
El grupo de neutropénicos presentó el doble de infecciones con respecto al no neutropénico, sin embargo, esto no tuvo correlación estadísticamente significativa debido, quizás, al bajo número de la muestra.