Introducción
La vasculitis por inmunoglobulina A (VIgA), anteriormente llamada púrpura de Schonlein Henoch (PSH), es la vasculitis sistémica más frecuente en la infancia, asociada a depósitos de inmunoglobulina A (IgA) en pequeños vasos. Su incidencia anual es variable según las áreas geográficas; oscila entre 3 y 27 casos por cada 100.000 menores de 17 años. Ocurre a cualquier edad, pero su pico es de los 4 a 6 años. No se conoce con exactitud su patogenia; pueden desencadenarla diversos factores medioambientales, infecciones de la vía aérea superior, fármacos, vacunas y neoplasias.
Se caracteriza por púrpura palpable no trombocitopénica en todos los casos, que puede aparecer antes, durante o posteriormente a otros signos y síntomas característicos, como las artralgias y/o artritis, afectación gastrointestinal y compromiso renal, con pronóstico favorable en la mayoría de los casos1,2,3,4.
SARS-CoV-2 es un virus ARN que causa la enfermedad COVID-19. Este virus afecta frecuentemente el sistema respiratorio con presentaciones que varían desde una rinitis hasta condiciones severas y potencialmente fatales como el síndrome de distress respiratorio, shock séptico o síndrome de inflamación multisistémica (multi-system inflammation syndrome, MIS)3,4. Puede tener manifestaciones hematológicas, cardíacas, renales y dermatológicas que se asemejan a otros cuadros como la enfermedad de Kawasaki4,5,6.
El objetivo de este trabajo fue reportar el caso de un niño de 5 años de edad con clínica de VIgA/PSH como forma inicial de presentación, a quien posteriormente se le diagnosticó infección por SARS-CoV-2.
Caso clínico
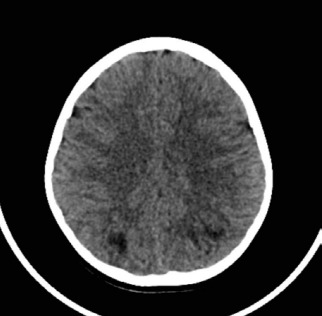
Al inicio de la pandemia por SARS-CoV2 en Argentina, un niño de 5 años de edad consulta a un hospital general de la provincia de Buenos Aires por dolor abdominal intenso, vómitos, diarrea y petequias en miembros inferiores de 5 días de evolución, con hematuria microscópica y cilindros hemáticos, sin fiebre. Se descarta conducta quirúrgica (ecografía abdominal que informa engrosamiento parietal a nivel de fosa ilíaca derecha) y se sospecha VIgA/PSH, por lo cual recibe dexametasona 0,6 mg/k/día endovenosa con mejoría del cuadro abdominal y resolución de la hematuria. A las 48 horas de su internación presenta melena con descenso del hematocrito sin descompensación hemodinámica y convulsión tónica clónica generalizada asociada a registros de hipertensión arterial interpretada como emergencia hipertensiva; se le realiza tomografía computada de cerebro (TC) (Figura 1) con hallazgos presuntivos de síndrome de encefalopatía posterior reversible (posterior reversible encephalopathy syndrome, PRES), por lo cual se lo deriva al Hospital de Alta Complejidad en Red El Cruce.
Al ingreso en la institución se constata: petequias y púrpura palpable en miembros superiores e inferiores, artralgias en muñecas y tobillos con edema de manos y pies, hipertensión arterial y dolor abdominal (Figura 2).
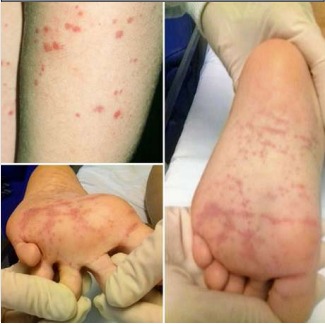
Figura 2: Petequias y púrpura palpable en miembros superiores e inferiores, artralgias en muñecas y tobillos con edema de manos y pies.
Los estudios arrojan leucocitosis, anemia, proteína C reactiva (PCR) elevada con función renal y orina normal, y sangre oculta en materia fecal negativa (Tabla 1).
Tabla 1: Resultados de laboratorio clínico.
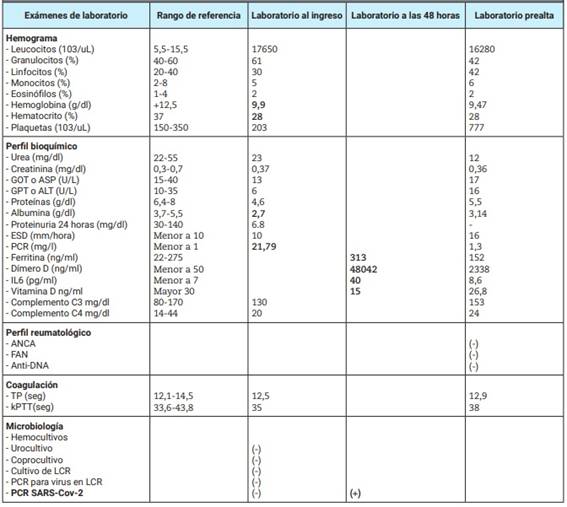
Got: glutámico oxalacetico transaminasa; ASP: aspartato aminoaminotransferasa; GPT: glutámico pirúvico transaminasa; ALT: alanino aminotransferasa; ESD: eritrosedimentación globular; PCR: proteína C reactiva; IL6: interleuquina; ANCA: anticuerpos anticitoplasma de neutrófilos; FAN: factores antinucleares; anti DNA: anticuerpos antinucleares; TP: tiempo de protrombina; KPTT: tiempo de tromboplastina parcial activada; LCR: líquido cefalorraquídeo.
Debido al antecedente de convulsión, se realiza fondo de ojo normal, resonancia magnética nuclear (RNM) de cerebro (Figura 3), donde se observa hiperintensidad de señal en sustancia blanca subcortical parietal bilateral en flair y T2, sin realce luego de la administración de gadolinio y sin cambios en coeficiente de difusión aparente (apparent diffusion coefficient, ADC), pudiendo corresponder a lesiones secundarias a vasculitis.
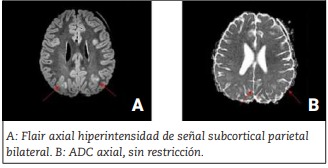
Figura 3: Resonancia nuclear magnética. Hiperintensidad de señal en sustancia blanca subcortical parietal bilateral que restringe en difusión y no realza con contraste pudiendo corresponder a vasculitis, PRES o SARS-CoV-2.
El examen fisicoquímico y el estudio virológico del líquido cefalorraquídeo (LCR) resultan normales, y los cultivos de LCR, sangre y orina, negativos.
Por las características del compromiso cutáneo se considera realizar biopsia de la lesión purpúrica, la cual es desestimada por la mejoría del cuadro dermatológico y abdominal coincidente con el uso de esteroides. En ese momento, teniendo en cuenta la infección emergente de COVID-19, se piden nuevos laboratorios que informan reactantes proinflamatorios elevados (dímero D, IL 6, ferritina), hipoalbuminemia y vitamina D baja. Se solicitan anticuerpos anticitoplasma de neutrófilos (ANCA), factores antinucleares (FAN) y anticuerpos antinucleares (anti-DNA) en búsqueda de otras vasculitis de pequeños vasos, que resultan negativas (Tabla 1). En el ecocardiograma (Figura 4) se observa ecorrefringencia aumentada del tronco de la arteria coronaria izquierda, la bifurcación y la arteria descendente anterior, y se recibe el resultado de PCR SARS-CoV-2 positivo pedida al ingreso a la unidad de internación por protocolo hospitalario, por lo cual el cuadro se reinterpreta como vasculitis sistémica por COVID-19 (SARS-CoV-2).
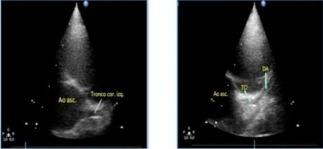
Figura 4: Ecocardiograma. Leve aumento de la ecorrefringencia del tronco de la coronaria izquierda, la bifurcación y arteria descendente anterior, sin dilatación y calibre homogéneo.
Interdisciplinariamente se decide el tratamiento con esteroides, aspirina (AAS), y antihipertensivos (furosemida y amlodipina) para el control de la presión arterial, externándose a los 9 días con evolución favorable y seguimiento ambulatorio. La medicación se suspende gradualmente con control ecocardiográfico normal y restitución completa del cuadro clínico al mes del evento.
Nuestro caso presenta púrpura palpable como criterio obligatorio, y dolor abdominal con sangrado gastrointestinal, artralgias y hematuria. Esta nueva definición proporciona sensibilidad y especificidad para la clasificación de VIgA/PSH del 100% y 87% respectivamente.
Discusión
Nuestro paciente cumplió con los criterios de clasificación de la European League Against Rheumatism/Pediatric Rheumatology International Trials Organization/ Posterior reversible encephalopathy syndrome (EULAR/PRINTO/PRES)1 para VIgA/PSH (Tabla 2).
Tabla 2: Criterios clasificatorios EULAR/PRINTO/PRES para VIgA/PSH.


EULAR/PRINTO/PRES: European League Against Rheumatism/Pediatric Rheumatology International Trials Organization/ Posterior reversible encephalopathy syndrome.
Su clínica inicial fue la afectación del tracto digestivo, presente hasta en el 70% de los pacientes con VIgA/PSH, manifestada con dolor abdominal tipo cólico debido a isquemia intestinal y hemorragia digestiva aguda con melena, hematoquecia o hematemesis. A veces puede presentarse solo con dolor abdominal, apareciendo posteriormente las lesiones purpúricas, simulando un abdomen agudo que puede conducir en ocasiones a una intervención quirúrgica7. Manifestaciones gastrointestinales similares se describieron en la infección por virus SARS-CoV-28.
También presentó manifestaciones dermatológicas compatibles con VIgA/PSH de distribución difusa. La biopsia cutánea en los pacientes pediátricos con VIgA/PSH está reservada para casos con erupción atípica (lesiones extensas o de distribución difusas). En este caso no se realizó teniendo en cuenta la buena evolución de las lesiones en piel y el resultado de la PCR positiva para SARS-CoV-2. Las manifestaciones cutáneas producidas por este virus muestran una gran diversidad, siendo las lesiones maculopapulares uno de los patrones dermatológicos más frecuentemente encontrados. Las lesiones purpúricas maculares o papulares se observan en las superficies palmares y plantares, parecidas a la vasculitis o eritema multiforme. Las lesiones petequiales aparecen en cualquier momento durante el curso de la enfermedad; se localizan en el tronco, glúteos y extremidades, con tendencia a una distribución flexural o periflexural9,10.
El factor desencadenante más común de la VIgA/PSH es una infección previa del tracto respiratorio superior, pudiendo el SARS-CoV-2 haber inducido este proceso en nuestro paciente. El hallazgo característico es la vasculitis leucocitoclástica acompañada de complejos inmunológicos de IgA dentro de los vasos sanguíneos de los órganos afectados.
El virus SARS-CoV-2 ingresa a la célula humana al unirse a los receptores de la enzima convertidora de angiotensina 2 (angiotensin-converting enzyme 2, ACE 2)11. Estos receptores se encuentran en el endotelio vascular, lo cual explicaría la inflamación endotelial generalizada, induciendo posteriormente una respuesta sistémica con producción exagerada y no controlada de citoquinas proinflamatorias, especialmente IL1 e IL612. Estas últimas producen fiebre, intervienen en la activación de la cascada de la coagulación, aumentan los reactantes de fase aguda y serían las causantes de la llamada “tormenta de citoquinas”4,12. Esta infección viral emergente también desencadena una respuesta humoral, entre ellas, la mediada por IgA a nivel sistémico siendo el hallazgo característico la vasculitis acompañada de complejos inmunológicos de IgA dentro de los vasos sanguíneos, conduciendo al desarrollo de enfermedad autoinmune3,4.
No existe una prueba diagnóstica que demuestre la asociación entre vasculitis por IgA/PSH y el virus SARS-CoV-2.
Los pacientes con COVID-19 presentan marcadores inespecíficos de infección e inflamación (proteína C reactiva, procalcitonina, ferritina y LDH), especialmente en aquellos sintomáticos. No existen datos suficientes para conocer qué alteraciones analíticas se asocian con mayor gravedad, aunque la elevación de marcadores de inflamación, la linfopenia y el índice neutrófilos/linfocitos parecen asociarse más frecuentemente a los casos graves13.
Si bien nuestro paciente presentó marcadores proinflamatorios elevados descriptos en la infección por COVID-19, estos hallazgos de laboratorio no son patognomónicos.
Los estudios por imágenes se emplean para descartar otras patologías y para conocer el alcance de la enfermedad. Frente a la expresión clínica de nuestro paciente, los estudios realizados demostraron compromiso vascular de los órganos afectados. Los patrones de neuroimagen más frecuentemente encontrados en niños con afectación neurológica asociada a infección por SARS-CoV-2 fueron similares a la encefalomielitis diseminada aguda, como en nuestro caso. Las complicaciones neurovasculares son menos frecuentes que en adultos y la mayoría evoluciona favorablemente14. Las nuevas técnicas de RM (como inversión-recuperación con atenuación del líquido cefalorraquídeo, difusión, perfusión y angio-RM de alta resolución) aumentan la sensibilidad de la RM en esta patología15,16.
Su fisiopatología no es bien conocida. Se han postulado tres mecanismos principales con probable efecto sinérgico: a) daño neuronal directo del virus; b) efecto desmielinizante de origen autoinmune para o post-infeccioso secundario a la hiperrespuesta inflamatoria; c) lesión del endotelio vascular. En la VIgA/PSH la afectación neurológica puede ser multifactorial: por vasculitis, hipertensión arterial o alteraciones hidroelectrolíticas.
La ecografía abdominal muestra cambios inflamatorios en el íleon terminal, similares en ambas entidades14. El ecocardiograma de nuestro paciente evidenció inflamación de las arterias coronarias. La afectación cardíaca por el virus SARS-CoV-2, presente en un alto porcentaje de pacientes, incluye la disfunción miocárdica, aneurismas de las arterias coronarias, pericarditis, arritmias, shock refractario y/o elevación de biomarcadores cardíacos, como la troponina I o del péptido natriurético cerebral, aun sin compromiso cardíaco importante17.
Al momento del diagnóstico se disponía de bajo nivel de evidencia acerca del tratamiento de la vasculitis desencadenada por el SARS-CoV-2. Sin embargo, considerando la similitud con enfermedades bien conocidas en las que se había demostrado la eficacia de ciertos tratamientos, el uso de esteroides, gammaglobulina y agentes biológicos fueron alternativas válidas ante este nuevo desafío para el equipo interdisciplinario12.
La presentación de nuestro caso tuvo algunas limitaciones: no pudo confirmarse la vasculitis asociada a IgA debido a la falta de confirmación histopatológica, no obstante, la clínica inicial fue altamente sugestiva. Otra limitante fue su presentación al inicio de la pandemia, en la cual la información respecto de las consideraciones diagnósticas y estrategias de tratamiento eran escasas y variadas.
Conclusiones
En un principio no quedaba claro si el virus SARS-CoV-2 fue el causante de la VIgA o si el paciente presentaba ambas entidades de manera simultánea. Si bien reunía criterios clínicos de vasculitis por IgA, la falta de evidencia histológica no permitió confirmarlo. El avance en el conocimiento de la COVID-19 en pediatría nos posibilitó inferir que esta infección viral emergente desencadenó la vasculitis en nuestro paciente, debiendo tener un alto índice de sospecha para un diagnóstico precoz y tratamiento oportuno.