INTRODUCCIÓN
Desmodium incanum (Sw.) DC. es una especie forrajera perenne, apetecible y de buena calidad para los animales (Fernández et al., 1988; Scandaliaris et al., 2013). Es muy común en pastizales naturales de la provincia de Entre Ríos. Se ha determinado que las semillas de esta especie, provenientes de los departamentos Paraná y Diamante de la provincia de Entre Ríos, presentan diferente profundidad de dureza física en el tegumento seminal, lo que se refleja en los niveles de dormición (Gillij et al., 2021). Si bien la cubierta de la semilla otorga la defensa primaria contra el medio ambiente adverso, ya que un tegumento duro la protege de la tensión mecánica, los microor- ganismos y cambios en temperatura y humedad (Yassen et al., 1994) también pueden ser un problema a la hora de la germinación. Esto se debe, en gran medida, a que impide la entrada del oxígeno y del agua necesaria para el desarrollo del embrión y además, ofrece resistencia mecánica al crecimiento de la radícula (Cortés, 1980). El término semilla dura se aplica a la semilla que presenta una cubierta impermeable al agua, que no germina porque su embrión no puede embeber (ISTA, 2016). Esta dormición física, en algunas especies de Fabaceae, se relaciona con diversas caracte- rísticas de las semillas, como la anatomía y la composición de sustancias químicas en el tegumento seminal, que ocasionan diferentes grados en la profundidad de la dormición (Galussi et al., 2019; Gillij et al., 2021).
En la naturaleza, las semillas de una misma especie pueden desarrollarse bajo diferentes condiciones ambientales, lo que provoca diferencias en la dureza del te- gumento seminal y en la dormición física asociada (Quinlivan, 1971).
La dormición representa un mecanismo ecológico fundamental, que permite en el largo plazo el mantenimiento de bancos de semillas en condiciones naturales. Esta característica se encuentra en semillas de especies de las familias Convolvula- ceae, Chenopodiaceae, Fabaceae, Liliaceae, Malvaceae, Solanaceae (Nikolaeva, 1980; Popinigis, 1985; Besnier Romero, 1989; Zimmermann et al., 1998; Baskin y Baskin, 2004; Zeng et al., 2005; Pérez -García, 2008; ISTA, 2016; Orsenigo et al., 2019; Paul et al., 2019 ).
La presencia de semillas duras en las especies anuales invernales de Fabaceae, es un mecanismo de supervivencia fundamental ya que les permite mantener una gran longevidad en el suelo (Carámbula, 1977). En el análisis de germinación en algunas especies de Fabaceae, se menciona la presencia de semillas duras como manifestación de dormición física (Galussi et al., 2013a, 2013b; Galindez et al., 2016; Orsenigo et al., 2019; Paul et al., 2019).
Los tejidos del tegumento seminal en Fabaceae según Esau (1987) y Cortés (1980), mantienen una distribución particular: la epidermis constituida por una capa de macroesclereidas, debajo la hipodermis compuesta por una o más capas de osteoesclereidas e internamente se dispone parénquima lagunoso. Las paredes secundarias de las macroesclereidas y osteoesclereidas pueden tener variaciones en el espesor y en los contenidos de celulosa, hemicelulosa, lignina, taninos, cutina y sustancias pécticas; características que se relacionan con la dormición, dureza y resistencia mecánica (Salisbury y Ross, 1992; Taiz y Zeiger, 1998; Galussi et al., 2015). En este sentido, Van Assche et al. (2003) menciona la presencia de taninos
condensados (compuestos fenólicos) en la cubierta seminal de Lotus corniculatus L. La impregnación de estas sustancias en las paredes secundarias de la semilla le confiere características impermeables (Zavaleta et al., 2003).
Las semillas de D. incanum producidas en áreas naturales de la región compren- dida entre las localidades de Colonia Ensayo y Paraná presentaron un elevado por- centaje de semillas duras (cercano al 95%) con un 90% de embriones viables (Gillij et al., 2021). El modelo de permeabilidad al agua propuesto por Gillij et al. (2021) mostró dureza física de diferentes profundidades en el tegumento seminal, que se tradujo en la ruptura lenta de la dormición y el desarrollo de plántulas normales aun después de 22 meses de almacenamiento. Esta variabilidad hallada en las semillas pertenecientes a una población, coincide con lo mencionado por diversos autores en otras especies de Fabaceae (Nikolaeva, 1980; Moreira de Carvalho y Nakagawa, 1988; Côme y Courbineau, 1992; Galussi et al., 2019). Teniendo en cuenta estos antecedentes, se desprende que las causas relacionadas con el impedimento a la en- trada de agua en las semillas de la especie no están completamente dilucidadas. Por esto, se propuso conocer las características anatómicas y químicas de los tegumentos seminales asociados a los niveles de dormición física en semillas de D. incanum.
MATERIALES Y MÉTODOS
Material biológico
Se trabajó con semillas de Desmodium incanum (Sw.) DC. cosechadas manualmente entre los años 2017-2020, en las localidades de Colonia Ensayo (31°51’14,0’’S y 60º 33’02,0’’O) a 100,1 m snm y Paraná (31°45’44,0”S y 60°31’57,0”O) a 93,1 m snm en la provincia de Entre Ríos (Argentina). En los periodos reproductivos durante los ensayos (noviembre-febrero), la humedad relativa osciló entre el 60 y 72% con temperaturas ambientales promedio de 24 ± 4 °C y precipitaciones de 49 mm a 240 mm. La precipitación anual promedio oscilo entre 1088 mm y 1314 mm para los años en estudio (INTA, EEA Paraná, 2017-2020).
Las semillas seleccionadas para este estudio se observaron con microscopio es- tereoscópico (lupa 10x) y se descartaron aquellas con daños físicos visibles.
Determinación de niveles (grados) de permeabilidad
Los grados de permeabilidad fueron establecidos acorde a los propuestos por Gillij et al. (2021); para ello, en el tiempo cero, inicio del ensayo, las semillas se colocaron en agua destilada a temperatura ambiente en vasos de precipitado de 200 ml, el agua se renovó cada 72 h. Luego, se registró el tiempo transcurrido hasta la imbibición, clasificando y seleccionando las semillas por nivel de permeabilidad según la velocidad de hidratación: grado 1: semillas que se hidrataron completamente antes o hasta 240 h (10 días) de inmersión; grado 2: semillas que se hidrataron entre 1000 h (42 días) y hasta las 5000 h (208 días) de inmersión y grado 3: semillas que aun luego de 6456 h (269 días) de inmersión (momento en que se dio por finalizado el ensayo) no embebieron agua.
Estudio de los tegumentos seminales
Análisis morfológicos y anatómicos del tegumento seminal con microscopía electrónica de barrido (MEB).- Considerando una semilla por replica, se analiza- ron por triplicado tegumentos pertenecientes a los grados 1 y 3 de permeabilidad.
Para la obtención de tegumentos con grado 1 de permeabilidad, se seleccionaron semillas hidratadas en las primeras 240 h y se colocaron en papel de germinación hu- medecido, enrollado y puestos en bolsa de nylon. Se ubicaron en cámara de germina- ción (25 °C) en un ángulo de 45˚. Posteriormente los tegumentos desprendidos de las plántulas germinadas se recolectaron en cajas de Petri y se secaron en estufa a 25 °C. Para la colecta de tegumentos con grado 3 de permeabilidad, se seleccionaron aquellas semillas que no embebieron a las 6456 h, a las mismas se les hizo un corte en el tegumento en la zona distal de los cotiledones, y se dejaron 4 h en agua destilada para la imbibición. Luego se pusieron a germinar, y se procedió del mismo modoque para la obtención de tegumentos de grado 1.
Las muestras se sumergieron en nitrógeno líquido y luego se fracturaron con bisturí. Posteriormente, las secciones se adhirieron con cinta doble faz de grafito y cinta de aluminio sobre un soporte y luego se metalizaron con Au (oro) en un Sputter Coater en Plasma de Argón -aproximadamente 200 Å de espesor- (Sorrivas y Morales, 1986). Se observó, fotografió y comparó cada tegumento seminal en vista superficial y lateral con diferentes aumentos. En sección transversal se identificaron los estratos celulares y las dimensiones de las células presentes. La zona seleccionada para estos estudios fue cercana al punto central (Aniszewski, 2009), observándose el área circundante a dicho punto y la lente.
Los tegumentos seminales se examinaron con un microscopio electrónico de barrido, marca JEOL, modelo JSM-35C. Los registros fotográficos se realizaron con microscopio marca LEO, modelo EVO 40 X VP (Cambridge, England, 2003).
Pared celular de las macroesclereidas en cortes transversales con microsco- pio electrónico de transmisión (MET).- Los tegumentos seleccionados según los grados de permeabilidad (1 y 3), se hidrataron por cuatro días en agua destilada. Luego, se cortó una pieza de tegumento con una hoja de afeitar en trozos de 0,5 mm de lado y se colocó durante 24 h en la solución fijadora (glutaraldehído al 2,5% en tampón fosfato de sodio 0,1 M, pH 7,2). Posteriormente, se realizaron 3 lavados de 15 min con la solución tampón. A continuación, se realizó una post-fijación con tetróxido de osmio 2% por 2 h y se lavó con agua destilada (2 h). Se deshidrató en una serie de concentraciones crecientes de acetona (25%, 50%, 80% y 100%) tres veces, por 15 minutos cada vez. Se incluyó en resina Spurr (Spurr, 1969) en vacío en concentraciones ascendentes de resina (R) - acetona (A) [2A: 1R (2 h); 1A: 1R (2 h); 1A: 2R (16 h)] y finalmente en resina pura 8 h en estufa a 70 °C (16 h). Con posterioridad, se realizaron secciones ultrafinas (75 a 90 nm) con un ultramicróto- mo LKB con cuchilla de diamante. El contraste se realizó con acetato de uranilo, solución saturada en agua, por un minuto y citrato de plomo por un minuto. Las observaciones se llevaron a cabo en un microscopio electrónico de transmisión marca JEOL 100 CXII a 80 KV.
El espesor del tegumento seminal se obtuvo promediando los valores obteni- dos de tres semillas correspondientes a cada grado de permeabilidad (1 y 3). Los promedios de la longitud y el ancho de las macroesclereidas y osteoesclereidas, se calcularon a partir del registro de cuatro células de cada replica (n=12 para cada nivel de permeabilidad). El grosor de la pared celular de las macroesclereidas se obtuvo considerando tres células para cada replica realizada (n=9 para cada nivel de permeabilidad) y tomando los valores mínimos y máximos. Las medidas de lon- gitud se obtuvieron mediante el programa ImageJ® 1.43u (Rasband, 2018) sobre los registros fotográficos digitales tomados.
Los análisis con MEB y MET se realizaron en el Servicio de Microscopía Elec- trónica del Centro Científico Tecnológico Bahía Blanca (CCT-BB). En todos los casos se tomaron registros fotográficos.
Determinación de contenidos de polímeros estructurales, sustancias pécticas, polifenoles, taninos y cutinas.- Los tegumentos con grado 1, 2 y 3 de permeabi- lidad se obtuvieron siguiendo el procedimiento descripto para el análisis con MEB. En el caso de la colecta de los tegumentos de grado 2 y 3 se realizó un pool con los mismos de modo de lograr la cantidad necesaria para dicho estudio. Los procedi- mientos mencionados se realizaron hasta colectar un total de 1,5 g de tegumentos (aproximadamente 1.764 tegumentos), peso necesario para realizar las determinacio- nes analíticas por duplicado de 0,5 g por replica (600 tegumentos aproximadamente). La determinación de polímeros estructurales de la pared celular, polifenoles totales y taninos condensados se realizó en el Instituto de Tecnología Celulósica (Facultad de Ingeniería Química, Universidad Nacional del Litoral, Santa Fe, Ar- gentina). Las muestras de tegumentos fueron analizadas según los métodos citados en Van Soest (1994), que permitió calcular los porcentajes de celulosa, lignina, cutina, hemicelulosa, goma y mucilago; asimismo de contenidos celulares (Cc), que incluye: glucosa, fructosa, sacarosa, galactosa, almidón y fructosanos (protoplastos y sustancias pécticas). La determinación de polifenoles totales se realizó utilizando la técnica de Folin-Denis (Reicher et al., 1981); mientras que para taninos condensados se utilizó el método de la vainillina (Broadhurst y Jones, 1978).
La asociación de los componentes químicos en función de la permeabilidad de los tegumentos, se efectuó a través de un análisis descriptivo según los resultados obtenidos.
Análisis Estadístico
El análisis de los datos de las medidas de longitud de las células para la compara- ción de los tegumentos de diferentes grados de permeabilidad, se realizó mediante la prueba estadística de comparación de media (Prueba t) con un 5% de nivel de significancia, usando el paquete estadístico Infostat (Di Rienzo et al., 2017).
Para las sustancias químicas se calculó el desvío estándar de cada una para ambas repeticiones, las cuales eran de 0,5 g (600 tegumentos aproximadamente).
RESULTADOS
Estudio de los tegumentos seminales
Análisis morfológicos y anatómicos del tegumento seminal con microscopía electrónica de barrido (MEB).- En la superficie de las semilla de D. incanum de grado 1 (Fig. 1A) y grado 3 (Fig. 1B) de permeabilidad se distingue claramente el hilo (anillo y surco hilar), el micrópilo y la lente. En las semillas grado 1 se observó la sutura hilar abierta y un anillo hilar de menor desarrollo en comparación con las grado 3 (Figs. 1C y D). Los tegumentos seminales presentaron diferencias en el patrón de ornamentación según el grado de permeabilidad. En las semillas de grado 1, se observó la cutícula craquelada o finamente partida y un patrón rugulado ligeramente irregular con depresiones en la cutícula (Fig. 1E); mientras que en las de grado 3, el patrón se clasificó como rugulado con pliegues conspicuos (Fig. 1F).
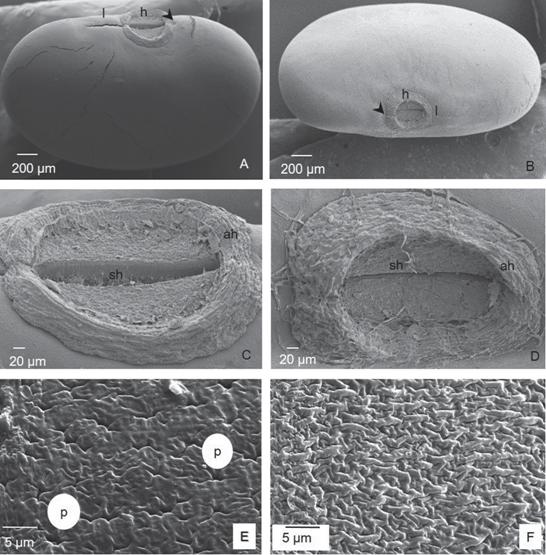
Fig. 1 Desmodium incanum. Exomorfología del tegumento seminal observada con MEB (microscopio electrónico de barrido). 1A, 1C y 1E) Tegumento seminal de semilla de grado 1. 1B, 1D y 1F) Tegu- mento de semilla de grado 3. 1A y 1B) Vista de la semilla. 1C y 1D) Vista superficial de la zona hilar, (ah) Anillo hilar, (sh) surco hilar. 1E y 1F) Vista superficial del tegumento seminal, (p) depresiones en la cutícula. Abreviaturas: cabeza de flecha, micrópilo; h, hilo; l, lente. Fig. 1. Desmodium incanum. Seed coat exomorphology SEM view (scaning electron microscopy). 1A, 1C y 1E) Seed coat grade 1. 1B, 1D y 1F) Seed coat grade 3. 1A and 1B) seed view, (l) lens, (h) hilum, (arrow head) micropyle. 1C y 1D) Surface view of the hilar zone, (ah) hilar ring, (sh) hilar groove. 1E y 1F) Seed coat surface view, (p) cuticular pits.
En el corte transversal de tegumento seminal de semillas grado 1, se registró un grosor de 83 ± 7 μm y en las de grado 3 de 91 ± 8 μm. Se observó una capa de macroesclereidas en empalizada, por debajo, una de osteoesclereidas correspondientes a la testa y luego un parénquima esponjoso de células planas.
En corte transversal se observa que las macroesclereidas, se disponen en un úni- co estrato en empalizada (Fig. 2A-D). No se detectaron diferencias significativas en el largo ni en el ancho en las macrosclereidas (Tabla 1) entre las semillas de diferentes grados de permeabilidad estudiadas, sin embargo, en las semillas de grado 1 (Fig. 2E) se evidenció un mayor desarrollo de espacios intercelulares, en comparación con las de las semillas de grado 3 (Fig. 2F). En la zona de la lente, las macroesclereidas se presentan bi-estratras, con una disposición más laxa en las semillas de grado 1 (Fig. 2A) respecto de las de grado 3 (Fig. 2B). En ambos niveles de permeabilidad (grado 1 y 3) las osteoesclereidas no presentaron diferencias significativas respecto de sus dimensiones (Tabla 1) (Figs. 2C y D).
Pared celular de las macroesclereidas en cortes transversales con microscopio electrónico de transmisión (MET).- Las macroesclereidas se caracterizaron por mostrar contorno poligonal irregular (5-7 lados), de paredes anticlinales alargadas (Fig. 3), dispuestas en un único estrato en empalizada, con espacios intercelulares evi- dentes en semillas de grado 1 (Fig. 3A), en comparación con la compactación regis- trada en las semillas de grado 3 (Fig. 3B). En corte transversal, las macroesclereidas de grado 1 (Fig. 3A) evidenciaron contenido celular y una pared de grosor variable que osciló entre 0,8 a 7,9 μm. En tanto, las semillas de grado 3 (Fig. 3B) mostraron lumen celular y un grosor irregular de pared celular que varió entre 0,7 y 9,2 μm.
Determinación de contenidos de polímeros estructurales, sustancias pécticas, polifenoles, taninos y cutinas.- Los tegumentos de semillas de diferentes grados de permeabilidad presentaron los mismos componentes, sin embargo se registraron diferentes cantidades y baja variabilidad entre repeticiones (Tabla 2). Por un lado, las muestras con diferente permeabilidad evaluadas (grado 1 y muestra de tegumen- tos grado 2 y 3) mostraron igual porcentaje de polifenoles totales. Sin embargo, los tegumentos provenientes de semillas de grado 1 se caracterizaron por presentar un incremento del 96,6% de hemicelulosa (Hc) y del 81,3% de cutina (Cu), respecto a los valores determinados para las muestras de los tegumentos provenientes de semillas de grado 2 y 3 de permeabilidad, mientras que estos últimos se caracterizaron por mostrar una mayor cantidad de taninos condensados (Tc), sustancias pécticas (Cc), celulosa (C) y lignina (L).
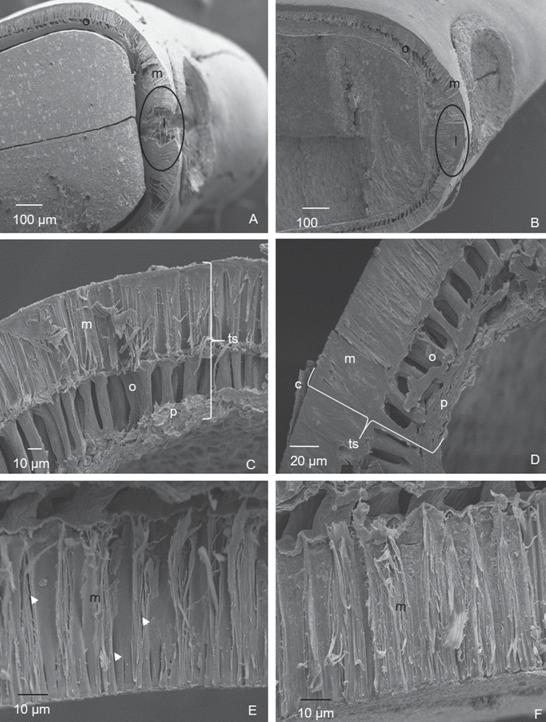
Fig. 2 Desmodium incanum. Corte transversal de tegumento seminal observado con MEB (mi- croscopio electrónico de barrido). 2A, 2C y 2E) Tegumento grado 1. 2B, 2D y 2F) Tegumento grado 3. 2A y 2B) Corte transversal de semilla. (l) lente, (o) osteoesclereidas. 2C y 2D) Vista de tegumento sem- inal, (c) cutícula que se desprende, (m) macroesclereidas, (o) osteoesclereidas, (p) parénquima, (ts) tegumento seminal. 2E y 2F) Vista en detalle de macroesclereidas (flecha) separación entre células. Fig. 2. Desmodium incanum. Seed coat cross-section SEM view (scanning electron microscopy). 2A, 2C y 2E) Tegument grade 1. 2B, 2D y 2F) Tegument grade 3. 2A y 2B) Seed cross-section. (l) les, (O) osteosclereids. 2C y 2D) Seed coat view, (m) Macrosclereids, (o) Osteosclereids, (p) Parenchyma, (ts) seed coat. 2E y 2F) Detail view of macrosclereids (arrow) gap between cells.
Tabla 1 Dimensiones de macroesclereidas y osteoesclereidas en tegumento seminal con diferente permeabilidad de semillas de Desmodium incanum.Table 1Macrosclereids and osteosclereids dimentions of Desmodium incanum seed coats with different seed permeability.
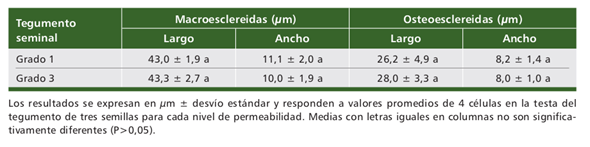
Tabla 2 Determinación de componentes orgánicos (%) en materia seca de tegumentos de diferente permeabilidad de semillas de Desmodium incanum. Table 2. Determination of organic components (%) in dry matter of Desmodium incanum seed coats with different permeability.
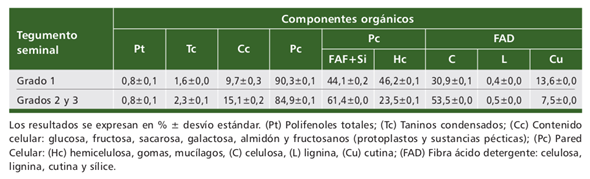

Fig. 3 Desmodium incanum. Corte transversal de macroesclereidas de tegumento seminal obser- vada con MET (microscopio electrónico de transmisión). A) Grado 1. B) Grado 3. (cabeza de flecha) separación entre células, (cc) contenido celular (l) lumen, (lm) laminilla media, (pc) pared celular.Fig. 3. Desmodium incanum. Cross section of the seed coat macrosclereids TEM view (transmission electron microscopy). A) Grade 1. B) Grade 3. (arrow head) gap between cells, (cc) cellular content (l) lumen, (lm) middle lamella, (pc) cell wall.
DISCUSIÓN
La distribución de estratos celulares del tegumento seminal (macroesclereidas, os- teoesclereidas y parenquimáticas) halladas coinciden con lo mencionado por Esau (1987) y Cortés (1980) para las fabáceas. Específicamente en Desmodium motorium (Houtt.) Merr. se determinó que la semilla proviene de un óvulo bitegmico (Unnisa et al., 1994) por lo cual el estrato más interno (células parenquimáticas) podría co- rresponder al tegmen, aunque para la determinación precisa se requiere realizar un estudio ontogenético.
Lersten (1981) define patrones topográficos en leguminosas papilinoideas, de estos el patrón hallado en este estudio para D. incanum resultó ser rugulado, pero se evidenciaron diferencias en el patrón de ornamentación cuticular del tegumento seminal entre grados, siendo rugulado ligeramente irregular con depresiones en la cutícula para el grado 1 y rugulado con pliegues conspicuos para el grado 3. Estos resultados concuerdan con los caracteres de semillas de Medicago sativa L. y Trifolium repens L. para ambos grados de dormición (Galussi et al., 2013a, 2013b, 2015). Las cantidades de ceras y cutina detectadas en los tegumentos se asocian al impedimento al ingreso de agua, alterando la velocidad de hidratación (Van Staden et al., 1989; Ferrer Amorós, 1997).
El grosor del tegumento seminal varió entre 83 y 91 μm en las semillas de los grados 1 y 3 de permeabilidad respectivamente y es conferido principalmente por el tamaño de las macroesclereidas y osteosclereidas. Estos valores son mayores a los encontrados en tegumentos seminales de forrajeras de leguminosas cultivadas como Trifolium repens L. y Medicago sativa L. (Galussi et al., 2019). La profundidad de dor- mición de D. incanum es mayor y en mayor cantidad de semillas, lo cual se diferencia en disitntos niveles de dormición entre las especies mencionadas anteriormente, aunque se debe contemplar también los tipos de sustancias químicas presentes.
En cuanto a la entrada de agua, Baskin y Baskin (2000) mencionan que la ruptura de la dormición en muchas especies con dormición física se daría por la formación de una apertura especializada en la estructura anatómica del tegumento seminal, a través de la cual entra el agua y se hidrata el embrión, que en el caso de las Facebaceae sería a través del lente o estrofiolo. De forma similar, para D. incanum, Gillij et al. (2023) observaron que la entrada de agua se inició por la zona de la lente en semillas de distintos grados de dormición física. Esto indica que las características anatómicas (macroesclereidas bi-estratras, con una disposición más laxa) halladas en la zona de la lente podrían ser uno de los aspectos determinantes para la permea- bilidad del agua, además la compacta empalizada de macroesclereidas y sustancias químicas halladas en el resto del tegumento seminal aseveran este ingreso por la zona antes mencionada, ya que impiden la entrada de agua.
Los valores de celulosa registrados (30,9% y 53,5%) para el grado 1 y para la muestra grado 2 y 3 respectivamente, incluyen tanto a los de pared primaria como secundaria, y estarían dentro de los rangos generales mencionados para los vegetales (Salisbury y Ross, 1992; Taiz y Zeiger, 1998). Sin embargo, la cantidad de hemicelu- losa conjuntamente con gomas y mucilago (46,2%) hallada en tegumentos del grado 1 fue mayor que la mencionada por dichos autores. Dicho componente es característico principalmente de la pared primaria de la célula (Ferrer Amorós, 1997), es un polímero hidrófilo abundante (Jie et al., 2021), pero según la combinación con otras sustancias podría pasar a tener un carácter hidrófobo (Farhat et al., 2017). Funcio- nan como almacén de sustancias de reserva, además realizan funciones reguladoras, estructurales y de control de la expansión celular (Siota, 2014).
Para lignina los valores entre grado 1 y la muestra grado 2 y 3 de permeabilidad fueron de 0,4 y 0,5 %, respectivamente, y resultan menores que los señalados en se- millas de Glycine max (L.) Merr., M. sativa y T. repens (Baciu-Miclaus, 1970; Faner, 2007; Galussi et al., 2015, 2019). La lignina confiere mayor dureza al tegumento seminal, por ser un componente cementante que mantiene unidas las fibras de ce- lulosa, proporcionando también mayor rigidez. Además, brinda impermeabilidad al agua al ser un componente hidrófobo (Ferrer Amorós, 1997; Capeleti et al., 2005; Sandoval, 2005). Esau (1987) menciona que el endurecimiento del tegumento seminal en leguminosas se da por la formación de paredes secundarias muy lignificadas en las macroesclereidas alargadas y la presencia de osteoesclereidas. Barros et al. (2015) señala que la lignificación de una célula puede darse de forma cooperativa. Este hecho permitiría entender las diferencias en la compactación de la empalizada y los espesores de pared celular en las macroesclereidas de tegumentos pertenecientes a semillas de grado 1 y grado 3, con distintos contenidos de lignina que confiere diferente permeabilidad al agua.
Según, Bewley y Black (1986) las semillas acumulan importantes cantidades de fenoles en sus tegumentos seminales que actúan como un filtro para que el oxíge- no no llegue al embrión, inhibiendo su germinación. Estos compuestos presentan actividad antioxidante al proteger el organismo de los radicales libres, moléculas altamente reactivas que pueden dañar el organismo a nivel celular, y pueden proteger plantas y semillas contra enfermedades, depredadores y estrés abiótico, o apoyar sus interacciones con organismos beneficiosos o simbióticos (Padilla et al., 2008; Corso et al., 2020). En el caso de los tegumentos de D. incanum, el contenido de polifenoles totales no presentó diferencias significativas en las semillas de los diferentes grados de imbibición estudiadas.
Por otro lado, los taninos tienen la propiedad de desnaturalizar las proteínas, con lo cual son altamente astringentes, confiriendo la característica impermeable a las semillas (Zavaleta et al., 2003). Además, fortalecen mecánicamente las paredes celulares, como agentes antimicrobianos, en la defensa contra herbívoros, entre otros. Pueden actuar como antioxidantes y, por tanto, limitar la difusión de oxígeno en la cubierta de la semilla (Harborne y Williams, 2000; Pietta, 2000; Debeaujon et al., 2007; Pourcel et al., 2007). Según Demonsais et al. (2020) en Arabidopsis thaliana (L.) Heynh. la pared celular tánica hace que la cubierta de la semilla sea menos permeable a los compuestos externos. En los tegumentos seminales analizados, los taninos condensados se presentaron en mayor proporción (2,3%) en tegumentos de semillas de grado 2 y 3 comparada con las de grado 1 (1,6%), por lo que puede ser un componente determinante en el contenido de agua de la semilla, la cantidad y profundidad de la dureza, aspectos que protegen la viabilidad de las mismas.
La variabilidad de los caracteres morfoanatómicos y componentes químicos de los tegumentos se ve reflejada en los niveles de permeabilidad al agua hallados en las semillas. Esta variabilidad, puede entenderse según lo mencionado por Quinlivan (1971) al sostener que al momento de la formación de la semilla en la planta madre no todas las semillas se encuentran sometidas a las mismas condiciones ambienta- les. Los estudios de la floración en esta especie indicaron que la misma se completa entre 10 y 13 días y finaliza la madurez entre los 22 y 32 días (Gillij et al., 2021). En algunas especies ya sea el estrés hídrico, la humedad relativa, la temperatura, pueden inducir la formación de semillas duras (Nikolaeva, 1980; Besnier Romero, 1989; Harper, 1991; Baskin y Baskin, 2004). Por, lo cual se, puede entender el elevado porcentaje de semillas duras hallado, considerando que la especie es de característica subtropical de veranos cálidos (Baseggio et al., 1998; Peters et al., 2010). Por esto, es probable que alguno de los factores climáticos en interacción con el genotipo durante el periodo de fructificación y embriogénesis, hayan inducido los diferentes niveles de dormición física de las mismas.
Se plantea la conveniencia de estudiar la interacción entre los genotipos po- blacionales y diferentes condiciones ambientales de producción, sea en campo o invernadero, a fin de conocer los factores determinantes de la dureza física.
Además, otra posible línea investigativa podría considerar indagar la ubicación específica de las sustancias químicas en los estratos celulares de los tegumentos seminales de distintas especies con semillas duras y sus implicancias en los grados de permeabilidad al agua.
CONCLUSIÓN
Se puso en evidencia que los diferentes niveles de permeabilidad al agua en semillas de D. incanum se asocian con las características morfoanatómicas y a las proporciones de los componentes químicos de los tegumentos seminales. Las diferencias observa- das entre tegumentos de distintos grados de permeabilidad al agua se encontraron en: la ornamentación, la estructura anatómica de la lente, la compactación de la empalizada, el grosor de la pared celular en las macroesclereidas. Así como, en las proporciones de sustancias químicas como FAD+S, celulosa, lignina, ceras, taninos condensados, que ocasionan diferentes grados de impermeabilidad del tegumento. Aspectos que reflejan niveles de dormición física de las semillas y contribuyen a preservar la viabilidad de los embriones.














