INTRODUCCIÓN
El sling de la arteria pulmonar consiste en un desarrollo anormal de los arcos aórticos en el que la arteria pulmonar izquierda se origina de la arteria pulmonar derecha, pasando entre la tráquea y el esófago. Cerca de un 50 % de los pacientes pueden presentar un anillo traqueal completo, que se conoce como complejo ring- sling, 1 ’ 2 más frecuente en varones.1-3
Los signos y síntomas aparecen en su mayoría en el primer año de vida y entre ellos se destacan: estridor bifásico que aumenta con el llanto o con la alimentación, tos crónica, síndrome bronquiolítico, neumonías recurrentes, apneas, cianosis e hiperextensión cervical.4
La evaluación inicial en los niños con sospecha de anillo vascular incluye el esofagograma y la endoscopia respiratoria. Confirman el diagnóstico la angiotomografía computada (angioTC) o angiorresonancia (angioRMN) que proveen al cirujano cardiovascular y al cirujano infantil la información necesaria para realizar la intervención quirúrgica de manera conjunta y oportuna.2
Dada la asociación frecuente de dichas patologías, orientar el proceso diagnóstico prequirúrgico resulta de vital importancia para la planificación multidisciplinaria del tratamiento. Se reporta el caso clínico de un niño con diagnóstico inicial de sling de arteria pulmonar y malformación traqueal congénita intraoperatoria.
CASO CLÍNICO
Niño de 1 año y 9 meses de edad que ingresó a la urgencia pediátrica de un hospital provincial de Buenos Aires por dificultad respiratoria asociada a estridor laríngeo. Como antecedentes personales de relevancia, el embarazo y el parto ueron normales, y presentó dos internaciones por síndrome bronquiolítico a los 5 y 6 meses de vida. No surgió el antecedente de disfagia. Sin antecedentes familiares de importancia. Al examen físico presentaba peso 9 kg (percentil <3), talla 82 cm (percentil 10) y perímetro cefálico 46 cm (percentil 10), sin rasgos dismórficos, rosado, sin edemas ni hepatomegalia, pulsos arteriales periféricos y centrales normales, auscultación pulmonar normal y auscultación cardíaca con soplo mesosistólico 2/6 en foco pulmonar.
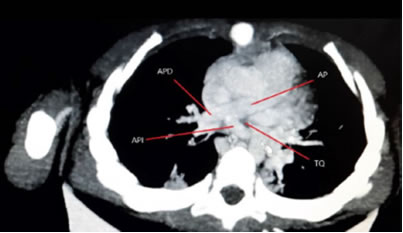
El electrocardiograma y la radiografía simple de tórax fueron normales. En la ecocardiografía transtorácica, no se detectó cardiopatía estructural. Se solicitó evaluación por el Servicio de Endoscopia Respiratoria. Se realizó fibrolaringoscopia que informó compresión traqueal en tercio superior con disminución del calibre de la luz. Se completó estudio con angioTC de tórax (Figura 1), en la que se observó origen anómalo de la arteria pulmonar izquierda que nacía de la arteria pulmonar derecha pasando entre la tráquea y el esófago; esto provocaba compresión traqueal a nivel distal, hallazgo compatible con sling de arteria pulmonar. En el mediastino superior, se evidenció un bronquio accesorio derecho que se originaba en la tráquea y llegaba al lóbulo superior derecho. Durante la internación presentó reagudización del cuadro respiratorio por la infección simultánea con SARS-CoV-2, que requirió ingreso a asistencia respiratoria mecánica (ARM).
Superado el cuadro, fue derivado a nuestro hospital para la resolución quirúrgica.
Debido a las diferencias encontradas entre el informe de la angioTC de tórax y la endoscopia respiratoria realizadas en el otro centro, se programó el abordaje conjunto5 entre Cirugía Cardiovascular Infantil y Cirugía Pediátrica (Sección Endoscopia Respiratoria). Se realizó la cirugía con bomba de circulación extracorpórea (CEC). Se observó el nacimiento de la rama pulmonar izquierda a partir de la rama pulmonar derecha, se realizó sling por detrás de la tráquea cercana a la carina, sección de dicha rama y reimplante en tronco de arteria pulmonar. Durante el procedimiento, se realizó videobroncoscopia con broncoscopio 3.5, y se observó el origen anómalo de bronquio traqueal derecho y en tráquea media zona estenótica no franqueable. Se cambió a óptica de 1,9 mm, que se avanzó por la zona estenótica, observando anillos traqueales completos distales y compresión vascular causada por el sling de arteria pulmonar. Asimismo, se realizó traqueobroncografía (Figura 2) con contraste hidrosoluble e isoosmolar, que confirmó el diagnóstico de estenosis traqueal congénita larga de 3 cm y distal a la estenosis la carina con ambos bronquios fuentes. Se realizó una traqueoplastia deslizada de dicho segmento.5-7 Con el paciente normotérmico, se programa la salida de la CEC. Permaneció con drenaje pleuromediastínico bilateral 5 días.8
En la evolución posquirúrgica, presentó síndrome bronquial obstructivo grave con requerimiento de altos parámetros de ARM. Resuelto este cuadro y no habiendo ocurrido otras complicaciones asociadas a la cirugía, se inició el
Figura 1: Angiotomografía computada
destete de la ARM y de la sedación. Por presentar cirugía reciente de vía aérea, ventilación mecánica por más de 30 días, neuropatía grave de paciente crítico, bajo peso y altos requerimientos de sedación, se decidió, junto con el cirujano infantil de vía aérea, realizar una traqueostomía 10 días después de la cirugía; se logró el retiro de ARM a los 30 días luego de la traqueostomía. Egreso hospitalario sin requerimiento de oxígeno.
DISCUSIÓN
Los anillos pulmonares son el resultado del desarrollo anormal de los arcos aórticos, sus ramas y/o las ramas pulmonares.
El nacimiento anómalo de la arteria pulmonar izquierda, también llamado sling o cabestrillo, es una malformación poco frecuente en la que la arteria pulmonar izquierda nace de la cara posterior de la rama pulmonar derecha.9-11 Esto genera un recorrido anormal: cruza hacia la izquierda y se ubica entre la tráquea y el esófago. La rama pulmonar izquierda suele ser ligeramente hipoplásica.
Se desconoce la verdadera incidencia dado que es una patología infrecuente. Solo se calcula la incidencia global de los anillos vasculares menor al 1 % de las anomalías vasculares congénitas. Si bien su etiología es multifactorial, se ha visto predisposición genética en los síndromes de Down, Edwards y Mowat-Wilson, asociación VACTER y en gemelares.9
El origen embriológico normal de las arterias pulmonares es mixto. La porción proximal se origina a partir del arco aórtico VI derecho e izquierdo, respectivamente, para cada rama. La porción distal procede de las arterias pulmonares primitivas del plexo vascular pulmonar. Se postula una ausencia en el desarrollo del arco aórtico VI izquierdo, debiendo de forma anormal originar la vascularización pulmonar del arco aórtico VI derecho.9
La evolución clínica depende del grado de compresión que estas estructuras vasculares producen sobre la vía aérea y/o el esófago.2
Hasta el 90 % de los pacientes presenta síntomas respiratorios en el primer año de vida:9 estridor bifásico que aumenta con el llanto o la alimentación, tos traqueal, infecciones respiratorias recurrentes, síndrome bronquiolítico, hiperextensión cervical y fallas en la extubación.1,2,4 Entre los síntomas digestivos secundarios a la compresión esofágica, se destacan la disfagia, los vómitos y la deglución lenta.2 La estenosis traqueal se produce como consecuencia de la compresión extrínseca y su asociación con diversas malformaciones traqueales; la más frecuente son los anillos traqueales completos, conocida como complejo ring-sling. 9,10,12 También se han encontrado segmentos estenóticos largos, anomalías en la distribución de los cartílagos, anomalías de la bifurcación bronquial (pig bronchus o bronchus suis), 9 que es la presencia de un bronquio accesorio derecho que se origina de la tráquea con destino al lóbulo superior derecho e, incluso, agenesia pulmonar derecha.13
Los defectos congénitos asociados más frecuentes son las cardiopatías congénitas (30 50 %), entre las que se destacan los defectos septales interauriculares e interventriculares, ductus arterioso permeable, anomalía del drenaje venoso pulmonar, persistencia de vena cava superior izquierda y excepcionalmente la tetralogía de Fallot.3,6,9,10,12
El plan de estudio debe incluir:1,4,8
Radiografía de tórax frente, que permite identificar una lateralización anormal de la tráquea. La radiografía perfil podrá evidenciar una disminución del calibre traqueal.
Esofagograma con bario: el 95 % de los pacientes muestra algún tipo de indentación esofágica.
Ecocardiografía: permite observar la ausencia de continuidad entre tronco de arteria pulmonar y rama pulmonar izquierda. Por otro lado, es el estudio necesario para diagnóstico de malformaciones cardíacas asociadas.
Laringotraqueobroncoscopia y traqueobron- cografía: constituye uno de los estudios más importantes para realizar en estos pacientes. Permite observar la compresión pulsátil de la vía aérea, los anillos completos, la gravedad de la malformación y descartar otras causas de estridor respiratorio.13
AngioTC y angioRMN: confirman el diagnóstico del anillo vascular y de la malformación de la vía aérea con una sensibilidad cercana al 100 %.2 Se recomienda realizar laringotraqueobroncoscopia y traquebroncografía previo a intervención quirúrgica para minimizar los tiempos de CEC y disminuir el riesgo de complicaciones infecciosas.
El tratamiento es quirúrgico con o sin CEC.10,15
Consiste en desinsertar la arteria pulmonar izquierda y reimplantarla en el tronco de la arteria pulmonar, situándola por delante de la tráquea, y resolver la estenosis traqueal congénita.6-8 La mortalidad global de los anillos vasculares es menor al 1 %.1 Pero si se evalúan solo los complejos ring-sling, asciende hasta un 36 %, según las series y las malformaciones asociadas.6-9 La mayor sobrevida se observa en aquellos que no tienen cirugía traqueal.7
La sintomatología traqueal suele disminuir de manera progresiva. En caso de persistir, deberá replantearse una reevaluación endoscópica de la vía aérea.1-4
La traqueostomía no es un procedimiento que se realice de rutina, sino que queda reservada para aquellos pacientes con patología laríngea asociada, laringomalacia grave, dificultades en la extubación y/o ARM prolongada.1