Introducción
La úlcera de pie diabético constituye una de las complicaciones más frecuentes en la evolución de la diabetes. Se estimó que del 15% al 25% de los pacientes presentan úlceras de pie diabético a lo largo de su vida.1 Estas son de curación lenta, refractarias y suelen complicarse con infecciones, gangrena y amputación. Esta última fue la causa principal de internación, con el 50% al 95% de las amputaciones no traumáticas de los miembros inferiores.1
La mayoría de las úlceras presentan componentes neuropáticos e isquémicos que llevan a la pérdida de la sensibilidad e isquemia, que provocan amputación de dedos, pie o pierna, no solo con impacto en la morbimortalidad, sino también a nivel social, laboral y económico.2 El 80% de las amputaciones de las extremidades inferiores estuvieron precedidas de úlceras y el 75% se deben a pie diabético.3,4
La incidencia anual fue del 1% al 4%, con una prevalencia del 4% al 10%.5 El tratamiento debe incluir el control de las causas primarias como control glucémico,6 desbridamiento,7 descarga de pie8 y curación de la herida manteniendo su humedad.9
A pesar de ello, muchas de estas úlceras no curan y persisten por meses o años y muchas reaparecen luego de su curación.10
El plasma rico en plaquetas (PRP) es un tratamiento que se encuentra en desarrollo desde la década de 1990,11 y en sus inicios su empleo estuvo asociado con el tratamiento de úlceras crónicas.
Existen varios métodos no estandarizados o aprobados; la técnica más usada incluye la obtención de sangre periférica del propio paciente (autóloga), que luego se centrifuga para separar las plaquetas de los glóbulos rojos y blancos. Estas plaquetas son ricas en factores de crecimiento y se activan para que se liberen dichos factores. Se cuenta con dos métodos de activación, el primero mediante el agregado de trombina o calcio (liberación plaquetaria),12 y el segundo mediante lisis física de las plaquetas congelándolas13 o usando métodos ultrasónicos que provocan la ruptura de la membrana celular.14
El uso de PRP y su aplicación tópica se encuentran en auge, por lo que su estudio es de relevancia dado el impacto sobre la salud y los aspectos sociales y económicos, teniendo en cuenta el padecimiento que conlleva la úlcera de pie diabético y los resultados limitados con los tratamientos actuales.
Es de importancia la valoración de la evidencia científica existente que sustente el uso de PRP autólogo en gel o solución en la úlcera de pie diabético, para facilitar la toma de decisiones en la práctica clínica.
El PRP contiene altas concentraciones de factores de crecimiento que facilitarían la curación de la herida;15 cuando son liberados se desencadena el proceso de curación.16 El PRP contiene otros componentes que podrían favorecer la implantación celular y la multiplicación lateral.17 El uso de componentes autólogos podría reducir el riesgo de reacción inmune, y su aplicación tópica disminuiría el riesgo de infección por inyectables y mejoraría la calidad de vida y el dolor de los pacientes.
El objetivo de esta revisión fue determinar la eficacia del uso de PRP autólogo tópico para la curación de úlcera de pie diabético, sobre la base de la evidencia científica actualizada.
Material y métodos
Para la revisión sistemática se llevó a cabo la búsqueda de artículos en las siguientes bases de datos: PubMed, Cochrane Central, Lilacs y Clinical Trials. Las palabras claves que se usaron fueron: “diabetic foot [Mesh]”, “diabetic foot ulcer”, “DFU”, “diabetic feet”, “platelet-rich plasma [Mesh]”, “PRP”, “platelet rich plasma autologous”, “platelet rich plasma gel” y “platelet rich plasma solution”. Se realizó una búsqueda línea a línea en PubMed y Cochrane Central con integración de operadores booleanos. En Lilacs y Clinical Trials se realizó una búsqueda con integración de conceptos con operadores booleanos “AND” y “OR”. La búsqueda no tuvo límites de fecha o idioma.
Se evaluaron estudios de forma independiente por parte de los autores para identificar aquellos que cumplieran con los criterios de elegibilidad y sesgo. Se realizaron valoraciones por criterios de exclusión de diseño de estudios en primera instancia,); luego se analizaron duplicados para su exclusión, posteriormente se valoraron trabajos por títulos y abstracts, y finalmente análisis de estudios a texto completo. Se esquematizó todo en un diagrama de flujo PRISMA. Toda la selección se realizó con el software online RAYYAN.
Se efectuó extracción de datos de los estudios, obteniéndose los siguientes datos:
Características del estudio: ensayo clínico aleatorizado a doble ciego o abierto.
Contexto del estudio: intrahospitalario o extrahospitalario, país de realización.
Características de los participantes: número, edad, sexo y herida.
Características de las intervenciones: PRP de aplicación tópica en gel o solución, modo de preparación, aplicación.
Características de las comparaciones: curaciones estándar y placebo.
Características de los desenlaces: curación completa de úlcera al final de la intervención, total del área epitelizada al final de la intervención medido en cm2, calidad de vida y dolor.
Fuentes de financiamiento.
Conflicto de interés.
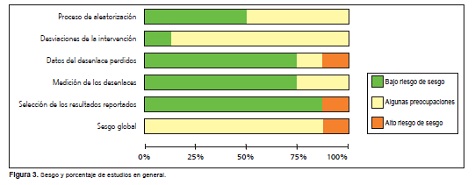
Se valoraron los dominios de sesgo durante el proceso de aleatorización, desviación de las intervenciones, sesgo por pérdida de datos, sesgo en medición de desenlace, sesgo en selección de resultado informado y sesgo global. Se clasificó cada estudio en “bajo riesgo”, “alto riesgo” y “algunas preocupaciones”.18Para los resultados dicotómicos se calculó una estimación estándar del riesgo relativo y su intervalo de confianza (IC) del 95%; para los resultados continuos se estimó la diferencia de medias entre los grupos.
Se valoró el impacto de la heterogeneidad estadística mediante el uso del estadístico I 2. Si era ≥ 50% o donde se manifestara heterogeneidad clínica se investigaron las posibles causas, como presencia de infección en la úlcera o modo de preparación del PRP.18
No se realizó valoración del sesgo de publicación con el uso del Funnel Plot dado que el número de estudios incluidos es menor de 10.
Se resumieron los datos mediante un modelo de efectos aleatorios, salvo marcada homogeneidad entre los estudios. Se interpretaron los metanálisis de efectos aleatorios con consideración de toda la distribución de los efectos.. Para los resultados dicotómicos se utilizó el método de Mantel‐Haenszel; para los resultados continuos, se usó el método de la varianza inversa. Se procesaron los datos a través del software Review Manager 5.4.1.
Se protocolizó el análisis de sensibilidad para investigar el efecto de la exclusión de estudios con alto riesgo de sesgo.
Resultados
Los criterios de inclusión fueron: pacientes con diabetes tipos 1 y 2, mayores de 18 años, ensayos controlados aleatorizados, aplicación tópica. Los criterios de exclusión fueron: pacientes menores de 18 años, intervenciones en aplicación inyectable, sangre que no fuera de extracción periférica (p. ej., cordón umbilical) para la preparación de PRP, asociación de otros compuestos (p. ej., injerto de grasa), úlceras de otra etiología, comparaciones que no sean los cuidados estándar y placebo (p. ej., plasma escaso en plaquetas).
La búsqueda arrojó el resultado de 153 estudios. Se excluyeron 28 trabajos duplicados, 59 por título y abstract. Luego de la valoración por texto completo se excluyeron 52 artículos, lo que dio como resultado final 14 estudios. Para la síntesis cualitativa quedaron ocho trabajos.19-26 Se identificó un ensayo en curso: NCT0231259627, y cinco estudios NCT02402374,28 NCT04090008,29 NCT03716141,30 CTRI/2018/11/01647031 y ISRCTN5547481332 en espera de clasificación.
Se incluyeron 14 estudios, de los cuales ocho calificaron para revisión cualitativa y seis para revisión cuantitativa. La población fue de 536 pacientes, con 270 en el grupo intervención y 266 en el grupo control. Sin contar el ensayo de Khorvash,23 que no informó el número de participantes por sexo, existió un 68.23% de varones y 31.76% de mujeres. La edad promedio, sin contar Karimi,22 Khorvash23 y Li24 que no lo presentaron, fue de 55.24 años para el grupo de intervención y de 57.2 años para el grupo control. El promedio de seguimiento de cada estudio fue de 11.37 semanas, con un rango de 3 a 20 semanas. Excepto el estudio de Khorvash23 que no indicó el método de preparación de PRP, todos los demás realizaron el procedimiento de liberación plaquetaria. Solo Karimi22 presentó el uso de PRP en solución embebida en gasa estéril, mientras que el resto realizó la colocación de PRP en gel. Solo dos trabajos determinaron el cálculo del tamaño de la muestra: Karimi22 y Elsaid.21
Existió un desequilibrio en los grupos en la línea de base en tres estudios: Driver,20 Elsaid21 y Li25 presentaron distintos tamaños de úlcera, y Elsaid,21 valores de hemoglobina glucosilada (HbA1c) diferentes entre grupos. En el trabajo de Driver20 se aleatorizaron 72 participantes y 32 fueron excluidos del estudio debido a fallas para completar el tratamiento y violaciones de protocolo, lo que resultó en 19 integrantes en el grupo de intervención y 21 en el grupo control. En la investigación de Karimi22 se aleatorizó a 60 pacientes y se informaron pérdidas de datos similares en ambos grupos, a razón de 5 participantes, 2 debido a sepsis y 3 debido a amputación. En el ensayo de Xie26 se registró el abandono de dos participantes en el grupo control. Excepto el estudio de Xie,26 que permitió la inclusión de úlceras de tracto sinuoso y con presencia de inflamación, así como los de Khorvash23 y Li24 que no la presentaron, el resto de los estudios realizó preparación de las heridas (cultivo de herida y desbridamiento) y excluyó úlceras infectadas. Existieron diferencias entre los trabajos para definir el tiempo de no curación de la úlcera antes del ingreso al estudio. Xie26 lo definió en una semana, Li24,25 en dos, Driver20 en cuatro, Ahmed19 en seis, Elsaid21 en 12, en tanto que Karimi22 y Khorvash23 no lo mencionaron. Solo el trabajo de Driver20 tuvo financiación de la industria en relación con la producción de PRP en gel.
Se excluyeron 15 estudios33-47 por distinto fármaco de intervención, cinco trabajos48-52 por presentar extracción de PRP que no era de sangre periférica, cinco ensayos53-57 por no ser aleatorizados, nueve investigaciones58-66 por estudiar úlceras de etiología no diabética, 11 estudios67-77 por analizar la aplicación de PRP inyectable, un trabajo78 por ser reseña de resúmenes de la Conferencia sobre Pie Diabético 2019, cuatro estudios79-82 por encontrarse terminados por quita de respaldo económico y dos investigaciones83,84 por distinta comparación a las establecidas.
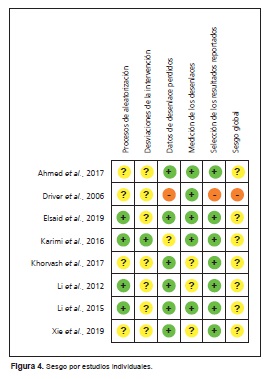
El trabajo de Driver de 2006 20 tuvo alto riesgo de sesgo; el resto presentó algunas preocupaciones.
Solo cuatro autores: Driver,20 Elsaid,21 Karimi22 y Li24,25 informaron los procesos de aleatorización mediante herramientas electrónicas y software en línea; Ahmed19 y Khorvash23 indicaron que sus estudios fueron aleatorizados, pero no informaron la metodología de dicha aleatorización.
El dominio de las desviaciones de las intervenciones intencionadas valora si los participantes y los investigadores están al tanto de las intervenciones, si hay desviaciones de la intervención intencionadas que puedan surgir del contexto del estudio y si existe un correcto análisis por intención de tratar. El estudio de Ahmed19 relató que los grupos se formaron por métodos de aleatorización, pero no manifestó si participantes e investigadores se encontraban cegados, y no realizaron análisis por intención de tratar. La investigación de Driver20 indicó que cada grupo presentó una persona no cegada que se encargó de tener la documentación en un área privada para mantener el cegamiento del equipo, los investigadores y pacientes, y llevó a cabo estudios por intención de tratar. El trabajo de Elsaid21 fue abierto, de modo que participantes e investigadores no estaban cegados, no existieron desviaciones intencionadas de la intervención y no se realizó análisis por intención de tratar. El ensayo de Karimi22 fue aleatorizado, a doble ciego, sin desviaciones intencionadas de la intervención. Los trabajos de Khorvash23 y de Li24 no informaron cegamientos y no hay datos sobre desviación intencionada de la intervención. El ensayo de Li25 fue abierto, no existieron desviaciones intencionadas de la intervención y se realizó por intención de tratar. El de Xie26 no manifestó cegamientos, no presentó datos que supongan desviaciones en la intervención y efectuó un correcto análisis por intención de tratar.
Las investigaciones de Ahmed,19 Elsaid,21 Khorvash,23 Li,24,25 y Xie26 no informaron pérdidas de datos. El estudio de Driver20 indicó pérdidas de datos del 44.4% (n = 21) para el grupo experimental y del 34.4% (n = 11) para el grupo control. El trabajo de Karimi22 informó pérdida de cinco pacientes en cada grupo; existe la posibilidad de que los datos faltantes constituyeran un sesgo en el resultado, ya que señaló que dichos pacientes tuvieron sepsis (dos en cada grupo) y amputación (tres en cada grupo).
Los métodos de medición de los desenlaces fueron apropiados en todos los estudios. Los trabajos de Ahmed,19 Driver,20 Karimi22 y Li25 presentaron cegamiento del asesor de la intervención; Li24 y Khorvash23 no lo informaron.
El estudio de Driver20 manifestó, en el apartado “método”, la valoración de desenlaces tales como porcentaje del cambio en el área de la herida al final del estudio en visita desde el inicio (EOSV) y el porcentaje de cambio de volumen al EOSV desde el inicio, pero luego no se mencionó en los resultados. El resto de los estudios presentaron congruencia entre lo establecido en sus métodos y los resultados.
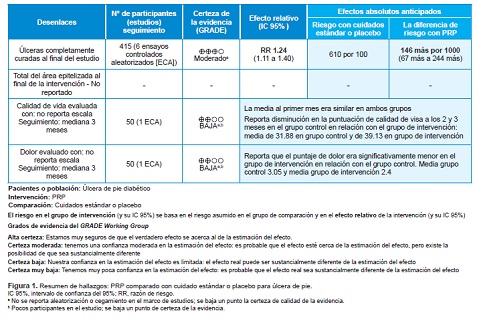
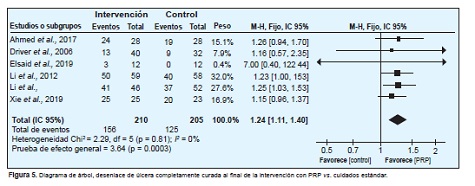
Seis estudios19-21,24-26 incluyeron datos sobre el desenlace de úlcera completamente curada al final de la intervención. En total, 415 participantes en estudios que comparaban PRP en gel y solución con cuidados estándar y placebo. Existe evidencia de certeza moderada de que el PRP autólogo de uso tópico puede incrementar la curación de las úlceras de pie diabético (riesgo relativo 1.24; intervalo de confianza [1.11 a 1.40]). Se estableció por protocolo el análisis de subgrupos para comparar con preparaciones de distintos métodos, pero todos los estudios usaron técnicas similares. Se establecieron también subgrupos con úlceras infectadas y no infectadas, pero los trabajos excluían úlceras infectadas, solo el de Xie26 permitió la inclusión de úlceras con presencia de inflamación y no de pus en sus heridas. Se realizó análisis de sensibilidad, en el que se excluyó el estudio de Driver20 por el alto riesgo de sesgo y no presentar efecto en los resultados en relación con su ausencia.
No se mencionó en ningún estudio el desenlace total del área epitelizada de la úlcera al final de la intervención (medida en cm2).
Solo el trabajo de Khorvash23 mostró el desenlace acerca de la calidad de vida. Manifestó que, en el primer mes, la media de ambos grupos era similar. Indicó disminución en la calidad de vida a los dos y a los tres meses en el grupo control en relación con el grupo de intervención (31.88 ± 2.8 vs. 39.13 ± 1.35 respectivamente, p = 0.001). No mencionó la escala utilizada.
Solo el estudio de Khorvash23 presentó el desenlace sobre dolor. El puntaje de dolor en el grupo de intervención fue significativamente menor luego de un mes, en comparación con el grupo control, y se mantuvo con una relación significativa a los tres meses (PRP 2.4 ± 0.59 vs. control 3.05 ± 0.7, p = 0.003).
Discusión
Todos los estudios tuvieron pacientes con úlceras no infectadas, excepto el de Xie,26 que incluyó enfermos con úlceras de tracto sinuoso con presencia de inflamación. Todos los trabajos prepararon el PRP mediante el método de liberación plaquetaria con activación por medio del uso de trombina y cloruro de calcio. La evidencia demostró que existe un posible efecto beneficioso que deriva del uso de PRP autólogo tópico para la curación de úlceras de pie diabético. Cabe destacar que los estudios tuvieron una moderada calidad de evidencia debido a la presencia de “algunas preocupaciones” o “alto riesgo de sesgo”, en cuanto al desenlace curación completa de la úlcera. Solo un trabajo valoró calidad de vida y puntaje de dolor, y mostró resultados beneficiosos con el uso de PRP autólogo tópico en gel, pero se destaca la necesidad de explorar dichos desenlaces con mayor cantidad de estudios para evaluar el impacto en la cotidianeidad del paciente que, en definitiva, es el principal beneficiario de dicho tratamiento. Se destaca que existen pocas referencias a investigaciones latinoamericanas, ya que se hallaron solo tres resultados que no cumplían con los criterios de inclusión. La imposibilidad de contar con información completa en algunos casos supone un sesgo a tener en cuenta en esta revisión.
Conclusión
Existe evidencia de que el uso de PRP autólogo en gel y solución podría ser beneficioso para la curación de úlceras de pie diabético, pero se necesitarían estudios aleatorizados de alta calidad para vencer los sesgos que presentan los trabajos actuales y sustentar las acciones de salud en evidencia de alta calidad. Se precisa mayor cantidad de investigaciones que exploren la calidad de vida y el dolor del paciente, que es el destinatario del tratamiento, así como fomentar la producción científica en Latinoamérica sobre el uso del PRP autólogo tópico. Es importante explorar todas las alternativas para mejorar la calidad de vida de los pacientes con diabetes, donde el PRP autólogo tópico supone un tratamiento que promete buenos resultados para la curación de las úlceras de pie diabético.