Introducción
La enfermedad del hígado graso no alcohólico (HGNA) es la manifestación hepática del síndrome metabólico y se define como la acumulación de grasa en el hígado de personas, causado por el consumo excesivo de grasas y azúcar combinado con sedentarismo. Sus etapas van desde la esteatosis simple (EH), una entidad relativamente benigna, hasta la esteatohepatitis no alcohólica (EHNA), en la cual ocurre esteatosis, muerte de hepatocitos e inflamación, con o sin fibrosis. La EHNA es considerada la variante más agresiva, con mayor riesgo de progresar a fibrosis hepática, cirrosis y carcinoma hepatocelular (Takahashi et al. 2014, Rada et al. 2020).
Los factores de riesgo para HGNA son de naturaleza metabólica e incluyen la obesidad, resistencia a la insulina, diabetes tipo 2, hipertensión y dislipemia. Se estima que entre el 25% y el 30% de la población adulta vive con HGNA, mientras que el 90% de los obesos mórbidos y más del 50% de las personas con diabetes tipo 2 tienen HGNA (Younossi et al. 2021).
La patogenia de HGNA es multifactorial y considera múltiples alteraciones: resistencia a la insulina, secreción inadecuada de adipocinas y citocinas inflamatorias del tejido adiposo disfuncional, factores nutricionales, disbiosis de la microbiota intestinal, susceptibilidades genéticas y modificaciones epigenéticas; que actúan sinérgicamente para inducir HGNA. La resistencia a la insulina es un importante impulsor de la EH. Mientras que la lipotoxicidad de los lípidos acumulados en el hígado junto con la activación del sistema inmunitario innato son los principales impulsores de EHNA (Parthasarath et al. 2020, Tilg et al. 2021).
Los ácidos grasos saturados (principalmente los ácidos palmítico y esteárico), los ácidos grasos poli-insaturados n-6 (en particular el ácido linoléico y sus productos oxidados) (Musso et al. 2018), el colesterol libre (Musso et al. 2013) y los ácidos grasos trans de origen industrial (particularmente el trans-9 18:1 o ácido elaídico) son promotores de la EHNA (Obara et al. 2010, Oteng et al. 2019). De un modo opuesto, los ácidos grasos cis-9, trans-11 18:2 (ácido ruménico) y trans-11 18:1 (ácido vaccénico) han demostrado tener un efecto “hepatoprotector” en cultivos celulares y en modelos animales de obesidad y degeneración grasa hepática. El ácido ruménico es el principal isómero natural del ácido linoleico conjugado (CLA) capaz de promover efectos beneficiosos en la obesidad, el cáncer, las enfermedades cardiovasculares y la degeneración grasa hepática (Basak et al. 2020). Las dietas altas en grasas suplementadas con 1% de ácido ruménico sintético demostraron reducir la dislipidemia y la esteatosis hepática en ratas JCR:LA-cp; estos efectos aumentaron con la adición de 1% de ácido vaccénico sintético (ruménico + vaccénico) (Jacome-Sosa et al. 2010). En cultivos de hepatocitos, el ácido vaccénico tuvo un efecto nulo en el metabolismo de los lipidos y el colesterol; es decir, no incrementó el contenido de colesterol, de trigliceridos y no modificó la expresión de genes lipogénico y colesterogénico (Krogager et al. 2015, Vahmani et al. 2016a,b). En ratas obesas alimentadas con dieta occidental (1% de colesterol, 43,1% de carbohidratos, 28% de proteínas, 8% de fibras y 15% de lípidos) suplementada con 1% de ácido vaccénico sintético resultó en una menor concentración de trigliceridos hepáticos y reducidos niveles hepáticos de las enzimas acetil-CoA carboxilasa-1 y ácido graso sintasa (encargadas de la biosintesis de ácidos grasos), cuando se comparó con ratas obesas sin suplementación (Wang et al. 2009).
Enriquecer los productos lácteos con ácidos ruménico y vaccénico podría mejorar el valor para la salud de las grasas derivadas de los lácteos, especialmente para aquellas personas con síndrome metabólico. Los reportes de los efectos sobre el HGNA de lácteos enriquecidos con estos ácidos grasos aún son escasos. Hasta el momento, se reportó el efecto de leches bovinas alimentas con pastura vs. cereal (Benoit et al. 2014), de una grasa ovina con altos niveles de ácidos grasos vaccénico y ruménico vs. una grasa vegetal industrial hidrogenada (Brito Medeiros et al. 2021) y de una leche bovina funcional (reducida en grasas saturadas y enriquecida con ácidos vaccénico y ruménico) vs. una leche bovina estándar (Gerstner et al. 2021). Estos trabajos reportaron un efecto hepatoprotector al prevenir la acumulación de grasa en el hígado de las ratas y ratones alimentados con grasa rumiante enriquecida con los ácidos vaccénico y ruménico. Hasta el momento, no hay datos sobre leches bubalinas con diferente composición de ácidos grasos en un contexto de una dieta rica en grasas sobre la enfermedad del hígado graso. Así, el objetivo del presente estudio fue comparar los efectos de una grasa láctea de origen bubalino con altos niveles de ácidos ruménico y vaccénico y reducida en grasas saturadas con los de una leche bubalina estándar, ambos incorporados en una dieta rica en grasas, sobre la degeneración grasa hepática en ratones.
Materiales y Métodos
Animales y ambiente experimental. Se emplearon 18 ratones cepa C57BL/6J, de 2 meses de edad, machos, con un peso de 25 g obtenidos del Centro de Experimentaciones Biológicas y Bioterio de la Universidad Nacional de La Plata. Los ratones fueron alojados en jaulas metálicas individuales, con una temperatura ambiente de 22º C, un ciclo de luz/oscuridad de 12 horas, con agua de bebida y alimento “ad libitum”. El cuidado de los animales y los procedimientos de la experiencia fueron aprobados por el Comité de Ética y Bioseguridad de la Facultad de Ciencias Veterinarias, UNNE (protocolo nº 83).
Grasa láctea. Se emplearon dos grasas lácteas de búfalas alimentadas con pastura natural (GLP) y de búfalas alimentadas con pastura natural + suplemento lipídico diseñado para reducir las grasas saturadas e incrementar las grasas insaturadas de la leche (GLE) (Patiño et al. 2017). La grasa láctea de pastura presentó una concentración de 67,12g de grasas saturadas/100g lípidos; 4,29 g de ácido vaccénico/100 g lípidos y 1 g de ácido ruménico/100 g lípidos. Comparada con la leche de pastura, la grasa láctea experimental registró menos ácidos grasos saturados (-31,6%), más ácido ruménico (+257%) y más ácidos grasos trans monoinsaturados (+387,5%), representado predominantemente por el ácido vaccénico (Tabla 1). El contenido de colesterol no difirió (prueba t bilateral para muestras independientes= p 0,727) entre las leches de pastura (10,30 ± 2,27 mg de colesterol/100 g) y experimental (9,68 ± 2,55 mg de colesterol/100 g) (Patiño et al. 2017).
Tabla 1. Composición de ácidos grasos en leche de búfalas a pastura sin suplementación lipídica (GLP) y suplementadas con 300 ml/día de una mezcla de aceite de girasol y de pescado (70:30 wt/wt) durante 24 días (GLE).
| Ácidos grasos | 44.GLP | 45.GLE | 46.p valor | 47. 48.
|---|---|---|---|
| (g de ácidos grasos/100 g de ácidos grasos) 49. 50. 51. | 52. 53.|||
| 4:0 (butírico) | 54.3,86 ± 0,38 | 55.1,86 ± 0,90 | 56.0,0012w | 57. 58.
| 6:0 (caproico) | 59.1 ± 0 | 60.0,46 ± 0,11 | 61.<0,0001t | 62. 63.
| 8:0 (caprílico) | 64.0,51 ± 0,09 | 65.0,14 ± 0,05 | 66.0,0006w | 67. 68.
| 10:0 (cáprico) | 69.0,99 ± 0,04 | 70.0,33 ± 0,05 | 71.<0,0001t | 72. 73.
| 10:1 (caproleico) | 74.0,03 ±0,01 | 75.0,01 ± 0 | 76.0,0005t | 77. 78.
| 11:0 | 79.0,01 ± 0 | 80.0,01 ± 0 | 81.>0,9999w | 82. 83.
| 12:0 (láurico) | 84.1,29 ± 0,49 | 85.1 ± 0 | 86.0,4615w | 87. 88.
| 12:1 | 89.0,09 ± 0,02 | 90.0,10 ± 0 | 91.0,4615w | 92. 93.
| 14:0 (mirístico) | 94.8,14 ± 1,07 | 95.4 ± 0,82 | 96.<0,0001t | 97. 98.
| 14:1 | 99.0,73 ± 0,14 | 100.0,54 ± 0,05 | 101.0,0105t | 102. 103.
| iso 15:0 | 104.0,30 ± 0,08 | 105.0,09 ± 0,02 | 106.0,0006w | 107. 108.
| 15:0 (pentadecílico) | 109.1,43 ±0,53 | 110.1 ± 0 | 111.0,1923w | 112. 113.
| 15:1 | 114.0,36 ± 0,08 | 115.0,21 ± 0,04 | 116.0,0029w | 117. 118.
| 16:0 (palmítico) | 119.27,57 ± 2,70 | 120.20,57 ± 0,53 | 121.0,0006w | 122. 123.
| 16:1 (palmitoleico) | 124.1 ± 0 | 125.1 ± 0 | 126.- | 127. 128.
| 17:0 (margárico) | 129.1,14 ± 0,38 | 130.1 ± 0 | 131.>0,9999w | 132. 133.
| 17:1 (heptadecenoico) | 134.0,27 ± 0,08 | 135.0,17 ± 0,05 | 136.0,0326w | 137. 138.
| 18:0 (esteárico) | 139.21 ± 2,45 | 140.15 ± 2,77 | 141.0,0010t | 142. 143.
| trans-8 18:1 | 144.0,49 ± 0,07 | 145.1,71 ± 0,49 | 146.0,0006w | 147. 148.
| trans-9 18:1 (elaídico) | 149.0,26 ± 0,05 | 150.1 ± 0 | 151.0,0006w | 152. 153.
| trans-10 18:1 | 154.0,26 ± 0,08 | 155.0,96 ± 0,08 | 156.<0,0001t | 157. 158.
| trans-11 18:1 (vaccénico) | 159.4,29 ± 1,25 | 160.22,14 ± 3,44 | 161.<0,0001t | 162. 163.
| cis-9 18:1 (oléico) | 164.21,29 ± 1,50 | 165.19,14 ± 2,73 | 166.0,0939t | 167. 168.
| cis-11 18:1 | 169.0,67 ± 0,05 | 170.1,86 ± 0,38 | 171.0,0006w | 172. 173.
| trans-9,trans-12 18:2 (linoelaídico) | 174.0,01 ± 0 | 175.0,03 ± 0,01 | 176.0,0006w | 177. 178.
| cis-9,cis-12 18:2 (linoleico) | 179.0,97 ± 0,05 | 180.1 ± 0 | 181.0,4615w | 182. 183.
| cis-9,trans-11 18:2 (ruménico) | 184.1 ± 0 | 185.3,57 ± 0,79 | 186.0,0006w | 187. 188.
| cis-9,cis-12,cis-15 18:3 189. (α-linolénico) | 190.0,54 ± 0,14 | 191.0,27 ± 0,05 | 192.0,0019t | 193. 194.
| 20:4 (ARA) | 195.0,09 ± 0,01 | 196.0,05 ± 0,02 | 197.0,0027t | 198. 199.
| 20:5 (EPA) | 200.0,06 ± 0,01 | 201.0,05 ± 0,01 | 202.0,2183t | 203. 204.
| 22:6 (DHA) | 205.0,01 ± 0 | 206.0,01 ± 0 | 207.- | 208. 209.
| Ʃ AGS | 210.67,12 ± 2,07 | 211.45,89 ± 2,37 | 212.<0,0001t | 213. 214.
| Ʃ 12+14+16 | 215.37 ± 3,87 | 216.25,57 ± 0,98 | 217.0,0006w | 218. 219.
| Ʃ cis AGM | 220.24,44 ± 1,65 | 221.23,03 ± 2,43 | 222.0,2301t | 223. 224.
| Ʃ cis AGP | 225.1,67 ± 0,17 | 226.1,39 ± 0,07 | 227.0,0031t | 228. 229.
| Ʃ trans* | 230.5,30 + 1,26 | 231.25,84 ± 3,76 | 232.<0,0001t |
Perfil de ácidos grasos realizado por INTI Lácteos, según Norma ISO 15884 - IDF 182: Milk fat-preparation of fatty acid methhyl esters. AGS: ácidos grasos saturados. AGM: ácidos grasos monoinsaturados. AGP: ácidos grasos poliinsaturados. ARA: ácido araquidonico. EPA: ácido eicosapentaenoico. DHA: ácido docosahexaenoico. *La suma no incluye a cis- 9,trans-11 18:2. t: Prueba t bilateral para muestras independientes. w: Prueba Wilcoxon para muestras independientes.
Formulación de las dietas. Se elaboraron dos alimentos altos en grasas (≈20% de lípidos) (Tabla 2) y diferente composición de ácidos grasos (Tabla 3). Un alimento fue elaborado adicionando grasa láctea de pastura al alimento balanceado comercial para ratones. Este alimento, denominado GLP, registró 21,12% de lípidos totales, con 55 g de grasas saturadas/100 g de ácidos grasos totales; 3,5 g de ácido vaccénico/100 g de ácidos grasos y 0,8 g de ácido ruménico/100 g de ácidos grasos. El segundo alimento fue elaborado adicionando grasa láctea experimental al alimento balanceado comercial para ratones. Este alimento, denominado GLE, presentó 20,58% de lípidos totales, con bajo contenido de grasas saturadas (37,6g/100 g de ácidos grasos) y alto contenido de ácido vaccénico (16,8 g/100 g de ácidos grasos) y ruménico (2,5 g/100 g de ácidos grasos). Por otra parte, el alimento balanceado comercial (control) presentó bajo contenido graso (3,55%); con 22,9 g de grasas saturadas/100 g de ácidos grasos totales y 0,5 g de ácido vaccénico/100 g de ácidos grasos totales. El alimento control proporcionó el 65% de la energía dietética en forma de carbohidratos, el 25,55% de la energía dietética como proteínas y el 7,43% de la energía dietética como grasa total. La energía dietética del alimento GLP fue suministrada por carbohidratos: 41,64%; proteínas: 16,48% y grasas: 40,99%. Mientras que la energía dietética del alimento GLE fue suministrada por carbohidratos: 42,15%; proteínas: 16,14% y grasas: 40,35%.
Tabla 2 Composición nutricional del alimento balanceado (control) y de los alimentos altos en grasas lácteas de pastura (GLP) y experimental (GLE).
| Determinación | 240.Control | 241.GLP | 242.GLE |
|---|---|---|---|
| Humedad (%) | 245.2,4 | 246.2,34 | 247.4,39 |
| Materia seca (%) | 250.97,60 | 251.97,66 | 252.95,60 |
| Proteína bruta (%) | 255.23,22 | 256.19,44 | 257.18 |
| Extracto etéreo (%) | 260.3,55 | 261.21,12 | 262.20,58 |
| Carbohidratos (%) | 265.59,63 | 266.48,01 | 267.47,72 |
| Fibra bruta (%) | 270.4,09 | 271.2,24 | 272.3,03 |
| Cenizas (%) | 275.7,11 | 276.6,85 | 277.6,27 |
| Energía (Kcal g-1) | 280.3,63 | 281.4,61 | 282.4,46 |
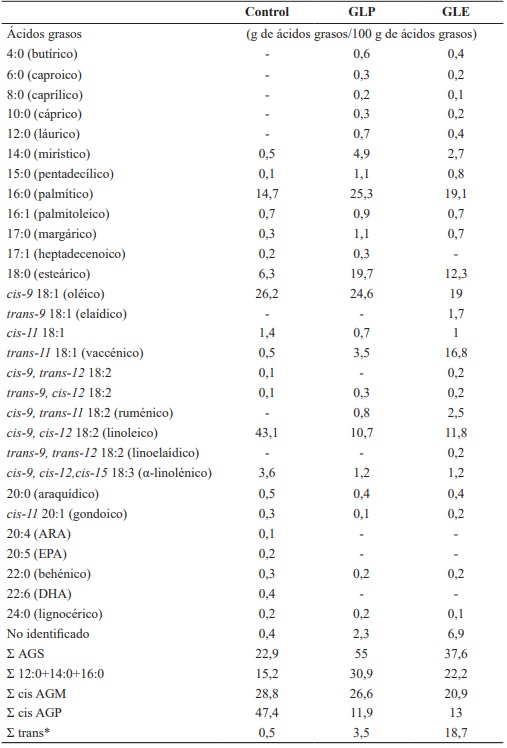
Tabla 3 Composición de ácidos grasos (g de ácidos grasos/100 g de ésteres metílicos de ácidos grasos) del alimento control y los alimentos altos en grasas lácteas de pastura (GLP) y experimental (GLE). AGS: ácidos grasos saturados. AGM: ácidos grasos monoinsaturados. AGP: ácidos grasos poliinsaturados. *La suma no incluye a cis-9,trans-11 18:2. ARA: ácido araquidonico. EPA: ácido eicosapentaenoico. DHA: ácido docosahexaenoico. Perfil de ácidos grasos realizado por INTI Agroalimentos (AOCS Ce 1k-09:2009 “Direct methylation of lipids in foods for the determination of total fat, saturated, cis-monounsaturated, and trans fatty acids by gas chromatography” e ISO 12966-4:2015 “Animal and vegetable fats and oils-gas chromatography of fatty acid methyl esters- Part 4: Determination by capillary gas chromatograph”).
Plan experimental. Luego de un período de adaptación, los ratones fueron asignados, al azar, a 3 diferentes tipos de dietas (seis animales por dieta): una dieta estándar para ratones (control); alimento GLP, que constituyó el control más apropiado, y la tercera consistió en el alimento GLE. Las dos dietas suplementadas con grasa presentaron altos niveles de aporte energético derivado de las grasas (≈40% de calorías) por lo que podrían considerarse como dietas altas en grasas (Speakman 2019). La experiencia tuvo una duración de 154 días.
Evaluaciones durante la experiencia. El consumo de alimento se registró diariamente y el peso corporal se registró al inicio del experimento y semanalmente en todos los animales.
Necropsia y toma de muestras. Luego de 154 días, se procedió a la extracción de sangre, eutanasia y necropsia de todos los animales. Esto se realizó bajo anestesia general, empleando una combinación de ketamina 200 mg kg-1 y xilacina 10 mg kg-1, vía intraperitoneal. Previo ayuno de 8 horas, se realizó exanguinación mediante punción de la vena cava caudal empleando una aguja 25G x 5/8´ y jeringas de 3 ml. El hígado fue disecado, pesado, se evalúo su aspecto macroscópico y una muestra de 5 mm de espesor del lóbulo lateral izquierdo fue fijada en formol bufferado al 10% durante 24 hs para su análisis histológico. El resto del hígado fresco fue congelado para la determinación de lipidos totales. La grasa epididimal fue disecada y pesada.
Bioquímica sérica. Con las muestras de sangre se determinó colesterol total (colesterol-oxidasa-peroxidasa); la enzima aspartato aminotransferasa (AST-aspartato cetoglutarato) y la enzima alanino aminotransferasa (ALT- alanina cetoglutarato) (lectura a 505 nm y reactivos de Weiner).
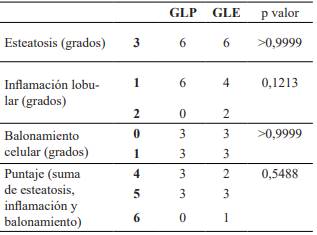
Histopatología hepática. Las muestras formoladas de hígado fueron procesadas según la técnica histológica clásica para bloques parafinados, cortadas a 5 μm y teñidas con hematoxilina-eosina (HE) y tricrómica de Mallory para fibras colágenas. Se utilizó el sistema de graduación y estadificación para la degeneración grasa hepática no alcohólica propuesta por Kleiner et al. (2005). Brevemente, el sistema comprende la evaluación de 4 caracteristicas histológicas semicuantitativas del hígado, las cuales son:
Los componentes esteatosis (0 a 3), inflamación lobular (0 a 3) y balonamiento hepatocelular (0 a 2) se sumaron para asignar a cada caso un puntaje de 0 a 8. Este sistema de puntuación ayuda a distinguir casos con degeneración grasa hepática no alcohólica no progresiva (puntaje ≤ 2), de aquellos con esteatohepatitis no alcohólica (puntaje ≥ 5) y con un potencial de progresar a formas de daño hepático más avanzado como la cirrosis (Kleiner et al. 2005).
Contenido total de lípidos en hígado. Fue determinado gravimétricamente mediante el método de extracción Soxhlet, AOAC.
Análisis estadístico. Los resultados fueron expresados como la media ± desvío estándar. Para determinar las diferencias entre los tres grupos de los parámetros nutricionales, bioquímicos y los pesos corporal, hepático y de la grasa epididimal se utilizó un análisis de varianza de una vía (ANAVA), seguido de una prueba de Tukey post hoc. La prueba de Kruskal-Wallis fue aplicada a las variables que no cumplieron los supuestos del ANAVA. Las variables categoricas de la histopatología hepática fueron comparadas entre los dos grupos tratados con dietas altas en grasas mediante una tabla de contingencia. Las diferencias entre los grupos fueron declaradas significativas con p ≤ 0,05.
Resultados
Consumo de alimento. Durante la experiencia, todos los ratones mostraron un estado saludable. Las dietas fueron bien aceptadas y el consumo de alimento no difirió entre los grupos (p=0,8102). No se registró diferencia en el consumo de calorías entre los ratones que recibieron los alimentos altos en grasas lácteas a pastura y experimental, los cuales consumieron ≈3,4 Kcal día-1 más que los ratones control (p<0,0001) (Tabla 4).
Peso corporal. Los ratones que recibieron ambos tipos de dietas alta en grasa láctea se volvieron obesos y pesaron ≈49% más que el grupo control (p<0,0001). El peso de la grasa epididimal de los ratones que recibieron ambos tipos de dietas alta en grasa fue ≈60% superior, comparado al peso de la grasa epididimal del grupo control (p=0,0003). El tipo de grasa láctea no modificó el peso corporal final, ni el peso de la grasa epididimal de los ratones (Tabla 4).
Tabla 4 Efectos de alimentos altos en grasas lácteas bubalinas de pastura (GLP) y experimental (GLE) sobre parámetros nutricionales, peso corporal y peso de la grasa epididimal de ratones C57BL/6J.
| 310. | Control | 311.GLP | 312.GLE |
|---|---|---|---|
| Consumo de alimento (g kg-1) | 315.4,20 ± 0,76a | 316.4,06 ± 0,82a | 317.4,17 ± 0,65a |
| Consumo de energía (Kcal día-1) | 320.15,27 ± 2,74a | 321.18,75 ± 3,80b | 322.18,62 ± 2,87b |
| Consumo de energía aportada por 325. las grasas (Kcal día-1) | 326.1,14 ± 0,20a | 327.7,69 ± 1,56b | 328.7,51 ± 1,16b |
| Peso corporal inicial (g) | 331.25,80 ± 1,15a | 332.27,46 ± 1,50a | 333.27,69 ± 1,29a |
| Peso corporal final (g) | 336.32,49 ± 3,49a | 337.48,77 ± 2,76b | 338.50,24 ± 2,76b |
| Ganancia de peso (g) | 341.6,70 ± 2,44a | 342.21,32 ± 1,90b | 343.22,55 ± 2,13b |
| Grasa epididimal (g) | 346.1,14 ± 0,31a | 347.1,89 ± 0,38b | 348.1,75 ± 0,23b |
En una misma fila, medias con una letra común no son significativamente diferentes (p>0,05).
Bioquímica sérica. La colesterolemia no registró diferencia entre los tratamientos (p>0,667). Comparado con el grupo control, los niveles séricos de ALT se incrementaron en los ratones GLP (p=0,05). Mientras que los niveles séricos de ALT no difirieron entre los grupos que recibieron dieta alta en grasas (p>0,05). Los niveles séricos de AST no registro diferencias entre los tratamientos (p=0,657) (Tabla 5).
Tabla 5 Efectos de alimentos altos en grasas lácteas bubalinas de pastura (GLP) y experimental (GLE) sobre la colesterolemia y aminotransaminasas séricas de ratones C57BL/6J.
| 356. | Control | 357.GLP | 358.GLE |
|---|---|---|---|
| Colesterol total (mg dl-1) | 361.105,67 ± 13,53a | 362.113,67 ± 41,48a | 363.126,00 ± 33,68a |
| ALT (U l-1) | 366.41,00 ± 6,36a | 367.72,33 ± 9,67b | 368.56,17 ± 20,40ª,b |
| AST (U l-1) | 371.76,67 ± 7,94a | 372.80,67 ± 28,56a | 373.92,00 ± 32,71a |
En una misma fila, medias con una letra común no son significativamente diferentes (p>0,05).
Peso, aspecto macroscópico y contenido de grasa en hígado. Los ratones que recibieron alimento con grasa láctea experimental tuvieron un significativo (p<0,0001) incremento del peso del hígado (Figura 1, Tabla 6). Macroscopicamente, los hígados evidenciaron hepatomegalia y coloración parda (Figura 1G) con respecto al grupo control (Figura 1A). Los ratones que recibieron ambos tipos de grasas lácteas bubalinas registraron mayor contenido de extracto etéreo hepático, con respecto a los ratones control (p<0,0001). El tipo de grasa láctea no modificó el contenido de grasa en el hígado de los ratones (p>0,05) (Tabla 6).
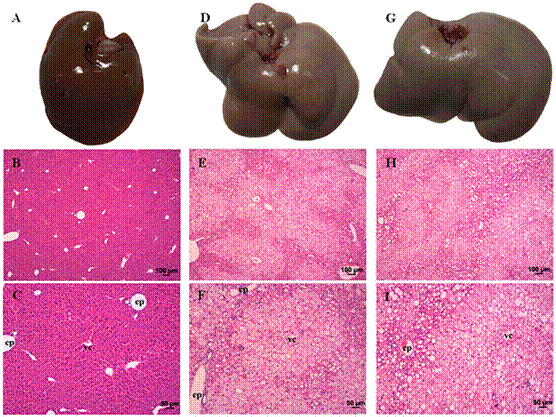
Figura 1: A, B y C: Hígados de ratones control (B: 5x, C: 10x; HE). D, E y F: Hígados de ratones con dieta alta en grasa láctea de búfalas alimentadas con pastura natural (grupo GLP). Hígado aumentado de tamaño, color pardo y con patrón lobulillar (D), debido a esteatosis grado 3 de tipo microvacuolar en zona centrolobulillar y macrovacuolar en zona periportal (E: 5x, F: 10x; HE). G, H e I: Hígado de ratones con dieta alta en grasa láctea de búfalas alimentadas con pastura natural + mezcla de aceites de girasol y pescado (grupo GLE). Hígado aumentado de tamaño y color pardo (G), debido a esteatosis grado 3 de tipo microvacuolar en zona centrolobulillar y macrovacuolar en zona periportal (H: 5x, I: 10x; HE). (ep: espacio porta; vc: vena central).
Tabla 6 Efectos de dos alimentos altos en grasas lácteas bubalinas de pastura (GLP) y experimental (GLE) sobre el peso y contenido de grasa en hígado de ratones C57BL/6J.
| 384. | Control | 385.GLP | 386.GLE |
|---|---|---|---|
| Peso del hígado (g) | 389.1,54 ± 0,18a | 390.3,45 ± 0,73b | 391.4,60 ± 0,62c |
| Relación peso hepático/peso corporal (%) | 394.4,74 ± 0,15a | 395.7,02 ± 1,13b | 396.9,15 ± 1,12c |
| Extracto etéreo (%) | 399.4,14 ± 2,04a | 400.26,06 ± 4,26b | 401.30,91 ± 5,69b |
En la misma fila, medias con una letra común no son significativamente diferentes (p>0,05).
Histopatología hepática. No se detectó una relación (p>0,999) entre el tipo de grasa y el grado de esteatosis hepática (Tabla 7). En todos los ratones que recibieron dieta alta en grasas, predominó una esteatosis grado 3 (>66% del parénquima afectado) de tipo microvacuolar en los hepatocitos de la zona centrolobulillar y mediozonal del parénquima; y de tipo macrovacuolar en los hepatocitos de la zona periportal (Figura 1 E,F,H e I). La inflamación lobular (Figura 2), el balonamiento hepatocelular y el puntaje de actividad no fue modificada por el tipo de grasa láctea (p>0,05, Tabla 7). Los ratones control no evidenciaron esteatosis (Figuras 1B y C). No se evidenció fibrosis en ninguno de los ratones de los diferentes grupos.

Figura 2: A: Hígado de ratón control (40x, HE). B: Hígado de ratón con dieta alta en grasa láctea de búfalas alimentadas con pastura natural (GLP). Esteatosis grado 3 y un foco de infiltrado neutrofílico alrededor de hepatocitos necróticos (inflamación lobular) (flecha) (40x; HE). C: Hígado de ratón con dieta alta en grasa láctea de búfalas alimentadas con pastura natural + mezcla de aceites de girasol y pescado (GLE). Esteatosis grado 3 y tres focos de inflamación lobular (flechas) (40x, HE).
Discusión
Este trabajo comparó los efectos de dos alimentos altos en grasas de una leche con perfil natural de ácidos grasos obtenida de búfalas en un sistema pastoril vs. una leche de búfalas experimental reducida en grasas saturadas (-31%), reducida en grasas cis insaturadas (-11,9%) y enriquecida con ácido ruménico (+212,5%) y con grasas trans (+434,2%, predominantemente por el ácido vaccénico), en un modelo murino de HGNA. Comparado con el grupo control, los ratones que recibieron las dietas GLP y GLE desarrollaron una severa degeneración grasa hepática (>66% de parenquima afectado), con inflamación lobular y balonamiento hepatocelular; tres componentes necesarios para el diagnóstico de EHNA en el humano (Takahashi et al. 2014, Bertola 2018). Estos cambios histopatológicos del hígado se produjeron en el marco de obesidad e incrementos séricos de ALT. Similar a nuestro registro del peso corporal, ratones C57BL/6J expuestos a una dieta alta en grasas, alta en carbohidratos simples y baja en fibra desarrollaron obesidad (≈50 gr de peso corporal) asociada a diabetes. El ratón C57BL/6J tiene una predisposición genética a desarrollar obesidad y diabetes no dependiente de insulina (diabetes tipo II) cuando es sometido a dietas alta en grasas (Surwit et al. 1988). Los incrementos séricos de ALT y AST indican fuga citoplasmática de los hepatocitos y, usualmente, son buenos predictores de la degeneración grasa hepática no alcohólica (Sattar et al. 2014). Humanos con esteatosis hepática no alcohólica registraron niveles elevados de ALT con niveles de AST normales. Cuando la esteatosis hepática progresa a esteatohepatitis y a fibrosis hepática, los niveles de AST tambien aumentaron (Sattar et al. 2014). En ratones C57BL/6J los niveles de ALT y AST plasmático no cambiaron durante 19 semanas de alimentación, a pesar del desarrollo de esteatosis hepática, aumentando significativamente después de 34 semanas de dieta muy alta en grasas (60% de calorias aportada por grasas) (Ito et al. 2007). En nuestra experiencia, los niveles de ALT se incrementaron significativamente en los ratones que recibieron dieta alta en grasa láctea de pastura, mientras que el incremento en los ratones que consumieron grasa láctea experimental tuvo alta variabilidad de respuesta, por lo tanto, sus incrementos no fueron significativos con respecto a los grupos control y pastura. Los niveles sericos de AST no se modificaron, a pesar de la esteatosis que desarrollaron todos los ratones de ambos grupos con dieta alta en grasas lácteas. Este patrón bioquímico de las transaminasas, con niveles de ALT superiores a los de AST, fueron los típicamente observados en humanos con esteatosis hepática no alcohólica (Sattar et al. 2014).
Los resultados mostraron que las dietas GLP y GLE, en un periodo de 154 días, no modificaron significativamente el peso corporal, el depósito de grasa epididimal, el contenido de grasa hepática o el grado de la degeneración grasa hepática en los ratones C57BL/6J. A diferencia de nuestros resultados, estudios previos han demostrado que el consumo durante 53, 60 o 84 días de dietas altas en grasas rumiante (22%, 23,99% o 27%) reducida en grasas saturadas (56,79% o 57%) y con niveles moderados de ácido vaccénico (0,69%, 4,46% o 4,56%), de ácido ruménico (0,5% o 1,21%) y de ácido α-linolénico (0,69% o 0,98%) han prevenido o reducido el depósito de grasa en el hígado de las ratones C57BL/6J (Benoit et al. 2014) y ratas Wistar (Brito Medeiros et al. 2021, Gerstner et al. 2021). La ingesta de grasa láctea con menos grasas saturadas y más ácidos ruménico y vaccénico aumentó la tasa de secreción de triglicéridos, aumentó la β-oxidación y redujo la absorción de ácidos grasos en el hígado de las ratas (Gerstner et al. 2021). El consumo de ácido ruménico y vaccénico disminuyó la lipogénesis hepática (Jacome-Sosa et al. 2010), redujo el grado de esteatosis hepática (-42%) y atenúo la progresión del HGNA en ratas obesas JCR:LA- cp (Jacome-Sosa et al. 2014). Teniendo en cuenta varias diferencias en el diseño de los estudios, una comparación exacta de nuestros resultados con los resultados de estudios previos puede no ser fiable. La leche de búfala experimental registró niveles inferiores de grasas saturadas y niveles de ácido ruménico y vaccénico superiores a los reportados previamente para dietas con efecto reductor o preventivo de la acumulación de grasa hepática en ratas (Jacome-Sosa et al. 2014, Brito Medeiros et al. 2021, Gerstner et al. 2021) y ratones (Benoit et al. 2014). Sin embargo, comparada con la leche de búfalas a pastura y con los trabajos previos, el contenido de grasas cis insaturadas y de grasas trans de la leche de búfala experimental no serían adecuados.
La leche bubalina experimental registró 50% menos ácido α-linolénico que la leche bubalina de pastura y fue inferior a los trabajos reportados previamente para dietas con efecto reductor de la grasa hepática (Benoit et al. 2014, Brito Medeiros et al. 2021). La ingesta de ácidos grasos poliinsaturados n-3 (α-linolénico, EPA y DHA) indujeron a una reducción de la grasa hepática (Hodson et al. 2020). El ácido α-linolénico disminuyó la esteatosis y la inflamación del hígado, ya que redujo la lipogénesis hepática (Lottenberg et al. 2012), incrementó las citocinas anti-inflamatorias (Brito Medeiros et al. 2021) e incrementó la oxidación de lípidos en el hígado (Benoit et al. 2014).
Con respecto a las grasas trans, el perfil de ácidos grasos de la leche experimental registró incrementos entre 3,5 y 4 veces en los ácidos grasos trans-8 18:1, trans-9 18:1 (ácido elaídico) y trans-10 18:1; e incrementó 3 veces el contenido de trans-9,trans-12 18:2 (ácido linoelaídico). Se estimó que las grasas trans, incluido el ácido vaccénico, aportaron ≈7,5% de las calorías diarias (≈0,15 g de grasas trans/día) en los ratones GLE. Ya se han reportado que los incrementos sustanciales de las grasas trans rumiante, cuyo principal isómero trans 18:1 es el acido vaccénico, pueden contrarrestar el efecto saludable que se desea lograr al reducir las grasas saturadas e incrementar las grasas insaturadas en la leche y sus productos. Por ejemplo, a nivel cardiovascular, los incrementos sustanciales de las grasas trans en la leche, con ingestas que aportaron el 3,3- 3,7% de las calorías diarias, causó hipercolesterolemia e incrementó las subfracciones aterogénicas de las lipoproteínas en humanos (Motard-Bélanger et al. 2008, Gebauer et al. 2015) y en cobayos (Rice et al. 2010). Este efecto no fue corroborado en nuestros resultados, donde se registró un efecto neutro sobre la colesterolemia. También se han documentado efectos hepatotoxicos de algunos ácidos grasos trans que estuvieron incrementados en la leche bubalina experimental del presente trabajo. La degeneración grasa, la respuesta inflamatoria (FNTα) y la respuesta pro-fibrogénica (pro-colágeno) en el hígado de ratones, fueron sustancialmente mayores cuando recibieron una dieta con 30% de grasas trans; comparado con una dieta isocalórica conteniendo grasas saturadas (Tetri et al. 2008). En otra experiencia, el exceso de grasa trans (28,5%) incrementó la expresión hepática de genes lipogénicos, la afluencia de ácidos grasos no esterificados al hígado, la acumulación hepática de peróxidos lipídicos e indujo una severa degeneración grasa hepática en los ratones (Obara et al. 2010). El ácido graso trans-10 18:1, extraido de la grasa de bovinos alimentados con granos, resultó ser más citotóxico que trans-9 18:1 (extraido de aceite parcialmente hidrogenado) (Vahmani et al. 2016b) e indujo degeneración vacuolar de hepatocitos, rarefacción del citoplasma hepatocelular y activación de las células de Kupffer, asociado a incrementos de triglicéridos y colesterol-LDL, en ratas (Anadón et al. 2010). Los isómeros trans-6, trans-9 y trans-10 18:1 extraidos de la grasa de rumiantes alimentados con cereales tuvieron efectos lipogénicos, colesterogénico y citotóxico en cultivos de hepatocitos (Krogager et al. 2015, Vahmani et al. 2016a,b). En un estudio que determino el perfil de ácidos grasos en el plasma de personas con HGNA, se descubrio que el ácido linoelaídico (trans-9, trans-12 18:2) estuvo significativamente elevado y se correlacionó positivamente con marcadores de necrosis y apoptosis de hepatocitos (Tabuchi et al. 2014).
La principal limitación de este trabajo fue que las grasas reemplazaron una porción de la dieta de los ratones. Por lo tanto, no podemos descartar que al menos una fracción de los efectos nocivos observados en ambas dietas altas en grasas lácteas pudiera ser explicada por la reducción de nutrientes junto al incremento de las grasas.
Aunque la composición de la grasa en la dieta puede jugar un papel en la acumulación de grasa en el hígado (Lottemberg et al. 2012, Benoit et al. 2014, Hodson et al. 2020, Gerstner et al. 2021); en la presente experiencia pareciera que el exceso de grasa y no el tipo de grasa láctea pudo haber sido responsable de los cambios observados. Los estudios que investigaron el papel de la grasa dietaria en la esteatosis hepática han demostrado claramente que la ingesta total de energía, más que la ingesta de grasas per se, es un mediador clave en el contenido de grasa en el hígado (Hodson et al. 2020). Otra explicación de la falta de efecto protector de la leche bubalina GLE sobre la degeneración grasa hepática estaría en la proporción entre grasas con efecto reductor vs. grasas con efecto promotor del depósito de grasa hepática. En la leche bubalina experimental, la reducción de las grasas saturadas y el incremento de los ácidos grasos ruménico y vaccénico que pudieran haber atenuado el depósito de grasa hepática, posiblemente fue neutralizado por el alto nivel de grasas trans y la reducción de grasas poliinsaturadas n-3 que pudieron promover dicho depósito.
En conclusión, una grasa láctea de búfalas a pastura y una grasa láctea bubalina reducida en grasas saturadas y altos niveles de ácidos ruménico y grasas trans, ambos incorporados en una dieta alta en grasas, causaron cambios similares y ninguna atenuó la degeneración grasa hepática en ratones C57BL/6J.