INTRODUCCIÓN
La definición de un “corazón sano” determina en sí misma un buen pronóstico. Por otro lado, un corazón “enfermo”, de por sí, empeora el pronóstico para cualquier sujeto estudiado. Por lo tanto, es esencial diferenciar los individuos sanos de los pacientes enfermos.
La falta de compactación del ventrículo izquierdo es un diagnóstico cada vez más frecuente. Desde sus inicios fue considerado una patología. La mejoría de las técnicas de imágenes no invasivas, como la ecocardiografía, la tomografía computada y sobre todo la resonancia magnética cardíaca (RMC), han ayudado a incrementar su diagnóstico. 1 Sin embargo, aún se debate si el miocardio no compacto (MNC) es una condición patológica en sí misma o un cambio histológico de un miocardio normal, debido a un fenómeno fisiológico adaptativo.
Para la organización mundial de la salud (OMS) la definición de enfermedad es una “Alteración o desviación del estado fisiológico en una o varias partes del cuerpo, por causas en general conocidas, manifestada por síntomas y signos característicos, y cuya evolución es más o menos previsible” Para conocer si el MNC cumple con estos criterios y puede ser considerado una enfermedad en sí mismo, nosotros hemos realizado un análisis observacional en 161 estudios de RMC realizados a 140 pacientes con diagnóstico de MNC. Los datos de la población estudiada fueron comparados con un grupo de sujetos sanos (grupo control), a fin de determinar si fueron “patológicamente diferentes” al utilizar y exponerlos al concepto de enfermedad definido por la OMS.
MATERIAL Y MÉTODOS
Entre julio de 2007 y enero 2022 se realizaron 161 estudios de RMC, a 140 pacientes con diagnóstico de MNC. Los pacientes fueron referidos a nuestro centro para estudio de RMC por diferentes patologías (Figura 1). El criterio utilizado para el diagnóstico de MNC fue la detección de dos capas miocárdicas, una trabecular no compacta (NC) y otra compacta (C) ubicadas en algún segmento de las paredes ventriculares con una relación entre ellas mayor a 2,3 según el criterio de Petersen 2 (Figura 2-A). Para analizar la localización del MNC se utilizó la clasificación de 17 segmentos ventriculares propuesta por Cerqueira y col., 3 donde el segmento apical fue tomado como uno solo sin segmentación. El grupo de pacientes con diagnóstico de MNC se comparó con un grupo de 14 sujetos normales considerados como grupo control. Los sujetos del grupo control se realizaron la RMC por diversos motivos no cardiovasculares; no tenían antecedentes de hipertensión arterial, enfermedad coronaria, ni valvulopatías al momento del examen. Además, se utilizó como variable de seguridad para definir normalidad, que no presentaran área auricular izquierda mayor a 22 cm2. Se utilizó esta variable debida su sensibilidad para detectar cualquier tipo de disfunción diastólica ventricular izquierda. 4
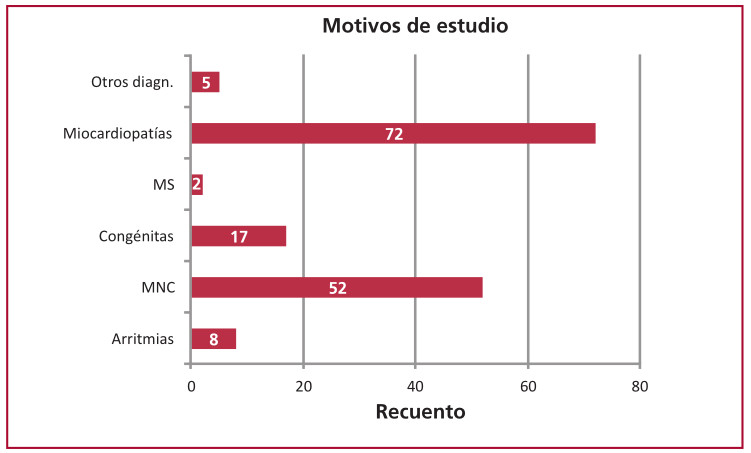
Fig. 1. Motivos de estudio de la RMC (n = 156)Diferentes patologías asociadas al MNC en nuestra población de pacientes. MS: Muerte súbita, MNC: Miocardio no compacto

Fig. 2. Secuencias diagnósticas de RMCSecuencias diagnósticas de RMC. A: Imagen cine con secuencia SSFP, en eje corto a nivel medio del corazón, donde se observa la trabeculación ventricular con la medición de las dos capas del miocardio, presentando criterios de MNC (4,7/1,35=3,48) B: Secuencia de doble inversión recovery, con Gadolinio en análisis tardío, donde se puede observar hiperintensidad intramiocárdica lineal, a nivel del septum interventricular y pericárdica lateral. C: Secuencia de mapping miocárdico, con aumento del T1 a nivel septal, de 1440 ms, en un paciente con miocarditis repetitivas. D: Paciente con miocardiopatía dilatada y deterioro severo de la función ventricular. Imagen de la izquierda en diástole y a la derecha en sístole. Durante la sístole, se puede observar mejor motilidad miocárdica en los segmentos con MNC en la cara lateral (flechas) en comparación con los segmentos septales “sin MNC”.
Estudio de resonancia: Las resonancias se realizaron con un equipo de 3T (scanner Philips Innova). Para el análisis de la motilidad y función ventricular se utilizaron las secuencias de cine steady-state free precession (SSFP) en cortes de eje largo, cuatro cámaras y múltiples cortes en eje corto, cubriendo todo el ventrículo desde la base hasta la punta, como fuera previamente publicado. 5 En los segmentos donde se evidenció hipertrabeculación, se analizó, en diástole, el espesor de las capas miocárdicas trabeculada y no trabeculada. Se consideró MNC cuando esta relación fue superior a 2,3 (Figura 2-A). Para las imágenes contrastadas, se utilizó 0,2 mmol/kg de Gadopentato de Dimeglumina (Viewgam, Bacom) en forma endovenosa. Para el mapeo de T1 se utilizó una secuencia de Inversión “Look-Locker” modificada con una sola apnea, con tres cortes a nivel del eje corto basal y medio ventricular antes y después de la administración del contraste. Las imágenes tardías se tomaron entre 10 y 20 minutos después de la administración de contraste, según los parámetros previamente publicados. 6
Estadísticas
Los datos fueron analizados con el programa IBM SPSS statistics V25 (IBM). Las variables dicotómicas se expresan como porcentajes, y las variables continuas como medias ± DS. En la comparación de las variables continuas con distribución normal se utilizó el T test para muestras diferentes, o pruebas de U de Mann-Whitney en caso contrario. Para el análisis de las variables categóricas se utilizó el test de Chi cuadrado, considerándose una diferencia significativa cuando el valor de p fue < 0,05.
RESULTADOS
Características basales. En el grupo de estudio (n=140) el 51,4 % (72) fueron hombres. La edad promedio fue 31,37 ± 20,01 (rango 1-89 años), y la mediana de 30 años. El grupo control presentó un promedio de edad de 39,9 ± 3,45 años, sin diferencias significativas con el grupo de MNC. La edad de los pacientes presentó una distribución normal. El mayor porcentaje de pacientes, 62,42%, tenía edad entre 26 y 65 años. La fracción de eyección ventricular izquierda (FEVI) en los pacientes con MNC estaba globalmente conservada (56,66 ± 19,41) con grado variable de compromiso (Tabla 1, Figura 3).
Tabla 1 Datos biométricos comparativos entre los grupos estudiados
| MNC total pacientes | Grupo control | p (*) | MNC con corazón normal | p (†) | |
|---|---|---|---|---|---|
| (n = 140) | (n = 14) | (n = 38) | |||
| Edad, años | 31,37 ± 20,01 | 39,92 ± 12,46 | 0,011 | 39,9 ± 3,45 | 0,02 |
| Sexo | 72/68 | 10/4 | |||
| VFD (ml) | 164,42 ± 86,03 | 138,50 ± 22,07 | 0,017 | 132,50 ± 51,55 | 0,36 |
| VFS (ml) | 81,03 ± 82,17 | 52,43 ± 13,17 | 0,01 | 47,03 ± 24,43 | 0,001 |
| VS (ml) | 83,39 ± 37,57 | 86,07± 11,72 | 0,01 | 85,47 ± 32,41 | 0,54 |
| FEVI (%) | 56,66 ± 19,41 | 62,43 ± 5,39 | 0,001 | 66,86 ± 9,67 | 0,001 |
| Mio. Trabecular (mm) | 14,44±4,16 | - | - | 13,74±3,78 | 0,71 |
| Mio. Compacto (mm) | 5,21±1,92 | - | - | 4,94±1,31 | 0,27 |
| Relación C/NC | 2,95±0,91 | - | - | 2,82±0,92 | 0,63 |
| T1 mapping (ms) | 1302 ± 62,41 | 1236 ± 29 | 0,006 | 1280,00 ± 8,49 | 0,05 |
| T2 mapping (ms) | 42,45 ± 6,46 | 43,53 ± 2,07 | 0,107 | 43,00 ± 1,41 | 0,38 |
VFD: volumen de fin de diástole ventricular izquierdo, VFS: volumen de fin de sístole ventricular izquierdo, VS: volumen sistólico, FEVI: fracción de eyección ventricular izquierda, Mio. trabecular: miocardio trabeculado, Mio. Compacto: compacto. C: compacto. NC: no compacto. T1 mapping, T2 mapping. (*) = significancia entre el grupo total de MNC vs. el grupo control, (†) = significancia entre el grupo control vs. el grupo con MNC y corazón normal.

Fig. 3 Diversas fracciones de eyección ventricular izquierda en el MNC Fracciones de eyección observadas en los pacientes con MNC. Fey: Fracción de eyección.
Distribución y magnitud del MNC: se observó que el 59,6% de los segmentos correspondían a las caras anterolateral y apical del ventrículo izquierdo. Los segmentos ventriculares menos comprometidos por el MNC fueron los segmentos basales de ambos ventrículos y el septum interventricular (7,14%y 12,9% de los pacientes, respectivamente) (Figura 4). El promedio global del espesor parietal de la porción NC fue de 13,91 ± 4,1 mm vs. 5,14 ± 1,80 mm en la C, con una relación NC/C de 2,87 ± 0,92.
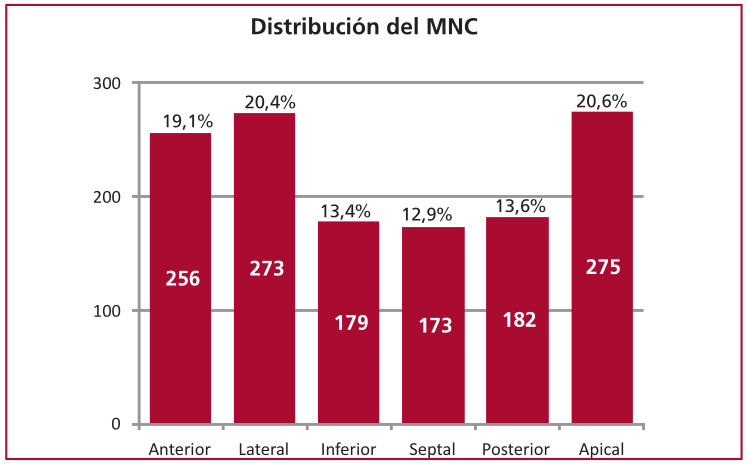
Fig. 4 Ubicación ventricular del MNC. Número de segmentos comprometidos Fracciones de eyección observadas en los pacientes con MNC. Fey: Fracción de eyección.
Comparación de pacientes con MNC y corazón
Treinta y ocho sujetos, el 27,1% del total de los pa cientes con el diagnóstico de MNC, no presentaban ninguna otra alteración patológica en el corazón, más allá que el hallazgo del MNC, y se los consideró portadores de corazones normales con hipertra beculación en el estudio de RMC. En el 91,5% de estos pacientes, el motivo para la indicación de la RMC fue por presentar arritmias cardíacas (67%) o sospecha de alguna miocardiopatía (24,5%). (Figura 1) Al comparar “globalmente” al grupo control con los pacientes con MNC, estos últimos, presentaban mayores volúmenes y menor FEVI, aunque los valores observados permanecieron dentro de los rangos de normalidad (Tabla 1). No se observó diferencia con respecto a la magnitud del MNC entre el total de los pacientes y el grupo de pacientes con MNC y corazón considerado normal. La única diferencia funcional significativa observada entre los pacientes con MNC y “corazón con características normales” y los controles es que los primeros tenían mejor FEVI: 66,86 ± 9,67% vs. 62,43 ± 5,39%, p<0,001 (Tabla 1).
DISCUSIÓN
El criterio diagnóstico de MNC fue desarrollado a partir de la relación entre el miocardio trabeculado y no trabeculado, en una población de sujetos normales; no a partir de signos y síntomas clínicos en pacientes en quienes se observaron estas “anormalidades”. Se podría decir, que primero se observó algo en el ventrículo y luego se lo empezó a asociar a múltiples hallazgos clínicos.
Este es uno de los primeros trabajos que estudia la presencia de MNC “en el mundo real”, independientemente de la patología de base por la que fue solicitado el estudio, evitando de esta manera “el sesgo de inclusión” en los pacientes.
Según la OMS, la definición de enfermedad, es la “Alteración o desviación del estado fisiológico en una o varias partes del cuerpo, por causas en general conocidas, manifestada por síntomas y signos característicos, y cuya evolución es más o menos previsible”. Nosotros analizamos punto por punto esta definición para ver si el MNC tiene criterio para ser considerado una enfermedad o no.
1. “Es una alteración o desviación del estado fisiológico en una o varias partes del cuerpo” Si analizamos la primera parte de la definición de la OMS para ser considerado una enfermedad, la presencia de trabéculas en los ventrículos es normal. En nuestra población estudiada, el 27% de los sujetos tenía MNC con corazón normal. El alto porcentaje de individuos sanos con MNC, avalaría el concepto de ser un hallazgo de mayor o menor magnitud dentro de la normalidad. El dato interesante es que en los pacientes con MNC y corazón normal, la FEVI fue más alta que en el grupo control sin MNC (Tabla 1). Estos conceptos de “normalidad mejorada” coinciden con los hallazgos de Moore y col., que estudian la función ventricular por análisis fractal, y exponen que las trabéculas no son deletéreas para la función ventricular, sino todo lo contrario, ya que “ayudan” a la adecuada contracción y relajación ventricular en corazones normales. 7 Tampoco en el Mapping miocárdico realizado con RMC se observó diferencias entre estos grupos de pacientes, a pesar de ser un método de alta sensibilidad para determinar anormalidades miocárdicas (Figura 2-C, Tabla 1).
Por lo tanto, un miocardio normal, expuesto a condiciones de estrés, puede desarrollar hipertrabeculaciones. Esto se ha visto en los deportistas de alto rendimiento: los sujetos entrenados presentan significativamente más trabeculaciones que los no entrenados (18,3% vs. 7%) como lo han publicado es sus respectivos trabajos Fermia y Gati.8,9
2. La segunda parte de la definición de enfermedad de la OMS expresa “…por causas en general conocidas…”. Si bien existen varias teorías sobre el desarrollo del MNC en el ser humano, como la detención en el mecanismo de compactación ventricular, o alteraciones genéticas que llevan a la disyunción de los discos intercalares provocando un miocardio no compacto, no tenemos una teoría única y ciertamente documentada que sea aplicada a todos los individuos con MNC. Las teorías son tan diversas como asociadas a gran cantidad de patologías en las que aparece esta hipertrabeculación. El dato coincidente, en la gran mayoría de las personas con MNC, es que el miocardio donde se desarrollan estas trabéculas, está expuesto a un mayor estrés, ya sea por condiciones patológicas o fisiológicas, como se observa en áreas de isquemia, edema por miocarditis o en los deportistas de alto rendimiento.
3. El “Origen genético…” Mientras que la American Heart Association incluye al MNC entre las miocardiopatías de origen genético, la Sociedad Europea de Cardiología la considera como una miocardiopatía no clasificada. El diagnóstico de MNC en neonatos con insuficiencia cardíaca, ha llevado a considerar un principio genético de estos hallazgos. La presentación esporádica o en forma familiar 10 del MNC siguen siendo un tema de investigación. La mayoría de los casos familiares identificados hasta la fecha están asociados con mutaciones genéticas que también causan otras miocardiopatías, no pudiendo aislarse de estas, como las mucopolisacaridosis, defectos congénitos 11,12 miocardiopatía hipertrófica o insuficiencia cardíaca del recién nacido. 13 En nuestra población el MNC estuvo asociado a múltiples y diversas patologías bien definidas (Figura 1).
Clásicamente, se considera que el MNC es el resultado de una interrupción del normal desarrollo miocárdico, que ocurre entre las quinta y octava semanas de la embriogénesis. 14 Si asumimos que el MNC es la expresión fenotípica de una alteración genética, deberíamos explicar por qué algunos MNC varían con el tiempo y tienen comportamientos tan erráticos, aumentan o disminuyen de magnitud, sin un comportamiento definitivo, como suelen ocurrir en patologías “marcadas” por los genes. La superposición genética con otras patologías es la regla en el MNC, a tal punto que Arbustini y col. propusieron siete subtipos de alteraciones genéticas para el MNC. 15
Hipótesis del origen NO genético… El desarrollo de MNC en la edad adulta (MNC adquirido), como se observa en los deportistas de alto rendimiento 9 o durante el embarazo, donde ocurre en más del 25% de las pacientes, 16 irían en contra de estas teorías genéticas. En los casos adquiridos, el desarrollo del
MNC se debería a un “remodelamiento” ventricular secundario a un aumento de las condiciones de carga o isquemia miocárdica. La necesidad de buscar oxígeno en la cavidad ventricular sería el estímulo que desencadenaría en algunos pacientes las trabéculas endocárdicas, aumentando de esta manera, la superficie en contacto con la sangre ventricular, como lo hacía en la etapa embrionaria de su desarrollo. 17 A esto se lo podría denominar “miocardio adaptativo” por estar adaptado a diferentes condiciones de carga o a diferentes estados isquémicos, desencadenantes de las trabéculas 18 (Figura 5). De igual manera, si el estímulo que desencadena el MNC cesa, se ha visto reversión de las trabéculas en diferentes estados patológicos o no, como lo describen Philip y Fang 19 en un paciente con insuficiencia cardíaca al que se trató con un resincronizador, o en las embarazadas, donde se ha visto la aparición y desaparición del MNC con la preñez. 16.
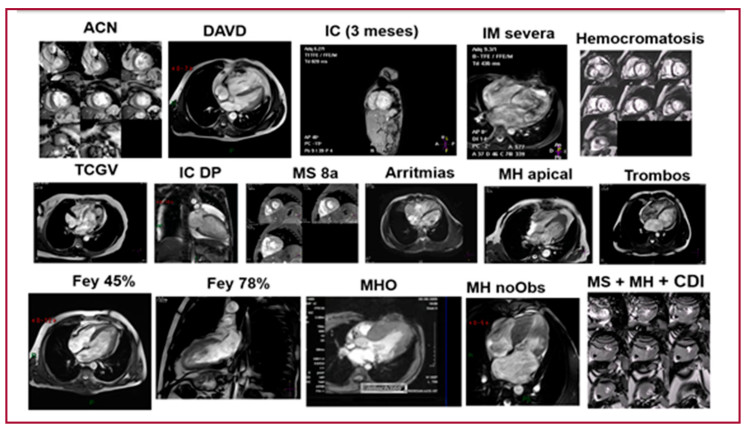
Fig. 5. Presencia del MNC en múltiples patologíasAlgunos ejemplos de las múltiples patologías donde se observó la presencia de miocardio no compacto en nuestros pacientes. MNC: miocardio no compacto ACN: ángor con coronarias normales. DAVD: displasia arritmogénica . IC: Insuficiencia cardíaca en paciente de 3 meses. IM: insuficiencia mitral Hemocromatosis. TCGV: transposición corre gida de grandes vasos. IC DP: insuficiencia cardíaca con derrame pericárdico(miocarditis). MS: muerte súbita 8 años. Arritmias. MH apical: miocardiopatía hipertrófica apical. Trombos. Fey: Fracción de eyección. MHO: miocardiopatía hipertrófica obstructiva. MH no Obs: Miocardiopatía hipertrófica no obstructiva. MS+MH+CDI: muerte súbita, mio cardiopatía hipertrófica con cardio desfibrilador implantable.
4. La tercera parte de la definición considera la presencia de “…síntomas y signos característicos…” Al MNC se lo ha asociado a arritmias cardíacas, accidente cerebrovascular e insuficiencia cardíaca, con signos y síntomas característicos de estas patologías. Del total de 140 pacientes de nuestra población, solamente el 21% presentó una FEVI menor al 55%; la gran mayoría de los pacientes con MNC (el 79%), no tenían deterioro de la función ventricular izquierda (Tabla 1). Al comparar los pacientes con FEVI normal, con los pacientes con FEVI deprimida, no se observaron diferencias con relación a la magnitud del MNC, ni en la relación de miocardio compacto/no compacto (Tabla 2). Por lo tanto, la magnitud del MNC, no se puede asociar en forma directa con la disfunción ventricular. Es interesante marcar acá algunas dudas con respecto a los pacientes con deterioro de la función ventricular y MNC. Nosotros hemos observado, que las alteraciones más importantes en la motilidad de la pared regional del ventrículo izquierdo ocurren en las regiones “sin MNC” como puede observarse en pacientes con insuficiencia cardíaca y acinesia severa en las regiones septales o basales del ventrículo izquierdo, cuando el MNC comprometía la cara anterolateral y apical (Figura 2-C). Esto iría en contra de la afirmación de que el MNC es la causa primaria de disfunción ventricular en estos pacientes.
Tabla 2 Tabla comparativa del MNC y mapping con fracción de eyección conservada o deprimida
| Variables | FEVI ≥55% (n = 51) | FEVI <55% (n = 30) | p |
|---|---|---|---|
| No compacto (mm) | 1419 ± 4,14 | 15,04 ± 4,23 | 0,52 |
| Compacto (mm) | 5,24 ± 2,09 | 5,23 ± 1,62 | 0,56 |
| Compacto/No compacto | 2,90 ± 0,92 | 3,04 ± 0,91 | 0,70 |
| T1 mapping (ms) | 1303 ± 45,66 | 1301 ± 77,78 | 0,11 |
| T2 mapping (ms) | 43,33 ± 2,94 | 41,40 ± 9,52 | 0,19 |
NC: Miocardio no compacto; FEVI: fracción de eyección ventricular izquierda
No compacto: porción trabeculada del miocardio, Compacto: porción compacta del miocardio.
5. Y finalmente, al analizar el concepto de enfermedad que señala “…y cuya evolución es más o menos previsible” Al MNC se lo ha asociado con diferentes evoluciones como ser en la miocardiopatía hipertrófica, cardiopatía isquémica, insuficiencia cardíaca con baja FEVI, arritmias, embolias periféricas y hasta muerte súbita. Esta gran variedad de patologías tiene en sí misma diferentes evoluciones; por lo tanto, si asociamos al MNC con ellas, tendríamos que asumir, que tiene el pronóstico es absolutamente errante e imprevisible. Al analizar los pacientes con MNC que tenían deterioro de la función ventricular, la presencia de MNC en sí misma no se asoció con peor pronóstico en los pacientes, como lo demuestran en su trabajo Ivanov y col. 20 Aún en pacientes con diagnóstico establecido de miocardiopatía dilatada el MNC no demostró ser un indicador independiente de mal pronóstico, como sí lo fueron la FEVI y la fibrosis miocárdica. 21,22 Además, si el MNC es solo un hallazgo en un paciente con función ventricular normal, la sobrevida es la misma que población general, como fuera recientemente publicado por Vaidya y colaboradores. 23
Basándonos en la definición de enfermedad de la OMS, el MNC no cumpliría con los criterios para ser considerado una enfermedad en sí mismo, por no tener una causa conocida para su desarrollo, sin signos ni síntomas específicos, como tampoco una evolución previsible. La evolución dependería de las otras patologías de base que presenten los pacientes.
Implicancias clínicas de los hallazgos
Es de vital importancia definir si el MNC es una enfermedad o no. Esto ayudaría, sobre todo a sujetos normales evitando enfermarlos con un diagnóstico erróneo. No obstante, es conocida, la asociación del MNC con diversas patologías o estados que estresan al miocardio (Figura 5); su aparición debería tomarse como una “bandera roja” para investigar la causa de su presencia. Por otro lado, el desarrollo de MNC observado en los deportistas y embarazadas, nos estaría enseñando que la presencia de estas trabeculaciones podría ayudar al mejor desempeño ventricular en condiciones de estrés en sujetos normales.
Futuras direcciones
Por lo anteriormente expuesto, el MNC no debería ser considerado una miocardiopatía en sí mismo, si no, un “miocardio adaptativo” ante diversas condiciones de estrés. Su presencia no ha demostrado tener mal pronóstico, sino todo lo contrario. El MNC ha demostrado mejorar la función ventricular tanto en forma segmentaria como global, lo cual abre una ventana para futuros estudios genéticos, donde el poder aislar el gen que genera el MNC, podría ser tenido en cuenta como terapéutica en pacientes con función ventricular deteriorada.
CONCLUSIONES
Nuestros resultados y razonamientos justifican un marcado replanteo del concepto de que el MNC es una enfermedad en sí misma; es más bien, una respuesta miocárdica adaptativa ante condiciones de estrés fisiológicas o patológicas. El diagnóstico de MNC debería ser tomado como un indicio para estudiar otras patologías o cambios funcionales que lo están produciendo.















