INTRODUCCIÓN
Las reacciones adversas cutáneas se consideran frecuentes en el tratamiento con medicamentos antineoplásicos1, y dentro del tratamiento sistémico de las leucemias mieloides agudas (LMA) los protocolos que incluyen a la citarabina son comunes y suelen generar diferentes reacciones adversas medicamentosas como la mielodepresión y otros efectos negativos en el sistema nervioso central, hepático, gastrointestinal y ocular2.
En diversas publicaciones, tanto en idioma español como en inglés, se comenta una aparente baja incidencia de la reacción adversa a medicamentos con compromiso cutáneo (RAMc) asociado a la citarabina, aunque esto se podría atribuir a que se subestima la real incidencia por la gravedad de la patología de base que padecen los pacientes y la relativa baja severidad de las lesiones cutáneas2,3.
La citarabina pertenece al subgrupo de medicamentos antimetabolitos análogos a la pirimidina junto a la gemcitabina, capecitabina y decitabina, este grupo farmacológico es fundamental para el tratamiento de la LMA desde hace más de cuatro décadas4,5.
Este documento fue sometido al Comité de Ética en Investigación de la Fundación Valle del Lili, quienes aprueban la integridad del documento con el consecutivo 547 en el acta número 16 de 2021.
PRESENTACIÓN DE CASO
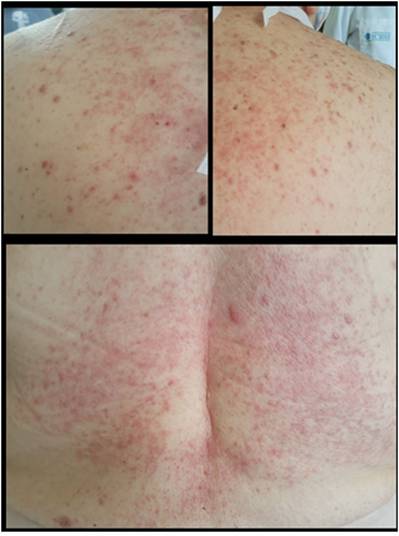
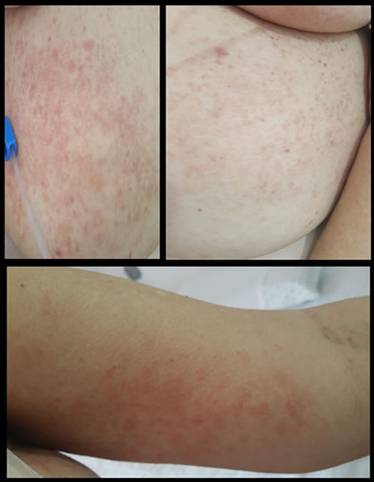
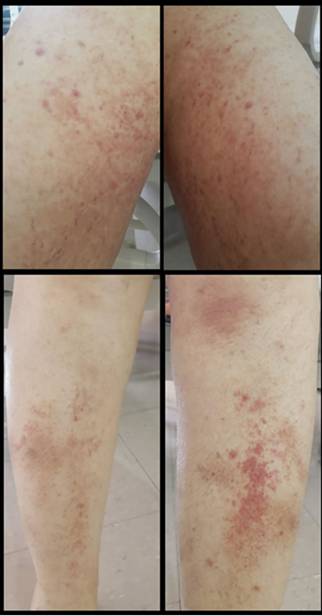
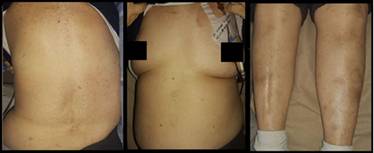
Paciente de sexo femenino de 67 años, natural y residente de Cali, Colombia, jubilada con antecedentes de hipertensión arterial, dislipidemia y melanoma cutáneo en remisión. Se diagnosticó LMA por el cual recibió un esquema de inducción por siete días de quimioterapia con citarabina a dosis de 500 mg/m2. Nueve días posterior a la primera dosis presentó una erupción maculo-papulosa pruriginosaque se inició en el abdomen y fue afectando progresivamente las regiones del tórax, espalda superior, los miembros inferiores a nivel pretibial simétrico, cara medial de brazos y cuero cabelludo, generando un compromiso de aproximadamente el 30% de la superficie corporal total (Figuras 1, Figuras 2 y Figuras 3).
Adicionalmente presentó infección de vías urinarias por E. coli multisensible tratada con cefepime y recibía profilaxis con aciclovir y posaconazol. En los laboratorios resaltaba una pancitopenia, sin evidencia de daño renal o hepático.
Se decidió obtener dos biopsias cutáneas en tórax y espalda a los tres días del inicio del cuadro, concomitante con aféresis de plaquetas por la trombocitopenia, con el fin de evaluar como posibles presunciones diagnósticas una reacción medicamentosa y una hidradenitis ecrina neutrofílica, por la relación temporal establecida con la citarabina. Se indicó tratamiento tópico con betametasona crema 0,1% cada 12 horas durante 10 días.
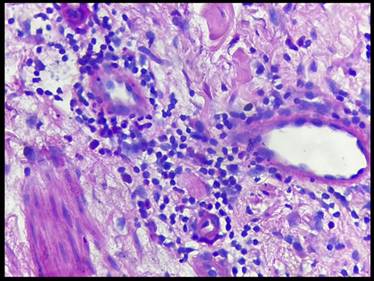
Dentro de los signos anatomo-patológicos encontrados cabe resaltar la presencia de un infiltrado linfocítico perivascular superficial y profundo marcados, asociado a presencia de eosinófilos. Se consideró un patrón compatible con reacción adversa a medicamentos bajo el contexto clínico descrito. (Figura 4 y Figura 5)
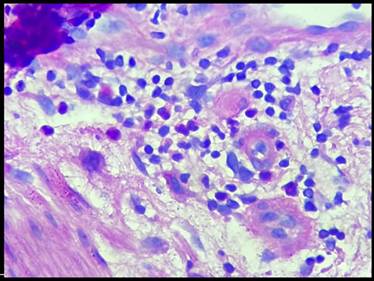
Figura 5: Corte de piel con tinción H&E a 40x. Se muestra el infiltrado linfoide asociado a eosinófilos.
Se realizó el análisis retrospectivo sobre los medicamentos recibidos: se estableció la pauta antibiótica durante 14 días y una pauta antifúngica - antiviral profiláctica durante 25 días, la citarabina fue el fármaco de más reciente aplicación respecto al comienzo de la dermatosis. Considerando la temporalidad referida asociada las manifestaciones dermatológicas y su distribución topográfica, se concluyó que el antineoplásico fue el agente causal más probable de este fenómeno de toxicidad cutánea.
Se realizó el seguimiento durante la hospitalización y se documentó una resolución de la dermatosis a los diez días del inicio de la terapia instaurada (Figura 6). En la etapa de consolidación esta paciente fue nuevamente expuesta a la misma terapia con citarabina, además de cefepime, posaconazol y aciclovir, por indicaciones similares, pero sin desencadenar manifestaciones cutáneas.
DISCUSIÓN
El uso extensivo de la citarabina como antimetabolito útil en el tratamiento de diversas neoplasias hematológicas ha llevado al reconocimiento del espectro de efectos secundarios que este provoca1,7. Actualmente la hipótesis más aceptada para la RAMc es la acumulación epitelial con posible concentración en glándulas ecrinas y se considera poco probable que se produzca por una respuesta inmunitaria al medicamento, ello basado en la experiencia de que en exposiciones posteriores no siempre reaparece la dermatosis, como ocurrió en este caso particular.
Es destacable el polimorfismo de las lesiones cutáneas descritas, tales como máculas, pápulas y placas eritematosas, con frecuencia pruriginosas, siendo menos comunes la aparición de hidradenitis ecrina neutrofílica, vasculitis y siringometaplasia escamosa ecrina. Aproximadamente el 43% de los casos el comienzo de la dermatosis ocurre entre el sexto y décimo día posterior a exposición, concordante con lo presentado por esta paciente y finalizando en una fase descamativa3.
La localización topográfica de las lesiones también es relevante para el diagnóstico presuntivo de esta entidad, algunas publicaciones indican que la aparición de las lesiones en la ingle, las axilas, la parte posterior del cuello, orejas y cuero cabelludo, puede respaldar el diagnóstico y poder prescindir de un tratamiento sistémico u otras pruebas diagnósticas, condiciones similares en el actual caso clínico, especialmente por la aparición de las mismas en la cara medial de los brazos y porque las lesiones estaban más acentuadas en la región abdominal inferior1,3
Otro aspecto por resaltar es la dosis baja con la cual se presentó esta reacción medicamentosa, dado que las series de casos publicadas han encontrado una aparente vinculación dosis dependiente, considerando dosis altas aquellas que reciben más de 1000 mg/m2, mientras que la pacienteque hemos presentado recibió el 50% de esta dosis.3,6
El diagnóstico diferencial sospechado fue la hidradenitis neutrofílica que se caracteriza por pápulas eritematosas urticariformes, purpúricas y placas comúnmente en el tronco, y también pueden presentarse en extremidades y cara; se acompaña de fiebre, fenómeno de patergia y neutropenia.1,7,8