Introducción
Se considera al hipotiroidismo subclínico (HS) como un factor de riesgo de ateroesclerosis1 por asociarse a disfunción endotelial (DE) e inflamación vascular2. Sin embargo, los mecanismos fisiopatológicos implicados en dicha alteración no resultan claros3. Existen dudas si el HS “per se” es capaz de provocar las alteraciones del endotelio o lo hace de manera indirecta a través de la dislipidemia, la insulinorresistencia, el estrés oxidativo u otros mecanismos4. Asimismo, se desconoce la repercusión que la autoinmunidad tiroidea (AIT) pueda tener sobre el endotelio5
Existen distintos métodos para evaluar DE, como flujo mediado por vasodilatación en arteria braquial (FMD)6, grosor de la capa arterial íntima-media (CAIM)7 y medición de sustancias vasoactivas como óxido nítrico8, endotelinas y otros.
La Endotelina (ET1), una de las tres isoformas de la familia de endotelinas, es una potente proteína vasoconstrictora de 21 aminoácidos, reguladora del tono vascular que se sintetiza predominantemente en el endotelio vascular. La medición de ET1 y de Proteína C Reactiva ultrasensible (PCRus) como marcadores de DE e inflamación vascular, respectivamente, ha mostrado resultados controvertidos en el HS5,9-14. Asimismo, el rol que desempeñan el estrés oxidativo y la actividad antioxidante plasmática (TRAP) sobre el endotelio vascular es aún incierto.
El objetivo de este trabajo es establecer si el HS y la autoinmunidad tiroidea (AIT), excluyendo otros factores de riesgo cardiovascular, pueden causar DE e inflamación vascular, evaluadas a través de la medición de ET1 y PCRus. También tratará de establecerse si TRAP juega algún rol. Finalmente, se buscará evaluar cambios en ET1 y PCRus bajo tratamiento con levotiroxina (LT4).
Material y métodos
Se evaluaron prospectivamente 70 pacientes, 62 ♀ y 8 ♂ divididos en 3 grupos:
- Grupo HS: 41 pacientes hipotiroideos subclínicos (T4 normal, TSH >4,2 y <10 mUI/L) - Grupo AIT: 10 pacientes eutiroideos (TSH <4,2 mUI/L) con aTPO y/o aTg (+) - Grupo Control: 19 pacientes eutiroideos sin AIT Los pacientes y los controles debían cumplir estrictos criterios de inclusión: edad <50 años, índice de masa corporal (IMC) <30, sin dislipemia (triglicéridos <150, HDL >40 y LDL <150 mg/dl), insulinorresistencia, diabetes, ni otros factores de riesgo coronario.
Se midió en suero: T4 por Quimioluminiscencia (VN: 4-12 mcg/dl), TSH por Quimioluminiscencia (VN: 0,5-4,2 mUI/L) ET1 sérica por ELISA, PCRus por inmunoturbidimetría y TRAP por quimioluminiscencia. ET1 y PCRus se midieron nuevamente bajo tratamiento con LT4, en 24 pacientes del grupo HS, a tiempo suficiente de alcanzado el eutiroidismo.
Análisis estadístico
Los resultados se expresaron en media ±desvío estándar. Se aplicó ANOVA para la comparación entre los distintos grupos basales y bajo LT4. Se trazó Curva ROC para establecer valor de corte de ET-1 como parámetro emergente, determinado por la mayor área bajo la curva. Para la correlación entre parámetros se aplicó Pearson. Se consideró significativo un valor de p <0,05.
Resultados
No se observaron diferencias significativas en edad, IMC y niveles de lípidos entre HS, AIT, y controles (tabla 1). Los niveles de TRAP, expresados en µMol, tampoco mostraron diferencias significativas entre pacientes con HS (354,06 ± 153,89) y con AIT (314,07 ± 109,2) versus el grupo control (353,43 ± 79,13).

Tabla 1 Valores basales de edad (años), índice de masa corporal y per l lipídico (mg/dl) en pacientes con HS, AIT y controles (media ± DS)
En la tabla 2se observa que, tanto los niveles de ET1 como de PCRus, fueron significativamente mayores en los pacientes con HS que en los controles p <0,0001 y <0,008, respectivamente. Del mismo modo, se observa en dicha tabla que los niveles de ET1 y PCRus resultaron ser significativamente más altos en pacientes eutiroideos con AIT que en el grupo control (p <0,0001 y 0,034, respectivamente). La TSH, aunque dentro del rango normal, fue mayor en el grupo AIT que en el control (p = 0,002).
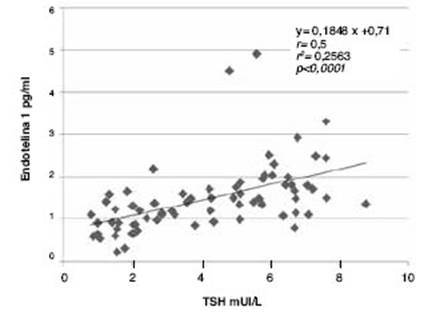
Veinticuatro pacientes con HS fueron reevaluados luego de 8,7 ± 3,8 meses de tratamiento con LT4 (tabla 2). Se observó significativa caída en los niveles de ET1 (p = 0,01) aunque dichos niveles permanecieron más altos que los del grupo control. En cambio, los niveles de PCRus, aunque descendieron, no llegaron a hacerlo significativamente. ET1 tuvo una correlación altamente significativa (p <0,0001) con los niveles de TSH: r = 0,5 (fig. 1).
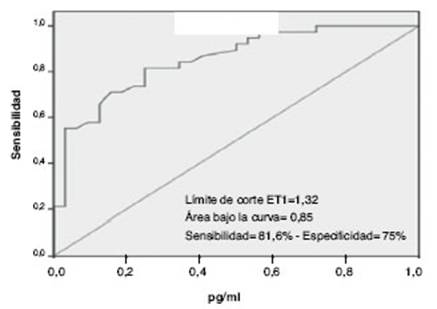
Mediante curva ROC se estableció un nivel de corte de ET1 = 1,32 pg/ml, determinado por el mayor área bajo la curva, implicando una sensibilidad de 81,6% y especificidad de 75% (fig. 2).
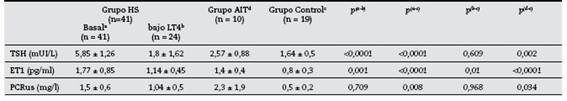
Tabla 2 Niveles de Endotelina-1 (ET1) y Proteína C Reactiva ultrasensible (PCRus) en pacientes con hipotiroidismo subclínico (HS), autoinmunidad tiroidea (AIT) y en controles. Efectos del reemplazo con levotiroxina (LT4) (Xmedia ± DS)
Discusión
La mayoría de los trabajos que han demostrado que el hipotiroidismo subclínico podría provocar disfunción endotelial, lo han hecho a través de estudios vasculares: reducción del FMD15-17, mayor rigidez arterial16 y cierto grado de ateroesclerosis a través del engrosamiento de la CAIM18. Si bien la ET1 ha surgido en los últimos años como biomarcador de DE, son muy pocos los trabajos clínicos que la han medido en pacientes con patología tiroidea. En el 2001, Dieckmann y col.9 hallaron niveles indetectables de ET1 tanto en pacientes con hiper como con hipotiroidismo. Dicho hallazgo motivó a que los autores atribuyeran sus resultados a alteraciones técnicas en la recolección o en el mantenimiento de las muestras o bien al empleo de un RIA de baja sensibilidad. Dos años más tarde, Tilly y col.5 observaron valores elevados de ET1 en pacientes con tiroiditis de Hashimoto. Algunos de ellos sólo presentaban autoinmunidad tiroidea, lo cual no permitía dilucidar si la disfunción, la autoinmunidad o ambas, eran responsables de la elevación de ET1. De allí la importancia de que en nuestro trabajo hayamos incluido un grupo de pacientes con AIT sin disfunción al que comparamos con un grupo control para tratar de obtener conclusiones válidas.
Recientemente, Ahirwar y col.10 midieron ET1 en pacientes con síndrome metabólico, algunos eutiroideos y otros con HS. Si bien observaron niveles de ET1 más elevados en aquellos que tenían HS concomitante, la diferencia no resultó estadísticamente significativa, quizás por el pequeño número de la muestra y el hecho de que los pacientes incluidos con síndrome metabólico ya tenían factores de riesgo para disfunción endotelial. En nuestro trabajo, en cambio, aplicamos estrictos criterios de exclusión para minimizar la posibilidad de incluir pacientes con otros factores de riesgo cardiovascular.
Nosotros observamos una elevación significativa de ET1 no sólo en los pacientes con HS sino también en aquellos eutiroideos con AIT respecto del grupo control. Si bien la AIT “per se” podría tener algún rol, hemos observado que, aunque dentro del rango normal, los pacientes con AIT tenían niveles de TSH significativamente mayores que los del grupo control, por lo cual un “mínimo” grado de HS subyacente no puede descartarse.
Respecto de PCRus, algunos autores11-13 observaron elevación de la misma en hipotiroidismo subclínico pero otros no encontraron cambios14. En nuestro trabajo, PCRus se comportó de manera similar a ET1 observándose niveles elevados tanto en pacientes con HS como en aquéllos con AIT. Esto sugeriría que el componente inflamatorio vascular podría estar implicado.
Entre los mecanismos por los cuales el HS podría generar DE se postula, por un lado, una acción indirecta a través de la dislipidemia19, la insulinorresistencia20 y/o el estrés oxidativo21 provocados por la disfunción tiroidea y, por otro, una acción directa del HS sobre el endotelio. Nosotros no creemos que aquellos factores indirectos hayan tenido influencia destacable por cuanto pacientes y controles tenían valores normales sin diferencias significativas en el índice de masa corporal ni en los niveles lipídicos clásicos y no se incluyeron pacientes con insulinorresistencia. En cuanto al estrés oxidativo, este podría tener importancia en los eventos iniciales que conducen al daño endotelial, pero poco se conoce en pacientes con hipotiroidismo21 y no hay conclusiones claras respecto a uno de los componentes de estado oxidativo como es la defensa antioxidante. Nosotros no observamos que la actividad antioxidante del plasma fuera diferente en pacientes con HS y AIT respecto de los controles. Sin poder descartar de manera absoluta, que otras lipoproteínas aterogénicas22, agentes pro-oxidantes u otros elementos de la capacidad antioxidante (como la intracelular) estuvieran alterados, creemos que los resultados de nuestro estudio sugieren una acción directa del HS sobre el endotelio. En tal sentido, se ha postulado a la TSH como responsable de dicha acción ya que se han descrito receptores de TSH en el endotelio23. Balzan y col. observaron producción de AMP cíclico por estimulación con TSH en células endoteliales en cultivo24. Otros autores han demostrado que la TSH inhibe la expresión de óxido nítrico sintetasa alterando la síntesis de óxido nítrico y aumenta la expresión tanto del ARNm como de la proteína ET1 en células endoteliales de vena umbilical humana25. Estos cambios llevarían a DE por disbalance de sustancias vasoactivas. Dardano y col.26 evaluaron el impacto de la administración de TSH recombinante (TSHrh) sobre el endotelio en pacientes con cáncer de tiroides en remisión. Ellos observaron un significativo descenso del FMD a las 24 hs de la segunda inyección de TSHrh vs el basal. En base a ello, los autores postularon no sólo un efecto directo sino también agudo de TSH sobre el endotelio.
El valor de corte de ET1 como parámetro emergente, obtenido del mayor área bajo la curva ROC, es la primera vez que se establece en nuestro medio. Sumado a la correlación positiva que encontramos entre TSH y ET1, avalaría que esta última podría ser un biomarcador de impacto del hipotiroidismo sobre el endotelio cuando presente un valor mayor a 1,32 pg/ml y que la DE podría ser mayor en pacientes con hipotiroidismos más severos. Coincidentemente, Ahirwar y col.10 demostraron una correlación positiva entre TSH y ET1 (r = 0,341; p = 0,001) con niveles de ET1 más elevados en los pacientes con hipotiroidismo clínico.
La mayoría de los trabajos que evaluaron cambios en marcadores vasculares de DE una vez restaurado el eutiroidismo con LT4, han descrito mejoría en el FMD15,16,27,28 y reducción del grosor de la CAIM29-31. Sin embargo, algunos otros no observaron cambios32. En nuestra experiencia, el tratamiento con levotiroxina en pacientes con HS permitió descender de manera significativa los niveles de ET1, aunque sin normalizarlos. Ello podría ser atribuido a que el tiempo de tratamiento no fue el suficiente para revertir totalmente la DE. En concordancia con ello, Clausen y col.33 observaron que aún existía alteración en los marcadores de DE después de un año de reemplazo con LT4.
Por lo expuesto, creemos haber hallado en ET1 y PCRus biomarcadores útiles para evaluar, en la práctica clínica, disfunción endotelial e inflamación vascular en pacientes con hipotiroidismo subclínico y también en aquéllos con anticuerpos positivos y TSH “normal”. El tratamiento con LT4 puede mejorar el impacto vascular que el hipotiroidismo subclínico produce, aunque se necesitaría un tiempo más prolongado para revertirlo totalmente.
Responsabilidades éticas
Se obtuvo consentimiento informado y el protocolo fue aprobado por el Comité de Ética del Hospital Durand.