INTRODUCCIÓN
En el mundo, unas 500.000 personas sufren lesiones medulares cada año, esto aumenta entre dos y cinco veces la probabilidad de morir prematuramente. Los países de ingresos medios y bajos registran las peores tasas de supervivencia. El costo directo durante la vida oscila entre 1,1 y 4,6 millones de dólares por paciente; en Norteamérica, hay 1,3 millones de pacientes que generan un gasto global de entre 1,43 y 5,98 billones de dólares (National Spinal Cord Injury Statistical Center 2014/2021).1 El Servicio Nacional de Rehabilitación de la Argentina publicó que había 2.176.123 pacientes con algún tipo de discapacidad, de los cuales el 54% eran hombres, y el 30% tenía una discapacidad motora pura (Anuario Estadístico sobre Discapacidad, Ministerio de Salud de la Nación Argentina, 2013).2 Esta problemática genera la necesidad de contar con nuevas estrategias terapéuticas para reducir las secuelas de los pacientes con lesiones medulares. Dentro de este abanico se encuentran los estudios de laboratorio sobre hipotermia.
En nuestro laboratorio, hemos aplicado la hipotermia terapéutica para reducir el daño del sistema nervioso central producido en un modelo experimental de asfixia perinatal severa, con resultados alentadores en enfermedad medular y ocular,3,4,5,6,7,8,9,10y en modelos de traumatismo del nervio óptico.11La reducción de la temperatura corporal protege al sistema nervioso y la retina contra daños de diversa índole al disminuir el metabolismo por reducción de especies reactivas del oxígeno e inhibir la liberación tóxica de óxido nítrico.3,5,8,12,13,14 La hipotermia durante la asfixia perinatal tiene efectos preventivos contra el daño del sistema nervioso central3,5,13,15y se ha propuesto como tratamiento neuroprotector en seres humanos.13,15,16,17
En términos de lesión de la médula espinal, las publicaciones muestran que los niveles relativamente leves de hipotermia después de una lesión mejoran la función y reducen el daño histopatológico.18,19,20,21,22 Aún no se han develado por completo los procesos intrínsecos por los cuales el frío produce protección tisular. Sin embargo, se ha descrito la expresión de diferentes proteínas inducibles por frío, tales como la proteína de unión al ARN inducible por frío (cold-inducible RNA binding protein, CIRBP) y la proteína 3 del motivo de unión al ARN (RNA binding motif protein 3, RBM3)7,9,11,23,24,25,26,27,28 que podrían ser de gran relevancia.
La CIRBP, también conocida como CIRP o ribonucleoproteína heterogénea nuclear A18 (hnRNP A18), es una proteína de 18 kDa compuesta por 172 aminoácidos cuyo gen en los seres humanos se encuentra en el cromosoma 19 región p13.3. Al igual que otros miembros de la familia de las hnRNP, la CIRBP se une al ARN mensajero y ribosomal presente en la célula y regula su semivida, la expresión potencial de múltiples genes y, por tanto, su función.29 Tal como sucede con otras proteínas de unión al ARN, se ha visto que la CIRBP es capaz de modular la apoptosis jugando un papel antiapoptótico en situaciones de hipotermia.30,31 En células neuronales de rata, este efecto parece darse a través de la ruta de apoptosis mitocondrial, ya que muestran una disminución de la expresión de moléculas proapoptóticas (Bax, Bad, Bak, Cycs, Apaf1, caspasa-9 y caspasa-3).30 El estudio exhaustivo de las proteínas inducidas por frío (CIRBP y RBM3) podría abrir un nuevo horizonte respecto a su relación con mecanismos de protección tisular.
A pesar de las grandes aplicaciones potenciales de la hipotermia, hay un problema inherente: la dificultad de aplicar frío a algunos órganos o regiones concretos del cuerpo debido a su capacidad de autorregular la temperatura.32 Para aplicar hipotermia en órganos internos, como el cerebro, es necesario enfriar la sangre con un sistema de circulación externo,33 sin olvidar que la hipotermia puede generar efectos secundarios adversos, como disminución de la respuesta inmune o insuficiencia renal.34
Sobre la base de la experiencia previa publicada,10,28,35 decidimos aplicar nuestro modelo experimental sencillo y económico, útil en ensayos in vivo, para el enfriamiento medular y estudiar la expresión de la CIRBP a nivel estructural mediante inmunohistoquímica e inmunofluorescencia, y a nivel molecular usando Western blot en la médula espinal de ratas expuestas al frío.
Considerando todo lo descrito previamente, el objetivo de este estudio fue evaluar la expresión de la CIRBP en las motoneuronas del asta anterior de la médula espinal de ratas expuestas a este modelo de hipotermia sistémica.
MATERIALES Y MÉTODOS
Modelo y diseño experimental
Todos los procedimientos relacionados con el manejo y el tratamiento de los animales se llevaron a cabo de acuerdo con la guía para el cuidado y uso de animales de laboratorio de los NIH (National Institutes of Health Guidelines for the Care and Use of Laboratory Animals-CCAC 2002; CCAC 2003) y las pautas de la Society for Neuroscience, 1992). El protocolo experimental fue revisado y aprobado por el CICUAL (Comité Institucional para el Uso y Cuidado de Animales de Laboratorio) resolución Nro. 970/2015 (Universidad de Buenos Aires, Argentina).
Se utilizaron 24 ratas Spargue-Dawley macho adultas de 60 días de vida, distribuidas en dos grupos: grupo 1, normotermia (control, n = 6) a temperatura controlada de 24 ºC y grupo 2 (hipotermia, n = 18) en cámara fría a 8 ºC durante 180 minutos. Luego de la hipotermia fueron colocadas en cajas individuales y mantenidas en condiciones de bioterio estándar a 24 ºC, con ciclos de luz/oscuridad de 12/12 h, hasta su sacrificio por decapitación con guillotina, según lo descrito por Contartese y cols.35 y Larrayoz y cols.28
Obtención y procesamiento del tejido
Los animales fueron sacrificados a las 12, 24 y 48 h del tratamiento. Las médulas fueron extraídas e inmediatamente sumergidas en solución fijadora de paraformaldehído al 4% en buffer fosfato 0,1 M, pH 7,4, a 4 ºC durante 2 h y luego transferidas a una solución de sacarosa en concentraciones crecientes al 10%, 20% y 30% en buffer fosfato 0,1 M a 4 °C, durante tres días sucesivos.
Hematoxilina-eosina
Para estudiar las alteraciones estructurales de las médulas fijadas con paraformaldehído se deshidrataron con concentraciones crecientes de etanol seguido de xileno y se incluyeron en parafina. Se obtuvieron cortes de 5-10 µm de grosor mediante un micrótomo (Leitz, Lauda MGW, Alemania), se colocaron sobre portaobjetos gelatinizados y se procesaron con la tinción de hematoxilina-eosina. Finalmente los preparados se montaron con resinas sintéticas DPX (Fluka®, Suiza). Los cortes se observaron con un microscopio óptico (Carl Zeiss Axiophot, Alemania) conectado a una cámara digital (Olympus, Q-Color 5, EE.UU.) y se fotografiaron para su análisis mediante el programa NIH Image (desarrollado por Wayne Rasband, 1995, NIH, Research Services Branch, NIMH, Bethesda, MD, EE.UU.). Se analizaron tres animales por grupo experimental.
Inmunohistoquímica
Las médulas fijadas y crioprotegidas fueron embebidas en Tissuetek TEC®, congeladas a –70 °C y cortadas en secciones de 20 µm de espesor con un criostato Leitz “Lauda”. Las secciones se montaron en portaobjetos que previamente se recubrieron con gelatina al 1,5%. Las secciones medulares se incubaron toda la noche a 4 ºC con anticuerpo anti-CIRBP policlonal de conejo (Proteintech, Reino Unido, Cod. 00055668) a una dilución 1:1000, seguido de un anticuerpo secundario biotinilado anticonejo (Vector Labs, EE.UU.). La tercera capa se incubó durante una hora con el complejo estreptavidina peroxidasa (ABC Complex, Vector Labs, EE.UU.). La marcación se detectó mediante diaminobencidina, usando el kit comercial SK-4100 (Vector Laboratories, EE.UU.). El análisis del grado de respuesta y el número de células inmunorreactivas se realizó con un microscopio óptico (BX40, Olympus Optical Corporation, Tokio, Japón), acoplado a una cámara digital (390CU 3.2 Megapixel CCD Camera, Micrometrics, España), empleando el programa Micrometrics SE P4 (Standard Edition Premium 4, Micrometrics, España). Se analizaron tres animales por grupo experimental.27
Inmunofluorescencia
Se utilizó anticuerpo primario anti-CIRBP policlonal de conejo (Proteintech®, Reino Unido, Cod. 00055668) a una dilución 1:1000, que se detectó con anticuerpo secundario Alexa Fluor® 488 de burro anti-IgG de ratón (Life Technologies, EE.UU. Lot: 1423052) en una dilución 1:300. Se utilizó DAPI (4’,6-diamino-2-fenilindol, Sigma-Aldrich, EE.UU.) como marcador específico de núcleos, a una dilución 1:1000. Por último, las secciones fueron evaluadas y fotografiadas con microscopio confocal láser Nikon C1 Plus (Nikon Inverted Research Microscope Eclipse Ti, Nikon Corp., Tokio, Japón) y las imágenes se analizaron con el programa EZC1 (Software EZ-C1 v3.9, Nikon Ltd., Tokio, Japón). Se analizaron tres animales por grupo experimental.
Procesamiento del tejido para Western blot
Se siguió el procedimiento descrito por Rodrigo y cols.36,37 Se utilizaron sobrenadantes homogenados de concentración de proteínas determinadas por el método de Bradford. La electroforesis se llevó a cabo en condiciones desnaturalizantes en geles de poliacrilamida con SDS. Las bandas fueron transferidas a 350 mA durante 90 min sobre membranas de PDVF. Finalizada la transferencia, se bloqueó la membrana con una solución de TBS con Tween 20 al 0,05% v/v (TBST) que contenía leche descremada en polvo a una concentración de 3% p/v (TBST-leche) durante 1 h en agitación suave. Se desechó la solución de bloqueo y se incubó con un anticuerpo anti-CIRBP de conejo (Proteintech®, Reino Unido) diluido 1:3000 en TBST-leche durante 16 h, en agitación suave a 4 °C. Luego de tres lavados con TBST en agitación suave de 10 min cada uno, se incubó con un anticuerpo anti-IgG de conejo (Amersham Pharmacia Biotech, EE.UU.) conjugado a peroxidasa de rábano picante diluido 1:5000 con TBST-leche durante 1 h, en agitación suave. Se efectuaron lavados con TBST y luego TBS en agitación suave de 10 min cada uno, se realizó el revelado utilizando el kit de detección ECLTM (AmershamTM) y las bandas se visualizaron con un fotodocumentador UVP Biospectrum/Biolite (Analytik Jena). Se analizaron tres animales por grupo experimental.
Para el control de carga se incubó la membrana con anticuerpo monoclonal de ratón antiactina (Sigma-Aldrich, St. Louis, MO, EE.UU.) en una dilución 1:5000, durante 16 h en agitación suave a 4 °C. Luego de tres lavados con TBST en agitación suave de 10 min cada uno, se incubó con un anticuerpo de cabra anti-IgG de ratón conjugado a peroxidasa de rábano picante (Jackson Immuno Research Laboratories, Pensilvania, EE.UU.) diluido 1:5000 con TBST-leche durante 1 h en agitación suave. Como se mencionó antes, se realizaron los lavados y el revelado.
Análisis de imágenes
Las imágenes obtenidas en microscopia y los Western blot fueron digitalizadas. Tanto para inmunohistoquímica como para inmunofluorescencia las secciones de médula espinal fueron seleccionadas de modo que fueran comparables entre los distintos animales. Para una misma técnica, todas las imágenes fueron tomadas el mismo día, bajo condiciones de captura estandarizadas, para evitar el efecto de variabilidad externa. La densidad óptica relativa, el área celular, el área reactiva y el espesor se determinaron con un programa de análisis de imágenes (ScionImage). Se consideró marca inmunopositiva a aquella cuya densidad óptica superó 4 veces o más la densidad óptica del fondo. Para el ajuste digital del brillo y el contraste de las imágenes se utilizó el programa de edición de imágenes Adobe Photoshop (Adobe Photoshop CS5, Adobe Systems Inc., Ontario, Canadá). Los valores de CIRBP obtenidos en los Western blot fueron normalizados según el valor de ß-actina correspondiente y los resultados expresados como el valor medio del grupo ± la desviación estándar y en porcentaje respecto al grupo de control. Todos los experimentos fueron realizados por duplicado.
Análisis estadístico
Los datos obtenidos se cargaron en una base de datos que fue analizada con el paquete estadístico InfoStat versión 2020 y se graficaron utilizando el programa GraphPad Prism (versión 5.0 para Windows, GraphPad Software). Para determinar si las diferencias observadas entre los grupos resultaban estadísticamente significativas, se realizó un análisis de varianza (ANOVA) de una vía seguido del test de Tukey. Antes de la prueba de hipótesis, se verificaron los supuestos de normalidad mediante la prueba de Shapiro-Wilk modificada y de homogeneidad de varianzas mediante la prueba de Lavene. Se consideró estadísticamente significativa a una diferencia p <0,05.
RESULTADOS
Western blot
Se obtuvo como resultado una única banda de un peso molecular de 19 kDa, que indica la expresión específica de CIRBP en las médulas espinales de las ratas estudiadas (Figura 1). La expresión de CIRBP aumentó significativamente en ratas sometidas a hipotermia y sacrificadas a las 24 h con respecto a las ratas de control (p <0,05, ANOVA de una vía con test de Tukey); sin embargo, no se observaron diferencias significativas en animales hipotérmicos de 48 h con respecto a los otros grupos estudiados.
Morfología
Se obtuvieron imágenes del asta anterior de la médula espinal, correspondientes a las láminas VII, VIII y IX de Rexed, y se analizaron las motoneuronas alfa tanto con histología clásica con hematoxilina-eosina como por inmunohistoquímica e inmunofluorescencia.
Hematoxilina-eosina
En el corte de médula de las ratas de control (Figura 2), se observaron el asta anterior y la sustancia blanca circundante con las motoneuronas correspondientes a la sustancia gris, las cuales miden entre 30 y 70 µm de diámetro, entre ellas, hay pequeñas interneuronas, como las células de Renshaw. La misma zona fue evaluada tanto por inmunohistoquímica como por inmunofluorescencia (Figuras 3 y 4).
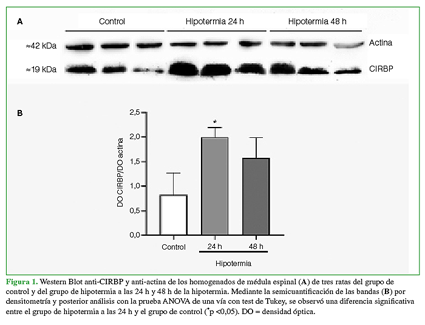
Figura 1 Western Blot anti-CIRBP y anti-actina de los homogenados de médula espinal (A) de tres ratas del grupo de hipotermia a las 24 h y 48 h de la hipotermia. Mediante la semicuantificación de las bandas (B) por densitometría y posterior análisis con la prueba ANOVA de una vía con test de Tukey, se observó una diferencia significativa entre el grupo de hipotermia a las 24 h y el grupo de control (*p<0,05).DO=densidad óptica.
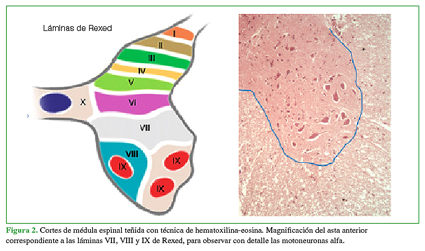
Figura 2 Cortes de médula espinal teñida con técnica de hematoxilina-eosina. Magnificación del asta anterior correspondiente a las láminas VII, VIII y IX de Rexed, para observar con detalle las motoneuronas alfa.
Inmunohistoquímica
El anticuerpo para CIRBP en algunas secciones del grupo de control no mostró marca y, en otras, una débil marca en el neuropilo (Figura 3). En las médulas espinales de las ratas hipotérmicas, a las 12 h del tratamiento, se observó inmunorreactividad específica leve para CIRBP en el núcleo de las motoneuronas alfa del asta ventral, mientras que los grupos de 24 y 48 h postratamiento hipotérmico mostraron un gran aumento en la expresión de CIRBP tanto en el núcleo y nucléolo, como en el citoplasma (en forma de “grumos”) de estas células (Figura 3).
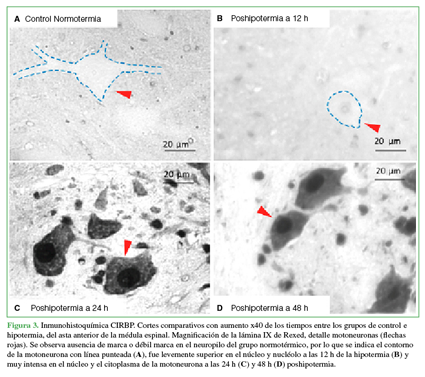
Figura 3 Inmunohistoquímica CIRBP. Cortes comparativos con aumento x40 de los tiempos entre los grupos de control e hipotermia, del asta anterior de la médula espinal. Magnificación de la lámina IX de Rexed, detalle motoneuronas (flechas rojas). Se observa ausencia de marca o débil marca en el neuropilo del grupo normotérmico, por lo que se indica el contorno de la motoneurona con línea punteada (A), fue levemente superior en el núcleo y nucléolo a las 12 h de la hipotermia (B) y muy intensa en el núcleo y el citoplasma de la motoneurona a las 24 h (C) y 48 h (D) poshipotermia.
Inmunofluorescencia
Los resultados con esta técnica coinciden con lo observado en la inmunohistoquímica (Figura 4).
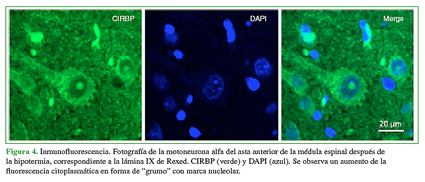
Figura 4 Inmunofluorescencia. Fotografía de la motoneurona alfa del asta anterior de la médula espinal después de la hipotermia, correspondiente a la lámina IX de Rexed. CIRBP (verde) y DAPI (azul). Se observa un aumento de la fluorescencia citoplasmática en forma de "grumo" con marca nucleolar.
Análisis de imágenes
Se realizó con microscopia óptica de la inmunohistoquímica. Se observaron diferencias significativas en la expresión de CIRBP con el tratamiento hipotérmico. Se determinó un aumento progresivo de la densidad óptica para CIRBP, que fue escaso en normotermia, leve a las 12 h poshipotermia en el núcleo, incrementándose en el núcleo y a nivel citoplasmático a las 24 h y 48 h (Figura 5).
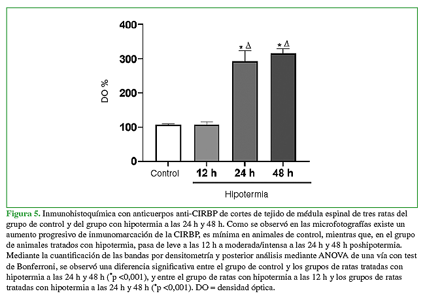
Figura 5 Inmunohistoquímica con anticuerpos anti-CIRBP de cortes de tejido de médula espinal de tres ratas del grupo de control y del grupo con hipotermia a las 24 h y 48 h. Como se observó en las microfotografías existe un aumento progresivo de inmunomarcación de la CIRBP, es mínima en animales de control, mientras que, en el grupo de animales tratados con hipotermia, pasa de leve a las 12 h a moderada/intensa a las 24 h y 48 h poshipotermia.Mediante la cuantificación de las bandas por densitometría y posterior análisis mediante ANOVA de una vía con test de Bonferroni, se observó una diferencia significativa entre el grupo de control y los grupos de ratas tratadas con hipotermia a las 24 h y 48 h (*p<0,001), y entre el grupo de ratas con hipotermia a las 12 h y los grupos de ratas tratadas con hipotermia a las 24 h y 48 h (*p<0,001). DO=densidad óptica.
La evaluación estadística de las densidades ópticas relativas mostró que los grupos tienen diferencia, particularmente a partir de las 24 h poshipotermia donde se incrementa la concentración, en especial, a nivel nuclear y, luego a las 48 h, se observa intensamente en el citoplasma, en forma de grumos (p <0,001, ANOVA de una vía con test de Bonferroni) (Figura 5).
DISCUSIÓN
En la actualidad, no hay cura para la lesión de la médula espinal. Por ello continuamente se desarrollan modelos de lesión medular en animales, que sean fiables, coherentes y que reproduzcan las lesiones que se observan en los seres humanos.38,39,40 Persisten interrogantes sobre su validez y si son comparables con las condiciones clínicas en los seres humanos. Algunas revisiones han examinado los modelos de lesión de médula espinal y sus usos potenciales en la imitación de este cuadro.41,42,43 Las terapéuticas posibles con frío, planteadas para evitar el daño neuronal por lesión de la médula espinal, son de dos tipos: la local y la sistémica. La terapéutica local se ha utilizado en la profilaxis de la isquemia medular durante la cirugía aórtica. En este caso, la hipotermia mediante enfriamiento epidural proporciona citoprotección,44 pero por lo complejo del procedimiento, se opta por la hipotermia sistémica.45 La evidencia sugiere utilizar esta última cuando hay una lesión medular aguda.46
A la CIRBP se la considera una proteína citoprotectora y que acelera la recuperación de las células ante el estrés.47,48 Zhang y cols. describen que es un modulador de las telomerasas tanto a 32 °C como a 37 °C. La CIRBP se asocia con el complejo de la telomerasa activa a través de la unión directa del componente del ARN de telomerasa (telomerase RNA component, TERC) y regula la localización de la telomerasa en el “cuerpo de Cajal”.30,49La posible interacción de estos cuerpos con ribonucleoproteínas pequeñas nucleares podría tener implicaciones en fenómenos de protección generados a nivel nuclear, un tema que se está estudiando minuciosamente en la actualidad.
Los ensayos de hipotermia sistémica en modelos experimentales generan grandes dificultades debido a los costos, la complejidad de los sistemas y del manejo de enfriadores por circulación de agua,50 o el coma inducido en cámara fría,51o incluso sistemas transrectales que requieren varias horas. Se han desarrollado varios modelos, pero la mayoría tiene dos inconvenientes: son invasivos y costosos.
En trabajos de nuestro laboratorio, hemos determinado que una breve exposición al frío (“shock hipotérmico”) induce la expresión de CIRBP y RBM3 en la retina. Hemos observado un aumento significativo de la CIRBP a nivel nucleotídico 6 h después de la hipotermia. Por este motivo, utilizamos grupos sometidos a hipotermia a partir de las 12 h.7,9,11 Pudimos observar la presencia de la CIRBP en los controles, que se consideró como la expresión basal que tiene el tejido nervioso del asta anterior de la médula. Obtuvimos un aumento leve de la expresión de la CIRBP a las 12 h de la hipotermia. El fenómeno es observable en la evaluación comparativa de densidades que se realizó tanto en Western blot como en los preparados de inmunohistoquímica. También observamos una localización diferente de la marca inmunofluorescente en los animales a las 12 h poshipotermia (nucléolo y citoplasma), donde se ve una aparente marca nucleolar y la aparición de “grumos” citoplasmáticos positivos para la CIRBP. En los tiempos iniciales, la marca se incrementa en el nucléolo y en el citoplasma perinuclear, luego cae a nivel nucleolar, pero se incrementa en el citoplasma en forma de grumos, así como también aumenta la expresión en el neuropilo. Los resultados presentados tienen cierta similitud con lo publicado previamente por nuestro laboratorio en los estudios de retina, donde se observa el incremento de la CIRBP y la RBM3 en sus diversas capas a las 12, 24 y 48 h posteriores a la aplicación de la hipotermia.10,27
En resumen, la presencia de la CIRBP en la médula espinal a nivel torácico (T8-T9-T10) se encuentra tanto en animales a temperatura ambiente como en animales expuestos a hipotermia, su expresión es significativamente mayor en los animales expuestos a hipotermia con una cinética de expresión y localización diferente entre las 12, 24 y 48 h posteriores a la intervención.
Hasta la fecha, no se ha publicado ninguna descripción de la expresión proteica ni la localización de esta proteína en la médula espinal de modelos de hipotermia, lo que afirma la originalidad de la tarea que estamos desarrollando. En este modelo, por primera vez, se observan los efectos del frío y la expresión de las proteínas inducidas por el frío a corto y mediano plazo, y podría ser de utilidad para el estudio de patologías de la médula, aportando valiosa información sobre los mecanismos fisiopatológicos que se desencadenan en el paciente normal y en el sometido a hipotermia.
Sobre la base de lo observado y desarrollado en nuestro laboratorio con este modelo, podemos afirmar su utilidad para producir hipotermia sistémica a partir de la exposición de los animales a un frío moderado (8 ºC de temperatura ambiente) que disminuye la temperatura corporal en alrededor de 2 ºC, generando cambios bioquímicos con un estímulo suficiente para aumentar la expresión de la CIRBP.
Las ventajas del modelo son: es no invasivo y produce un estado de hipotermia global, transitorio y reversible, reproduciendo lo que ocurre en situaciones de exposición al frío. Finalmente el costo de este sistema y su complejidad son en extremo bajos, solo se requiere una cámara fría (heladera) a 8 °C, una jaula y un cronómetro.















