Introducción
Los antibióticos están entre los más destacados avances en medicina y han traído grandes beneficios al tratamiento y control de enfermedades infecciosas. Sin embargo, la habilidad de los microorganismos de evolucionar rápidamente junto al uso excesivo e inapropiado de los antibióticos han conducido a la expansión de la resistencia antimicrobiana en las bacterias patógenas(1,2). La resistencia a los antimicrobianos es una amenaza a la salud humana y animal, con grandes pérdidas económicas, fallas en los tratamientos y aumento en la morbilidad y mortalidad. Esto hace indispensable la reducción del uso de antimicrobianos y la búsqueda de nuevas opciones preventivas y terapéuticas para el control de las infecciones(2).
Una de las alternativas al uso de antibióticos son los probióticos(2), los cuales se definen como microorganismos vivos que administrados en cantidades adecuadas brindan un beneficio a la salud del hospedador(3,4).Un microorganismo probiótico debe estar identificado a nivel de cepa, estar suficientemente caracterizado en términos de su inocuidad y estabilidad genética, y poseer un beneficio para la salud respaldado por estudios clínicos en el huésped en que se pretende usar(5,6,7). Además, los microorganismos probióticos deben permanecer viables en el producto en el que se incorporan y mantener una dosis eficaz durante toda la vida útil del producto(6).
Los probióticos pueden tener diversos efectos beneficiosos para la salud, por ejemplo, a nivel digestivo, inmunológico, cardiovascular y neurológico(1,4). El consenso general es que los beneficios para la salud inducidos por los probióticos son cepa específicos y no se pueden extrapolar a otras cepas, ni siquiera de la misma especie, sin estudios que lo respalden(1,3). El efecto más reconocido de los probióticos y su principal aplicación, tanto en las personas como en los animales, es la prevención y tratamiento de infecciones gastrointestinales y diarrea(3, 8,9). En medicina humana y veterinaria se ha documentado que el consumo de probióticos disminuye el riego de enfermedades infecciosas, y también reduce la duración media de los síntomas en cuadros agudos comunes, reduciendo de este modo la necesidad de usar antibióticos(1,10).
Los mecanismos a través de los cuales los probióticos pueden mejorar la resistencia a infecciones son variados e incluyen la regulación de la microbiota intestinal, la inhibición de microorganismos patógenos, y la modulación de la respuesta inmune(1,4,11). Los probióticos pueden contribuir en la eliminación de microorganismos patógenos mediante la mejora de la barrera mucosa, al estimular la producción de mucus, defensinas, IgA y reforzar uniones intercelulares. También pueden ejercer la exclusión competitiva de patógenos al utilizar los sitios de unión y los nutrientes disponibles, o a través de la producción de sustancias con efecto antimicrobiano como ácidos orgánicos, peróxido de hidrogeno, óxido nítrico y bacteriocinas(1,4,12). Se ha demostrado la efectividad de algunas cepas probióticas en la inhibición de bacterias patógenas gastrointestinales como Salmonella spp., Escherichia coli, Campylobacter jejuni, Shigella spp., Helicobacter pylori (11-13).
Los principales orígenes de aislamiento de los microorganismos probióticos son el tracto digestivo humano o animal, alimentos de origen animal o vegetal, fermentados o no fermentados, y leche materna humana o animal(14,15,16). Diversas cepas aisladas desde leche animal han mostrado características probióticas prometedoras, como la capacidad de sobrevivir al tránsito gastrointestinal, la adherencia a la mucosa intestinal, inmunomodulación y actividad inhibitoria de patógenos. Se han evaluado cepas de leche de cabra(17,18) , leche de cerda(19,20) , leche de perra(21,22), leche de vaca(18) y leche de llama(23), entre otras.
Frecuentemente los probióticos se estudian como cepas individuales y luego se formulan comercialmente como productos multicepa( 24), para lograr efectos aditivos o sinérgicos(25). Algunos efectos sinérgicos propuestos son el aumento en la adherencia al mucus intestinal y el incremento de la actividad antimicrobiana, aunque también se han registrado efectos negativos como el antagonismo entre las cepas combinadas(25,26). Existe evidencia de la efectividad de los probióticos multicepa y multiespecie, tanto en animales como humanos, por ejemplo, en problemas digestivos, infecciones respiratorias, e inmunomodulación(13,26,27-29). Sin embargo, pocos estudios comparan probióticos multicepa y multiespecie con cepas individuales para evaluar si hay diferencia en su efecto. Se ha reportado que algunas combinaciones probióticas tienen mejor adherencia al mucus intestinal que cada cepa individualmente(30), o mayor inhibición de la adherencia de patógenos a la mucosa(31,32). En otros estudios hay resultados variables, donde solo algunas de las combinaciones probióticas muestran mayor efectividad que las cepas individuales, y en algunos casos las dosis utilizadas no son equivalentes para la combinación y la cepa individual, por lo que no se puede concluir que el efecto sea debido a la sinergia de las cepas y no a una mayor concentración total de las bacterias probióticas(25,27).
Este trabajo se enfocó en la búsqueda de nuevas combinaciones de cepas de lactobacilos potencialmente probióticos que sean capaces de inhibir patógenos bacterianos de importancia en medicina humana y animal, para su potencial uso en la prevención y tratamiento de enfermedades infecciosas. Para ello, se evaluó la actividad antimicrobiana in vitro de las cepas de lactobacilos en diferentes combinaciones, con el objetivo de encontrar aquellas que fueran sinérgicas en la inhibición de patógenos, y que tengan mayor probabilidad de ser efectivas clínicamente.
Materiales y método
Microorganismos
Las cepas de bacterias lácticas utilizadas pertenecen a la colección de cultivos del Laboratorio de Microbiología de los Alimentos, Facultad de Ciencias Veterinarias, Universidad de Concepción (Chillán, Chile). Las cepas fueron previamente aisladas desde leche materna de diferentes animales y caracterizadas para su resistencia a pH 3, y a diferentes concentraciones de Oxgall y NaCl. Levilactobacillus brevis TUCO-5E(20) (leche de cerda), Ligilactobacillus salivarius TUCO-L2(23) (leche de llama), Lactiplantibacillus plantarum TUCO-2 (leche de cabra), Pediococcus pentosaceus TUCO-3 (leche de gata), Lactiplantibacillus plantarum TUCO-5 (leche de cerda), Lactobacillus sp. TUCO-16 (calostro de perra), y TUCO-17 (leche de perra). Se empleó además la cepa Lacticaseibacillus casei Shirota como control.
Para lo experimentos se emplearon además las cepas Escherichia coli ATCC 25922, aislado de patotipo de E. coli enterohemorrágica (EHEC), Salmonella enterica ATCC 13076, Klebsiella pneumoniae ATCC 13883, y Acinetobacter baumannii ATCC 19606.
Se evaluaron seis combinaciones de bacterias lácticas, cada una compuesta por dos cepas potencialmente probióticas: TUCO-5E + TUCO-L2, TUCO-5E + TUCO-2, TUCO-5 + TUCO-2, TUCO-3 + TUCO-16, TUCO-3 + TUCO-17, y TUCO-16 + TUCO-17.
Estudio del efecto antimicrobiano de cepas de bacterias lácticas individuales
El efecto inhibitorio fue evaluado mediante la técnica spot soft agar(33,34), también llamada spot on lawn(35,36), adaptada con algunas modificaciones. Las cepas de bacterias lácticas fueron sembradas en agar MRS (DE MAN, ROGOSA y SHARPE, Oxoid) y fueron incubadas a 37ºC, en microaerofilia, durante 48 h. Fueron traspasadas a caldo MRS e incubadas en las mismas condiciones. Un mililitro de cada cultivo se centrifugó a 3000 rpm por 5 minutos para recolectar el pellet, se hicieron dos lavados con buffer y se resuspendió en buffer ajustando a la concentración equivalente de 0,5 McFarland usando un dispositivo DensiCHECK Plus. Dos microlitros de la concentración recién preparada fueron depositados como gota en la superficie del agar MRS. Las placas se mantuvieron a temperatura ambiente durante 30 minutos para que se absorbieran las gotas y se incubaron en microaerofilia, a 37°C, por 24 h para el desarrollo de las bacterias lácticas.
En paralelo, las cepas patógenas fueron sembradas en agar nutritivo e incubadas en aerobiosis, a 37ºC, durante 24 h. Se traspasaron a caldo BHI (Oxoid) y se incubaron en aerobiosis, a 37ºC, por 24 h. Se centrifugaron y el pellet fue resuspendido en buffer y ajustado a una concentración equivalente de 0.5 McFarland. Se tomó 1 ml de esta suspensión y se mezcló con 9 ml de agar BHI semisólido fundido. La mezcla se vertió sobre cada placa de agar MRS con las cepas de bacterias lácticas desarrolladas. Las placas se incubaron en aerobiosis, a 37°C, durante 24 h. Se midieron los diámetros de los halos de inhibición producidos alrededor del desarrollo de las bacterias lácticas (originado desde la gota absorbida).
Estudio del efecto antimicrobiano de cepas de bacterias lácticas combinadas
Cada cepa de bacterias lácticas de la combinación se ajustó por separado a una concentración de 0,5 McFarland como se describió anteriormente, y se mezclaron en volúmenes iguales. Se tomaron inóculos de 2 µl de esta mezcla y se sembraron sobre agar MRS. Las placas fueron incubadas a 37°C, en microaerofilia, durante 24 h. Las cepas patógenas fueron ajustadas a una concentración de 0,5 McFarland, de donde se tomó un volumen de 1 ml y se agregó a un tubo con 9 ml de agar BHI semisólido fundido, se vertió sobre el cultivo de cepas de bacterias lácticas ya desarrolladas y se incubó en aerobiosis a 37°C, durante 24 h. Se midió el diámetro de los halos de inhibición producidos.
Evaluación del efecto inhibitorio entre cepas de bacterias lácticas
Cada cepa de bacteria láctica se ajustó a una concentración de 0,5 McFarland, una cepa fue sembrada sobre agar MRS y se incubó en microaerofilia, a 37°C, durante 24 h. Se tomó 1 ml de la otra cepa y se mezcló con 9 ml de agar MRS semisólido fundido, luego se vertió esta mezcla sobre las placas de agar MRS con la primera cepa ya desarrollada y se incubó en microaerofilia, a 37°C, durante 24 h. El mismo procedimiento se repitió con las dos cepas en roles invertidos. Se midió el diámetro de los halos de inhibición producidos.
Los halos de inhibición producidos fueron clasificados en 4 categorías: sin inhibición, halos de diámetro menor a 0,7 cm; inhibición leve para diámetros de inhibición entre 0,7 y 1,5 cm; inhibición moderada para diámetros de inhibición entre 1,6 y 2,5 cm; inhibición fuerte para diámetros de inhibición mayores a 2,5 cm.
Análisis estadísticos
Los experimentos de inhibición de patógenos se realizaron en triplicado y los resultados se expresan como el valor de la media ± la desviación estándar (DE)(37,38). Se realizó una Prueba de Kruskal-Wallis para evaluar diferencia entre medias de los grupos(39). Valores de p < 0.05 se consideraron estadísticamente significativos(40). El análisis estadístico fue realizado con el programa estadístico InfoStat.
Resultados
Efecto inhibitorio de cepas de bacterias lácticas sobre cepas patógenas
Al evaluar la actividad antimicrobiana de las 7 cepas de bacterias lácticas individuales, se observó que todas presentaron actividad inhibitoria sobre las cepas patógenas evaluadas. La formación de halos de inhibición alrededor de las colonias de bacterias lácticas en forma de gota se puede observar en la Figura 1.

Figura 1: Ejemplo del efecto inhibitorio de la cepa TUCO-L2 sobre la cepa patógena de E. coli enterohemorrágica (EHEC) mediante técnica spot soft agar.
Los diámetros de los halos de inhibición producidos por las cepas de bacterias lácticas se muestran en la Tabla 1. Las cepas de bacterias lácticas con mayores halos de inhibición sobre E. coli ATCC 25922 fueron TUCO-L2, TUCO-3 y TUCO-5, con un efecto inhibitorio similar al de la cepa probiótica de referencia L. casei Shirota. Las cepas TUCO-L2, TUCO-16, TUCO-3 y L. casei Shirota mostraron el mayor efecto inhibitorio sobre EHEC mientras que las bacterias lácticas con mayores halos de inhibición sobre S. enterica ATCC 13076 fueron TUCO-L2, TUCO-5E, TUCO-5, TUCO-3 y L. casei Shirota (Tabla 1).
Tabla 1: Efecto inhibitorio de cepas de bacterias lácticas sobre cepas patógenas.
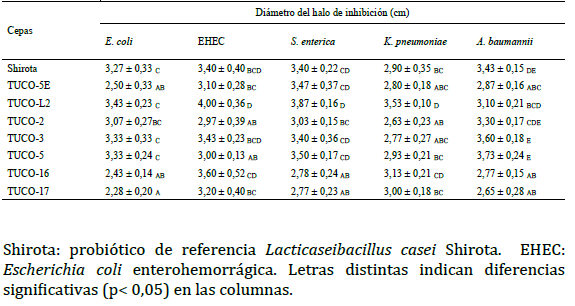
Shirota: probiótico de referencia Lacticaseibacillus casei Shirota. EHEC: Escherichia coli enterohemorrágica. Letras distintas indican diferencias significativas (p< 0,05) en las columnas.
Las cepas TUCO-L2 y TUCO-16 presentaron el mayor efecto inhibitorio sobre K. pneumoniae ATCC 13883. La cepa TUCO-L2 presentó halos de inhibición significativamente mayores (p < 0,05) que los observados para L. casei Shirota (Tabla 1). Por otro lado, el mayor efecto inhibitorio sobre A. baumannii ATCC 19606 fue producido por las cepas TUCO-5, TUCO-3, TUCO-2 y L. casei Shirota (Tabla 1).
Efecto inhibitorio de combinaciones de bacterias lácticas sobre cepas patógenas
Los resultados del efecto inhibitorio de las combinaciones de las cepas de bacterias lácticas sobre las cepas patógenas se muestran en la Tabla 2. El mayor efecto inhibitorio sobre E. coli ATCC 25922 y sobre EHEC fue producido por la combinación de las cepas TUCO-5E + TUCO-L2 (Tabla 2). El mayor efecto inhibitorio sobre S. enterica ATCC 13076 se observó con las combinaciones de cepas TUCO-5E + TUCO-L2 y TUCO-3 + TUCO-16 (Tabla 2).
Tabla 2: Efecto inhibitorio de las combinaciones de cepas de bacterias lácticas sobre las cepas patógenas.
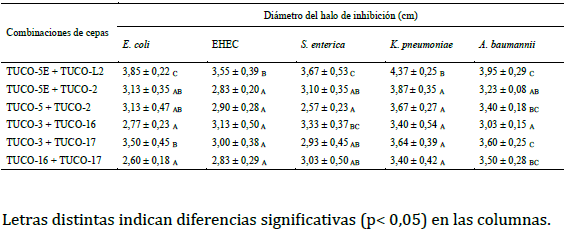
Letras distintas indican diferencias significativas (p< 0,05) en las columnas.
El mayor efecto inhibitorio sobre K. pneumoniae ATCC 13883 fue producido por la combinación TUCO-5E + TUCO-L2, la cual presentó un efecto sinérgico en la inhibición de esta cepa patógena, con halos de inhibición significativamente más grandes que los producidos por cada cepa de forma individual (p < 0.05). Las combinaciones TUCO-5E + TUCO-2, TUCO-5 + TUCO-2, y TUCO-3 + TUCO-17 también tuvieron efectos sinérgicos en la inhibición de K. pneumoniae, aunque no son tan eficaces como la combinación TUCO-5E + TUCO-L2 (tabla 2). El mayor efecto inhibitorio sobre la cepa de A. baumannii ATCC 19606 se observó con las combinaciones de cepas TUCO-5E + TUCO-L2, TUCO-3 + TUCO-17, y TUCO-16 + TUCO-17 (Tabla 2). De estas combinaciones, TUCO-5E + TUCO-L2 y TUCO-16 + TUCO-17 presentaron efectos sinérgicos en la inhibición A. baumannii.
Cabe destacar que la combinación TUCO-5E + TUCO-L2 fue la más efectiva para inhibir el desarrollo de todos los patógenos evaluados, observándose este efecto en forma más contundente para K. pneumoniae y A. baumannii.
Evaluación del efecto inhibitorio entre cepas de bacterias láctica
No se observó efecto inhibitorio (halo de inhibición menor a 0,7 cm de diámetro) entre las cepas TUCO-5E y TUCO-2, ni entre las cepas TUCO-5E y TUCO-L2 (datos no mostrados). Se encontró inhibición leve (halos de inhibición entre 0,7 y 1,5 cm de diámetro) entre las cepas TUCO-2 y TUCO-5, entre las cepas TUCO-3 y TUCO-16, y entre las cepas TUCO-3 y TUCO-17. Hubo inhibición moderada entre las cepas TUCO-16 y TUCO-17 (halos de inhibición entre 1,6 y 2,5 cm de diámetro). No se encontró inhibición fuerte (halos mayores a 2,5 cm de diámetro) entre las cepas evaluadas.
Discusión
Los beneficios para la salud proporcionados por los probióticos son diversos e incluyen su capacidad para incrementar la resistencia a patógenos(34). En este estudio, se utilizaron cepas de bacterias lácticas previamente aisladas de la leche de diferentes animales para evaluar el efecto inhibitorio in vitro de las cepas individuales, así como de combinaciones contra patógenos importantes en medicina humana y veterinaria. Se evaluó el efecto antimicrobiano de las cepas de bacterias lácticas sobre patógenos gastrointestinales y extraintestinales incluidos en la lista de la Organización Mundial de la Salud (OMS) de bacterias prioritarias por su alta resistencia a los antibióticos. Dicha lista incluye patógenos prioritarios en los que se recomienda centrar la investigación y el desarrollo de nuevas alternativas antimicrobianas(41).
Las cepas de bacterias lácticas analizadas tuvieron distintos grados de inhibición frente a los patógenos evaluados: EHEC, S. enterica, K. pneumoniae, y A. baumannii. La inhibición del desarrollo de los patógenos en la prueba spot soft agar indica que las cepas de bacterias lácticas evaluadas producen compuestos activos que difunden al medio de cultivo y tienen actividad antimicrobiana(42). Se ha descrito que entre los compuestos con actividad antimicrobiana producidos por las bacterias lácticas se encuentran los ácidos orgánicos, peróxido de hidrogeno, óxido nítrico y bacteriocinas(1,4,12). La naturaleza de los antimicrobianos producidos por las bacterias de esta investigación todavía no ha sido dilucidada. Además, fue posible encontrar combinaciones de cepas de bacterias lácticas con efecto sinérgico para la inhibición in vitro de diferentes cepas patógenas. Dado que existen pocos estudios publicados que comparan los efectos de las combinaciones de cepas de bacterias lácticas potencialmente probióticas con los efectos de las mismas cepas individualmente, nuestro trabajo hace un aporte original en este sentido. Se ha reportado que algunas combinaciones de probióticos tienen mejor adherencia a la mucosa intestinal que sus cepas individualmente(30), o mayor inhibición de la adherencia de patógenos a mucosa intestinal humana(31) o porcina(32). Los resultados presentados acá demuestran además, que combinaciones apropiadas de cepas de bacterias lácticas pueden también potenciar el efecto inhibitorio contra patógenos.
Todas las combinaciones de bacterias lácticas tuvieron una interacción aditiva entre sus cepas constituyentes con respecto a la inhibición de patógenos entéricos. Notablemente, se observó que cinco de las combinaciones evaluadas tuvieron efectos sinérgicos en la inhibición de patógenos extraintestinales: a) se observó efecto sinérgico entre las cepas TUCO-5E + TUCO-L2 para la inhibición de K. pneumoniae y A. baumannii, b) efecto sinérgico para TUCO-5E + TUCO-2, TUCO-5 + TUCO-2, y TUCO-3 + TUCO-17 sobre K. pneumoniae y, c) efecto sinérgico para TUCO-16 + TUCO-17 sobre A. baumannii. Los resultados muestran que la potenciación del efecto inhibitorio entre cepas combinadas varía según el patógeno contrastado y, por lo tanto, los productos probióticos deben diseñarse considerando cada patógeno en particular. Nuestros resultados están en línea con trabajos previos. Chapman et al.(37) evaluaron el efecto inhibitorio sobre patógenos bacterianos de combinaciones de 4 a 15 cepas de bacterias lácticas empleando el método spot soft agar. Sus resultados mostraron que solo algunas combinaciones de bacterias lácticas tuvieron mejores resultados que las cepas individuales, y el efecto inhibitorio fue específico para cada patógeno. En otro estudio, no se encontraron diferencias significativas entre las combinaciones y las cepas individuales para la inhibición de patógenos(43).
E. coli enterohemorrágica (EHEC) es un patógeno de transmisión alimentaria que puede causar diarrea severa en el hospedador y complicaciones extraintestinales potencialmente letales, como falla renal aguda y anormalidades en el sistema nervioso central(44,45). Es una infección zoonótica, cuyo principal reservorio son los animales rumiantes, los que suelen ser portadores asintomáticos(45). En el tratamiento, generalmente se evita el uso de antibióticos, ya que puede inducir la liberación de toxinas por el patógeno, en este caso, los probióticos representan una potencial opción terapéutica, aunque se requieren estudios adicionales(44).
S. enterica no tifoidea es una de las principales causas de enfermedades transmitidas por alimentos en todo el mundo(46). Distintos serotipos pueden causar infección en el ser humano, entre ellos, S. enterica serovar Enteritidis tiene la mayor incidencia y puede infectar tanto a personas como a animales(47). Su principal fuente de transmisión son las aves y el consumo de sus productos mal cocinados, la enfermedad en el ser humano se manifiesta generalmente como una gastroenteritis autolimitante(46,47). Aunque no es común, se han encontrado cepas de S. enterica con resistencia a distintos antimicrobianos(46,47).
Entre las cepas de bacterias acido lácticas utilizadas en este estudio, las cepas L. brevis TUCO-5E(20) y L. salivarius TUCO-L2(23) han demostrado proteger contra la infección de S. enterica Typhimurium en un modelo murino, además, ensayos in vitro muestran que TUCO-5E tiene la capacidad de excluir y desplazar patógenos como E. coli y Salmonella del epitelio intestinal(20), y TUCO-L2 tiene actividad inmunomoduladora(23). La combinación TUCO-5E + TUCO-L2 fue la más efectiva para inhibir el desarrollo de todos los patógenos evaluados, además, presentó sinergia en la inhibición de K. pneumoniae ATCC 13883, y A. baumannii ATCC 19606. Por otro lado, las cepas TUCO-5E y TUCO-L2 no presentaron inhibición entre ellas. Esto hace que la combinación TUCO-5E + TUCO-L2 sea un excelente candidato probiótico multicepa para ser evaluado in vivo en la protección contra la infección de los distintos patógenos evaluados en este estudio.
K. pneumoniae y A. baumannii son importantes patógenos nosocomiales que pueden causar diversas infecciones oportunistas, tanto en humanos como en animales, por ejemplo, infecciones del tracto respiratorio, infecciones del tracto urinario, infecciones de tejidos blandos, septicemia y meningitis(48-51). Ambas especies han desarrollado cepas multirresistentes a los antibióticos que se propagan rápidamente, esto sumado a su capacidad de formar biopelículas, hace que sean patógenos difíciles de controlar y que representen una seria amenaza para la salud pública(48-50). Por esto, la OMS los clasifica entre las especies bacterianas patógenas con mayor prioridad en la resistencia a los antibióticos(41). Las combinaciones TUCO-5E + TUCO-2, TUCO-5 + TUCO-2, y TUCO-3 + TUCO-17, presentaron un efecto sinérgico en la inhibición de K. pneumoniae ATCC 13883; mientras que la combinación TUCO-16 + TUCO-17 presentó un efecto sinérgico en la inhibición de A. baumannii ATCC 19606. Esto hace que las cuatro combinaciones sean interesantes candidatos probióticos multicepa para ser evaluado in vivo en la protección contra infecciones respiratorias y urinarias causadas por patógenos multirresistentes.
Existen varios métodos in vitro para evaluar el efecto inhibitorio sobre patógenos de las cepas probióticas(52). Cada técnica puede dar resultados diferentes, por ejemplo, la cepa con mayor eficacia inhibitoria puede variar según el método utilizado(34,53). Se ha descrito, además, diferencias en la misma técnica, por ejemplo, con la prueba spot soft agar, diferentes investigadores utilizan distintos medios de cultivo, volúmenes, concentraciones de células probióticas y patógenas, e incluso distinto modo de medir la zona de inhibición (diámetro, radio o zona de inhibición de la cepa probiótica). Por ello, sería de gran importancia confirmar el efecto sinérgico de las combinaciones, realizando variaciones en concentraciones de células, medios de cultivos, así como mediante el empleo de otras técnicas. Por otro lado, es necesario considerar que las evaluaciones in vitro no repliquen por completo las condiciones reales in situ de las superficies mucosas como las del tracto intestinal o respiratorio. Sin embargo, estas técnicas son herramientas útiles para la selección rápida de cepas con potencial probiótico, ya que permiten una enorme simplificación del sistema en estudio ayudando a evaluar un gran número de cepas en busca de una propiedad probiótica específica. Esto permite seleccionar las cepas o combinaciones más efectivas para continuar las investigaciones in vivo, que consumen más tiempo y recursos económicos(38).
Conclusión
Se encontraron cinco combinaciones con un efecto sinérgico para la inhibición del desarrollo de las cepas patógenas. El efecto sinérgico fue específico para la cepa patógena y se presentó principalmente sobre patógenos del tracto respiratorio y urinario. Las combinaciones que mostraron sinergia son buenas candidatas para el desarrollo de productos probióticos multicepa para la prevención y el tratamiento de infecciones bacterianas específicas. Sin embargo, se necesitan más estudios en aspectos tecnológicos y de formulación y estudios in vivo para demostrar su eficacia y seguridad en los hospedadores en los que se pretenda su uso.













