Introducción
Fue estimada para 2019 la aparición de 74 200 casos de linfoma no Hodgkin en los Estados Unidos, lo que representaría el 4,3% de los pacientes con cáncer, y 19 970 muertes, es decir, el 3,3% de las muertes por cáncer1.
En la Argentina, según el Instituto Nacional del Cáncer, en 2018 se diagnosticaron 3405 casos de linfoma no Hodgkin, 2,7% del total de neoplasias ma lignas en uno y otro sexo2. Se entiende como linfomas extranodales aquellos originados en órganos extralin fáticos sin mínimo componente ganglionar o con él. Se estima que corresponden a alrededor del 30% de los linfomas3,4.
La región cabeza y cuello es la segunda en fre cuencia en presentar linfomas extranodales, luego del aparato digestivo. Comprenden un conjunto heterogé neo de neoplasias, con distintas formas de presenta ción y de agresividad3-7. El conocimiento de esta entidad es importante para el cirujano ya que debe ser conside rada en el diagnóstico diferencial de la patología de la región, y a que la biopsia quirúrgica es necesaria para su adecuado diagnóstico y orientar el tratamiento actí nico y/o sistémico.
A fin de actualizar la experiencia en este tema, el objetivo de este trabajo fue describir las característi cas histopatológicas, clínicas y quirúrgicas en una serie consecutiva de pacientes operados por linfomas extra nodales de cabeza y cuello (LECC).
Material y métodos
Se llevó a cabo un estudio de diseño retrospec tivo, descriptivo, observacional en un hospital universi tario de tercer nivel. Se revisaron los registros informa tizados de anatomía patológica empleando el término “linfoma”, y filtrando aquellos en ubicaciones “no gan glionares” y “cabeza y cuello”, correspondientes a 5489 pacientes operados durante el período comprendido entre junio de 2009 y junio de 2019. Se excluyeron los enfermos operados en otras Divisiones del Hospital, así como también aquellos pacientes en edad pediátrica.
Diecinueve pacientes (0,35%) presentaron LECC. Se consignaron los siguientes datos de sus histo rias clínicas: la edad, el sexo, su localización, la preexis tencia de enfermedades sistémicas concomitantes, la anatomía patológica y la técnica quirúrgica efectuada.
Se tomaron los recaudos éticos según las reco mendaciones de Helsinki y Tokio y sus modificaciones posteriores. Los datos clínicos fueron protegidos de modo que no se pueda identificar a quién pertenecen ni sean accesibles a personas no comprometidas con el secreto profesional. Todos los pacientes firmaron el consentimiento informado aprobado por el Comité de Ética de la Institución.
Resultados
El promedio de edad fue de 56 años (rango 17- 84, DS 19,3); 16 fueron mujeres (84%).
La localización de los LECC fue: glándula paró tida en 12 casos (63%), glándula submaxilar en 3 casos (16%), glándula salival menor en 2 casos (11%), glándu la lagrimal en 1 caso (5%), glándula tiroides en 1 caso (5%).
Todos fueron linfomas no Hodgkin. Los tipos citológicos fueron: linfoma de tejido linfoideo asociado a mucosas (MALT) 9 (48%), linfoma folicular 4 (21%), linfoma de células B grandes 3 (16%), linfoma de células B pequeñas 1 (5%), linfoma del manto 1 (5%), linfoma anaplásico 1 (5%). La distribución por órgano puede verse en la Tabla 1.

Tabla 1 Localización y tipos histológicos en 19 pacientes con linfomas extranodales de cabeza y cuello.
Cuatro pacientes (21%) presentaron síndrome de Sjögren en el momento del diagnóstico de linfoma, de los cuales tres fueron linfoma MALT y uno linfoma folicular.
Ningún caso presentó compromiso ganglionar, por lo que todos fueron clasificados como estadio IE, según el sistema de clasificación de Lugano8,9.
Entre los 12 pacientes con LECC en parótida, 7 presentaron masas heterogéneas con compromiso glandular difuso, y 5 nódulos más o menos definidos, sin adenopatías. Solo uno de ellos tuvo parálisis facial en el momento de la consulta.
Los estudios complementarios por imágenes (ecografía de partes blandas, tomografía axial com putarizada [TAC] y/o resonancia magnética nuclear [RMN]) confirmaron el hallazgo (Figs. 1 y 2).
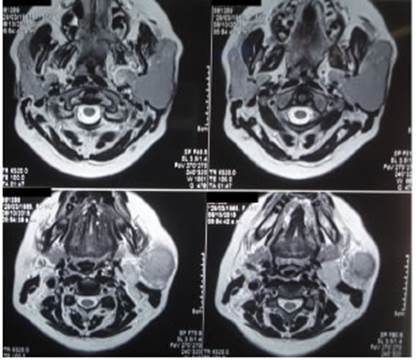
Figura 1 Resonancia magnética nuclear sin contraste de paciente con linfoma MALT de parótida izquierda.

Figura 2 Resonancia magnética nuclear con contraste con gadolinio de paciente con linfoma MALT de parótida izquierda.
A todos se les realizó biopsia por punción-as piración con aguja fina (PAAF), pero los resultados ob tenidos no fueron concluyentes y solo se confirmó el diagnóstico mediante estudio histológico diferido. Los procedimientos quirúrgicos fueron: 6 biopsias quirúrgi cas de parótida (por sospecha de linfoma o tumor ma ligno irresecable), 5 parotidectomías superficiales y una parotidectomía total (por sospecha de tumor benigno o maligno de parótida).
Los 3 pacientes portadores de linfoma de glán dula submaxilar tuvieron biopsia por PAAF no conclu yente y se les practicó la submaxilectomía por sospe cha clínica de malignidad. Ninguno de ellos presentó afección clínica del nervio de Jaffé en el momento de la consulta ni posterior a la cirugía.
Los casos localizados en glándula salival menor, glándula lagrimal y glándula tiroides fueron diagnosti cados mediante biopsia quirúrgica. El primero en el curso del estudio del síndrome de Sjögren, el segundo por sospecha de malignidad e imposibilidad de reali zar PAAF y el tercero por sospecha imagenológica de linfoma tiroideo (presentaba 4 puntos en la escala de Deauville para PET-TC con 18-FDG10. Luego del alta qui rúrgica continuaron su tratamiento y seguimiento en la División de Hematología.
Discusión
A fin de definir y estadificar los linfomas según la clasificación de Lugano, se consideran órganos linfáti cos los ganglios, el timo, el bazo y el anillo de Waldeyer (amígdala, base de lengua, paladar), y sitios extranoda les los demás tejidos.3,4,8
Sin embargo, diferentes investigadores inclu yen los originados en el anillo de Waldeyer entre los LECC, y representa el sitio más frecuente. 5-7,11
En su mayoría son linfomas no Hodgkin, ya que el linfoma de Hodgkin se manifiesta en forma extrano dal en muy baja frecuencia (3,5%)12,13.
En la presente serie no se incluyeron los linfo mas originados en el anillo de Waldeyer ni se presenta ron linfomas de Hodgkin.
Peña y col., de Chile, entre 4907 pacientes con linfomas no Hodgkin, encontraron 1215 con linfomas extranodales (25%). El promedio de edad fue 59 años y el 55% fueron mujeres. Los LECC ocuparon el segun do lugar en orden de frecuencia según su localización (24%), precedidos por los del tracto gastrointestinal (37%) y seguidos por los de piel (15%). Los sitios de ori gen fueron: anillo de Waldeyer (28%), fosa nasal (25%), cavidad oral (12%), tiroides (12%), glándulas salivales mayores (9%), glándula lagrimal (8%), senos paranasa les (6%)7.
En China, existe una alta prevalencia de linfo ma extranodal T/NK, y, en el 80%, la localización más frecuente es cabeza y cuello, en anillo de Waldeyer y/o rinosinusal, también conocidos como “granuloma letal de la línea media”14.
Entre el 12 y el 16% de los casos de LECC se ubican en las glándulas salivales, y representan entre el 2 y el 5% de las neoplasias en estas glándulas; la mayo ría asientan en la parótida y un 20% en la submaxilar y glándulas salivales menores. 11,15
En la serie aquí comunicada, el 63% se ubica ron en la parótida, seguramente por ser una patología ampliamente tratada en el centro, y por no haberse incluido ningún paciente con ubicación en el anillo de Waldeyer.
Las neoplasias linfoides suelen ser más fre cuentes en hombres. Sin embargo, los linfomas extra nodales en las glándulas salivales y tiroides presentan una distribución predominante en mujeres (8 de cada 10), como también ocurrió en la presente serie. La 7,15 preexistencia de enfermedades autoinmunitarias (más frecuentemente desarrolladas en pacientes de sexo femenino) podría justificar este hecho. La distribución por edad ha sido similar a lo referido por otros investi gadores 5,14.
Los linfomas primarios de la glándula tiroides son tumores poco comunes, con una frecuencia del 5% de todas las neoplasias tiroideas, y menos del 3% de los LECC. El linfoma difuso de células B grandes y el linfoma MALT (linfoma de tejido linfoideo asociado a mucosas) son los tipos más frecuentes. Clínicamente se presen tan como un bocio eutiroideo de rápido crecimiento y pueden dar síntomas por compresión de órganos veci nos (disfagia, disfonía, disnea).16,17
El linfoma MALT tiroideo ocurre principalmen te en pacientes de sexo femenino con historia previa de tiroiditis de Hashimoto18 y la coexistencia con un carci noma papilar es infrecuente pero ha sido descripta.19
Los métodos de diagnóstico por imágenes permiten conocer la extensión local de la enferme dad, pero no tienen características específicas. Recien temente se ha establecido que la RMN con gadolinio aporta información acerca del comportamiento de di chos tumores con respecto a la administración de con traste intravenoso. Se ha postulado que las neoplasias benignas (como los adenomas pleomorfos) presentan un realce tardío (superior a los 150 segundos) tras la administración de contraste, mientras que las neopla sias malignas (como los carcinomas mucoepidermoi des) realzan tempranamente (antes de los 150 segun dos). A su vez, el lavado de contraste o washout se da más rápidamente en los tumores benignos que en los malignos (washout rate > 30% versus < 30%, respectiva mente). Por su parte, los linfomas de glándulas salivales presentan un realce temprano tras la administración de contraste (como los carcinomas) pero también un was hout rápido (como los adenomas)20. La tomografía por emisión de positrones (PET-TC) con 18-FDG contribuye en el proceso diagnóstico de los linfomas de Hodgkin y los linfomas difusos de células B grandes. En el año 2009 fue publicado en Francia el puntaje (score) de Deauville. Se trata de una escala que compara el grado de captación del 18-FDG en los linfomas, con respecto a la captación basal, a la captación mediastinal y a la captación hepática10.
La biopsia por punción-aspiración con aguja fina (PAAF) ecoguiada es una herramienta diagnóstica útil en diversas patologías de cabeza y cuello. Sin em bargo, el estudio citológico no permite un diagnóstico de certeza en patología linfoproliferativa. La biopsia histológica por punción con aguja gruesa (Tru cut) eco guiada podría tener un lugar en el diagnóstico; tiene la limitación del tamaño de la lesión y la posibilidad de afectar algún nervio, especialmente en la parótida. Además, el estudio histopatológico requiere una mues tra tisular suficiente para incluir otros estudios, como la citometría de flujo y el análisis citogenético, que en los linfomas no Hodgkin son necesarios para una correcta tipificación5.
En la casuística aquí descripta, el empleo de métodos de diagnóstico por imágenes fue variable, se gún disponibilidad, y en pocos casos permitió presumir el diagnóstico, al igual que la biopsia por PAAF. En to dos los pacientes, el diagnóstico solo se confirmó con el estudio histopatológico de la pieza quirúrgica, que correspondió a resecciones de distinta magnitud según el grado de sospecha preoperatoria.
Las enfermedades tiroideas autoinmunitarias y el síndrome de Sjögren pueden evolucionar a linfomas de células B grandes (no Hodgkin) en la glándula tiroi des y en las glándulas salivales en un 0,5 y 5%, respec tivamente21.
Las enfermedades autoinmunitarias llevan a un estado de inflamación crónica, donde el estímulo antigénico sostenido por parte de distintas citoquinas proinflamatorias (IFN gamma, IL-10, etc.) promueve la activación y proliferación de las células B22. Esta rela ción molecular entre autoinmunidad y la proliferación linfática también es observada a nivel histológico. En pacientes con enfermedades autoinmunes, el infiltrado linfocitario en los tejidos glandulares es predominan temente de linfocitos T CD4+. Estos promueven el de sarrollo de estructuras de tipo centro-germinal, lugar de activación de células B21. El riesgo de desarrollar un linfoma en un paciente con diagnóstico de síndrome de Sjögren es cuatro veces mayor que en la artritis reuma toide, siete veces mayor que en el lupus eritematoso sistémico y diez veces mayor que en la población gene ral22. De estos, solo la minoría se localizará en cabeza y cuello.
La prevalencia de Sjögren en pacientes con linfoma de glándula salival es del 18%. Sin embargo, 23 existe un grupo de pacientes en quienes el diagnóstico de Sjögren se realiza luego del diagnóstico de la pato logía linfoproliferativa. Por lo tanto, aquellos pacientes con linfoma de glándula salival deberían ser estudiados para descartar esta entidad reumatológica24.
El síndrome de Sjögren y las enfermedades ti roideas autoinmunitarias se caracterizan por desarro llar un amplio espectro de anormalidades genéticas y moleculares que llevan a la proliferación no controlada de células B y su transformación neoplásica21.
En pacientes con síndrome de inmunodeficien cia adquirida, los linfomas no Hodgkin constituyen la segunda neoplasia maligna más frecuente, luego del sarcoma de Kaposi. El virus HIV incrementa entre 100 y 200 veces el riesgo de desarrollar un linfoma no Hod gkin25. En la Argentina, Corti y col. publicaron una serie de 24 pacientes HIV positivos con diagnóstico de linfo ma extranodal de cabeza y cuello. El 75% fueron hom bres y la media de edad fue de 39 años. Los sitios más frecuentes de localización fueron encía y paladar duro (62%), maxilar y mandíbula (26%), piel y partes blandas (21%), glándulas salivales y anillo de Waldeyer en el res to de los casos25.
Un reciente metanálisis identifica el virus de la hepatitis C (HCV) como factor de riesgo para desarrollar linfoma extranodal de órbita26.
El subtipo histológico y el órgano primario de origen constituyen los dos factores pronósticos más importantes en los linfomas extranodales, debido a las diferencias que se presentan en la historia natural de la enfermedad y a la estrategia terapéutica órgano-es pecífica. En la presente casuística no fue posible contar con un seguimiento completo para evaluar los resulta dos alejados, debido a que el tratamiento definitivo fue cumplido en varios casos en otras instituciones.
Peña y col. comunicaron una supervivencia global a 5, 10 y 15 años de 63%, 50% y 38%, respecti vamente, con una media de seguimiento de 9,6 años7.
Chi y col., de Taiwán, informaron una supervi vencia global a 5 y 10 años de 68,0% y 57,8%, y una supervivencia libre de enfermedad de 53,6% y 49,3%, respectivamente27.
Del análisis de la serie aquí comunicada es posible concluir que los LECC son neoplasias poco fre cuentes, que ocurren en pacientes de mediana edad y predominantemente mujeres. Su cuadro clínico se pue de superponer con el de otra patología de la región, y ni los estudios por imágenes ni la biopsia por punción con aguja fina pueden diagnosticarlos en el preoperatorio. Esto requiere el conocimiento y sospecha por parte del cirujano de cabeza y cuello a fin de realizar interven ciones quirúrgicas de distinta magnitud que permiten arribar a su diagnóstico y tratamiento.











 texto en
texto en 


