Introducción
El Síndrome Urémico Hemolítico (SUH) típico es la causa más común de Insuficiencia Renal Aguda (IRA) en pediatría. En Argentina es la segunda etiología que lleva a la enfermedad renal crónica (ERC) y al trasplante renal (TxR).1
En nuestro país, cada año se registran entre 12 y 14 casos por cada 100.000 niños menores de 5 años. Así, la incidencia acumulada de la enfermedad ha alcanzado recientemente 500 nuevos casos por año.1
En el 90 % de los casos, el SHU es causado principalmente por E. coli productora de verotoxina (STEC); serotipo O157:H7. En el 85 al 90 % de los casos, el SHU típico se resuelve sin más secuelas dentro de la semana siguiente de su comienzo.2 Entre el 10 al 15 % de los niños afectados por STEC desarrollan SHU, con un periodo prodrómico de 7 a 14 días.2
En el SHU típico, aproximadamente el 25 % de los pacientes muestran compromiso de sistema nervioso central (SNC) y un 4 % aproximadamente, presentan secuelas neurológicas severas con riesgo de muerte o con secuelas graves y/o limitantes a largo plazo. 2-3,6
Desafortunadamente, hasta ahora, no ha habido ningún tratamiento estandarizado para los síntomas y signos neurológicos, tales como convulsiones, parálisis y coma.7
El mecanismo fisiopatológico primario del SUH es el daño endotelial causado por la toxina
Shiga seguido de activación de la cascada del complemento,3-6) que conduce a la trombosis microangiopática principalmente en el riñón. Otros órganos pueden ser afectados por daños microvasculares y celulares. La mayoría de las veces, el daño renal no es permanente y la función renal se recupera en un 90 % casos, con requerimiento dialítico transitorio entre 50 y 75 % de los casos. Sin embargo, así como la insuficiencia renal, el compromiso del SNC juega un papel importante en la patología del SUH, representando la causa más frecuente de muerte.3-5-6
Eculizumab
La utilización de esta droga fue aprobada por primera vez en 2007 para la hemoglobinuria paroxística nocturna, y posteriormente en 2011 para SUH atípico (SUHa).
El SUHa está asociado a alteraciones genéticas o adquiridas del complemento, que incluyen mutaciones en las proteínas reguladoras de complemento o formación de anticuerpos anti factor H. Su tratamiento aprobado, entonces, es el Eculizumab (Soliris), que se trata de un anticuerpo tipo IgG monoclonal humanizado generado con tecnología de ADN recombinante, que se une con alta afinidad a C5 y bloquea su escisión a C5a y C5b e impide la formación de C5b-9 conocido como Complejo de Ataque de Membrana.
Debido al mecanismo involucrado en la activación de la vía alterna del complemento por parte de la shiga toxina, y al catastrófico desenlace clínico de los pacientes con compromiso neurológico severo, se plantea como alternativa terapéutica para detener el daño neurológico, sus secuelas y el riesgo de vida que implica para el paciente.2
Resultados
En el caso 1, se trata de un paciente internado en el Hospital Italiano de Buenos Aires de seis años de edad, masculino, con antecedente de siete días de diarrea y que dos días previos a la internación presenta diarrea con sangre.
Al ingreso se interpretó como cuadro de shock hipovolémico secundario a foco enteral, con colitis hemorrágica. Recibió expansión con solución fisiológica a 100 ml/kg. Se medicó con
metronidazol-gentamicina.
Laboratorio al ingreso hospitalario: Hematocrito 45 %, Glóbulos Blancos 6400/ mm3, recuento plaquetas 107.000/mm3, urea 21 mg/dl, creatinina 0.39 mg/dl. (Tabla 1)
Al quinto día de internación se observó anemia hemolítica y plaquetopenia con caída de filtrado glomerular, insuficiencia renal aguda (IRA), valores uremia de 50 mg/dl, creatinina 1 mg/dl, e incremento de los parámetros de hemólisis; LDH 1600 UI, con activación de la vía alterna del complemento (C3:43 mg/dl y C4:5 mg/dl) en contexto de sedimento urinario con macrohematuria. Como parámetros de hemólisis intravascular el paciente presentó en el frotis en sangre periférica la presencia de esquistocitos con niveles altos de la enzima lactato deshidrogenasa (LDH) 3000 UI y niveles indetectables de haptoglobina. En el día siete las tres determinaciones de Shiga toxina fueron negativas, por lo que se envió anti LPS al Instituto Malbrán siendo positivo para E. coli O145.
Anca C y P negativos, FAN (-), anti DNA (-). (Tabla 1)
Homocisteína 7.3 umol/L (normal: 7-12 umol/L)/ Vitamina B12: 406 pg/ml (200-500 pg/ml). Ecografía abdominal: aumento difuso de la ecogenicidad renal, aumento del grosor de la pared del colon.
Al día siete presentó disminución del ritmo diurético con anuria, deposiciones sanguinolentas, y sensorio con tendencia al sueño. Comenzó hemodiálisis y plasmaféresis. Al día nueve, coincidente con el pasaje de plasmaféresis a días alternos, se observó hipertensión arterial (HTA) severa, presión arterial máxima: 140/100 mmHg y presión arterial media (PAM) de 120 mmHg (Pc95 PA 115/74 mm/Hg); requirió infusión de nitroprusiato de sodio, triple medicación antihipertensiva con enalapril, doxazosina y propranolol.
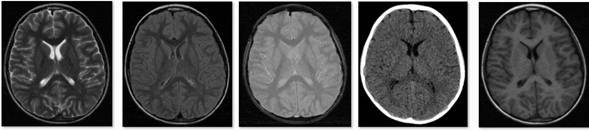
Posteriormente, el paciente presentó convulsiones con depresión del sensorio e ingresó en asistencia respiratoria mecánica (ARM). Se realizó TC cerebro que informó hipodensidades subcorticales en proyección fronto-parieto- occipital bilateral, compatibles con procesos isquémicos en evolución y múltiples imágenes hiperdensas compatibles con componente hemorrágico intraparenquimatoso parietal y occipital (Figura 1). Se realizó como estudio complementario RM de cerebro: múltiples lesiones hiperintensas en FLAIR. Edema vasogénico, hematomas intraparenquimatosos (frontal y parietal izquierdo), signos compatibles con PRESS. (Figura 2)
Al día diez, surgió en el interrogatorio antecedente familiar dudoso de SUHa. Que finalmente resultó ser SUH típico.
Se determinó en la Academia Nacional de Medicina C5b-9: 1151 ng/ml (rango valor normal: 172-355 ng/ml), se solicitó actividad e inhibidor de ADAMTS 13, y detección de anticuerpos anti ADAMTS 13: siendo ambos resultados dentro de límites normales. Comenzó tratamiento con Eculizumab según protocolo con franca mejoría clínica y neurológica.
En resumen, el paciente requirió treinta días de internación, estuvo diez días en anuria, requirió tres días de ARM, recibiendo en total seis sesiones de plasmaféresis y dos dosis de Eculizumab.
Egresó con el siguiente laboratorio: Hto 26%, glóbulos blancos 5800/mm3, recuento plaquetas 286.000/mm3, uremia 44 mg/dl, creatinina 0.5mg/dl; C3 100 mg/dl, C4 23 mg/dl,
LDH 249 UI, haptoglobina 25 mg/dl. Medio interno normal. C5b-9 muy elevado durante el episodio de depresión neurológica que luego se normalizó.
Se suspendió Eculizumab con estudio genético sin mutaciones asociadas a SUHa. Luego de un año, el paciente se encuentra sin secuelas neurológicas, con función renal normal y sin microalbuminuria patológica, normotenso y sin recurrencia de la enfermedad.
En el caso 2, se trata de un paciente de 9 años de edad, tratado en el Hospital Universitario
Austral, derivado con diagnóstico de SUH diarrea positivo con resultado de Coprocultivo negativo.
Se trata de un paciente previamente sano, que inició con cuadro de tres días de evolución caracterizado por disentería, fiebre y dolor abdominal tipo cólico. Consultó a centro asistencial en su lugar de origen (La Pampa) donde ingresó en regular estado general, se realizó diagnóstico de SUH diarrea positivo con resultado de coprocultivo negativo y se derivó al Hospital Universitario Austral. Al ingreso presentaba deshidratación leve, vigil y reactivo, insuficiencia renal aguda con anemia, plaquetopenia y acidosis metabólica. Laboratorio inicial mostró glóbulos blancos 15.420/mm3, hemoglobina 10,3 g/dl, hematocrito 28.1 %, recuento plaquetas 44.000/mm3, urea 267 mg/dl, creatinina 8.2 mg/dl, ácido úrico 12 mg/dl, GOT 68 U/l TGP 186. U/L.
Estado ácido base venoso: 7.28/33/37/17/-8.6 ionograma Na 134 meq/l potasio 4 meq/l cloro 99 meq/l LDH 3956. U/L. (Tabla 2)
Continuó con empeoramiento clínico y analítico, presentando oligoanuria y por lo tanto, se indicó comenzar con diálisis peritoneal.
A las 24 horas presentó movimientos incoordinados de miembro superior con retroversión ocular e hipertonía. TC y resonancia magnética de cerebro normales. Polisomnográfico patológico. Evolucionó a coma con requerimiento de RM. (Figura 3)
Se plantearon como diagnósticos diferenciales SUH típico con compromiso neurológico severo vs SUH atípico. Por este motivo, se decidió iniciar Eculizumab 600 mg a pasar en una hora y media, dentro de las 6 horas de iniciado el deterioro neurológico franco (previa aplicación de vacuna antimeningocócica ACWY y profilaxis con amoxicilina). A los 45 minutos de iniciada la infusión de Eculizumab se observó mejoría neurológica franca con lucidez y capacidad de contestar preguntas complejas. El paciente se recuperó neurológicamente por completo.
Luego se recibió resultado positivo para STEC 0157: H7/atx2a/atx2C. Resultado de actividad de ADAMTS 13 y complemento normal. No requirió otra dosis de Eculizumab.
Discusión
Pape et al., demostraron en su análisis retrospectivo que el uso temprano de Eculizumab se asoció con una evolución favorable del compromiso severo del SNC en niños con SUH típico.3
Walsh et al., concluyen en su revisión que el beneficio del uso de Eculizumab como tratamiento específico del SUH típico ha sido difícil de establecer.2
El SUH típico con compromiso neurológico severo, representa un cuadro de alta morbimortalidad que amenaza la vida y lleva a una enfermedad neurológica grave a largo plazo.1-3
Recientemente, Walsh y Johnson han publicado una revisión acerca del uso de Eculizumab en SUH típico,2) que evalúa los riesgos y beneficios de esta indicación propuesta, aunque debido a la falta de ensayos clínicos controlados y randomizados, es difícil concluir si realmente existe un efecto beneficioso del uso de la droga en SUH típico.
Existen actualmente dos ensayos doble ciego controlados con el fin de aportar pruebas para guiar el uso de esta terapia en el SUH típico. Comparan la utilización de Soliris vs. placebo: ECULISHU en Francia enfocado en el compromiso renal y el estudio ECUSTEC en Reino
Unido, evaluando el riesgo global de la enfermedad.2
Son necesarios más estudios acerca del beneficio de la infusión de Eculizumab en casos puntuales, para poder establecer una guía terapéutica en pos de disminuir o evitar las secuelas neurológicas severas e incluso la muerte del paciente.
Mehtap et al. describieron que la patogénesis de SHUa puede ser desencadenada por STEC, considerando que la shigatoxina tipo 2 (Stx2) es el principal factor de virulencia de la STEC, que desencadena la activación del sistema del complemento, especialmente en un paciente con un déficit del Factor H. Muchos estudios han demostrado que Stx2puede ser aceptado como un nuevo ligando para Factor H. Estos pacientes, inclusive, se benefician de la infusión de Eculizumab para disminuir o evitar las secuelas neurológicas severas e incluso la muerte.15
Conclusión
En conclusión, en los casos de SUH con compromiso neurológico, la administración temprana de Eculizumab podría ser una alternativa para reducir las secuelas neurológicas a largo plazo. El uso de Eculizumab (Soliris), disminuiría el daño mediado por el complemento (microangiopatía trombótica) y se debería considerar su uso en pacientes con SUH típico con compromiso neurológico severo.
Conflicto de intereses
Los autores declaran no poseer ningún interés comercial o asociativo que presente un conflicto de intereses con el trabajo presentado.