Introducción
La preeclampsia se caracteriza, histológicamente, por hipertrofia y tumefacción de las células endocapilares (endoteliosis), y por el engrosamiento de las paredes capilares con imágenes de doble contorno. Sin embargo, la preeclampsia también puede estar acompañada de lesiones de glomeruloesclerosis focal y segmentaria (GEFS) de novo o recurrente, especialmente las formas graves, con síndrome nefrótico o hipertensión severa, similares a la GEFS primaria, aunque clínicamente se diferencian por el curso autolimitado.1-2
La incidencia global de la preeclampsia se ha estimado entre el 3 al 5 % del total de los embarazos, siendo la principal causa de morbilidad y mortalidad en mujeres embarazadas y sus fetos en todo el mundo. En la preeclampsia la incorporación de citotrofoblasto en las arterias espirales es incompleta,3 la placenta modificada libera el receptor de crecimiento endotelial vascular (VEGF, por sus siglas en inglés Vascular Endothelial Growth Factor) soluble en la circulación de la madre (sFlt-1), lo que causa muchos trastornos, incluso daño renal.
El VEGF es producido por los podocitos glomerulares, necesario para la función normal de los mismos. El daño del número crítico de podocitos contribuye al desarrollo de la GEFS.4-6
Presentamos el caso de una mujer joven gestante que, posteriormente a un cuadro de preeclampsia severa asociada a falla renal aguda con requerimiento dialítico, desarrolló síndrome nefrótico debido a GEFS.
Reporte De Caso
Paciente mujer, ama de casa, 35 años de edad, natural y procedente de Huacho, provincia de Huaral, Departamento de Lima (Perú). Como antecedentes presentó:
1) Hipotiroidismo subclínico, sin tratamiento desde hace dos años.
2) Dos gestaciones previas, los dos productos vivos. Primer parto a los 28 años por cesárea debido a pelvis estrecha, primer embarazo sin complicaciones.
Ingresó a maternidad en abril de 2018, a las veintidós semanas de gestación, debido a una cefalea intensa. Se le halló presión arterial de 160/90 mmHg y fue diagnosticada con preeclampsia severa, fue operada por cesárea de emergencia.
La paciente ingresó a la Unidad de Cuidados Intensivos por requerir ventilación mecánica y desarrolló falla renal aguda oligúrica, que le produjo sobrecarga hídrica, refractaria a tratamiento diurético, por lo que recibió terapia de reemplazo renal (TRR) con un total de 16 sesiones de hemodiálisis convencional.
Por su evolución clínica favorable fue retirada de ventilación mecánica, recuperó la diuresis y la función renal. Se le dio el alta a fines de mayo de 2018, luego de dos meses de internación hospitalaria.
Cuatro meses después del alta, en septiembre de 2018, la paciente acudió al consultorio externo del Servicio de Nefrología del Hospital Nacional Dos de Mayo, con historia de edema progresivo de un mes de evolución, aumento de la sed y, finalmente, oliguria. El examen clínico reportó: PA=140/80 mmHg, FC=90 latidos por minutos, 18 respiraciones por minuto, edema generalizado, con fóvea 4+/4+ en miembros inferiores y superiores, ascitis y edema palpebral. En aparato respiratorio, rales crepitantes en 2/3 inferiores de ambos hemitórax, en abdomen signo de la oleada (+) y matidez desplazable. Se indica su hospitalización inmediata.
Los estudios de laboratorio evidenciaron creatinina sérica entre 2 y 4 mg/dl, albúmina sérica 1,89 g/dl, colesterol total 533 mg/dl, triglicéridos 300 mg/dl, proteinuria 10 g en 24 horas, hemoglobina 9,0 g/dl, junto a un examen de orina patológico, con urocultivo positivo para Proteus mirabilis.
Para descartar secundarismo se evaluaron anticuerpos antinucleares, anticuerpos anticitoplasma de neutrófilos, perfil de anticuerpos antifosfolípidos, proteínas del complemento; todos resultaron no contribuyentes. También se realizaron exámenes serológicos para asegurar la ausencia de infecciones.
La ecografía renal mostró tamaño renal en rangos normales, con parénquimas de 20 mm; la ecografía doppler de vasos renales no evidenció trombosis de venas ni signos de estenosis; la tomografía torácica, abdominal y pélvica tampoco reportó alteraciones significativas.
El tratamiento consistió en medidas de soporte: diuréticos, antiproteinúricos, anticoagulación profiláctica, fibratos, estatinas, albúmina humana y manejo electrolítico y nutricional, así como cefuroxima y levotiroxina.
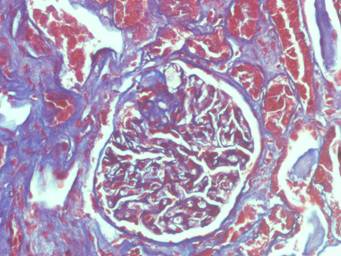
La biopsia renal, realizada en septiembre de 2018, por el síndrome nefrótico presentado informó: corteza y médula renal con 18 glomérulos, 2 de ellos globalmente esclerosados y 5 con esclerosis segmentaria (2 de localización perihiliar y con sinequia a la cápsula de Bowman), el resto de los glomérulos dentro de límites normales. Existe engrosamiento segmentario de asas capilares. Los túbulos tienen degeneración turbia, cilindros hialinos (1+) y hemáticos (1+), con atrofia tubular (20 %), intersticio con fibrosis leve, vasos sanguíneos sin alteraciones significativas. (Imágenes1y2)
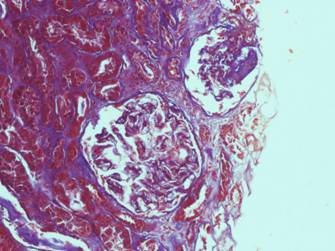
Imagen 1 Tinción tricrómica de Masson, en parte superior derecho de la imagen se evidencia glomérulo esclerosado (coloración PAS, 100x)
La inmunofluorescencia fue negativa para IgG, IgM, IgA, C3 y C1q. El diagnóstico histopatológico fue GEFS con variante perihiliar.
Posteriormente a la biopsia, la paciente fue atendida por consultorio externo de nefrología con corticoterapia, diuréticos, antiproteinúricos, manejo nutricional y medidas de soporte: su evolución clínica fue favorable. Al alta presentó: creatinina 1.0 mg/dl, proteinuria 300 mg en 24 horas y hemoglobina 10.1 mg/dl.
Discusión
En pacientes con preeclampsia se observa daño en los podocitos, se cree que ésta es la razón de la proteinuria. En el curso de la preeclampsia a menudo se manifiesta síndrome nefrótico y la pérdida renal de proteínas es mayor a 3.5 gr por día, sin otros cambios en el sedimento urinario.7-8 Las células epiteliales glomerulares viscerales, también llamadas podocitos, son células diferenciadas que recubren la superficie exterior de la membrana basal glomerular, por lo tanto, forman la barrera final contra la pérdida de proteínas. Hasta el momento se pensaba que los podocitos, durante el curso de la preeclampsia, permanecían intactos; algunos estudios han demostrado que la proteinuria en la preeclampsia está asociada con la podocituria.9)
La podocituria precede a los síntomas clínicos de la preeclampsia y a la presencia de la proteinuria por semanas. Poco se sabe sobre el proceso de recuperación de la lesión de los podocitos tras los embarazos con preeclampsia. Comúnmente, la proteinuria se resuelve a las doce semanas postparto, aunque algunos estudios indican que la podocituria puede persistir luego del parto.10 En nuestro caso, la paciente persistió con la proteinuria dieciséis semanas después del embarazo, por lo que la GEFS se encontraba aún activa. Presentó síndrome nefrótico puro, por lo cual tuvo que ser hospitalizada.
La pregunta sigue siendo si en presencia de cambios de la GEFS, que aparece luego de la preeclampsia, las mujeres deben ser tratadas con inmunosupresores o no. La terapia de inmunosupresión está reservada para la GEFS primaria. Al término del embarazo ya no es una causa subyacente.
En este caso en particular, la paciente presentó los síntomas del síndrome nefrótico luego del término del embarazo, respondiendo favorablemente a la corticoterapia, por lo que se deduce que se trataría de una GEFS primaria.
Nochy realizó un estudio en el cual once mujeres tuvieron GEFS postparto, de las cuales, diez de ellas presentaron preeclampsia severa. De esto se concluye que la preeclampsia es una causa de desarrollo de GEFS postparto.11
En la presencia de síndrome nefrótico postpreeclampsia con afectación renal, se aconseja considerar la presencia de una GEFS activa que requiere diagnóstico y manejo para mejorar el estado clínico de las pacientes.
Conflicto de intereses
Los autores declaran no poseer ningún interés comercial o asociativo que presente un conflicto de intereses con el trabajo presentado.