Introducción
El tratamiento de los dientes con exposición pulpar y desarrollo radicular incompleto es un procedimiento que aparece con cierta frecuencia en la clínica diaria. 1 Cuando se produce la exposición de la pulpa en un diente con desarrollo radicular incompleto, ya sea a causa de un traumatismo o durante la remoción de tejido cariado, el protocolo habitual indica un tratamiento de dos etapas. Primero, se debe proteger la pulpa con un material biocompatible y bioactivo que permita preservar su vitalidad y estimular el desarrollo del remanente radicular. El uso de este tipo de material para proteger y sellar la exposición favorece la concentración de células progenitoras (stem cells) en el área y su posterior proliferación y diferenciación en células potencialmente capaces de producir una matriz de dentina terciaria y la formación de un puente dentinario que aísle la pulpa remanente del medio externo. 1, 2
En ese sentido, el empleo de materiales biocerámicos (MBi) permite la mejor evolución de las patologías preexistentes como así también resultados ciertamente promisorios en aquellos casos considerados como de pronóstico reservado. 2 Los MBi son compuestos obtenidos mediante una serie de procesos químicos, con una estructura parecida a la hidroxiapatita. Luego de su hidratación, los MBi tienen la capacidad de producir el desarrollo de una respuesta regenerativa de los tejidos, especialmente los que funcionan por medio de la aposición de nuevo tejido calcificado. 2-3 Después de la inclusión en la fórmula del agregado de trióxido mineral (MTA) en 1993, se han desarrollado series de MBi para uso endodóntico, con propiedades fisicoquímicas mejoradas que ofrecen mayores ventajas para su uso clínico actual. 4-5
Entre ellos, el Biodentine (BDT; Septodont, Saint- Maur-des-Fossés, Francia) fue desarrollado para ser utilizado como material de reemplazo dentinario. 5-7
El Biodentine (BDT) tiene una presentación doble, en forma de polvo y de líquido. El polvo actúa como acelerador y está formado por silicato tricálcico, silicato dicálcico, carbonato de calcio, óxido de hierro y óxido de circonio. El líquido funciona como agente reductor y contiene cloruro de calcio y polímero hidrosoluble. La mezcla del polvo y el líquido reacciona al mezclarse con agua, formando un gel de silicato hidratado que contiene núcleos de hidróxido de calcio. 3 El gel polimeriza en un tiempo aproximado de 10 a 12 minutos, generando una estructura sólida que libera hidróxido de calcio.7 Su tiempo de endurecimiento es significativamente menor al del MTA y otros MBi disponibles en el mercado. 8 El BDT es bioactivo, biocompatible y tiene una excelente capacidad de sellado y acción antimicrobiana. 6, 8-13 Cuarenta y ocho horas después de su fraguado, su dureza Vickers es similar a la dentina natural sana (300 MPa) y su empleo ha sido indicado como una opción viable y ventajosa para el tratamiento de diferentes situaciones clínicas. 9, 14-26
Si bien se ha demostrado la excelente performance del BDT para la protección pulpar directa (PPD), la bibliografía referida a la acción del BDT en casos de exposición pulpar en dientes con desarrollo radicular incompleto es escasa. 1, 14-17 El objetivo del presente trabajo fue describir el tratamiento de un incisivo superior con exposición pulpar y desarrollo radicular incompleto utilizando BDT como material para la PPD.
Caso clínico
Un paciente de 9 años de edad con historia médica irrelevante se presentó a una consulta de emergencia exhibiendo una fractura amelodentinaria con exposición pulpar en la pieza 11, producto de un choque con la bicicleta en las 24 horas previas a la consulta.
El examen clínico reveló que los tejidos faciales se encontraban dentro de los límites normales. El diente presentaba una ligera giroversión y exposición pulpar rodeada por dentina sana (fig.1A). El paciente relató que tenía sensibilidad al frío, pero que la molestia desaparecía al retirar el estímulo. Al palparla, la pieza dentaria mostró una movilidad apenas perceptible. En el examen radiográfico se observó que el desarrollo radicular estaba incompleto con un área apical amplia (fig.1B) y que las estructuras perirradiculares eran normales. Las respuestas a las pruebas de vitalidad fueron positivas, por lo que se decidió realizar una PPD con BDT para la restauración de la fractura.
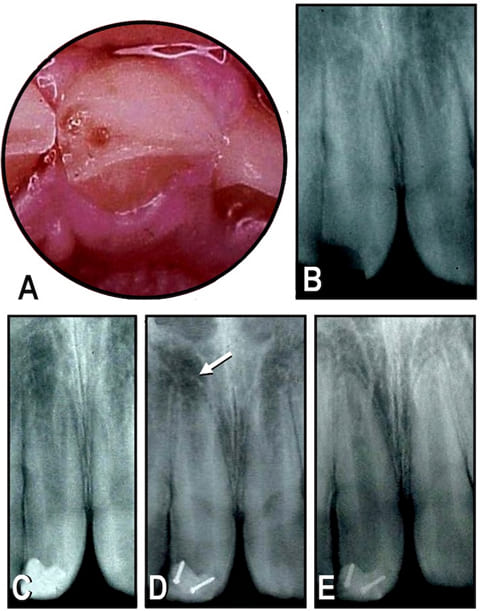
Figura 1 A: Imagen clínica de la fractura amelodentinaria y la exposición pulpar. B: Radiografía preoperatoria. C: Radiografía posoperatoria inmediata, donde se observa la protección pulpar y la restauración de la fractura. D: Control radiográfico a los 18 meses. Se observa la evolución del desarrollo radicular y la neoformación incipiente de la cortical alveolar (indicada con la flecha). Se observa también que la obturación original fue reemplazada. E: Control radiográfico a los 25 meses. Se evidencia que se ha completado el proceso de apexogénesis.
Luego de que el padre del paciente firmara el consentimiento informado, se aplicó anestesia local con clorhidrato de carticaína 4% combinada con L-Adrenalina 1:100.000 (Totalcaína Forte, Laboratorios Bernabó SA, Buenos Aires, Argentina) y se aisló el campo operatorio con goma dique. Se irrigó el área de la fractura con una solución de NaOCl al 1% y se removió cuidadosamente una capa superficial de la pulpa usando una cucharilla de Black (Dentsply, Ballaigues, Suiza). Luego de cohibir la hemorragia con una torunda de algodón estéril humedecida en suero fisiológico, se preparó y se utilizó el BDT de acuerdo con las especificaciones del fabricante. El BDT se aplicó sobre la herida pulpar sin ejercer presión. Pasados 15 minutos, se restauró la cavidad con un ionómero de vidrio (Vitremer™, 3M ESPE, St Paul, MN, USA) (fig.1C).
Los primeros días luego del procedimiento el paciente afirmó estar cómodo y sin sintomatología.
A los 18 meses se le realizó un control clínico y radiográfico donde se pudo apreciar la evolución del desarrollo radicular y la neoformación de una incipiente cortical alveolar (fig.1D). El ionómero vítreo fue reemplazado por una resina compuesta con dos retenciones adicionales (pins). El último control fue realizado a los 25 meses, y el diente estaba asintomático y respondía normalmente a las pruebas de sensibilidad.
El examen radiográfico reveló que la raíz había completado su desarrollo y no se observaron calcificaciones pulpares (fig.1E).
Discusión
En el presente informe se describe el caso clínico de un paciente con una pieza dentaria con exposición pulpar y desarrollo radicular incompleto tratada con BDT como material de protección directa. Luego de 25 meses, la vitalidad de la pulpa se había conservado y el remanente radicular había completado su desarrollo fisiológico. La preservación de la vitalidad pulpar permite aprovechar su capacidad para reparar la herida mediante la aposición de dentina terciaria, generando de esta forma un ambiente propicio para el posterior desarrollo radicular. 27 Tal como fue demostrado por Tziafas et al. 15 y Laurent et al. 28 , el uso del BDT permite la síntesis de la dentina reparativa de estructura tubular mediante la secreción y modulación del factor de crecimiento TGF-β1. Gracias al silicato tricálcico y a los iones calcio y silicio de su composición, el BDT estimula la proliferación y diferenciación celular. 28, 29
La ausencia de dolor posoperatorio en el presente caso clínico no fue totalmente inesperada. Han y Okiji30 demostraron en este sentido que, en contacto con la pulpa vital, tanto el BDT como otros MBi tienden a reducir la función del receptor de dolor TRPA1, limitando la secreción de factores proinflamatorios como la histamina, la bradiquinina (IBK) y las prostaglandinas. Este fenómeno podría explicar la ausencia de sintomatología en la mayoría de los casos de PPD tratados con MBi. 8, 16
El uso de NaOCl al 1% o al 2,5% ha sido indicado para obtener una desinfección más efectiva de la pulpa expuesta. 1, 2 En este caso se trabajó en concordancia con lo planteado por Ghoddusi et al. 2 y Nowicka et al. 16 , quienes consideran que en casos de exposición pulpar la ausencia de infección es un factor fundamental para la orientación del tratamiento. Los controles clínicos y radiográficos y la comparación con el desarrollo radicular de las piezas dentarias vecinas son requisitos necesarios para evaluar a distancia los resultados del tratamiento. Si bien el BDT demostró excelentes resultados como material de protección directa de la pulpa, es necesario recalcar que la información aportada por el presente caso clínico es limitada. La mayoría de las publicaciones registradas hasta el momento han sido ensayos realizados in vitro, 10,11,28, 29 estudios histológicos en animales de experimentación, 12,14,15, 31 estudios en dientes humanos sanos que debían ser extraídos por razones ortodóncicas,16 o casos clínicos aislados 32-35 .
Por lo tanto, aún se requieren ensayos prospectivos en cohortes de pacientes controlados a distancia para obtener información más precisa acerca del comportamiento clínico del BDT en dientes con exposición pulpar y desarrollo radicular incompleto.
Dentro de las limitaciones del presente caso clínico, es posible sugerir que el BDT puede ser considerado como una valiosa alternativa, no solo para la conservación de la vitalidad pulpar, sino también para favorecer e inducir el desarrollo fisiológico del remanente radicular.















