2.1. Introducción
Debido a la gran cantidad de pacientes con patologías respiratorias crónicas y neuromusculares atendidos en el domicilio1, se ha desarrollado una amplia gama de dispositivos, que van desde los más simples que proporcionan solamente una presión positiva continua hasta aquellos que dan soporte ventilatorio con opciones múltiples de monitoreo y alarmas. Actualmente, estas máquinas son altamente sofisticadas y están diseñadas para satisfacer las necesidades de los pacientes no solamente en el hogar sino también en el hospital de manera invasiva o no invasiva, o para el transporte seguro de pacientes en estado crítico.
2.2. Clasificación de los generadores de flujo continuo y Ventiladores domiciliarios
Existe una confusión considerable sobre lo que realmente constituye un “ventilador” versus un “ge nerador de flujo continuo”. En términos generales, un ventilador soporta o asiste la fase inspiratoria del paciente, independientemente de su aplicación invasiva o no invasiva. Según el grado de asistencia inspiratoria requerida, o el tipo de soporte, los ventiladores poseen diversos modos espontáneos, con trolados y semi controlados (ver subtitulo 2.3.a Modos Ventilatorios). En cambio, un generador de flujo continuo domiciliario, comúnmente llamado “CPAP” (continuous positive airway pressure), por medio de una turbina, aplica presión positiva constante a lo largo de todo el ciclo respiratorio (fase inspiratoria y espiratoria) en un paciente que respira espontáneamente y no provee soporte inspiratorio.
2.2.1. Tipos de Generadores de Flujo contínuo
2.2.1.a. De presión fija: Generalmente este tipo de generadores son utilizados para el tratamiento del AOS. Requiere de la programación de la presión de tratamiento que se mantendrá constante en ambas fases del ciclo respiratorio (Figura 2.2.1a). Según el equipo utilizado, es posible programar manual mente un tiempo de rampa (el tiempo que tardará el dispositivo en llegar a la presión de tratamiento programada). Algunos equipos permiten elegir la forma automática de rampa (“Autorampa”) donde el equipo a través de ciertos algoritmos determina cuando es necesario iniciar el tratamiento. Además, la mayoría de los equipos modernos posee la función de “alivio de presión espiratoria”, para optimizar el confort en caso de requerimiento de alta presión de tratamiento

Figura 2.2.1 Gráficos esquemáticos de presión/tiempo, flujo/tiempo y volumen/tiempo según la forma de apli cación de presión positiva. a). Presión positiva continua en la vía aérea. Durante la inspiración y la espiración no hay cambios de presión (CPAP). b). Ajuste automático de la presión positiva (APAP), el incremento de la presión está dada según la respuesta del algoritmo del dispositivo a determinados eventos (por ejemplo, limitación al flujo, ronquido, apneas obstructivas). Al igual que a, durante el ciclo respiratorio del paciente, la presión permanece invariable. c). Aplicación de presión binivelada. El dispositivo aplica una presión positiva mayor durante la inspiración (IPAP) y una presión de menor magnitud durante la espiración (EPAP)
Así pues la programación de esos dispositivos es muy simple:
1. Como obligatorio ajusto una presión fija
2. Como opcional, 2 ajustes de confort, como la rampa y la función de alivio de presión espiratoria.
2.2.1.b. Dispositivos automáticos de presión continua (APAP = automatic positive airway pressure): Este dispositivo ajusta automáticamente la presión necesaria y son también utilizados para el trata miento de AOS. Los dispositivos automáticos poseen sensores incorporados y un microprocesador con algoritmos para analizar el patrón ventilatorio del paciente en tiempo real (por ejemplo, ciertos APAP monitorean la morfología de la onda flujo inspiratoria respiración a respiración). En términos generales, los objetivos del algoritmo de estos dispositivos son: 1) detectar eventos entre los ciclos respiratorios normales; 2) distinguir si un evento detectado es un artefacto (por ejemplo, tos, deglución, respiración bucal) o es verdaderamente un evento respiratorio anormal (por ejemplo, limitación al flujo, ronquidos o apnea); 3) evaluar las fugas de aire; y 4) decidir si el valor de la presión positiva aplicada debe man tenerse, aumentarse o reducirse, según el trastorno detectado o la magnitud de la obstrucción. De esta manera, el dispositivo automático es capaz de adaptar continuamente la presión de tratamiento aplicada a lo largo de toda la noche (Figura 2.2.1b). De todas maneras, es necesario evaluar cómo funciona cada dispositivo y sus algoritmos, dado que el rendimiento real de un APAP dependerá del grado de inteligencia de su algoritmo, más allá de su posibilidad de respuesta2-5. En estos dispositivos es posible programar un valor mínimo y un valor máximo de presión para limitar descenso o el incremento de la presión positiva continua6. Así pues, la programación de esos dispositivos es también muy simple:
1. Como obligatorio ajusto una presión mínima y máxima
2. Como opcional, 2 ajustes de confort, como la rampa y la función de alivio de presión espiratoria.
2.2.2. Tipos de Ventiladores Domiciliarios (VD)
Los VD son tecnológicamente más complejos que los dispositivos de presión 1fija ya que, además de aplicar dos presiones (inspiratoria y espiratoria), deben detectar correctamente la respiración del paciente para activar de forma sincronizada estas dos fases del ciclo ventilatorio (Figura 2.2.1c). Una característica importante para clasificar los VD, es el requerimiento de asistencia ventilatoria necesaria, de menos a más importante en horas de dependencia, ver Figura 2.2.3)
Hay que tener en cuenta, si el ventilador posee una válvula exhalatoria (transformando el sistema paciente-ventilador en un sistema cerrado) o si funciona de forma abierta con fugas intencionales (puertos exhalatorios en las tubuladuras o máscaras). El primer caso, suele asociarse con un mayor requerimiento de asistencia ventilatoria, un control más estricto de las variables del ventilador y un monitoreo más extenso y completo; el segundo diseño suele asociarse con un menor requerimiento de asistencia (usado a menudo en tratamientos no invasivos) y suele tener menos capacidad de monitori zación. Estas características han llevado clasificarlos como “ventilador de soporte de vida” a aquel que posee válvula exhalatoria y además de batería interna incorporada y se utilizará más de 16 horas al día) y “equipo/ventilador no soporte de vida” (también llamados de una manera simplificada “binivelado” al que trabaja con puertos exhalatorios, ver tabla 2.2.1. Entonces los equipos domiciliarios de ventilación a presión positiva pueden clasificarse en:
2.2.2.a. Ventiladores de soporte de vida: La nueva generación de ventiladores domiciliarios para soporte de vida combinan algunas características de los ventiladores binivelados con los ventiladores convencionales de las unidades de terapia intensiva (UTI), como sofisticados sistemas de alarmas y monitorización, batería interna, modos volumétricos, barométricos y modos no convencionales, amplio ajuste de las presiones inspiratorias y espiratorias. Una incorporación en este tipo de VD que hace a la característica de “ventilador de soporte de vida”, es la posibilidad de operar con circuito de doble rama y válvula exhalatoria incorporada en el equipo. La válvula exhalatoria puede ser una válvula simple que se cierra en el fin de la fase inspiratoria (una válvula de hongo o de diafragma), o una válvula de apertura proporcional. Normalmente, la válvula exhalatoria también controla la presión de la fase espiratoria (variable de base, ver 2.3.a. Modos Ventilatorios), que puede ser la presión atmosférica (0 cm H2O) o una presión positiva espiratoria llamada PEEP, también denominada EPAP. La válvula inspiratoria de un ventilador está destinada a controlar las fases del ciclo respiratorio, junto con la válvula espiratoria. En la mayoría de los VD, la válvula inspiratoria sólo tiene una función de cierre o apertura y la presión o el flujo dependen del sistema mecánico (por ejemplo, el pistón o la velocidad de rotación de la turbina). Es importante aclarar, que dependiendo el funcionamiento del VD, los fabri cantes cambiaran la será la terminología utilizada para denominar a la presión positiva inspiratoria, IPAP o PS (Presión de Soporte), y a la presión positiva espiratoria EPAP o PEEP. La IPAP es la presión aplicada durante la inspiración nominada desde el 0 de presión, mientras que la PS es esa misma pre sión durante la inspiración pero nominada desde el valor de PEEP. El valor de IPAP será equivalente a la presión total del sistema, mientras que en los respiradores que usen la nomenclatura de PS/PEEP, el valor de la PS será la presión total del sistema menos el valor de PEEP, ver Figura 2.2.2. Aun, son maneras diferentes de denominar las mismas cosas. Hay que estar muy atento para no confundirse (Gonzalez-Bermejo ERJ 2005)

Tabla 2.2.1 Comparación de ventiladores según de “ventilador de soporte de vida” o “ventilador binivelado”

Figura 2.2.2 Esquematización de la nomenclatura de la presión positiva inspiratoria y espiratoria. El término de “IPAP” corresponde a la presión positiva inspiratoria desde el valor de 0, por el contrario el término “PS” hace referencia a la presión inspiratoria aplicada desde el nivel de PEEP. La presión total ejercida sobre el paciente será el valor de IPAP o el valor de la PS + PEEP. (i: inspiración, e: espiración) según la nomenclatura del VD.
2.2.2.b. Equipos/ventiladores non soporte de vida: también denominados “dispositivos de asistencia respiratoria” o “binivelado” o “biPAP™” que es aún una marca , suelen tener circuitos de una sola rama, puerto de exhalación pasivo, menos alarmas y según el dispositivo, pueden tener o no una fre cuencia respiratoria (FR) de respaldo (los dispositivos que no tienen posibilidad de programación de FR de respaldo son usados generalmente para el tratamiento de AOS (no adherente al tratamiento convencional) o para el Síndrome de Hipoventilación-Obesidad (SHO). Todos estos dispositivos, deri van su nombre a su capacidad de dar soporte a la ventilación del paciente con dos niveles de presiones diferentes: una presión positiva inspiratoria en las vías respiratorias (IPAP, Inspiratory positive airway pressure) y una presión positiva espiratoria más baja (EPAP, expiratory positive airway pressure). Según el funcionamiento del equipo utilizado, tendrá grado variable de eficiencia en la compensación de fugas de aire. Son de fácil manejo, altamente transportables y con un sistema de monitorización básico, y de bajo costo. Usan tubuladura de rama única, llamados circuitos “ventilados” o “venteados” dado que no poseen una verdadera válvula espiratoria. La exhalación del aire espirado se realiza a través de los puertos de fuga intencional (puertos exhalatorios) presentes en el circuito o en la máscara (Ver subti tulo 2.3.b. Circuito Respiratorio). Estos dispositivos son capaces de proporcionar una gran cantidad de modalidades de ventilación, con la inclusión de “modos no convencionales” barométricos que aseguran volumen pudiendo cambiar dinámicamente medido en base a diferentes algoritmos.
2.2.2.c. Ventiladores no soporte de vida con batería: Estos ventiladores existen en algunos países, cuando el requerimiento de asistencia ventilatoria necesaria es mas de 12 horas pero menos de 16 horas.
Esta clasificación mencionada anteriormente sobre los VD se utiliza solamente en algunos países en donde se utiliza el rembolso monetario. Por este motivo y debido al avance tecnológico de los todos los VD es cada vez menos útil, dado que la gestión del VD debe estar determinada por las necesidades clínicas del paciente y la capacidad del satisfacción de las mismas por parte del dispositivo. Primero hay que evaluar las características clínicas y requerimientos de cada paciente para ver qué características debe tener el dispositivo a indicar para su tratamiento en domicilio, así como también es necesario recurrir a los manuales de los dispositivos para ver las indicaciones y contraindicaciones para su uso8.
Hoy en día, algunos enfermos pueden requerir VD mas de 16h/24, con puertos exhalatorios, así pues los más lógico es clasificar los equipos domiciliarios según los requerimientos en horas de utilización.
En términos generales, se puede resumir las formas de aplicación de presión positiva en la Figura 2.2.3 y podemos ver las características generales e indicaciones para el uso de presión positiva en la Figura 2.2.4.

Figura 2.2.4 Características generales e indicaciones para el uso de generadores de presión positiva.
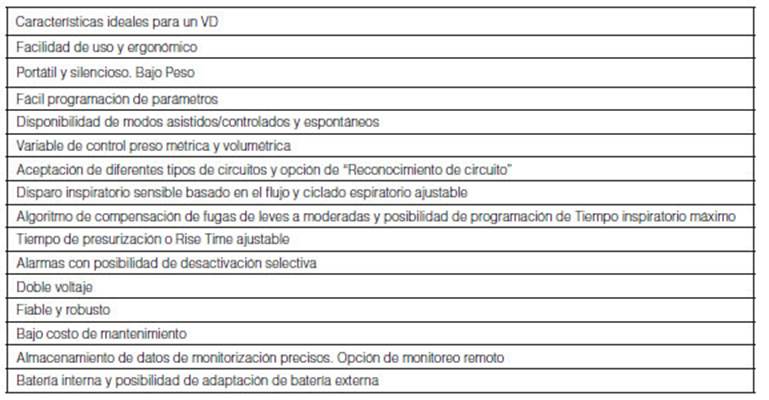
2.2.2.d Elección de Ventilador: La elección del VD debe depender tanto de la condición del paciente como de las características del dispositivo, incluyendo: 1) la situación clínica y el diagnóstico subyacen te (en particular, el grado de dependencia y movilidad del paciente); 2) la comodidad del paciente; 3) la versatilidad en función a la disponibilidad de diferentes modos ventilatorios; 4) el rendimiento del dispositivo; 5) los mecanismos de compensación de fugas; 6) la calidad y la precisión en el monitoreo (sincronía y detección de fugas no intencionales); y 7) la experiencia del equipo de profesionales tra tante. A su vez, los dispositivos deben ser sencillos y fáciles de manejar. De esta forma, debe tenerse en cuenta la ergonomía de los VD, ya que los beneficios derivados de un buen rendimiento a veces pueden ser superados por una interfaz de usuario confusa (ver 2.3.g Software de equipos, Interfaz de usuario). Los mecanismos de detección de fugas y las capacidades de compensación de las mismas, son cuestiones críticas que dictan la elección del ventilador, ya que determinan el rendimiento del dispositivo, sobre todo cuando se aplica VNI o en pacientes con traqueotomía que utilizan “ventilación a fuga” (cánula de traqueostomia sin balón de neumo taponamiento o con balón desinflado). Además, otro aspecto impor tante es cómo el dispositivo estima o mide el VT (Volumen Tidal), ya que es esencial para proporcionar el apoyo ventilatorio deseado, (2.3.f. Sistema de Alarmas y Monitoreo). Afortunadamente, casi todos los VD más nuevos funcionan tan bien como los ventiladores de la UTI y son capaces de satisfacer a altas demandas ventilatorias2. Las condiciones que debe cumplir un ventilador “ideal” se enumeran en la Tabla 2.2.2
2.3. Aspectos tecnológicos de los generadores de presión positiva
2.3.1. Modos ventilatorios:
Los modos ventilatorios presentes en los VD responden a las mismas variables de los modos ventilato rios de los ventiladores convencionales: 1) variable de control (flujo - volumen o presión), 2) Variable de disparo; 3) Variable de límite; 4) Variable de ciclado; y 4) variable de base
En el caso de los VD que permiten configurar diferentes tipos de circuitos, los modos disponibles variarán dependiendo del tipo de circuito elegido. Los VD poseen modos no convencionales, con algorit mos diversos y nombres determinados por los fabricantes, y es necesario consultar los manuales para entender su correcto funcionamiento9. A continuación, se describirán brevemente los modos conven cionales más frecuentemente encontrados en los VD:
2.3.1.1 Modalidad volumétrica: En este modo, el ventilador ofrece un volumen fijo durante un de terminado tiempo prefijado, generando la presión que sea necesaria para alcanzar dicho volumen, sin tener en cuenta la contribución del paciente en la ventilación. Así, la presión en las vías aéreas no es constante y es el resultado de la interacción entre los parámetros del ventilador, compliance (C), resis tencia del sistema respiratorio (R) y el esfuerzo inspiratorio espontáneo. Este modo puede ser denomi nado volumétrico o flujométrico. La ventaja de este modo es que ofrece al paciente de manera estricta el volumen predeterminado, en ausencia de fugas, sin importar la C ni la R. En contraposición, si el paciente cambia sus requerimientos, este modo no cambia su ofrecimiento de volumen, es decir si el paciente realiza mayor esfuerzo inspiratorio, este modo no ofrecerá mayor volumen, de allí el disconfort del paciente, otra desventaja importante es, su incapacidad para compensar las fugas. El uso de este modo está decreciendo en comparación con el modo controlado por presión, dada la comodidad para el paciente y la compensación de fugas que este modo ofrece. Para este modo es necesario ajustar como mínimo el VT y el tiempo inspiratorio (Ti).
2.3.1.2. Modalidad presurométrica: En este modo, el ventilador ofrece un flujo de aire al generar una presión positiva predefinida en un determinado tiempo. El flujo es variable, depende de la interacción entre la presión establecida, el esfuerzo espiratorio del paciente, las características del sistema respi ratorio y el tiempo inspiratorio. Las variaciones de flujos son determinadas por el análisis constante de la velocidad de flujo y de la presión en la vía aérea, así los esfuerzos del paciente serán compensados ciclo a ciclo ofreciendo mayor confort al paciente respecto al modo controlado por volumen otra ventaja es su capacidad para compensar las fugas12,13. Sin embargo, una desventaja teórica es que el volumen no está garantizado.
- Comparación entre modo a presión y a volumen:
2.3.1.3 Modos híbridos: Esta modalidad combina en teoría características de ventilación por presión y por volumen, de manera que el ventilador realiza una estimación de la presión necesaria para garan tizar un volumen fijado. Algunos ventiladores ajustan el volumen dentro de cada ciclo respiratorio14-16. Así, ciclo se inicia como con una presión limitada y si no se alcanza el volumen corriente establecido, se pasa a modalidad de flujo prolongando el tiempo inspiratorio, pero muchos ventiladores ajustan la presión durante varios ciclos para obtener el volumen prefijado difícil a controlar17-19. Este modo ha sido estudiado en pacientes con síndrome hipoventilación obesidad, hay estudios a favor de uso20 y otros donde no se demuestra diferencias21. Sin embargo, aún no está claro que este modo ventilatorio mejora la eficacia de la ventilación22, y la conclusión actual es que es un “gadget” difícil a controlar.
2.3.1.4 Definición de modos de control del ciclo: Este término se refiere a quien comanda la respi ración, y se ajusta dependiendo de la situación del paciente, así si el paciente está despierto, alerta y colaborador y puede iniciar la inspiración y espiración, se le puede proponer “libertad total” (Modo espontáneo) o “libertad condicional” (Modo espontáneo y controlado), si por el contrario se trata de un paciente sedado o sin control autónomo, será el ventilador que controla los ciclos respiratorios (Modo Controlado). A continuación se detallan las diferentes modalidades de ciclado.
a. Modo Espontáneo (S) y asistido (A)
En el modo espontáneo (S), el paciente controla el inicio y el fin de la inspiración, “disparando” el ventilador, para iniciar la inspiración, el ventilador ofrece la presión inspiratoria predetermina da23, manteniéndose durante el tiempo en el que el paciente produzca un flujo inspiratorio mínimo preestablecido, y finaliza cuando exista una caída de determinada de flujo (ciclado). Este modo no puede existir en volumen, porque en este caso, como se ha mencionado antes, es necesario tener un tiempo inspiratorio predeterminado. En el modo asistido el ventilador decide el tiempo inspiratorio (Ti) de la presión inspiratoria predeterminada que va a “disparar” el paciente. Lamentablemente también existen diferentes denominaciones según el fabricante: PS (Presión de soporte), AI (Ayuda inspiratoria), PSV (Pressure support Ventilation), S (Espontáneo) y PA (Presión asistida)
b. Modo totalmente Controlado (C) or Timed (T)”
Es también conocido como modo basado en Tiempo24-26 (modo T), el ventilador controla e impone el inicio y el fin de la inspiración y por lo tanto le Fr y el Ti, como consecuencia, inhibe o remplaza el centro respiratorio del paciente, quien sigue los parámetros impuestos por el ventilador. Con este modo, es el ventilador que realiza el trabajo respiratorio
Según los fabricantes se denomina en presión: PC (presión control), P (Presión), T (Timed); en vo lumen: VC (Volumen control), C (control).
c. Modo semi-controlado
Funciona como un modo asistido pero se controla el tiempo inspiratorio y una frecuencia de rescate. Con este fin existen 4 maneras de hacerlo:
1) Se puede fijar un Ti, de manera que es el enfermo el que dispara el ciclo, pero el Ti será impuesto por el ventilador. Este modo se llama clásicamente asistido/controlado
2) Se puede dejar libre el enfermo cuando dispara (como en modo espontaneo) y ajustar un Ti fijo cuando el ventilador está en Frecuencia de rescate
3) Se puede dejar libre el enfermo pero en una ventana de tiempo inspiratorio entre un Ti mínimo (Ti min) y un Ti máximo (Ti max) de manera que el paciente tiene una libertad como en modo asistido pero está delimitada en un rango (Ti min-Ti max). Algunos fabricantes denominan este modo S/T (spontaneous/timed), pero para otros fabricantes el modo S/T puede ser un modo combinado (ver más abajo).
4) Se puede controlar el Ti de 2 maneras combinadas: Cuando el enfermo dispara se puede dejar una ventana de tiempo inspiratorio entre un Ti mínimo (Ti min) y un Ti máximo (Ti max) y cuando el ventilador pasa a frecuencia de rescate, el Ti es fijo. Ver Figura 2.3.1.
Al igual que en el modo anterior, existen diferentes denominaciones según los fabricantes. En pre sión: PAC, P (A) CV, Assisted controlled pressure ventilation, PCV (A) pressure Control. En volumen se llamaran según los fabricantes: Ventilation (assited), VAC, V(A) CV, Assisted controlled Volumen ventilation, VCA, VCV (A) Volumen Control ventilation (assisted), recomendamos de no aprender las denominaciones pero fijarse en los parametrajes para entender lo que hace el ventilador
Para más información acerca de los modos convencionales, así como también de los modos no conven cionales propios de cada marca comercial se recomienda la lectura de los correspondientes manuales.
2.3.2. Circuito respiratorio
Tanto los generadores de flujo continuo como los VD, generan presión positiva en las vías respiratorias del paciente a través de un sistema de tubuladuras llamado circuito respiratorio. La parte distal del circuito respiratorio se conecta al paciente a través de una interfaz invasiva (cánula de traqueotomía) o no invasiva (máscara/pieza bucal). Existen tres tipos principales de circuitos posibles para los equipos domiciliarios:
- Circuito único/simple ventilado: Este circuito es utilizado por todos los generadores de flujo continuo y por algunos VD (generalmente equipos binivelados). Requiere de puertos de fuga intencional para permitir la salida del aire exhalado por el paciente. Estos puertos de fuga son conocidos como puertos exhalatorios pasivos y pueden encontrarse en el mismo circuito o en la máscara, ver Figura 2.3.2.1. Los circuitos de una sola tubuladura se conectan directamente a la interfaz del paciente (invasiva o no invasiva). Cuando se utiliza este circuito simple conectado a una cánula de traqueostomía es recomendable colocar una válvula de fuga en vez de un puerto exhalatorio, dado que la válvula de fuga además de permitir la salida del aire a través de los puertos tiene incorporada una válvula anti-asfixia.
- Circuito único/simple no ventilado: Es utilizado por los VD. Posee en la tubuladura una válvula ex halatoria por donde se elimina el aire exhalado. Durante la inspiración, la válvula se cierra, mientras que durante la espiración, a medida que la válvula se desinfla, se permite exhalar aire a través de ella. Por este motivo, esta válvula además de permitir la salida del aire, a menudo funciona como una válvula generadora de presión positiva al final de la espiración (PEEP/EPAP). Ver figura 2.3.2.1.
- Circuito doble: Este circuito también es exclusivo de algunos VD (ventiladores de soporte de vida). El circuito de doble tubuladura se compone de una rama inspiratoria y de una rama espiratoria cuyos extremos proximales están conectados a los puertos de salida inspiratoria y espiratoria del ventilador (donde se encuentran las válvulas inspiratoria y exhalatoria del VD), mientras que las extremidades distales están conectadas a una “pieza en Y”27 que permite la conexión con la interfaz del paciente (cánula de traqueostomía o pieza bucal/máscara no invasiva) (Figura 2.3.2.1).

Figura 2.3.2.1 Circuito Simple con puerto exhalatorio. a. VD con circuito simple con puerto de fuga en máscara (mascarilla ventilada, codo transparente). b. Circuito simple con puerto de fuga en la tubuladura y máscara no ventilada (codo azul sin puertos de fuga). En el caso de uso con traqueostomía debe utilizarse válvula de fuga en la tubuladura, que es un puerto de fuga con una válvula antiasfixia28,29incorporada.
Algunos VD proporcionan la compensación automática del volumen compresible y el cálculo de la impedancia del circuito, después de una maniobra de calibración. Esta función es un recurso ideal para mejorar la funcionalidad del VD sobre todo en términos de disparo inspiratorio30.

Figura 2.3.2.2: a. Circuito simple no ventilado (con válvula exhalatoria) a. con máscara sin puertos de fuga (máscara no ventilada, codo azul). b. con pieza bucal.
También muchos VD dan la opción de elegir entre configuraciones de circuitos para adultos y pe diátricos con diferentes calibres. Además, en algunos casos, un mismo VD puede ser configurado para admitir alguno de los 3 tipos de circuitos, solo dos, o simplemente dar la posibilidad de uso con un tipo de circuito.
2.3.2.a. Tipo de Circuito e interfaz y la reinhalación de CO2
Existe un potencial riesgo de reinhalación del Dióxido de carbono (CO2) del aire espirado según el circuito utilizado. Con los circuitos dobles o simples no ventilados (con válvula exhalatoria activa) el riesgo de reinhalar CO2 espirado es mínimo y estaría en relación solamente con el volumen de espacio muerto de la interfaz, pero aun así el impacto clínico es mínimo. Por el contrario, con los circuitos sim ples con puertos de fuga intencional, la reinhalación de CO2 dependerá de la cantidad de aire exhalado que quede dentro del circuito al momento de la siguiente inspiración. Estudios han demostrado que la posición del puerto exhalatorio influye en la reinhalación de CO2, obteniendo un lavado de CO2 más eficiente cuando la fuga se coloca en la máscara. Otro factor que interviene en el grado de reinhalación de manera inversamente proporcional es el valor de EPAP (a valores mayores de EPAP, menor es la reinhalación de CO2). Por este motivo, los nuevos dispositivos que utilizan rama simple con puertos de fuga, el valor mínimo posible de programación de EPAP es de 4 cm de H2O (para asegurar un lavado efectivo de CO2)31. Ver Figura 2.3.2.4)

Figura 2.3.2.4 (Imagen adaptada de Scala R, Naldi M. Ventilators for noninvasive ventilation to treat acute Respiratory failure. Respir Care. 2008 Aug; 53(8):1054-80). Con tubuladura simple no ventilada (presencia de válvula exhalatoria) o con la colocación de una válvula de plateau al circuito simple (en reemplazo de los puertos de fuga exhalatorios) los valores de reinhalación son mínimos. En cambio con una tubuladura simple con puertos exhalatorios pasivos (circuito ventilado la disminución signi ficativa de la reinhalación de CO2 se ve a partir de la colocación de 4 cm H2O de EPAP
2.3.3. Sistema de Compensación de fugas
La presencia de fugas no intencionales es una característica casi constante durante la VNI debido al tipo de interfaz utilizada. Sin embargo, en ciertas situaciones durante la ventilación invasiva en el domicilio a través de una cánula de traqueostomía, también existe la posibilidad de fugas no intencionales (por ejemplo, ventilación a fuga con balón desinflado, cánula con balón inflado pero pequeña en relación al tamaño del ostoma). Las fugas involuntarias excesivas están fuertemente correlacionadas con el fracaso de la VMD, debido a disconfort del paciente, asincronía paciente-ventilador o hipoventilación alveolar32,33. También, se asocia a mayores tasas de fracaso en el tratamiento de patologías respiratorias del sueño. Por consiguiente, es importante disponer de un dispositivo capaz de compensar adecuadamente las fugas de aire durante el tratamiento. La estimación del cálculo de las fugas intencionales y no intencionales por parte del ventilador, si es fiable, es una contribución útil a la monitorización de la VMD.
2.3.4. Fuente Generadora del Gas
La fuente generadora del gas puede ser: 1) un pistón o micropistones; o 2) una turbina. Las turbinas rápidas (“turbinas dinámicas”) que cambian de velocidad para alcanzar la presión preestablecida, y las turbinas que giran a velocidad constante (“turbinas constantes”) guiadas por una válvula proporcional, hacen que esta última generación de VD sea tan eficiente como los ventiladores de las unidades de cuidados intensivos (UCI) accionados por gas a alta presión34.
2.3.5. Fuente de O2 y Aire
Los ventiladores domiciliarios están provistos de un compresor o de una turbina alimentada eléctri camente para presurizar el aire ambiente y si es necesario un adicional de O2, solo tienen una entrada de oxígeno a baja presión (a través de un flujímetro de O2). Además, estos equipos, en su mayoría no tienen mezclador y entonces la FiO2 en estos casos, no es constante y está en relación con ciertas varia bles: 1) sitio de conexión del O2; 2) tipo y lugar del puerto exhalatorio y tipo de circuito (figura 2.2.1); 3) programación del ventilador (Tabla 2.3.5); 4) flujo de O2; 5) patrón respiratorio del paciente (VT); y 4) magnitud de la fuga35,36. En relación al puerto exhalatorio y la conexión del oxígeno, la misma tie ne que ser lo más distal posible al puerto exhalatorio. Los niveles de IPAP o la magnitud del esfuerzo inspiratorio del paciente afectan principalmente al VT. La variación del VT altera la FiO2, dado que a valores constantes de flujo de O2, el aumento del VT (ya sea por aumento del esfuerzo del paciente o por aumento de la IPAP) será a expensas de mayor cantidad de aire ambiente diluyendo la cantidad de O2 presente, disminuyendo la FiO2. Debido a la gran cantidad de variables que afectan la FiO2 (Tabla 2.3.6), algunos dispositivos dan la posibilidad de monitorearla a través de un sensor, así como también dan la opción de monitoreo de la oximetría de pulso del paciente.

Tabla 2.3.5 Adaptado de F. Thys, G. Liistro. Determinants of Fi O2 with oxygen supplementation during noninvasive two-level positive pressure ventilation, Eur Respir J 2002; 19: 653-657. Influencia de la IPAP en la fracción de oxígeno. Los valores son presentados en % de O2
2.3.6. Baterías
Todos los VD requieren energía eléctrica, ya sea como energía externa de corriente alterna o a través de una batería interna de corriente continua37.
- Batería interna: Todos los ventiladores de soporte de vida tienen una batería interna de larga duración (3-9 h), normalmente con un tiempo de carga corto. Sin embargo, la duración de la batería dependerá de la configuración de los parámetros, la impedancia del sistema respiratorio, las características del ventilador y su rendimiento difiere enormemente entre los diferentes VD. Esta batería solo tiene que ser una batería de seguridad y el enfermo no tiene que desplazarse solo son esta batería al exterior de su domicilio
- Batería Externa: Como alternativa, o además de las baterías internas, también es posible utilizar baterías externas que garantizan una autonomía prolongada del VD. Algunas baterías externas están incorporadas en el equipo, pero siendo amovibles, son consideradas como externas
2.3.7. Sistema de Alarmas y Monitoreo
La función del sistema de alarmas es alertar al profesional, cuidador o familiar, de un evento que requie ra una intervención. Al ajustar las alarmas del ventilador se debe asegurar que sólo funcionen cuando surja una necesidad genuina, en ocasiones pueden generar interpretaciones erróneas de los eventos. Estos eventos pueden ser técnicos (es decir, relacionados con el rendimiento del ventilador) o clínicos, debido a un cambio en el estado del paciente. Las nuevas generaciones de equipos binivelados y de soporte de vida están provistos de alarmas más sofisticadas (baja y alta presión, VT, FR, FiO2, fugas) y gráficos de monitoreo (curvas de flujo, VT y presión en tiempo) que pueden ser útiles en términos de seguridad y para mejorar la interacción paciente-ventilador38. Todos los VD deben tener alarmas, como se muestra en la Tabla 2.3.7

Figura 2.3.5 (Imagen adaptada de Scala R, Naldi M. Ventilators for noninvasive ventilation to treat acute Respiratory failure. Respir Care. 2008 Aug; 53(8):1054-80). Efecto de la ubicación y el tipo de puerto de fuga (puerto exhalatorio en la mascarilla, válvula Plateau o puerto exhalatorio en el circuito), el lugar de la inyección de O2 (conexión en la mascarilla o en el circuito) y el flujo de oxígeno (5 ó 10 L/min) en la concentración de oxígeno medida en un modelo pulmonar. La concentración de oxígeno es menor con el puerto de fuga en la mascarilla que con los otros dos puertos de exhalación. Por el contario, un puerto exhalatorio en la máscara con conexión de O2 en el circuito dará mayor FiO2, al igual que el puerto exhalatorio en la tubuladura con conexión de O2 en la máscara.
Existen valores predeterminados para los límites de alarma, más allá de los cuales se activará una alarma audible y/o un indicador visual. Estos valores deben establecerse de manera personalizada de acuerdo con la situación clínica del paciente, el modo ventilatorio, el tipo de interfaz y, si es posible, modificarse cuando estas condiciones cambien. Si el equipo es destinado a realizar VNI es aconsejable que disponga de alarmas de fugas no intencionales significativas.
Hay que tener cuidado con demasiadas alarmas. No estamos en cuidados intensivo, y demasiadas alarmas harán que no se utilizara el ventilador, o podrá introducir disconfort. Para el domicilio se aconseja, para un enfermo dependiente solo la alarma desconexión, y en caso de ventilación invasiva, alarma alta presión.
2.3.8. Telemonitoreo
En el ámbito de la medicina respiratoria, este método es una herramienta alternativa para el seguimien to cercano de los pacientes con asma, EPOC, SAOS y trasplante pulmonar, asegurando la transmisión oportuna de datos clínicos y fisiológicos y permitiendo la intervención médica de manera preventiva antes de que se produzcan cambios en las condiciones de los pacientes. En cuanto a pacientes con ELA, el se guimiento remoto mostró disminuir el costo de la internación en domicilio y estar en contacto frecuente con el medico de seguimiento para evacuar dudas de la ventilación no invasiva según el grupo de Pinto, De Almeida et al. Aunque a la fecha no existen estudios que muestren diferencias significativas en la supervivencia, ésta tiene una tendencia positiva para los pacientes seguidos a través de telemonito reo. Por lo tanto, las soluciones de telemonitoreo deben adaptarse cuidadosamente a la situación. Por el momento, se requiere una evaluación más detallada de las opciones de telemonitoreo y los grupos seleccionados de pacientes donde podría mejorar la supervivencia, antes de que puedan formularse recomendaciones generalizadas sobre la telemonitoreo.
2.4. Conclusiones
En la actualidad existe una amplia gama de dispositivos, con opciones múltiples de monitoreo y alar mas. La elección del dispositivo de presión positiva debe adaptarse al tipo de requerimiento según la gravedad del paciente y a la fisiopatología de la enfermedad respiratoria. Además en esta elección, debe tener en cuenta los costos y la experiencia del personal. El profesional tratante debe ser consciente de la diversidad de equipos de presión positiva y los accesorios correspondientes (tipo de interfaz, sistemas de exhalación, ajustes de presión) para asegurarse de estar brindando un correcto tratamiento al paciente.