El uso de mallas protésicas para las reparacio nes de la pared abdominal reduce drásticamente la tasa de recurrencias pero puede originar complicaciones como supuraciones crónicas y pseudoquistes.
Aquellas se presentan, generalmente, como colecciones que incluyen a la malla rodeada por “bio film” y no integrada a los tejidos, lo que explica el fraca so de la antibioticoterapia y la necesidad frecuente de retirar las prótesis.
Los pseudoquistes, por otra parte, son acumu laciones de líquido seroso estéril con una gruesa pared fibrótica que debe ser extirpada para garantizar la cu ración1.
Ambos cuadros tienen en común la presencia de una colección encapsulada por fibrosis exuberante como producto de la reacción inflamatoria desencade nada por la presencia de la prótesis2.
Presentamos una paciente de 75 años con antecedentes de EPOC e histerectomía por carcinoma de útero a los 45 años, que consultó por una masa ab dominal dolorosa de 6 meses de evolución asociada a astenia, hiporexia y reducción de peso no cuantificada.
Trece años antes se le había practicado, en otra institución, una operación de Dixon con colostomía de protección por recurrencia tumoral. Después de la re construcción del tránsito presentó una eventración que fue reparada con una malla de polipropileno y, durante el posoperatorio, una infección de la herida que se tra tó con desbridamiento y antibióticos.
El examen clínico reveló un tumor redondeado renitente e irreductible de aproximadamente 12 cm de diámetro ubicado por debajo de la cicatriz.
El laboratorio resultó normal. La ecografía de partes blandas mostró líquido encapsulado en el plano parietal rodeando una imagen sólida que se interpretó como material protésico; la tomografía computarizada (TC) confirmó la presencia de líquido, pero no permitió aclarar la imagen sólida (Fig. 1).
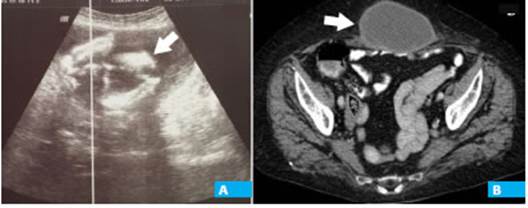
Figura 1 A: Ecografía que muestra colección líquida superficial e imagen sólida en su interior (flecha). B: Tomografía abdominal con contraste oral (corte transversal): gran colección líquida de la pared abdominal con pared gruesa (flecha).
Se abordó a través de una incisión losángica incluyendo la cicatriz; se halló marcado engrosamiento de la hoja anterior de la vaina de los músculos rectos que impresionaban atrofiados; al incidirla, se evacua ron 150 mL de líquido color ámbar, turbio, del cual se envió una muestra para examen bacteriológico.
La malla se encontraba plegada y libre en el plano preperitoneal, por lo que fue fácilmente extraída (Fig. 2). El lecho fue lavado y cureteado para eliminar los restos de “biofilm” y se colocó un catéter para ave namiento. La aponeurosis se cerró borde a borde con polipropileno 1.
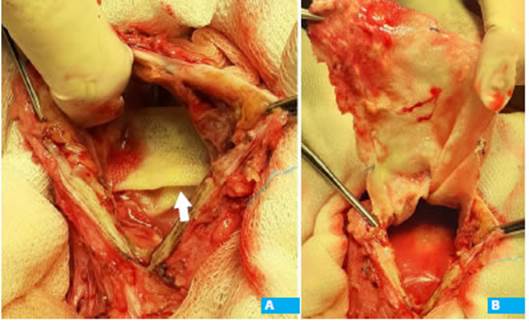
Figura 2 A: Vista operatoria: malla plegada en el plano preperitoneal (flecha). B: Vista operatoria: extracción de la prótesis y suturas de polipropileno.
El posoperatorio transcurrió sin incidentes y el catéter fue retirado 6 días después.
Se obtuvo desarrollo de estafilococo aureus sensible a trimetoprima-sufametoxazol, por lo que cumplió tratamiento oral durante 8 semanas.
La paciente experimentó buena evolución, con recuperación ponderal; la ecografía obtenida seis me ses después mostró integridad de la pared abdominal y escaso líquido laminar preperitoneal.
Durante las eventroplastias abiertas suele rea lizarse una disección amplia del plano subcutáneo que origina un proceso de curación extenso y prolongado en el tiempo por la producción sostenida de mediado res inflamatorios como reacción al material heterólogo. En ocasiones, el resultado es la producción de líquido y fibrosis densa que impide su reabsorción2. Las coleccio nes así formadas pueden seguir distintas evoluciones, a saber:
Reabsorción espontánea.
Formación de una cápsula y persistencia como pseu doquistes o seromas crónicos1.
Infección aguda, que suele responder al avenamiento asociado a tratamiento antibiótico.
Infección subclínica, de evolución lenta, que impide la integración completa de la malla y, meses o años después, se manifiesta como colección en torno a la prótesis3-5.
Creemos que gran parte de las infecciones cró nicas tienen su origen en complicaciones agudas de la herida: en una serie de 32 mallas removidas por infec ción, 16 pacientes habían sufrido seromas o infeccio nes posoperatorias aparentemente leves que fueron tratadas con antibióticos empíricos durante períodos cortos5. Otros autores han comunicado casos similares de infección crónica con prótesis no integradas a los te jidos: Aravind y Cook3 publicaron un seroma infectado gigante posterior a hernioplastia inguinal laparoscópica bilateral que comparte con nuestro caso la ubicación preperitoneal, la ausencia de cápsula propia y, como en el informe de Gukas y Massouh4, el hallazgo de la malla “flotando” en la colección.
En los pseudoquistes, por el contrario, las pró tesis se encontraron completamente integradas, a ex cepción del caso de Mantelou y col.6, quienes hallaron un “malloma” que fue extirpado en bloque con la pared del pseudoquiste.
En el caso presentado, los estudios por imáge nes nos orientaron hacia un pseudoquiste de la pared abdominal pero, a diferencia de la mayoría de los pu blicados, la colección no ocupaba el espacio supraa poneurótico sino el espacio preperitoneal y carecía de pared propia, ya que la “cápsula” dependía de la apo neurosis de los músculos rectos.
Nuestra paciente había presentado síntomas generales que podrían atribuirse a infección crónica, ya que remitieron después de la operación y el tratamien to con antibióticos. De haberse sospechado se habría intentado la evacuación percutánea de la colección y el tratamiento antibiótico guiado por el cultivo bacterio lógico, antes del abordaje quirúrgico. Probablemente, este hubiera resultado inevitable dada la falta de inte gración de la prótesis.
La TC dio información sobre las dimensiones de la colección y su ubicación superficial, pero fue la ecografía la que permitió sospechar la presencia de la malla plegada en su interior.
De acuerdo con Mayagoitía y col.1 creemos que ambos métodos son complementarios y no deben omi tirse, ya que la identificación preoperatoria de la próte sis no integrada permitiría distinguir los pseudoquistes de las infecciones crónicas de evolución solapada y pla nificar la cirugía con mayor certidumbre.











 texto en
texto en 


