Introducción
Los aneurismas de las arterias viscerales (AAV) tienen una frecuencia baja pero también difícil de estimar (0,1 a 2%), ya que las autopsias demuestran que su incidencia podría ser más alta de lo que se cree1,2. Sin embargo, los avances en diagnóstico por imágenes permiten encontrarlos cada vez con mayor frecuencia. Su hallazgo representa un desafío para el profesional, ya que muchas veces se dan en pacientes jóvenes, en su mayoría asintomáticos. A pesar de esto, hasta un 25% puede presentarse como rotura, la cual conlleva una alta mortalidad (hasta un 70%)1,3. Además, se describe en la literatura hasta un 20% de pacientes con múltiples AAV4.
Históricamente, los AAV han sido manejados con seguimiento clínico-imagenológico o con reparación quirúrgica abierta. Si bien las indicaciones de tratamiento no están estrictamente definidas, a lo largo de los años ha existido consenso entre la mayoría de los autores, sugiriendo intervenir a todos los de diámetro mayor de 2 cm, de crecimiento rápido, sintomáticos o rotos, o en mujeres en edad fértil1,4. En 2020, la Society for Vascular Surgery (SVS) publicó sus guías al respecto, estableciendo pautas y recomendaciones claras3.
En los últimos años, la terapia endovascular ha ganado terreno e incluso se considera como la primera opción en muchos casos, según las últimas recomendaciones2,3,5. Hoy en día, con el enorme arsenal disponible en técnicas endovasculares, es posible adaptarse a casi cualquier anatomía contando en muchos casos con tecnología cerebral como los diversores de flujo (DF) y coils de liberación por electrólisis (microcoils).
Nuestro objetivo fue describir la experiencia en el manejo endovascular de los AAV mediante diversas técnicas en un solo centro, con resultados a corto, mediano y largo plazo.
Materiales y métodos
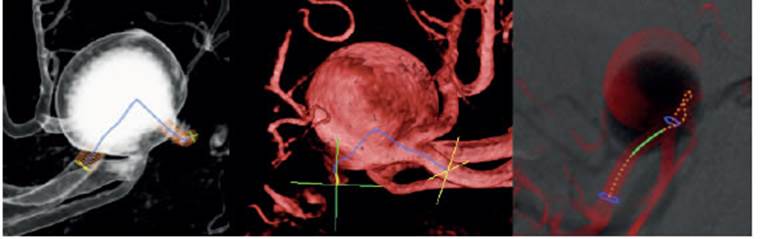
Se realizó una recolección retrospectiva de los pacientes tratados por AAV por vía endovascular en un solo centro (Clínica La Sagrada Familia, CABA, Argentina) entre mayo de 2010 y mayo de 2020. Solo se incluyeron aquellos pacientes con aneurismas verdaderos y seguimiento mínimo de 6 meses. No se incluyeron casos de aneurismas rotos, como tampoco pseudoaneurismas traumáticos, infecciosos o iatrogénicos. En todos los casos, el diagnóstico fue realizado por angiotomografía con reconstrucción 3D o angiorresonancia magnética, y la planificación preoperatoria se realizó mediante angiografía 3D (equipo monoplano Philips Allura Clarity FD20. 2012®) (Fig. 1)6.
Se analizaron datos clínico-demográficos como edad, sexo, hipertensión arterial (HTA), tabaquismo (TBQ), dislipemia (DLP), enfermedad coronaria (EC), anticoagulación oral e insuficiencia renal crónica (IRC). Los tratamientos empleados incluyeron DF, microcoils, combinación de ambos o stents cubiertos (SC). La decisión de emplear uno u otro se basó en aspectos técnicos y anatómicos, como diámetro de vaso, tortuosidad, longitud para cubrir y presencia de vasos colaterales, y asimismo en aspectos clínicos, como la urgencia del tratamiento (Fig. 2). Para diámetros pequeños y ante la necesidad de navegar por tortuosidades importantes, se optó por DF, como también para aquellos casos en los que una colateral importante nacía del segmento para cubrir con el dispositivo. La sola embolización con coils se reservó para casos de aneurismas saculares de cuello muy pequeño o bien para casos en los que la embolización definitiva del vaso era el plan. La combinación de stent no cubierto y coils fue utilizada en casos con un cuello más ancho, lo ya que el stent previene que los coils migren hacia la luz del vaso principal. Para casos en los que fuese deseada una exclusión más inmediata del aneurisma, con preservación de vaso, se optó por SC.
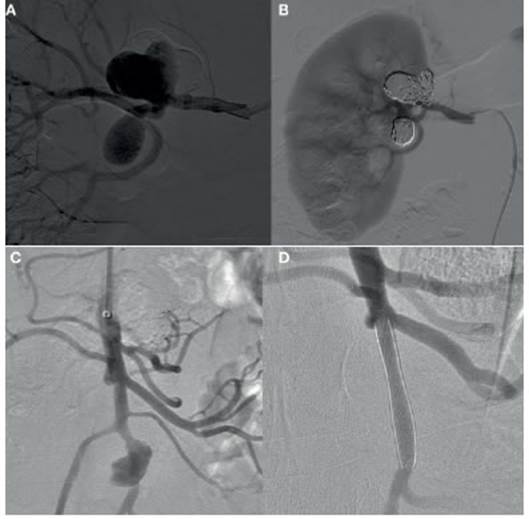
Figura 2 A y B: pretratamiento y postratamiento con microcoils de aneurismas renales. C y D: pretratamiento y postratamiento mediante DF de aneurisma de arteria mesentérica superior
El seguimiento se realizó mediante angiotomografía cuando fue posible, o de lo contrario mediante angiografía (por presencia de artefacto) a los 6 y 12 meses. Aquellos pacientes que recibieron algún tipo de stent fueron doblemente antiagregados (AAS 100 mg/ día y clopidogrel 75 mg /día en su mayoría) durante un mínimo de 6 meses y posteriormente solo AAS en forma indefinida. El trabajo fue aprobado por el Comité de Ética de la institución. Se definió como éxito técnico primario la confirmación angiográfica intraoperatoria de la exclusión completa del saco aneurismático, y, como éxito técnico secundario, la confirmación (por angiografía o angiotomografía) de la exclusión completa del saco aneurismático durante el seguimiento (posterior a la intervención primaria), sin ningún tipo de procedimiento adyuvante. La regresión del saco se definió como cualquier reducción registrada a lo largo del seguimiento con respecto al diámetro preoperatorio.
Para el análisis estadístico se utilizó como software Rstudio Team (2020)® (Rstudio: Integrated Development for R. Studio, PBC, Boston, MA). Las variables cuantitativas se expresaron como promedio y desvío estándar o rango, mientras que las cualitativas lo fueron mediante frecuencias y porcentajes. Las comparaciones entre grupos se analizaron mediante la prueba de la t de student o chi cuadrado, según correspondiera al tipo de variable. Se tomó como significativo un valor p < 0,05.
Resultados
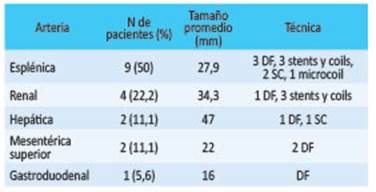
Durante el período de estudio, 22 pacientes se trataron en forma endovascular por AAV en nuestra institución. Cuatro (4) pacientes fueron excluidos por poseer un seguimiento menor de 6 meses. Por lo tanto, analizamos 19 procedimientos en 18 pacientes (9 hombres y 9 mujeres). El promedio de edad fue 61,9 ± 8,8 años (64,4 para los hombres y 59,4 para las mujeres), con un promedio de internación de 1,94 días y un promedio de tiempo de seguimiento de 40 meses. La arteria más comúnmente afectada fue la esplénica (n = 9, 50%); de estos casos, 5 fueron mujeres (55,6%). El tamaño preoperatorio promedio de los aneurismas fue de 30,1 ± 12,82 mm. La distribución de aneurismas, tamaños y técnicas empleadas se muestra en la tabla 1.
No hubo casos de mortalidad dentro de los primeros 30 días como tampoco casos de mortalidad relacionada con el aneurisma durante el período de seguimiento.
Dos pacientes debieron ser reintervenidos (11,1%). El primero fue un hombre con un aneurisma esplénico de 50 mm, quien ‒debido a una persistencia de llenado del saco‒ recibió al día siguiente una reparación quirúrgica mediante interposición protésica (dicha reintervención no fue analizada como procedimiento por no tratarse de una intervención endovascular). La segunda paciente fue una mujer con aneurisma esplénico de 46 mm, quien inicialmente recibió tratamiento mediante DF y microcoils. A los 58 meses se presentó con persistencia de llenado del saco y aumento de tamaño del 6,5%. Se trató mediante un SC, corroborándose exclusión completa del saco intraoperatoria y posterior seguimiento final de 8 meses (Fig. 3).
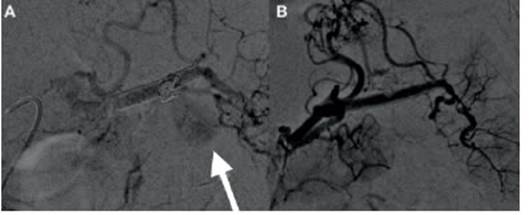
Figura 3 A: aneurisma esplénico tratado con DF y microcoils que continuaba permeable (flecha). B: reintervención mediante stent cubierto.
La estrategia más utilizada fue el DF (n = 9, 50%). Los tratamientos realizados se muestran en la tabla 2. Catorce (14) procedimientos se realizaron mediante acceso femoral, mientras que otros 5 lo fueron por vía humeral. Una sola paciente requirió una trombectomía humeral por una trombosis del sitio de punción, la cual resultó satisfactoria (5,3%).
El éxito técnico primario global fue del 38,4%, mientras que el éxito secundario fue del 47,4%, 68,4% y 94,7% a los 3, 6 y 12 meses, respectivamente. Sin embargo, el éxito técnico primario de los pacientes tratados con DF en comparación con el resto fue del 12,5% vs. 54,4% (p < 0,05). Asimismo, el éxito técnico secundario a 3, 6 y 12 meses fue, respectivamente, del 25%, 87,5% y 100% (pacientes tratados con DF) vs. 63,6%, 63,6% y 90,9% (demás tratamientos). Una sola paciente con aneurisma de la arteria gastroduodenal presentó una trombosis del stent a los 11 meses, asintomática, con una reducción del saco aneurismático del 31,3%. Esto arrojó una tasa de permeabilidad del 94,4% hacia el final del seguimiento. Tres (3) pacientes con aneurisma esplénico se trataron en el contexto de dolor abdominal inespecífico (26, 28 y 29 mm de diámetro): 2 de ellos fueron tratados mediante SC y el restante mediante embolización del saco con microcoils.
Solo una paciente presentó crecimiento del saco aneurismático (paciente que fue reintervenida), luego de lo cual el saco se mantuvo estable durante un seguimiento de 8 meses más. Trece (13) pacientes (72,2%) presentaron regresión del saco (en promedio del 16,5%), incluyendo 3 regresiones completas; mientras que en 4 el saco se mantuvo estable. El diámetro promedio de los sacos aneurismáticos al final del seguimiento fue de 23,4 mm (p = 0,02689).
Discusión
Según nuestro conocimiento, esta es la serie más grande de casos de AAV en una sola institución en la República Argentina hasta el momento. Nuestra casuística no dista de la publicada en el exterior7-10. Tanto Sessa como Cochennec publican 42 y 51 casos en períodos de 27 y 15 años, respectivamente7,9.
Nuestro enfoque diagnóstico y terapéutico se adecuó a las recomendaciones internacionales actuales, incluso teniendo en cuenta que estas fueron publicadas en 2020; por lo tanto, solo un paciente fue intervenido con posterioridad, mientras que los restantes lo hicieron antes de la publicación de las guías3. Orientándose exclusivamente por el tamaño recomendado por estas, 7 pacientes fueron tratados por fuera de las recomendaciones de la SVS. Esto representa un 42,1%, lo cual es una proporción significativa; sin embargo, 3 de ellos se presentaron con dolor abdominal inespecífico difícilmente atribuible a otra causa en particular (indicación de tratamiento), el cual se resolvió por completo en todos los casos. Otros 2 casos correspondieron a pacientes mujeres con deseos de maternidad y portadoras de aneurismas esplénicos (lo cual impulsó al tratamiento). Por lo tanto, quedarían solamente 2 pacientes tratados por fuera de las recomendaciones (10,5%). Como ya mencionamos, no incluimos pseudoaneurismas. El motivo de esta decisión fue que la tasa de rotura en casos de pseudoaneurismas no solo es significativamente mayor, sino también afecta a otra población ya que esencialmente se trata de otra patología5,11,12.
Nuestra tasa de reintervención también fue similar a la de otras series5,7. Cabe mencionar que nuestro único caso de conversión a cirugía abierta fue el primero de la serie, lo cual perfectamente pudo haber influido en la toma de decisión. Creemos que, de darse la misma situación con la experiencia y tecnología con las que contamos en la actualidad, tanto la decisión como el resultado podrían ser distintos. Lo que hemos encontrado interesante y creemos novedoso es la utilización de DF en este tipo de aneurismas, lo cual se distingue de la mayoría de las publicaciones sobre el tema. Las diferencias que observamos en cuanto al éxito técnico primario entre los DF y las demás técnicas son perfectamente explicables por el mecanismo de acción de este tipo de dispositivos. Este básicamente consiste en, mediante la mecánica de fluidos, disminuir o eliminar el flujo aneurismático y restaurar el flujo arterial normal13. Su principal utilización se destina a aneurismas cerebrales, y numerosas publicaciones de renombre proponen el uso de DF como primera alternativa, especialmente en aneurismas pequeños y no complicados, justamente debido al riesgo de rotura postratamiento que existe particularmente en aneurismas gigantes14,15 Es cierto que el porcentaje de éxito técnico primario en los pacientes en quienes no se utilizó un DF también fue bajo (54,4%). Sin embargo, es importante señalar que la mayoría de estos pacientes fueron tratados mediante stents no cubiertos y microcoils, lo cual muchas veces tampoco logra una exclusión intraoperatoria del saco. También es importante mencionar que no somos partidarios de embolización del vaso principal, ya que preferimos preservarlo siempre que sea posible, si bien ‒de tener que hacerlo, dependiendo del vaso por ocluir‒ muchas veces no hay repercusión clínica. Es por esto que nosotros preferimos, tal como sugiere Lagana, utilizar otras técnicas como SC o embolización con coils para casos de AAV sintomáticos, rotos o pseudoaneurismas (si bien estos no fueron incluidos en el trabajo), o incluso aneurismas de gran tamaño, ya que de esa manera se consigue una exclusión inmediata del saco, reservando otras técnicas para casos electivos. Sin embargo, algunos pacientes no son candidatos para el uso de DF debido a que poseen limitaciones anatómicas y técnicas referidas a perfil y navegabilidad5. El uso de stents cubiertos en AAV se describió por primera vez a principios del presente siglo16,17. La gran ventaja que ofrecen los DF se atribuye a su enorme versatilidad anatómica (diámetros pequeños, longitudes cortas, adaptabilidad a gran tortuosidad y bajo perfil), lo cual los convierte en una opción muy atractiva, incluso en ocasiones como la única opción viable. Cabe remarcar que ‒a pesar de la demora en la trombosis del saco‒ solo una paciente requirió reintervención por este motivo, por lo cual puede decirse que tuvo mínima repercusión clínica. Sumada a esto, la aplicación en el tratamiento de AAV de otros aspectos técnicos utilizados para el tratamiento de aneurismas cerebrales, como utilización de angiografías 3D, microguías, microcatéteres y coils de liberación por electrólisis, nos ha resultado de enorme utilidad.
Algunas publicaciones hablan de reperfusión tardía del saco aneurismático de hasta un 5%, pero nosotros no tuvimos casos de esto7. Si bien asumimos que nuestro caso de reintervención tardía se trató de un saco que nunca llegó a trombosarse en forma primaria debido a que no hubo en ningún momento una tomografía que lo evidenciara, tampoco podemos descartar que haya sido un caso de reperfusión dado que la reintervención se produjo casi 5 años después del procedimiento inicial, y las imágenes previas a esto abarcaron solo hasta el primer año. Otros autores informan tasas de trombosis de stent similares a las nuestras, sin repercusión clínica12.
Este trabajo tiene como limitaciones su diseño retrospectivo y, siello bien tuvimos un adecuado seguimiento, lo cual permitió hacer un análisis apropiado de los sacos aneurismáticos (40 meses), de algunos pacientes no contábamos con imágenes intermedias (solo preoperatorio y luego seguimiento alejado). Esto no nos permitió analizar más en detalle casos de reperfusión del saco. Por otra parte, es prometedor que ‒a pesar de no tener un seguimiento anual‒ la tasa de reintervención haya sido baja y la mortalidad asociada nula, especialmente teniendo en cuenta que muchos de estos pacientes son jóvenes y la radiación puede significar un problema a largo plazo. En segundo lugar, creemos que sería interesante analizar las distintas estrategias en escenarios clínicos diferentes, como electivos versus urgencias, y analizar resultados, pero consideramos que para esto aún necesitamos incrementar la casuística.
El tratamiento endovascular de los AAV es seguro y eficaz. Pero es menester contar con la tecnología adecuada, tanto para la planificación preoperatoria como para el tratamiento. La técnica por emplear debe adaptarse no solo a la anatomía sino también al contexto clínico.











 texto en
texto en