PUNTOS CLAVE
• Desde el primer caso de COVID-19 comunicado hasta ahora, las evidencias sobre la prevención y manejo epidemiológico del SARS-Cov-2 sufrieron cambios fre cuentes y claras diferencias entre organismos naciona les e internacionales, lo que generó cierta confusión e incertidumbre.
• El objetivo del presente documento es actualizar según la mejor evidencia disponible, el manejo de algunos tópicos con alto impacto en los Programas de Control de Infecciones, que resultan controvertidos:
• Indicaciones del uso de máscara/barbijo N95, uso pro longado, reúso y métodos seguros de decontaminación
• Criterios seguros para discontinuar el aislamiento en pacientes COVID-19.
• Consideraciones sobre reinfección por SARS-CoV-2. Puntos a tener en cuenta.
• Utilidad de la determinación de anticuerpos para SARS-CoV-2 en diferentes situaciones.
La pandemia de COVID-19 (SARS-CoV-2) produjo un impacto en la salud pública y la economía mundial. Desde el primer caso reportado hasta fecha, la evidencia sobre la prevención y manejo epidemiológico se modificó con claras diferencias entre organismos como la Organización Mundial de la Salud (OMS), Center Disease Control (CDC) o European Center Disease Control (ECDC).
En Argentina hemos adaptado numerosas estrategias con bajos niveles de evidencia que se implementaron se gún sitio geográfico y directivas locales y/o del Ministerio de Salud de la Nación (MSN). Los cambios periódicos de protocolo, conforme a la aparición de las publicaciones con diferente grado de evidencia científica generaron confusión -en ciertas situaciones- acerca de cuál sería la mejor recomendación. El objetivo de este documento es actualizar, según la evidencia disponible, el manejo de algunos tópicos controversiales con alto impacto en los Programas de Control de Infecciones y la atención diaria de los pacientes tales como: el uso rutinario de barbijo N95 para la atención de pacientes sospechosos o confirmados de COVID-19, reúso limitado y métodos de decontaminación de máscaras/barbijos N95, des-aislamiento de pacientes COVID positivos, necesidad de control por PCR en casos confirmados, la posibilidad de reinfección y rol de la medición de anticuerpos.
Resultados de la revisión
1) ¿Se requiere el uso de máscara/barbijo N95 para el cuidado rutinario de los pacientes sospechosos o confir mados de COVID-19? Respuesta: No.
Diversas publicaciones cuestionan los conceptos que brindaron organismos de referencia tales como la OMS o el CDC con relación al mecanismo de transmisión del virus SARS-CoV-2 y el rol de los diferentes tipos de más caras como parte integrante del equipo de protección personal (EPP) en el personal de la salud1-3. Desde el inicio de la pandemia, se adjudicó a este virus la transmi sión por gotas y transmisión por aerosoles, solo en situa ciones que favorecen dicho proceso (ej. aspiración de secreciones). Es por ello, la justificación de la normativa en los diferentes escenarios, del uso del barbijo quirúrgi co en el primer caso y del tipo N95 en el segundo, siem pre asociado a las medidas de aislamiento de contacto. Recientemente un grupo de especialistas emitieron un comunicado acerca de la necesidad de replantear las vías de transmisión viral4. Varios estudios compararon la efi ciencia de ambos tipos de máscaras durante la pandemia de H1N1, cuyos resultados fueron fuente de directivas frente al COVID-195,6. La evidencia actual sugiere que este virus, a diferencia del SARS-CoV-1 posee un mayor R0, que explica un mecanismo de transmisibilidad más eficiente7. Según el CDC, se transmite de persona a per sona de manera más eficiente que la influenza, pero no al punto de como lo hace el sarampión8. Sabemos que una proporción significativa de infecciones por SARS-CoV-2 (se estima que 40-45%) transcurren en pacientes asinto máticos y el virus puede ser transmitido de una persona a otra, en esta condición9. Por el contrario, si el SARS-CoV-2 se propagara principalmente a través de la transmisión por aerosoles, como el sarampión, se hubiera esperado observar una propagación global de la infección conside rablemente más rápida a principios de la pandemia, y porcentajes más altos de infección previa medida por encuestas serológicas. Algunos datos disponibles indican que el SARS-CoV-2 se ha propagado principalmente, como la mayoría de los otros virus respiratorios comunes, a través de la transmisión por gotas. La transmisión por aerosoles se produce a través de la vehiculización del microorganismo en el núcleo de partículas menores a 0.5 μm, capaces de quedar suspendidas en el aire más allá de 1.8 m, contrariamente, la transmisión por gotas en partículas mayores a 0.5 μm, caen por su propio peso antes de la distancia mencionada. No obstante, hemos aprendido a lo largo de estos meses que también debería mos incorporar otras variables en esta definición, como el distanciamiento, la acción realizada y la ventilación. En ciertas situaciones se describen contagios de SARS-CoV-2 de persona a persona a través de aerosoles, en ambien tes poco ventilados, y mientras el individuo infectado cantaba o gritaba (acciones de mayor potencialidad de transmisión). Es decir, la transmisión viral depende de múltiples factores tales como: características de vehicu lización, distanciamiento entre personas, ventilación del lugar, equipo de protección, entre otras7,10,11. Las enfer medades que se propagan de manera eficiente a través de la transmisión por aerosoles tienden a tener altas tasas de ataque, dado que infectan a muchos individuos en un corto período de tiempo. Recientes investigaciones pro mueven el concepto de que no hay una única y absoluta vía de transmisión posible de los microorganismos, sino que se establece un predominio de una sobre las otras. Esta situación ocurriría también con el SARS-Cov-25. La transmisión viral depende de múltiples factores tales como: características de vehiculización, distanciamiento entre personas, ventilación del lugar, equipo de protec ción, entre otras12. La evidencia actual demuestra que la transmisión del virus se realiza de persona a persona principalmente por vía respiratoria por gotas (sin protec ción ni distanciamiento pertinente), contacto de superficies contaminadas y por fomites13,14. En el personal de la salud, la mayor experiencia recogida en relación a la transmisión del SARS -Cov2 surge de sus antecesores (SARS, MERS) y del impacto del H1N1 en la pandemia del año 200915. Hasta la fecha, ningún estudio ha podido encontrar SARS-CoV-2 viable en muestras de aire. Inclu so si así ocurriese, sería necesario demostrar que el SARS-CoV-2 es competente, tanto para la replicación como para la infección, en el contexto de entornos de atención médica donde el EPP se usa de manera apro piada, junto con higiene de manos, para considerar que la transmisión aérea representa un modo importante de transmisión. Varios de los estudios publicados que ava larían la transmisión por aerosoles, se realizaron en condiciones de laboratorio, por lo cual se requieren más estudios para aceptar de manera acabada esta teoría10,16-19. Es probable que se produzca la transmisión por aerosol del SARS-CoV-2, pero según los datos epidemio lógicos actuales, no parece ser la vía principal de trans misión. El número reproductivo de SARS-CoV-2 es aproximadamente 2.5, (similar a la influenza); en contas te, el número reproductivo de sarampión (transmisión por aerosoles) es 18. El inóculo viral necesario para estable cer la infección por SARS-CoV-2 parece ser mucho mayor que el del sarampión. La tasa de ataque secunda rio sintomático del SARS-CoV-2 en los hogares, en los estudios publicados, ha oscilado entre 4.6% y 17.1% y esto es poco consistente con la transmisión aérea18. Di versas publicaciones concluyeron que el SARS-CoV-2 no se transmite -principalmente- por aerosoles y que las medidas básicas de control de infecciones, incluido el uso de barbijo, (guantes, camisolín, máscara facial/antipa rras), higiene de las manos y del medio ambiente, son adecuadas para prevenir la transmisión nosocomial del SARS-CoV-216,20-22. Una publicación no encontró diferen cias en el tasa de infección, comparando la utilización de ambos tipos de máscara/barbijo y le da más peso -como factor que disminuye la transmisión del virus-, al recambio de aire ambiental en situaciones de aerosolización23. Otros estudios promueven el uso de máscaras/barbijos de alta eficiencia en situaciones de ventilación inadecuada, in dependientemente de enfrentar maniobras de aerosoli zación24. Distintas sociedades científicas, y organismos como CDC y OMS, proponen el mantenimiento de los distintos escenarios para el uso de los diferentes tipos de máscaras/ barbijos. El N95 o equivalente, en lugar de un barbijo quirúrgico, se recomienda para los siguientes escenarios: a) Procedimientos que generan aerosoles y b) Procedimientos quirúrgicos que podrían presentar un mayor riesgo de transmisión si el paciente tiene COVID-19 (generan aerosoles o cirugías que involucran regiones anatómicas donde las cargas virales pueden ser más altas, como la nariz y la garganta, la orofaringe, el tracto respiratorio, etc.)18,22,25-27. Se debe tener presente que los respiradores con válvulas de exhalación no se recomien dan si no poseen filtro, o bien un barbijo quirúrgico sobre ellos, y no deben usarse durante los procedimientos quirúrgicos, ya que el aire exhalado sin filtrar comprome tería el campo estéril. En resumen, el riesgo de infección probablemente dependa de múltiples factores, incluidos: la duración de la exposición, las comorbilidades del paciente, ventilación y tamaño del inóculo viral. Si bien la experiencia mundial con el SARS-CoV-2 hasta ahora indica que la transmisión por gotas es el mecanismo principal de propagación de la enfermedad18, continúa la incertidumbre sobre su transmisión aérea, especialmen te por el riesgo que implica para los trabajadores de la salud9. No obstante, el CDC establece que la posibilidad de que la transmisión del virus no sea por gota, se puede identificar en tres escenarios: a) espacios cerrados, ven tilación inadecuada, exposición prolongada11. La efectivi dad del EPP depende de su disponibilidad, la capacitación adecuada del personal, el estricto cumplimiento de la higiene de manos, complementado con los controles ambientales físicos adecuados. Se requiere mayor inves tigación para responder a todos los interrogantes16,28,29. Se necesitan más estudios para ampliar las situaciones descriptas como “aerosolización” más allá de los procesos invasivos sobre el paciente, donde la ventilación del sitio juega un rol importante para disminuir la capacidad de transmisión30.
2. ¿Se puede hacer un uso prolongado y/o reúso del barbijo N95? Respuesta: Sí.
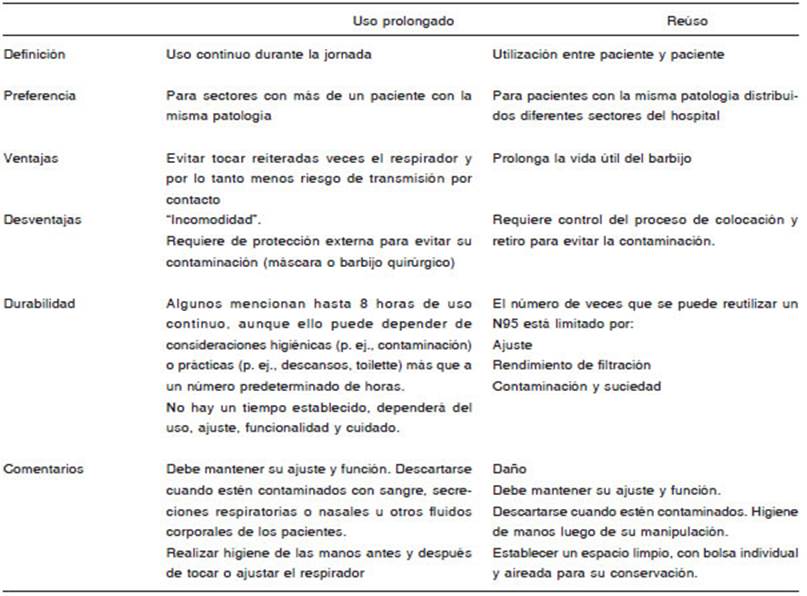
El uso prolongado hace referencia a su utilización en la atención de cohortes de pacientes, es decir, aquellos infectados por el mismo microorganismo e internados en la misma área, sin quitarse el mismo entre paciente y paciente. El reúso se refiere a usar la misma máscara/ barbijo N95 para atender varios pacientes, pero retirado y guardado entre la atención de cada paciente31 (Tabla 1). Las máscaras/barbijos N95 están diseñados para un solo uso, pero pueden reutilizarse en situaciones críticas como la experimentada en esta pandemia32. No obstante, su rendimiento disminuye a medida que aumenta el número de horas y modalidad de reúso. Durante los períodos de mayor demanda de atención médica y cuidados del personal de la salud, se sugiere optimizar su utilización reservándolo para procedimientos generadores de aero soles (PGA); utilizar máscaras faciales o barbijo quirúr gico cubriendo el barbijo N95 para evitar su deterioro; proponer el uso prolongado para el personal asignado a actividades específicas que utilizará el mismo barbijo N95 durante el turno en el cual se lleve a cabo la misma acti vidad; estrategias de reúso limitado y decontaminación33. Como describen Kobayashi y col., cada país ha puesto en práctica su propia recomendación, observándose ciertas discrepancias33. La Food and Drug Administration (FDA) y el CDC, sugieren una duración máxima de uso continuo que depende del lugar de trabajo -en relación al tipo de actividades que se desarrollen-, consideraciones higiénicas (por ejemplo, contaminación) o prácticas (por ejemplo, necesidad de usar el baño, los descansos para comer, etc.). No hay un número predeterminado de tiempo de uso continuo. Los barbijos N95 visiblemente contami nados con sangre, secreciones respiratorias o nasales u otros fluidos corporales, dañados (por ejemplo, correas rotas, pieza nasal rota), deformados o que no puedan aprobar una verificación de ajuste, deben desecharse32. Asimismo, se recomienda utilizar protector facial pasible de ser desinfectado para proteger el barbijo, colgar los barbijos usados en un área de almacenamiento designada o mantenerlos en un lugar limpio con un recipiente que no condense la humedad, como una bolsa de papel, entre usos (para que no se toquen el uno al otro). E l número de usos se puede limitar a no más de cinco, por dispositivo, según los cambios en el ajuste del barbijo, entendiendo que es posible que algunos modelos se puedan colocar más de cinco veces sin perder el ajuste31,32,34. Si bien en Argentina no existen recomendaciones desde organismos oficiales (ANMAT, Ministerio de Salud de la Nación), la Sociedad Argentina de Infectología elaboró un documento donde avala el uso extendido y reúso de barbijos N95 como una estrategia aceptable para cubrir la demanda frente a la pandemia35.
La decisión de implementar políticas que permitan el uso prolongado y/o la reutilización limitada de las más caras/barbijos N95 deben tomarla los profesionales del Servicio / Comité de Control de Infecciones y Seguridad e Higiene, bajo el marco de las recomendaciones existen tes. Se deben considerar los mecanismos de transmisión de la infección según el riesgo en la exposición (por ej. procedimientos generadores de aerosoles), cantidad de máscaras/barbijos N95 disponibles, calidad de los mismos, índice actual de uso y situación epidemiológica local. El objetivo es disponer de insumos adecuados y seguros para satisfacer la demanda durante la pande mia. Los centros de salud deben disponer de protocolos internos para aconsejar al personal que deseche cualquier máscara/barbijos N95 que esté dañada, sucia o que ge nere dificultad para respirar. En una misma institución se pueden implementar ambas estrategias dependiendo de las características edilicias donde se ubican los pacientes y las tareas específicas de cada sector. El CDC también sugiere otra estrategia de reúso que implica entregar cinco barbijos N95 a cada miembro del personal de salud, utilizando un barbijo para cada día, conservándolo en un recipiente que no condense la humedad al final de cada turno. El objetivo es reducir el riesgo de transferencia por contacto de patógenos del N95 al usuario durante la reutilización. Esta estrategia ofrecería el tiempo necesa rio para la pérdida de la viabilidad del microorganismo, durante el almacenamiento32.
3. ¿Es seguro realizar decontaminación de barbijos N95? Respuesta: Sí.
La decontaminación es un proceso para reducir la cantidad de patógenos en los barbijos N95, antes de reutilizarlos. Se emplea para limitar el riesgo de autoino culación. Para que sea aplicable en entornos sanitarios, el método de decontaminación debe eliminar las partículas virales, ser inocuo para el usuario, y no dañar su estructura ni propiedades originales. La decontaminación del N95 es una estrategia disponible durante una situación de crisis de disponibilidad. Es fundamental contar en la institución, de un protocolo riguroso para implementarla. Se consi dera un método efectivo para la decontaminación y la reutilización de los máscaras/barbijos N95, la que tenga en cuenta los siguientes elementos: a) el método debe inactivar los organismos contaminantes; b) no debe com prometer la estructura (posibilidad de ajuste adecuado), ni las propiedades (capacidad de filtración), c) no debe dejar residuos químicos que puedan ser nocivos para el usuario33. Asimismo, los barbijos son personales y deben estar identificados. El usuario debe respetar medidas generales al utilizar un N95 de contaminado: a) el barbijo debe ser inspeccionado visualmente antes de colocarlo y debe ser desechado en caso de que algún componen te parezca degradado o estructuralmente modificado; b) practicar una estricta higiene de las manos antes y después de su utilización, c) uso de guantes, d) solo debe tocarse la parte externa del barbijo; d) desechar el barbi jo, si la comprobación de ajuste falla33. Los métodos de decontaminación deben evaluarse para cada modelo de barbijo N95, revisando las medidas de manera continua según la disponibilidad del tipo de dispositivo vigente en el programa de protección respiratoria de la institución.
Dentro de los métodos de decontaminación en diferen tes países se mencionan: calor seco en estufa a 65-70° C (Alemania); vapor de peróxido de hidrógeno (Países Bajos, Europa y EE.UU.); irradiación germicida ultravioleta y calor húmedo (Europa y EE.UU.). La duración máxima de uso prolongado osciló entre 4 horas (Francia, Nueva Zelanda y Suecia) y 40 horas (México), y el número máximo de ciclos de de contaminación osciló entre 2 (Ale mania) y 5 (EE.UU.)33. Un estudio reveló que el peróxido de hidrógeno en fase de vapor (VHP) era eficaz para decontaminar los barbijos N95 de un organismo único en múltiples ciclos de decontaminación. El respirador mantu vo su función hasta después de 10-20 ciclos del VHP, pero a continuación presentaba signos de degradación36. Los estudios de decontaminación donde se utilizó VHP para el SARS-CoV-2 demostraron que no se recuperó ningún virus SARS-CoV-2 en el barbijo N95 y que se mantuvo la integridad estructural y funcional durante 10 ciclos de es terilización36. La National Institute for Occupational Safety and Health (NIOSH) reportó que la irradiación germicida ultravioleta, el VHP y el calor húmedo han mostrado ser los métodos más prometedores como métodos poten ciales para descontaminar las máscaras/barbijos N9532. Los métodos para la decontaminación y la reutilización de barbijos N95 se consideran solo como excepcionales y como un último recurso ante la escasez de suministros de estos elementos.
4. ¿Se debe medir la eficacia de la máscara/ barbijo N95 luego de la decontaminación? Respuesta: Sí.
Los empleadores deben poder demostrar la eficacia de cualquier método de decontaminación utilizado contra patógenos de interés, incluido el SARS-CoV-2. También deben asegurarse que los métodos de decontaminación utilizados no produzcan peligros adicionales para la seguridad (por ejemplo, arcos eléctricos resultantes de colocar el barbijo con partes metálicas en microondas), o que los trabajadores estén adecuadamente protegidos contra esos peligros a través de controles administrativos y de ingeniería apropiados, prácticas de trabajo seguras y equipo de protección personal32. La NIOSH ha evaluado el rendimiento de filtración y ajuste de algunos modelos de barbijos N95 utilizando una variedad de métodos de decontaminación37. Estas evaluaciones se realizaron en respiradores nuevos y sin usar que habían sido decon taminados. Para evaluar eficacia, se requiere de datos relacionados con el proceso de decontaminación, el uso de barbijos N95 y el seguimiento de cualquier reacción adversa como irritación de la piel, cefalea y dificultad ven tilatoria. Se deben incluir tres ciclos de decontaminación para cada barbijo, según modelo y técnica, y muestreo de respiradores de contaminados para medir la eficiencia de filtración y el rendimiento de ajuste32.
5. ¿Puede ser seguro desaislar a un paciente COVID-19? Respuesta: Sí.
La decisión de discontinuar las precauciones basadas en la transmisión para pacientes con infección confirmada por SARS-CoV-2, debe hacerse utilizando una estrategia basada en los síntomas. El período de tiempo depende de la gravedad de la enfermedad y de la presencia o no de inmunosupresión38. Tempranamente en la pandemia, tanto CDC como la OMS abogaron por finalizar el aisla miento con una estrategia basada en la prueba de PCR. Se sugería que los pacientes contaran con defervescencia sin antitérmicos, mejoría del cuadro clínico y 2 pruebas de PCR consecutivas negativas separadas por al menos 24 h38. Esta estrategia tuvo un gran impacto en los sis temas de salud, pues se observó rápidamente que los pacientes, con frecuencia, presentaban PCR positivas luego de resultados negativos, o aun persistentemente positiva por tiempo prolongado en ausencia de síntomas. Asimismo, en esta etapa se sugería mantener el aisla miento hospitalario de los pacientes confirmados. Esto implicó prolongación de la estadía hospitalaria -limitando la disponibilidad de camas-, sobreutilización de EPP y de pruebas diagnósticas.
En la actualidad, sabemos que, en base a diversos estudios, un porcentaje elevado de pacientes pueden cursar con PCR persistentemente positiva, pero que dicha situación no implica posibilidad de contagio a terceros. Esta situación se explica por la presencia de fragmentos virales residuales, sin demostración de replicación viral. En este sentido, ha cobrado importancia el umbral de ciclado (Ct por la sigla de la palabra en inglés, cycle thres hold)39,40. El Ct es el número de ciclos de PCR requeridos para que la fluorescencia de la muestra exceda un umbral predefinido. El valor de Ct es inversamente proporcional a la cantidad de ácido nucleico presente en la muestra. La mayoría de las pruebas de PCR de SARS-CoV-2 tienen un punto de corte de Ct < 40. Los pacientes con infec ciones en estadios precoces suelen tener valores de Ct menores o iguales a 20-30 y aumentan progresivamente como reflejo de menores concentraciones de ARN viral conforme la respuesta inmune controla la infección. La mayoría de los informes en los que se obtuvieron culti vos virales incluyeron pacientes con infecciones leves a moderadas39. Solamente se reportó un paciente en quien se encontró virus replicativo a los 20 días desde el inicio de los síntomas39. No se conocen otros informes con descripciones de cultivos positivos más allá del día 10 desde el inicio de los síntomas, aun en pacientes con PCR persistentemente positiva. Se observó que aquellos con Ct de 13-17 se relacionaron con cultivos positivos, en tanto que no hubo resultados positivos en pacientes con Ct > 24 o 34 (de acuerdo a la prueba utili zada). Debemos considerar que la transmisibilidad tiene relación con el periodo evolutivo de la enfermedad. Así, la probabilidad de cultivar SARS-CoV-2 fue mayor en los primeros 5 días desde el inicio de los síntomas39,41. En forma semejante, un estudio epidemiológico conducido en Taiwán halló una tasa de ataque secundaria de 0.7% entre contactos estrechos de un caso índice, expuestos en los primeros 5 días desde el inicio de los síntomas. La tasa de ataque secundaria fue del 0% pasado este periodo40. Un estudio realizado en los Países Bajos (n: 129), se centró específicamente en pacientes con enfermedad grave, incluyendo pacientes inmunocomprometidos39. El 69% correspondía a pacientes internados en unidades de cuidados intensivos, 31% a unidades de cuidados no críticos y 23% eran inmunocomprometidos. Los investigadores tomaron muestras de tracto respiratorio superior e inferior en distintos momentos y las inocularon en cultivos celulares, obteniendo cultivos positivos de 23 casos (17.8%). La mediana de excreción viral infectiva (determinada por cultivo) fue de 8 días desde el inicio de los síntomas (rango IQ 5-11). El intervalo máximo desde el inicio de los síntomas asociado a cultivo positivo fue de 20 días (n = 1); aunque no se reportaron las caracterís ticas clínicas ni el curso de la enfermedad del paciente. La carga viral mediana fue significativamente mayor en pacientes con cultivo positivo, y la probabilidad de detectar virus replicativo fue < 5% tras 15 días desde el inicio de los síntomas39,42. La evidencia sugiere que para desais lar debemos considerar al tipo de paciente, gravedad y tiempo de evolución de la infección41,43. No hay evidencia que demuestre la necesidad de realizar PCR de control. En la Tabla 2, se resume la estrategia recomendada para desaislar pacientes de COVID-19.
Finalmente, y dada la limitada evidencia en la pobla ción de pacientes inmunocomprometidos, se sugiere la consulta con un infectólogo para efectivizar el retiro de las medidas de aislamiento. El ECDC recomienda en pacientes inmunosuprimidos con más de 3 días sin fiebre y mejoría clínica, desaislar al día 20 post-inicio de sínto mas u optar por la estrategia basada en PCR. En caso de optar por la misma, tanto el CDC de EE.UU. Como el ECDC, en Europa, recomiendan obtener 2 resultados de PCR negativos consecutivos separados por al menos 24 horas para efectivizar la discontinuación de las medidas de aislamiento.
6. ¿Es posible la reinfección por SARS-CoV-2? Sí.
Es posible que pueda detectarse ARN de SARS-CoV-2 en muestras respiratorias durante semanas (hasta 104 días)44. La tasa estimada acumulada de recurrencia de ARN positivo de SARS-CoV-2 (1 a 60 días) es de 12% (IC 95%: 12-13%)45.
Debemos considerar que:
o Esto no significa que contenga virus con capacidad infectante, ya que se considera que una persona con COVID-19 leve a moderado puede excretar virus viable hasta los 10 días del inicio de los síntomas, mientras que los casos graves o en inmunocomprometidos pueden hacerlo hasta 20 días o más.
o Algunos pacientes pueden tener PCR intermitente negativa (cuando el valor es cercano al límite de detección del método).
El test de PCR puede tener falsos positivos (áreas con baja prevalencia, contaminación o error en la toma de la muestra, transporte o análisis)44,46.
Con respecto a la inmunidad
o No hay evidencias firmes de que los anticuerpos (ATC) contra SARS-CoV-2 que aparecen luego de la infección sean protectores; y si lo fueran, se desconoce el nivel de los mismos para proteger de la reinfección46.
o La duración de la inmunidad es aún desconocida. Para otros coronavirus, la reinfección podría ocurrir a partir de los 90 días de la infección inicial.
o La identificación y el título de ATC correlacionan con inmunidad antiviral.
o La mayoría de los pacientes desarrollan IgG y ATC neutralizantes.
o Éstos alcanzan un pico entre la 3° y 4° semana, y decaen después del 4° mes, así como la actividad neutralizante.
o El impacto de la inmunidad celular no ha sido sufi cientemente estudiado aún.
o El riesgo de reinfección con otros coronavirus no necesariamente se asocia a la caída del título de ATC, pudiendo ocurrir aún con títulos altos44.
Si bien en septiembre 2020, el ECDC reportaba solo 6 casos de reinfección documentada publicados, a la fecha continúan apareciendo nuevos casos (1 en Hong Kong, 1 en Bélgica, 1 en Nevada (EE.UU.), 1 en Ecuador y 2 en India)47-51.
En el mes de octubre, se publicó el primer caso de muerte de una paciente con reinfección por SARS-CoV-2. Sin embargo, más casos probables se encuentran bajo investigación52.
Criterios para reinfección:
o Confirmación de laboratorio de dos infecciones por dos cepas diferentes, con dos episodios separados en el tiempo.
o Investigación adicional: clínica, epidemiológica, metodología diagnóstica, título de ATC, cultivos virales, secuenciación genética.
Considerar:
o La sensibilidad de la PCR, que oscila entre 66 y 80% de acuerdo al instrumento utilizado54.
o Falsos positivos del test (áreas con baja prevalencia, contaminación o error en la toma de la muestra, transporte o análisis).
o La detección de material genético por RT-PCR solo, que no necesariamente correlaciona con infección activa o infectividad52.
o No se ha demostrado transmisión a los contactos, al menos en los primeros 6 casos confirmados de rein fección, hasta ahora.
o Intervalo de tiempo libre de síntomas entre episodios (punto de corte aún no establecido). Se sugieren 90 días55.
o dentificación de virus infectante (cultivos virales, cuantificación de la carga viral Ct (< 30 dentro de los 45 días de la primera infección), secuenciación y análisis filogenético56.
o Discordancia genética entre ambos SARS-CoV-2, mayor que la que podría ocurrir por volución in vivo a corto plazo, es decir: virus genéticamente diferentes.
En un documento emitido por OPS/OMS, el 27 de octubre 2020, se describe como caso sospechoso de reinfección por SARS-CoV-256:
o Persona sintomática o asintomática con resultado positivo para SARS-CoV-2, después de un periodo ≥ 90 días posterior a la primera infección por SARS-CoV-2, en la cual se descartó la excreción prolongada del SARS-CoV-2 o del ARN del virus y la infección por otro agente.
o Persona con sintomatología compatible con COVID 19, con resultados positivos en la prueba para SARS-CoV-2, después de un período ≥ 45 días posteriores a la primera infección por SARS-CoV-2, en la cual se descartó la excreción prolongada del SARS-CoV-2 o del ARN del virus y la infección por otro agente.
Se plantean las siguientes situaciones en la práctica cotidiana:
Una persona con COVID-19 confirmado por PCR clíni camente recuperada, es re testeada y la PCR es positiva, ¿debería ser considerada como potencialmente infecciosa y aislada nuevamente?45.
o No está indicado re testear a una persona asinto mática, recuperada de COVID, dentro de los 3 meses posteriores.
o La persistencia de PCR+ dentro de los primeros 3 meses es posible. Sin embargo, no se ha recuperado virus viable más allá de los 10 días del inicio de los síntomas.
o Luego de los 90 días, la probabilidad de reinfección debe ser considerada y debe ser evaluado caso por caso.
o Si reaparecen síntomas dentro de los 3 meses, se debe re testear si no se identifica un diagnóstico alter nativo.
Una persona previamente infectada y con resolución clínica presenta síntomas compatibles con COVID, ¿debe ser nuevamente testeada y aislada?2.
Debe ser testeada si presenta síntomas compatibles más allá de los 3 meses del episodio inicial.
o Si la PCR es positiva, debe ser considerado infec tante y aislado de acuerdo a las pautas ya establecidas.
Para trabajadores de la salud clínicamente recupera dos de COVID, con una exposición de alto riesgo a un caso confirmado:
o Dentro de los primeros 3 meses: no retestear, no aislar; hacer automonitoreo de síntomas.
o Más allá de los 3 meses: aislamiento y exclusión laboral17.
7. ¿Es útil la determinación de anticuerpos para SARS-CoV-2? Sí, en determinadas situaciones.
Los escenarios donde es útil solicitar anticuerpos IgM/ IgG para SARS-CoV-2 son:
a. Evaluación del paciente con alta sospecha clínica y epidemiológica, con pruebas moleculares negativas y con fecha de inicio de síntomas de más de 7 días (con 14 días se aumenta la sensibilidad del estudio)57,58.
b. Diagnóstico del síndrome inflamatorio multisistémico en niños.
c. Para estudios epidemiológicos de seroprevalencia.
El diagnóstico definitivo de la infección por SARS-CoV-2 se realiza mediante la detección de partículas vi rales por pruebas moleculares, la detección de respuesta inmunológica en el huésped puede ayudar a determinar la presencia actual o pasada de la infección en determinadas situaciones. Hay dos tipos de anticuerpos, neutralizantes y no neutralizantes o de fijación. La neutralización se define como la pérdida de infectividad de un virus cuando un anticuerpo neutralizante se le une, los anticuerpos de fijación no tienen habilidad para evitar la infección del virus a otras células. Los anticuerpos neutralizantes juegan un rol fundamental en controlar la infección, aunque no hay datos suficientes que demuestren que su presencia puede evitar la reinfección viral.
Las pruebas -a la fecha-, no permiten diferenciar la detección de anticuerpos neutralizantes o de fijación. Si se detectan anticuerpos IgG ello indica que hay respuesta de linfocitos T (los linfocitos T co-estimulan a los linfoci tos B en la producción de anticuerpos). Esta respuesta de linfocitos T se acompaña hasta el momento en todos los virus de la familia del SARS-CoV-2 de una respuesta citotóxica por parte de estos. Actualmente existen en el mercado diferentes pruebas que permiten detectar anticuerpos (IgA, IgM o IgG) frente a SARS-CoV-2. La mayoría se basa en la inmunocromatografía (lateral-flow), y se han denominado test rápidos, pues el resultado se genera en unos 15 minutos. Sin embargo, existen otras técnicas, de ELISA o quimioluminiscencia, que son más sensibles y específicas. Según la evidencia actual, la OMS59 únicamente recomienda el uso de test rápidos de anticuerpos para determinadas situaciones y estudios, y con fines de investigación. Las pruebas de detección rápida de anticuerpos no se consideran adecuadas para el diagnóstico de infección aguda. Tampoco la serología tipo ELISA u otras técnicas de inmunoensayo de alto ren dimiento están indicadas por sí solas para el diagnóstico en la fase aguda de la enfermedad. Recientemente se ha descrito que la mediana del tiempo de seroconver sión para anticuerpos totales (Ab) desde el inicio de los síntomas es en el día 11, para IgM en el día 12 y para IgG en el día 1459. La presencia de anticuerpos fue < 40% entre los pacientes dentro de 1 semana desde el inicio de síntomas, y aumentó rápidamente a 100% (Ab), 94.3% (IgM) y 79.8% (IgG) desde el día 15. En base a estos resultados la detección de IgM sería ligeramente más precoz que las de IgG60. Dicho estudio fue realizado mediante un método de ELISA. En el mismo trabajo se determinó la sensibilidad de anticuerpos totales siendo de 38%, 89% y 100% en la primera, segunda y tercera semana, respectivamente. Sin embargo, no hay informa ción certera para considerar si estos tiempos son válidos usando la inmunocromatografía60. Tampoco si en pacien tes asintomáticos la cinética de la respuesta inmunitaria es similar o no. En general las pruebas de IgM tienen menor sensibilidad que las pruebas de IgG o inmunoglobulinas totales, cuya sensibilidad llega a su pico en las semana 3 y 4 posteriores al inicio de síntomas, con una rápida caída de títulos a partir de la quinta semana, desde inicio de síntomas, hasta los 90 días, a partir del cual la velocidad en la caída de anticuerpos es menor. Se necesitan más es tudios para definir el tiempo real de duración de presencia y detección de anticuerpos posterior a la infección57,61. El valor predictivo del estudio depende no solo de la sensibilidad del método, sino también de la evaluación clínica pretest y de la prevalencia de la enfermedad de la población, en contrándose, por ello, una mayor tasa de falsos positivos IgM en poblaciones con baja prevalencia de la infección62. A la fecha no hay evidencias para recomendar el empleo de estas pruebas diagnósticas para certificar infección pasada, debido a que, en diferentes estudios clínicos, solo el 70% de las personas expuestas han mostrado desarrollar anticuerpos63.
Conclusiones
Desde el inicio de la pandemia, las medidas de prevención y control epidemiológico de casos han ido cambiando. La evidencia disponible actualmente no avala el uso rutinario de barbijo N95 para la atención de pacientes sospechosos o confirmados de COVID-19, priorizando su uso en los PGA y en condiciones donde el espacio sea cerrado, ventilación inadecuada y exposición prolongada. Las estrategias para prolongar la vida útil de los barbijos N95 están aprobadas por organismos internacionales en situaciones de crisis, falta de recursos y bajo protocolos controlados. La decisión de discontinuar el aislamiento de un paciente con COVID debe realizarse utilizando una estrategia basada en los síntomas, gravedad de la enfermedad e inmunosupresión. No se recomienda utilizar estudios de PCR para control. La reinfección es posible, aún falta evidencia acerca de la causa (mutación vs. falta de inmunidad). La medición de anticuerpos se reserva para situaciones específicas y su resultado de penderá de la sensibilidad del método y la prevalencia de la enfermedad.