El crecimiento demográfico y la migración de la población rural a las ciudades ampliaron las fronteras urbanas en América Latina para albergar a más del 80% de la población, y en Argentina el 89.3%. Su crecimiento no planificado, sumado a las crisis económicas de mediados del siglo XX, derivó en altas concentraciones de habitantes en áreas periurbanas y conflictos ambientales (Faggi y Martínez Carretero 2013).
Nos referimos a ambiente urbano cuando al menos el 50% del área está ocupada por construcciones, 10 construcciones/ha y 10 habitantes/ha (Marzluff et al. 2001). Estos difieren en cobertura de vegetación, proporción de vegetación exótica y autóctona y construcciones, diferencias que en general, se observan en gradientes, desde centros comerciales y administrativos (donde la impermeabilización del suelo supera los espacios verdes) a zonas residenciales donde la vegetación aumenta (Blair 1996, Clergeau et al. 1998, Jokimáki y Huhta 2000, Fernández-Juricic y Jokimáki 2001, Leveau y Leveau 2004, Vincent 2005).
Las ciudades comparten diseños comunes como impermeabilización de suelos, construcciones, erradicación y modificación de la vegetación, postes, cableado, etc., que no consideran la biodiversidad de la región en la que se insertan y pocas especies nativas pueden adaptarse a las nuevas condiciones (Fernán-dez-Juricic et al. 2004, Haedo et al. 2017, Haag et al. 2020). A medida que la urbanización aumenta disminuye la diversidad de la vida silvestre, por disminución de la riqueza y una mayor homogeneización biótica consecuencia del reemplazo de numerosas especies nativas por unas pocas muy abundantes (Mc-Kinney 2006, Silva et al. 2016, Cristaldi et al. 2017, Jokimáki et al. 2016).
Las aves son especialmente utilizadas para comprender el funcionamiento de sistemas naturales y su respuesta al impacto antrópico, por su sensibilidad a cambios del hábitat, bajo costo de estudio, facilidad de avistamiento y distribución, historia natural y sistemática bien conocidas (Wiens 1992, Lindenmayer et al. 2002, Coria et al. 2015, Fava y Acosta 2016, Benito et al. 2019).
Numerosos estudios muestran que a medida que el grado de urbanización aumenta hay menor riqueza y diversidad de aves y mayor biomasa total (Emlen 1974, Feninger 1983, Blair 1996, Clergeau et al. 1998, Miller et al. 2003); pocas especies son superabundantes, generalmente exóticas, o nativas generalistas, asociadas a ambientes modificados (Mills et al.1989, Blair 1996, Clergeau et al. 1998, Jokimáki et al. 2002, Lucero et al. 2002). La diversidad de aves aumenta con la cobertura de vegetación, pero las nativas especialistas solo responden al incremento de la vegetación autóctona (Emlen 1974, Mills et al.1989, Blair 1996, Marzluff y Ewing 2001, Fontana et al. 2011, Haedo et al. 2017, Haene 2018).
Conocer los patrones espaciales de abundancia y diversidad es importante para lograr una interpretación ecológica y de conservación, pero debemos considerar la composición de especies (Garaffa et al. 2009, Filloy et al. 2018) ya que la diversidad depende, especialmente, de la biología de las especies que habitan la región (Fernández-Juricic et al. 2004, Cristaldi et al. 2017) y como esta interactúa con las características de la ciudad.
Características ecológicas como gregarismo, no territorialidad, omnivoría o capacidad de usar estructuras humanas para nidificar, favorecen el éxito de ciertas especies en ciudades (Emlen 1974, Crooks et al. 2004, Heil et al. 2007) derivando en una homo-geneización de los ensambles de aves de centros más urbanizados. Al acercarnos a áreas suburbanas se incrementa la similitud con el pool de especies de la región en que se encuentra (Garaffa et al. 2009, Aronson et al. 2014, Leveau et al. 2017a).
La respuesta de las especies al hábitat urbano puede variar entre áreas geográficas (González-Oreja 2011, Jokimáki et al. 2017, Bulacia 2021), y diferentes biomas (Leveau et al. 2017b, Filloy et al. 2018), así, la pérdida y homogeneización de especies son procesos asociados a las respuestas de cada una al cambio en la estructura del ambiente por urbanización (Fernán-dez-Juricic et al. 2004, Juri 2007, Echevarría et al. 2011, Silva et al. 2016).
Los estudios de ecología urbana en Sudamérica son escasos comparados con el hemisferio norte, e igualmente sesgados hacia ciudades grandes (Mac-Gregor-Fors y Ortega-Álvarez 2013, Pauchard y Barbosa 2013, Silva et al. 2016, Leveau et al. 2017a). Es recomendable ampliar el espectro de conocimiento sobre patrones y procesos relacionados con la urbanización que comprenda una mayor diversidad de situaciones (MacGregor-Fors y Ortega-Álvarez 2013). En este estudio se seleccionó la ciudad cabecera de Chilecito, centro urbano pequeño con aproximadamente 40 000 habitantes.
Las hipótesis son: 1) la riqueza, abundancia y diversidad del ensamble de aves de la ciudad es afectada por los cambios en la cobertura de vegetación y la impermeabilización del suelo, 2) la respuesta de las especies a estas características es influenciada por el comportamiento de búsqueda de alimento y el origen biogeográfico. Basados en estas hipótesis los objetivos son 1) conocer la variación en riqueza, diversidad y abundancia del ensamble de aves en los distintos ambientes urbanos; y 2) analizar el origen biogeográfico y el comportamiento de búsqueda de alimento de las especies y su variación en los distintos ambientes urbanos.
MÉTODOS
Área de estudioChilecito se encuentra en la Provincia de La Rio-ja, al sur de un valle a 1080 msnm, entre la sierra de Famatina y la del Velasco. Según proyecciones, basadas en el último censo nacional (2010), para el 2015 la población de su ciudad cabecera, donde se realizó el estudio, era de 37 700 habitantes (Dirección General de Estadística y Censo 2017). Las principales perturbaciones del ambiente son los cultivos de vid y olivo, la extracción de leña y el sobrepastoreo, agregándose en la última década, una acelerada expansión de la frontera urbana sin planificación, que avanza sobre áreas naturales, en general, cauces de ríos secos.
La biodiversidad corresponde a la ecorregión de Monte Sierras y Bolsones, estepa arbustiva alta con precipitaciones estivales de hasta 200 ml anuales. Las comunidades vegetales más frecuentes son la asociación de Larrea cuneifolia, L. divaricata, Zuccagniapuncta-ta, Parkinsonia praecox, Senna aphylla y Bulnesia retama en conos de deyecciones, laderas y valles intermontanos y bosques de algarrobos (Neltuma sp) en zonas con mayor humedad; a medida que ascendemos se presentan grandes cactáceas y cojines de Bromeliáceas característicos de la prepuna (Morello 1958, Burkart et al. 1999, Pol et al. 2005, Cabido et al. 2018).
Diseño del estudio
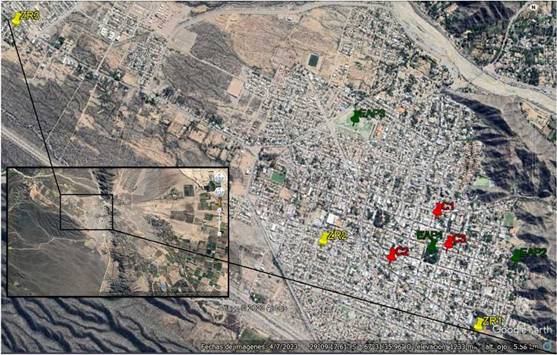
Se ubicaron sitios de observación en tres tratamientos con situaciones contrastantes en niveles de urbanización y cobertura de vegetación: centro, zona residencial y espacios abiertos de uso público (Fig. 1).
El centro (C) con alta concentración de edificaciones y reducida cobertura de vegetación, fuerte flujo de transeúntes y vehículos, calles y veredas angostas con escasos árboles o arbustos, en general, pequeños y exóticos. Los sitios se ubicaron al fondo de dos casas residenciales (C1 y C2) y de un edificio comercial (C3).
La zona residencial (ZR), son barrios periféricos, dos con más de cuatro décadas de antigüedad (ZR1 y ZR2) y el tercero 25 años (ZR3) caracterizado por casas familiares con terrenos de aproximadamente 15m X 30m, fondos y jardines con vegetación. Los espacios abiertos de uso público (EAP) son plazas y parques: Plaza Caudillos Federales (plaza principal, 1.6 ha), Parque Municipal (1.3 ha) y Parque de la Ciudad (7 ha.). Los dos primeros antiguos, con árboles maduros, el tercero de pocos años de creación con palmeras adultas y renovales de árboles.
Figura 1: Sitios seleccionados para los relevamientos en la Ciudad Cabecera de Chilecito, La Rioja, Argentina. En verde los espacios abiertos (EAP), en amarillo los sitios de zona residencial (ZR) y en verde los sitios de centro (C).
El grado de urbanización se define principalmente por la superficie impermeabilizada y la cobertura de vegetación, por lo que se calculó el porcentaje de cemento (suelo impermeabilizado), tierra (suelo desnudo), césped, así como el número de árboles y arbustos, en círculos de 30m de radio de los puntos de conteo de zona residencial y centro y del área total de espacios abiertos. En el caso de los árboles y arbustos se calculó, tanto para las áreas circulares como para los espacios abiertos, el número medio para 100m2.
En cada sitio de los tres tratamientos, entre 2015 y 2016, se realizaron 10 conteos de punto de radio fijo de 20 m, registrándose las especies vistas u oídas durante 10 minutos (Bibby et al. 2000), 5 conteos a la mañana y 5 a la tarde en picos de actividad, por sitio y estación del año totalizando 360 conteos. Las aves fueron observadas con binoculares de 10 x 50 mm; para su identificación se utilizaron guías de campo (Narosky e Yzurieta 2010, López-Lanús 2020).
Se clasificó las especies por su distribución geográfica siguiendo la Lista de las Aves Argentinas (Roesler y González Táboas 2016) en: exóticas (Ex); amplia distribución (AD), ocupan el norte y todo o gran parte del país; Monte (M), especies características del Monte, Puna, Prepuna y Altos Andes; y (OE), autóctonas, pero de otras ecorregiones del Argentina.
La estructura del ensamble de aves, en cada tratamiento, se estudió agrupando a las especies según cómo buscan el alimento (tácticas) y dónde (hábitats) (Juri 2007, Echevarría et al. 2011, Bulacia 2021), siguiendo la descripción de su biología de Canevari et al. 1991 y de la Peña 2015, resultando cuatro grupos funcionales (GF). GF1: aves que buscan el alimento desplazándose por el suelo, GF2: por la vegetación, GF3: por el suelo y la vegetación y GF4: desde el aire y/o perchas.
Análisis estadísticoSe calculó el índice de Diversidad de Shannon (H’), aplicando Test t de diferencias de Shannon, y números efectivos de especies o diversidad verdadera (Moreno et al. 2011, Jost y González-Oreja 2012, Cruz Flores et al. 2017).
La riqueza y abundancia fueron comparadas mediante la prueba de Kruskall-Wallis. Para los estimadores de riqueza se utilizó el programa EstimateS (Colwell 2013), empleando el estimador Jackknife 1 para comparar la curva de acumulación de especies, como estimador del límite inferior de la riqueza (Gon-zález-Oreja et al. 2010).
Se graficó la curva de rango-abundancia (curva de Whittaker) para cada tratamiento como el logaritmo (base 10) del pi (ni/N) de cada especie, cómo complemento se calculó el IR (índice de importancia relativa), como [(ni*Mi) / (N*n° de conteos)] * 100 (Bucher y Herrera 1981) donde ni es el número de individuos de la especie i; Mi el número de censos donde se presenta la especie i; N el número total de individuos del ensamble.
La presencia y abundancia de aves observadas en diferentes tratamientos se analizó con un análisis de escalamiento multidimensional no métrico (NMDS). Para el ordenamiento se utilizó el procedimiento metaMDS y el procedimiento envifit se evaluó la significancia estadística de los factores y variables que pudieran incidir sobre el ordenamiento. Entre los factores se analizó tratamiento y entre las variables ambientales se seleccionaron: cobertura de árboles, arbustos y cemento. Ambos procedimientos están incluidos en la librería Vegan (Oksanen et al. 2020) en el programa R (R Core Team (2021).
RESULTADOS
Se registraron 6828 individuos, 51 especies y 21 familias. Se sumaron 4 especies, fuera de los conteos, no consideradas en análisis estadísticos. De las 112 especies registradas por Lobo Allende (2019) en el Valle, 40 se encontraron en la ciudad (Tabla 1).
El modelo Jackknife 1 indica que el muestreo incluye el 81.09% de las especies en centro, 82.48% en zona residencial y el 100% en espacios abiertos.
De los espacios abiertos, el Parque Municipal es el que presentó mayor cobertura de árboles (Fig. 2a). En Parque de la Ciudad el 45% son palmeras, el resto árboles exóticos jóvenes, y solo tres adultos, dos exóticos y un autóctono. En el Parque Municipal hay 154 árboles, 3 autóctonos, el resto exóticos, de los cuales el 32% son olivos. La cobertura de cemento en Parque de la Ciudad y en Plaza principal es mayor que la de césped y tierra sumadas mientras que en Parque Municipal es menor (Fig. 2b).
Los sitios de zona residencial y centro fueron diferenciados por su cercanía al punto central de la ciudad. En centro, C3 es el que presenta mayor cobertura de cemento y C1 mayor cobertura de césped y tierra, quedando C2 en posición intermedia. En C1 se registraron 10 árboles, en C2 8 y en C3 5, pero sólo en C1 3 son autóctonos, al igual que 3 arbustos que se presentaron (Fig. 2a y b).
Tabla 1. Lista de las especies registradas en la Ciudad de Chilecito clasificadas por grupo funcional (GF). n: número de individuos por especie. Valle: especies registradas en el trabajo de Lobo Allende 2019 en el Valle Antinaco - Los Colorados. DO: distribución original de las especies (Ex: exótica, AD: de amplia distribución en Argentina, OE: de otras ecorregiones de Argentina, M: de las ecorregiones del Monte).
Tabla 2: Abundancia y Riqueza de aves por ambiente urbano. Resultado del análisis de Kruskal Wallis.
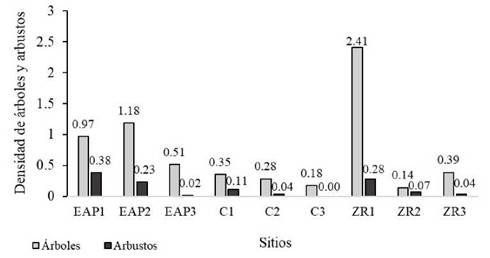
Figura 2: a. Densidad de árboles y arbustos cada 100 m2 en cada ambiente urbano de la Ciudad de Chilecito.
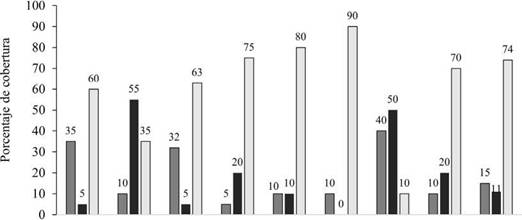
Figura 2: b. Porcentaje de cobertura de tierra, cemento y césped en cada tipo de urbanización de la Ciudad de Chilecito. C: centro, ZR: zona residencial, EAP: espacio abierto.
De los sitios de zona residencial, ZR1 es el que presentó mayor cobertura de tierra, césped y vegetación, con más del 50% de los árboles autóctonos, mientras que ZR2 se asemeja a C1, pero con mayor cobertura de césped; ZR3 tuvo una cobertura de cemento como la de C1, pero con mayor proporción de césped que de tierra (Fig. 2a y b).
La riqueza de especies de aves fue mayor en zona residencial y centro que en los espacios abiertos, mientras que la abundancia fue significativamente mayor en espacios abiertos (Tabla 2). La zona residencial presentó la mayor diversidad de orden 1 (1D), (Tabla 3), con un valor que representa casi el doble del número de especies efectivas del centro comercial, y este a su vez, casi el doble que los espacios abiertos. La 2D sigue tendencias similares, pero menos marcadas y H’ también es mayor en zona residencial y menor en espacios abiertos con diferencias significativas entre todos los tratamientos (p= 0.001).
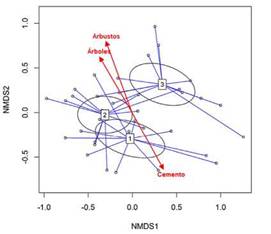
La ordenación NMDS mostró la agrupación de los conjuntos de especies de aves por niveles de urbanización (Fig. 3). El ajuste estadístico mostró que estos agrupamientos indican efectos significativos del nivel de urbanización (r2= 0.33, P < 0.001) y de las tres variables ambientales, cobertura de árboles (r2= 0.44, P < 0.001), arbustos (r2= 0.61, P < 0.001) y cemento (r2=0. 47, P < 0.001) sobre el ordenamiento.
De las especies registradas 62% es de amplia distribución, y de mayor a menor porcentaje, de Monte, otras ecorregiones del país (Chaco Seco y/o Espinal y una especie típica de Yungas) y dos exóticas: el Gorrión y la Paloma Doméstica (Columba livia) (Tabla 1).
En los tres tratamientos se encuentran las dos especies exóticas, siendo más abundantes en el centro, y las aves de amplia distribución contribuyen con el mayor número de especies, y representan el mayor porcentaje de individuos en la zona residencial y los espacios abiertos (Tabla 4).
Los cuatro grupos funcionales se encuentran en toda la ciudad, en el centro y zona residencial los grupos funcionales 1 y 3 fueron más abundantes, mientras que en los espacios abiertos el grupo funcional
1. Los grupos funcionales 1 a 3 presentaron el mayor número de especies en la zona residencial y el 4 en el centro (Tabla 5).
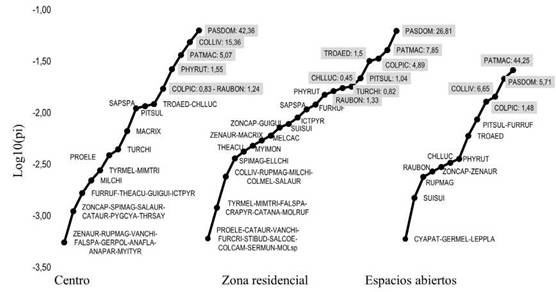
En la figura 4 se muestran las curvas del rango de abundancia y valores de IR de las especies con IR mayor a 0.5 en al menos uno de los tratamientos. La curva de la zona residencial, por su forma y longitud, muestra una diversidad mayor que la del centro y espacios abiertos, siendo este último el menos diverso. Se realizó una prueba de Kruskal Wallis, de cada una de las especies con IR alto, para definir si diferencias observadas en este índice entre los ambientes, se corresponden con diferencias en abundancia (Fig. 5).
El Gorrión es la especie que domina en centro y zona residencial y la Paloma Manchada (Patagioenas maculosa) es la que predomina en los espacios abiertos, quedando en segundo y tercer lugar las dos especies exóticas. Entre zona residencial y centro las diferencias se encuentran en las especies que ocupan del segundo lugar en adelante; en centro la Paloma Doméstica, luego la Paloma Manchada, el Cortarramas (Phytotoma rutila), el Naranjero (Rauenia bonariensis) y la Torcacita (Columbina picui). En zona residencial la Paloma Domestica se registró en un número muy bajo respecto a los otros tratamientos, solo 35 individuos contra 379 y 622 del centro y los espacios abiertos respectivamente; el orden de las especies con IR alto cambia y se agregan Benteveo (Pitangus sulphuratus), Ratona (Troglodites aedon), Zorzal Chiguanco (Turdus chiguanco) y Picaflor Verde (Chlorostilbon lucidus) (Figs. 4 y 5).
Tabla 4: Número de especies, abundancia y porcentaje de individuos de las especies de aves según su distribución original en cada ambiente urbano. C: centro, ZR: zona residencial, EAP: espacio abierto, Ex: exótica, AD: de amplia distribución en Argentina, OE: de otras ecorregiones de Argentina, M: de las ecorregiones del Monte.
Tabla 3: Diversidad de orden 0 (0D), 1 (1D) y 2 (2D) e Índice de diversidad de Shannon para los ensambles de aves en cada ambiente urbano. Entre paréntesis se presentan los intervalos de confianza al 95%.
Figura 3: Ordenamiento NMDS de los ensambles de aves de los tres ambientes estudiados. 1: centro, 2: zona residencial y 3: espacios abiertos. La figura también indica el efecto significativo y dirección de las variables ambientales sobre el ordenamiento: densidad de árboles, arbustos y cemento.
Figura 4: Rango de abundancia de las especies registradas por ambiente urbano. Se encuentran sombreadas las especies con IR mayor a 0.5 acompañadas de su valor de IR. Las especies se identifican con un código donde se encuentran las tres primeras letras del género seguidas de las tres primeras letras de la especie.
Figura 5: IR y número de individuos de las especies con IR mayor a 0.5. Las líneas corresponden a los valores de IR y las barras al número de individuos: las más oscuras a los espacios abiertos (EAP) y las más claras a la zona residencial (ZR), las de color intermedio al centro (C). Letras diferentes (a, b, c) indican diferencias significativas en el número de individuos.
Las diferencias también se dan en la abundancia entre los tratamientos, la Paloma Manchada con mayor abundancia en espacios abiertos y menor en centro con diferencias significativas entre los tratamientos (Kruskal Wallis: H= 63.05; p= <0.0001). El Gorrión ocupa el primer lugar en centro y zona residencial, pero es en el primero donde tiene una abundancia significativamente mayor (Kruskal Wallis: H= 57.79; p= <0.0001) y en espacios abiertos menor (Figs. 4 y 5).
La Paloma Doméstica es beneficiada por el centro, en segundo lugar, los espacios abiertos, siendo baja su abundancia en zona residencial, con diferencias significativas entre tratamientos (Kruskal Wallis: H=70.62; p= <0.0001). La Torcacita Picuí tuvo una abundancia significativamente menor en centro, respecto de zona residencial y espacios abiertos que no mostraron diferencias entre si (Kruskal Wallis: H= 12.33; p= 0.0003).
Tabla 5: Número de especies, abundancia y porcentaje de individuos de las especies de aves según su grupo funcional (GF) en cada uno de los ambientes urbanos y del ensamble total. C: centro, ZR: zona residencial, EAP: espacio abierto, GF1: aves que buscan el alimento desplazándose por el suelo, GF2: por la vegetación, GF3: por el suelo y la vegetación y GF4: desde el aire y/o perchas.
El Naranjero tiene una abundancia significativamente menor en espacios abiertos, no siendo significativa la diferencia entre zona residencial y centro (Kruskal Wallis: H= 6.84; p= 0.0006).
Benteveo, Ratona y Zorzal Chiguanco presentaron IR alto sólo en zona residencial. La primera con una abundancia significativamente mayor a la de centro, pero no a la de espacios abiertos (Kruskal Wa-llis: H= 4.18; p= 0.0226) y las otras dos especies con abundancia significativamente mayor a centro y espacios abiertos (Ratona: Kruskal Wallis: H= 17.09; p= 0.0001; Zorzal Chiguanco: Kruskal Wallis: H= 11.51; p= <0.0001).
El Cortarramas alcanzó un IR alto sólo en centro, aunque en zona residencial es de 0,43, y su abundancia fue significativamente mayor a la de los otros tratamientos (Kruskal Wallis: H= 18.54; p= <0.0001). El Picaflor Verde presenta IR de 0.45 en zona residencial donde su abundancia es significativamente mayor respecto a espacios abiertos (Kruskal Wallis: H= 18.54; p= <0.0001).
Por último, sólo el Cóndor Andino (Vultur gryphus) y el Loro Barraquero (Cyanoliseuspatagonus) fueron catalogadas como amenazadas en el Libro Rojo de Aves Argentinas (especies que, por exceso de caza, destrucción del hábitat, etc., son susceptibles de pasar a la situación de peligro de extinción), categoría equiparada con Vulnerable de la UICN (MAyDS y AA 2017).
DISCUSIÓN
La urbanización tiene un profundo efecto sobre la biodiversidad (Aronson et al. 2014, Jokimaki et al.
2016) afectando la abundancia de las especies tanto positiva como negativamente (Menon y Mohanraj 2016). Nuestros datos muestran que de las 112 especies registradas en el valle (Lobo Allende 2019), 40 se encontraron en la ciudad y las dos especies más abundantes fueron exóticas.
Respecto al primer objetivo, nuestros datos con-cuerdan con numerosos trabajos: la riqueza y diversidad de aves disminuye cuando se intensifica la urbanización, aumenta la superficie impermeabilizada y construida y disminuye la cobertura de vegetación (Garaffa et al. 2009, Fontana et al. 2011, Silva et al. 2016, Cristaldi et al. 2017, Benito et al. 2019).
Los espacios abiertos son los menos diversos. El Parque municipal, con alta proporción de suelo desnudo es el que tiene más árboles, pero en su mayoría exóticos y la tercera parte representada por una especie, el olivo. La plaza principal, tiene menos árboles, mayor impacto humano, y alta impermeabilización del suelo, como el Parque de la Ciudad con escasa vegetación (Fig. 2a y b). Los tres sitios con un estrato medio prácticamente inexistente. Numerosos trabajos demuestran que la falta de cobertura de vegetación y la ausencia de arbustos es un factor que incide negativamente en la diversidad de aves (Jokimaki y Huhta 2000, Juri 2007, Silva et al. 2016, Muñoz-Pedreros et al. 2018, Benito et al. 2019).
En Tucumán ciertas zonas residenciales presentaron mayor diversidad de aves que los parques, tres espacios verdes (255 ha en total) con una diversa arboleda, pero sin estratos de vegetación intermedios, representados en zonas residenciales por arbustos ornamentales y cercos (Lucero et al. 2002, Juri 2007, Bulacia 2021).
En Chilecito, la zona residencial presenta el mayor número de especies y diversidad, con diferencias significativas sólo con los espacios abiertos (Tabla 2). Pero 2D de centro y espacios abiertos son más similares entre sí, debido a que en ambos la abundancia relativa de las especies dominantes es mucho mayor (Fig. 5).
La zona residencial presentó el menor valor IR de la especie dominante, por el aumento de especies e individuos de nativas y la menor abundancia de especies exóticas, lo que coincide con otros trabajos donde una mayor cobertura y diversidad estructural de la vegetación, y menor impermeabilización del suelo, promueve la presencia de aves nativas (Juri 2007, Fi-lloy et al. 2010, Silva et al. 2016, Cristaldi et al. 2017, Jokimaki et al. 2016, Leveau et al. 2017a, Benito et al. 2019, Bulacia 2021).
Es importante destacar la escaza diferencia entre zona residencial y centro. En Sudamérica las áreas urbanas más desarrolladas son generalmente los centros administrativos y comerciales y la intensidad de desarrollo decrece a medida que nos alejamos de estos (Filloy et al. 2018). En ciudades grandes este gradiente es claro, pero en ciudades pequeñas como Chilecito, los centros comerciales y administrativos conservan residencias con jardines y fondos que contribuyen a disminuir las diferencias con la zona residencial tan marcada en otros estudios.
Los patrones reportados en la literatura indican que la biomasa total de aves aumenta hacia el núcleo urbano por el predominio de unas pocas especies que contribuyen a homogeneización biótica (Clergeau et al. 1998, Marzluff et al. 2001, Leveau y Leveau 2004, MacKieny 2006, Garaffa et al. 2009, Fontana et al. 2011, Menon y Mohanraj 2016). En general, estas especies corresponden a especies exóticas y nativas de amplia distribución, comunes en sistemas urbanos y agrícolas (Fava y Acosta 2016, Benito et al. 2019). Por su parte los hábitats suburbanos, con mayor volumen de vegetación, presentan especies del grupo regional adaptadas a los bordes (Leveau et al. 2017a).
Lo antes dicho se relaciona con el segundo objetivo que incluye analizar el origen biogeográfico de las especies. Numerosos estudios sugieren que las especies responden de diferente forma a las variaciones del ambiente, lo que resulta en una composición específica para el grado de urbanización (Blair 1996, Jo-kimaki et al. 2002, Crooks et al. 2004, Fernández-Ju-ricic et al. 2004, Heil et al. 2007), esto concuerda con nuestros resultados. Las características urbanas determinan, en gran parte, la composición funcional de los ensambles de aves en término de dieta y hábitat de forrajeo, la pérdida de grupos funcionales no es azarosa (Menon y Mohanraj 2016, Silva et al. 2016, Cris-taldi et al. 2017).
Los efectos del disturbio en las aves también dependen de la ecología del organismo que determina su capacidad para soportarlo, por lo tanto, especies de una determinada región biogeográfica, responden en forma similar a las condiciones de un ambiente urbano (Vides Almonacid 1992, González-Oreja 2011). La Paloma Doméstica y el Gorrión son comunes en los ensambles urbanos de todo el mundo y típicas de áreas intensamente urbanizadas (Leveau y Leveau 2004, Juri 2007, Menon y Mohanraj 2016, Cristaldi et al. 2017, Leveau et al. 2017 a-b, Filloy et al. 2018, Benito et al. 2019), su éxito responde a que son gregarias, omnívoras y usan estructuras humanas como sitios de descanso y nidificación (Emlen 1974, Crooks et al. 2004, Vincent 2005, de la Peña 2015).
Las especies exóticas y de amplia distribución, beneficiadas por la urbanización, presentaron abundancias relativas y absolutas diferentes entre tratamientos (Tabla 4). Algo similar ocurre con los grupos funcionales, siendo 1 y 3 los que incluyeron a las especies dominantes (Tabla 5) el Gorrión, una exótica del grupo funcional 3 y la Paloma Doméstica (exótica) y la Paloma Manchada, de amplia distribución, ambas del grupo funcional 1.
A continuación, analizaremos la variación en los distintos ambientes urbanos de los grupos funcionales, y dentro de estos, el origen biogeográfico de las especies que lo componen. En los espacios abiertos, de mayor abundancia y menor diversidad, el grupo funcional 1 es el más abundante como consecuencia de la Paloma Manchada, en segundo lugar, con IR mucho menor, la Paloma Doméstica y en tercer lugar la Torcacita Picuí, de amplia distribución (Figs. 4 y 5). En zona residencial la Paloma Doméstica presenta un número muy bajo relacionado a los otros tratamientos y en centro tiene un IR mayor que la Paloma Manchada (Fig. 4 y 5).
La Paloma Manchada, una especie en expansión que ocupa ambientes antropizados (Ortiz et al. 2018), es autóctona y característica de la región de Monte, y en el Valle es una de las de mayor frecuencia (Lobo Allende 2019). En nuestra ciudad es dominante y no la Paloma Doméstica, como ocurre en gran parte de las urbanizaciones, y junto a la cual es común observarla alimentándose (Juri obs. pers.), nidifica preferentemente en árboles y no en edificaciones. En ciudades de San Juan, Provincia incluida en Monte de Sierras y Bolsones, fue muy común (Fava y Acosta 2016, Ortiz et al. 2018), pero no se encuentra en urbanizaciones de Tucumán (Juri 2007). En Arequipa, Perú, sólo se registró en ambientes suburbanos y en Mar del Plata y La Plata (Buenos Aires, Argentina) su abundancia relativa es baja (Montalti y Kopij 2001, Perepelizin y Faggi 2009, Leveau et al. 2017a, Luque Fernández et al. 2018).
La Torcacita Picuí con IR alto en los tres tratamientos es común en urbanizaciones de Buenos Aires, Tucumán y San Juan (Leveau y Leveau 2004, Juri 2007, Perepelizin y Faggi 2009, Ortiz et al. 2018) y considerada indicadora de efecto antrópico junto a las exóticas (Perepelizin y Faggi 2009, Coria et al. 2015).
El Zorzal Chiguanco, especie típica del Monte, alcanzó un IR alto en todo el ensamble, pero sólo se destacó en zona residencial (Fig. 4 y 5), si bien Cane-vari et al. (1991) señalan que es común en parques y jardines, en urbanizaciones de ambientes más húmedos no se registró (Montalti y Kopij 2001, Juri 2007, Garaffa et al. 2009, Perepelizin y Faggi 2009, Leveau et al. 2017a, Haag et al. 2020, Bulacia 2021) solo en el presente trabajo y en los realizados en San Juan y Santiago del Estero, provincias de Ecorregiones áridas (Coria et al. 2015, Fava y Acosta 2016); mostrando que habita en ambientes urbanos en el rango de su distribución original.
Las especies del grupo funcional 1 se caracterizan por buscar alimento caminando, explotando suelos con césped y desnudos (Bulacia 2021). En Chilecito, con gran parte de su superficie cubierta de cemento, especies como el Hornero (Furnarius rufus), el Tordo Renegrido (Molothrus bonariensis) o el Picabuey (Ma-chetornis rixosa) si bien se registraron, no presentaron abundancias altas como en otras ciudades del país.
El grupo funcional 2 es el de mayor riqueza, y donde se encuentran 10 de las 12 especies de Monte, pero el de menor abundancia. Solo el Naranjero presentó un IR alto, es una especie de amplia distribución común en parques y jardines del país (Canevari et al. 1991, de la Peña 2015), que estuvo presente en los tres tratamientos (Fig. 4 y 5).
El Cortarramas, de amplia distribución, no es común en ambiente urbanos. En trabajos realizados en ciudades de Argentina (Tucumán, Buenos Aires y Mar del Plata) no se la menciona (Leveau y Leveau 2004, Juri 2007, Juri y Chani 2009, Perepelizin y Faggi 2009, Leveau et al. 2017a). En San Juan, de la misma ecorregión, pero más grande que Chilecito (700 000 habitantes), es común en ambientes urbanos (Or-tiz et al. 2018); es exclusivamente sudamericana, se alimenta de hojas, frutos y brotes, principalmente de hojas de Neltuma flexuosa y Lycium cestroides en su ambiente natural (López de Casenave 2001, Bucher et al. 2003, Ríos et al. 2014). No se cuenta con los datos para determinar de que se alimenta en Chilecito, pero Neltuma chilensis y Lycium sp., se encuentran en la ciudad y específicamente en el sitio de centro, donde se registró el mayor número y pichones en época de reproducción.
La Ratona, de amplia distribución, es común en ciudades de Argentina (Juri 2007, Coria et al. 2015, Leveau et al. 2015, Fava y Acosta 2016, Bulacia 2021), busca su alimento en los estratos bajos de la vegetación (Canevari et al. 1991). En Chilecito está presente en las tres urbanizaciones, pero con abundancia significativamente mayor en zona residencial (Fig. 4).
El Celestino (Thraupis sayaca) se encuentra en expansión y sería beneficiada por poblados y arboledas exóticas (Bodrati y Ferrari 2014).
Se registraron cuatro especies de picaflores, una fuera de censo y el resto con IR bajo, pero es importante destacar que el Picaflor Cometa (Sappho sparga-nurus) y el Picaflor Gigante (Patagonagigas), ambos del Monte, se observaron generalmente libando en especies autóctonas: Ligaria cuneifolia y Nicotiana glauca respectivamente, mostrando la importancia de incorporar plantas nativas para aumentar la presencia de estas especies (Haene 2018).
La cobertura de vegetación es un determinante de la diversidad en áreas urbanas (Mills et al. 1989, Blair 1996, Fernández-Juricic et al. 2004, Leveau y Leveau 2004, Haedo et al. 2017), el grupo funcional 2 se encuentra mejor representado en zona residencial y centro y es el que incluye casi todas las especies del Monte del ensamble, ambas urbanizaciones con una estructura más compleja de la vegetación y mayor proporción de especies vegetales autóctonas.
En otros estudios se demostró que la vegetación nativa provee más recursos alimenticios y estructuras para la nidificación a las aves autóctonas (Mills et al. 1998, Marzluff y Ewing 2001, Echevarría et al. 2011).
En Argentina se observó que los ensambles urbanos fueron más similares al natural en biomas húmedos que en áridos, sugiriendo que las urbanizaciones de los primeros conservan elementos del ambiente natural, cómo árboles nativos, mientras que las de ambientes áridos, tienen árboles exóticos y escasos elementos arbustivos (Filloy et al. 2018), lo que también sucede en Chilecito.
El grupo funcional 3 es afectado tanto por la vegetación como por la cobertura del suelo y en consecuencia el menos diverso.
El grupo funcional 4 es el único con más especies en centro (Tabla 5), en general necesita espacios abiertos y perchas para buscar el alimento (árboles, cables, postes y otros tipos de construcciones). Podemos diferenciar a las rapaces y golondrinas, que buscan el alimento en vuelo, y a los tiránidos que cazan en vuelo ‘elástico’ utilizando perchas (Bulacia 2021). En Chilecito solo el Benteveo alcanzó IR alto en zona residencial; es una de las especies más conspicuas del Centro y Norte de Argentina, de amplia distribución y común en urbanizaciones del país (Canevari et al. 1991).
Respecto a las especies amenazadas, no son comunes en la ciudad y por sus escasos registros asumimos que no la habitan. El Cóndor Andino tiene un registro fuera de los conteos en un área silvestres inserta en la urbanización. El Loro Barraquero presentó dos registros, uno de dos individuos y otro de cuatro volando bajo sobre la ciudad.
Los datos presentados muestran que la riqueza, abundancia y diversidad del ensamble de aves de Chi-lecito son afectadas por los cambios en las características del ambiente urbano como la estructura de la vegetación y la impermeabilización del suelo.
Al analizar los grupos funcionales y la distribución original de cada una de las especies observamos que su respuesta no es la misma que en urbanizaciones del país, de distintas ecorregiones.
Numerosos estudios muestran que factores ambientales como tamaño de terrenos, cobertura de especies nativas, estrato arbustivo y suelo desnudo, influyen en la presencia de especies de aves en ciudades, por lo que las decisiones de sus propietarios afectan la diversidad de aves urbanas (Fontana et al. 2011, Muñoz-Pedreros et al. 2018). Nuestros datos apoyan esta idea y sugieren que la vegetación en áreas residenciales promueve una mayor diversidad de avifauna de Chilecito que la vegetación en los espacios abiertos. Los espacios verdes, ofrecen servicios ambientales, como incrementar nichos para especies nativas (Romero et al. 2001, Echevarría et al. 2011, Cristaldi et al. 2017, Bulacia 2021), función que nuestros espacios abiertos no estarían cumpliendo por su escasa cobertura de vegetación y el alto porcentaje de suelo impermeabilizado.












 uBio
uBio