La Patagonia Norte está conformada por los valles de los ríos Colorado y Negro, y por los valles inferiores de los ríos Neuquén y Limay. Es una región productora de frutales de carozo y de pepita (Sosa et al., 2018). En los últimos años el cultivo de cerezos (Prunus avium L.) es el de mayor relevancia en términos de superficie y crecimiento. El principal destino de su producción es el mercado internacional. Solo en la temporada 2019-2020 se exportaron 2600 ton de cerezas. Es considerado un producto de alta calidad y estatus sanitario (Villarreal & Raffo, 2020).
En el departamento de Confluencia, Neuquén, se encuentra la mayor producción de fruta fina de la Patagonia Norte. Se cultivan frutillas (Fragaria x ananassa Duch.), frambuesas rojas (Rubus idaeus L.) y moras arbustivas (Rubus sp.). La superficie actual de estos cultivos en la zona es de 84,4 ha con una producción de 1.293 ton durante el periodo 2019-2020 (Lochbaum, 2020).
Desde la detección de Drosophila suzukii (Matsumura) (Díptera: Drosophilidae) en la región en el año 2014, dicha mosca se transformó en una limitante potencial para la producción y comercialización de frutas frescas, principalmente cerezas (Cichón et al, 2015, Cichón, 2018). Actualmente esta plaga es categorizada como A2 por la lista EPPO (plaga presente localmente) y cuarentenaria en algunos países como México (EPPO, 2020).
Drosophila suzukii, también conocida como ‘mosca de alas pintadas’, puede ocasionar daños en frutos con diferentes estados de madurez (Lee et al., 2011). La especie es originaria de Asia occidental y actualmente se encuentra ampliamente distribuida en el mundo (dos Santos et al., 2017; de la Vega & Corley, 2019). En Argentina está presente en casi todo el territorio, ha sido citada en las provincias de Río Negro, Neuquén, Buenos Aires, Santa Fe, Entre Ríos, La Rioja, Tucumán, Mendoza y Santa Cruz, siendo este último el reporte más austral en América del Sur (Cichón et al., 2015; Díaz et al., 2015, Santandino et al., 2015; Gonsebatt et al., 2017; Lochbaum, 2017; Lue et al., 2017; Dagatti et al., 2018; Escobar et al., 2018; Funes et al., 2018; Lavagnino et al., 2018; de la Vega & Corley, 2019). Es posible que su éxito de invasión se deba, en parte, a que es capaz de completar su desarrollo en frutos silvestres y ornamentales que se comportarían como hospederos alternativos (Lee et al., 2015).
El manejo de las poblaciones de D. suzukii representa un desafío debido principalmente a la ausencia de insecticidas registrados o la aparición de resistencia a algunos (Gress & Zalom, 2018; Cichón et al., 2019). Por su parte, los avances en el conocimiento de los enemigos naturales son aún limitados (Biondi et al., 2020), especialmente aquellos que tienen como fin implementar planes de control biológico y/o métodos integrados de manejo de plagas en frutales (Gabarra et al., 2015). Estudios en áreas recientemente invadidas demostraron que pueden establecerse gradualmente nuevas asociaciones entre D. suzukii y la fauna nativa o cosmopolita que potencialmente contribuyen a la supresión o regulación local de sus poblaciones (Rossi Stacconi et al., 2013).
A nivel mundial se conocen 30 especies de parasitoides asociadas a D. suzukii. El 40% de ellas son nativas de Asia, 9 son pupales y 21 larvales. En Argentina se reportaron los parasitoides de pupa Trichopria sp. y Pachycrepoideus vindemmiae Rondani, y de larva Dieucoila sp., Ganaspis sp., Hexacola sp., Ganaspis hookeri Crawford, Leptopilina boulardi Barbotin, Carton & Kelner-Pillault y Leptopilina clavipes Hartig (Kirschbaum et al., 2020).
El objetivo de este trabajo fue identificar potenciales enemigos naturales de D. suzukii presentes en la Patagonia Norte viables para su integración en el manejo de la plaga.
Se seleccionaron cuatro montes frutales ubicados en tres localidades de Neuquén y Río Negro con cultivos hospederos de la plaga (frambueso, cerezo, mora, nectarín) y diferentes tipos de manejo de plagas (Tabla I). En cada uno de los sitios muestreados se instaló una trampa para la captura de D. suzukii. Se ubicaron en la parte central del cultivo, en la canopia de la planta, a 1-1,5 m de altura. Se utilizaron botellas de plástico transparente de 1.500 ml con 12 orificios de 0,5 mm de diámetro en su parte media. Se agregaron 300 ml de un atrayente compuesto por vinagre de manzana al 50% y un cebo de amplio espectro (PHEROCON® SWD Broad Spectrum Lures, TRECE Inc.).
Las muestras fueron recolectadas quincenalmente entre el 8 de octubre de 2017 y el 15 de febrero de 2018. El contenido fue transferido a un recipiente hermético con etanol al 70% indicando cultivo, sitio y fecha para su posterior observación en el laboratorio de Sanidad Vegetal de la EEA INTA Alto Valle. Los individuos fueron contabilizados y determinados específicamente en D. suzukii, ‘otros Drosophilidae’ (el resto de moscas pertenecientes a la familia Drosophilidae), y microhimenópteros. Se tomaron fotografías mediante una cámara Canon Power Shot G9, con tubo adaptador G7 acoplado a una lupa binocular Zeiss Stemi DV4 40x. Los parasitoides fueron aislados en tubos individuales con etanol al 70% y enviados a la División Entomológica del Museo de La Plata para su determinación taxonómica.
Los ejemplares fueron montados mediante las técnicas convencionales (Noyes, 1990) y se identificaron utilizando las claves de Gibson et al. (1997) y Gibson (2009). Posteriormente fueron comparados con la redescripción de la especie realizada por Gibson (2009) y con material depositado en la colección de la División Entomología del Museo de La Plata, Buenos Aires (MLP). Los ejemplares voucher quedaron depositados en INTA Alto Valle, Rio Negro.
Se determinaron tres especies de himenópteros parasitoides. Dos se encontraban registradas en la zona: L. boulardi (Figitidae) (Garrido et al., 2018) y P vindemmiae (Pteromalidae. (Funes et al., 2020). Se reporta aquí el nuevo registro de la especie Spalangia endiusWalker (Pteromalidae) asociada a D. suzukii.
Spalangia endius Walker (Fig. 1)
Diagnosis. La especie fue descrita por Walker en 1839 y redescrita por Gibson (2009) en la revisión de las Spalangiinae del Nuevo Mundo. La incluye en el grupo de especies endius junto a S. nigripes Curtis por poseer un collar pronotal con puntos circulares aislados, separados por pequeños intersticios brillantes. Se diferencian principalmente porque S. endius posee en la zona posterior del collar pronotal una línea transversa punteada-crenulada, la esculturación en la región internotaular es mayormente lisa y brillante lateralmente a la región media punteada-rugosa, tarsos amarillos brillantes (excepto el apical), la carina media propodeal en vista lateral es plana o poco convexa y la depresión subalar es más rugosa, el ala anterior en general sin setas más allá del pliegue submarginal pero a veces con una a tres setas en el pliegue mediocubital. Para una descripción más detallada de la especie, ver Gibson (2009).
Distribución. Es una especie cosmopolita. Presente en América del Norte (Canadá, EUA, México), América Central (Belice, Guatemala, Nicaragua), islas del mar Caribe (Puerto Rico, República Dominicana, Trinidad y Tobago, San Vicente y las Granadinas), América del Sur (Bolivia, Brasil, Chile, Colombia, Perú, Uruguay, Argentina), Europa (República Checa, Eslovaquia), Asia (Chipre, Uzbekistán, India), Australia, islas del océano Pacífico (Filipinas, Hawái, Samoa, islas Fiyi, Nueva Caledonia, Galápagos). Respecto a la distribución en Argentina, se menciona un registro en la provincia de Tucumán (Boucek, 1963; Gibson, 2009).
Hospedadores. Según Noyes (2019), es un parasitoide primario de pupas registrado en al menos 50 hospedadores diferentes pertenecientes a ocho familias de Diptera y es hiperparasitoide de Bombyx morí L. (Lepidoptera: Bombycidae) y Diatraea spp. (Lepidoptera: Pyralidae). Los registros corresponden a especies de las familias Anthomyiidae, Calliphoridae, Drosophilidae, Muscidae, Otitidae, Sarcophagidae, Tachinidae y Tephritidae.
Usos. A nivel mundial es utilizado como agente de control biológico de la ‘mosca domestica’ Musca domestica L. (Zapater, 1998; La Rossa et al., 2002; Álvarez González et al., 2004; Inciso & lannacone, 2008). En Argentina, los programas de manejo integrado de moscas (MIP moscas) incluyen liberaciones inundativas en producciones pecuarias intensivas haras, feed-lots, criaderos de cerdos, granjas avícolas, tambos e industrias derivadas del sector pecuario (Crespo & Lecuona, 2004).
Spalangia endius fue encontrado en todos los montes frutales muestreados en la región de la Patagonia Norte. Los bajos valores de prevalencia de S. endius hallados en el presente trabajo pueden explicarse por el elevado número de otras especies de Drosophilidae distintas a D. suzukii. Por otra parte, se infiere sobre el efecto secundario del uso de insecticidas que perjudicaría el establecimiento de la especie en los sitios de muestreo. Por este motivo, en el sitio 3 (sin uso de insecticidas), la prevalencia de S. endius fue mayor. Si D. suzukii fuera su hospedero principal los valores de prevalencia se incrementarían. Se sugiere profundizar esta hipótesis con una metodología que incluya la recolección de pupas de D. suzukii en los cultivos afectados y evaluar el parasitoidismo en forma directa. Otras especies del género Spalangia han sido asociadas con D. suzukii.
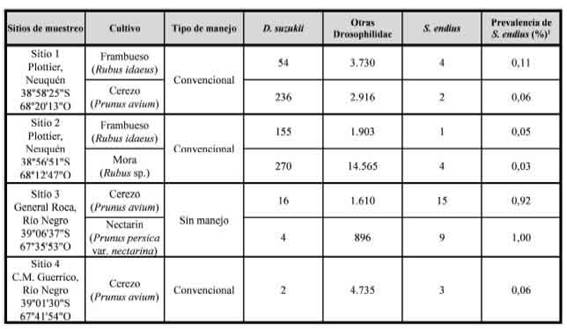
Tabla I: Número de individuos colectados y prevalencia de Spalangia endius en el periodo comprendido entre el 8 de octubre de 2017 y 15 de febrero de 2018 en frutales de carozo y fruta fina de la Patagonia Norte de Argentina.
En estudios de parasitoides realizados en México, con trampas centinela, se ha registrado la emergencia de S. simplex Perkins en pupas (García Cancino et al., 2015); y en ensayos de laboratorio realizados en España y Suiza confirmaron el parasitoidismo por parte de S. cameroni Perkins y S. erythromera Forster, respectivamente (García-Martínez et al., 2014; Knoll et al, 2017).












 uBio
uBio 


