Introducción
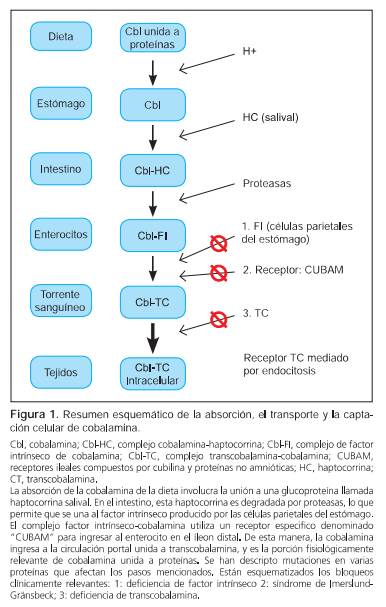
La vitamina B12 (cobalamina) es la vitamina del grupo B más compleja, y tiene un papel fundamental en el crecimiento, la reproducción, la síntesis de ADN, la metilación y el metabolismo mitocondrial.1 La cobalamina no es producida naturalmente por los seres humanos, sino que es sintetizada por bacterias y algas e incorporada a través de la ingestión de productos animales como pescado, vísceras, carnes y lácteos.2 La cobalamina es crucial para la mielinización de la médula espinal y el cerebro, y para la producción de glóbulos rojos. Es requerida como cofactor de dos reacciones: la conversión del ácido metilmalónico en succinil-CoA por la metilmalonil-CoA mutasa mitocondrial, una reacción anaplerótica que proporciona sustratos para el ciclo de Krebs y la biosíntesis del hemo, y la conversión de homocisteína en metionina catalizada por la enzima metionina sintasa citosólica. Esta reacción regenera el tetrahidrofolato a partir de metiltetrahidrofolato, que es fundamental para la biosíntesis de novo de ácidos nucleicos.1,3 La deficiencia de vitamina B12 es causada por ingesta inadecuada, malabsorción, inactivación química o alteración en el transporte o en el metabolismo intracelular. Una vez dilucidada la causa se podrá abordar el tratamiento apropiado evitando secuelas irreversibles. En muchas ocasiones, el perfil bioquímico y los datos clínicos no son suficientes para un diagnóstico preciso, por lo que se requieren pruebas terapéuticas, herramientas de biología molecular o ambas.3
Formas de presentación
Características hematológicas
La manifestación hematológica más frecuente es la anemia megaloblástica con macrocitosis, hipersegmentación de neutrófilos, leucopenia, trombocitopenia o pancitopenia y la presencia de células precursoras megaloblásticas en la médula ósea, con disincronía nuclear-citoplasmática.4,5 A largo plazo genera fallo de medro y declinación cognitiva.6
Características neurológicas
La vitamina B12 es necesaria para la mielinización del sistema nervioso central y periférico, por lo que su deficiencia da origen a desmielinización de las columnas dorsal, lateral, cervical y torácica de la médula espinal, de los nervios craneales y periféricos y de la sustancia blanca cerebral.7 Las manifestaciones neurológicas pueden preceder a las hematológicas o aparecer en ausencia de ellas.7,8
Biomarcadores del estado de vitamina B12
Pruebas de primera línea
Hemograma completo, con índices hematimétricos y frotis en sangre periférica. La presencia de anemia, particularmente si es macrocítica (volumen corpuscular medio 100 fl), aumenta la sospecha de deficiencia de cobalamina y requiere determinaciones de los niveles iniciales de vitamina B12 y folato. Es importante tener en cuenta que el volumen corpuscular medio puede ser normal en presencia de microcitosis concomitante, como sucede en la deficiencia de hierro o en la talasemia.
Vitamina B12 sérica. Representa la vitamina B12 unida a sus proteínas transportadoras: haptocorrina (80%) y transcobalamina (20%). No hay valores universalmente establecidos de esta vitamina y no hay consenso respecto de los valores de normalidad en niños. Se considera deficiencia los valores séricos < 200 pg/ml junto a la presencia de signos y síntomas, así como índices hematológicos de deficiencia de vitamina B12 o valores de cobalamina sérica < 200 pg/ml en combinación con niveles elevados de homocisteína plasmática o ácido metilmalónico.9
Holotranscobalamina sérica (HoloTC). Representa la fracción de cobalamina unida a transcobalamina, que es la que toman las células, por lo que se la llama “vitamina B12 activa”. Presenta una vida media corta, de manera que ante un balance negativo de cobalamina es la primera en ser afectada; así, algunos trabajos señalan que sería un marcador temprano de deficiencia. La edad, el sexo, determinados genotipos y el método utilizado son las principales fuentes de variabilidad y deben ser considerados para establecer los intervalos de normalidad. Se consideran valores normales aquellos entre 40 y 200 pmol/l, pero se recomienda que cada laboratorio establezca sus propios valores de referencia. Es un buen marcador de deficiencia aguda, pero no es útil para valorar la respuesta al tratamiento.10,11
Folato sérico. El metabolismo de la vitamina B12 y el del ácido fólico están íntimamente relacionados; al deficiencia de folato produce manifestaciones clínicas similares.1 Para que el folato cumpla con su función debe actuar de manera sinérgica con la vitamina B12, ya que el folato no se puede reciclar en ausencia de cobalamina, de modo que se debe revisar su nivel y corregirlo, si fuese necesario.
Pruebas de segunda línea
Se utilizan el ácido metilmalónico y la homocisteína plasmática. Estos marcadores son funcionales, por lo que reflejan la cantidad de vitamina B12 intracelular disponible para las dos enzimas ya nombradas: metilmalonil-CoA mutasa y metionina sintasa.
Ácido metilmalónico. Es el sustrato de la metilmalonil-CoA mutasa, dependiente de 5’-desoxiadenosilcobalamina, pero independiente del folato, por lo tanto, es el único biomarcador que se eleva frente a alteraciones de la vitamina B12, pero no del folato. También se puede elevar falsamente en determinadas enfermedades (insuficiencia renal, diabetes, afecciones hepáticas) y en casos de hemoconcentración, lo que reduce su especificidad. Es posible su cuantificación tanto en plasma o suero como en orina. Su elevado costo es el principal inconveniente para su uso generalizado. Es altamente sensible por sí mismo (86%), y en combinación con la homocisteína tiene una especificidad mayor del 99%. Es el marcador más sensible de depleción intracelular de cobalamina funcionalmente relevante.10 Sus concentraciones aumentan cuando la vitamina B12 cae por debajo de 389 pg/ml.12
Homocisteína plasmática. De los cuatro biomarcadores es el más susceptible a influencias preanalíticas; en su metabolismo intervienen las vitaminas B12, B6, B2 y el ácido fólico, por lo que es susceptible a cambios en estos metabolitos y, por tanto, es poco específica del déficit de cobalamina. Dada esta susceptibilidad a influencias preanalíticas, se recomienda una centrifugación inmediata para que los eritrocitos no eliminen homocisteína al plasma aumentando falsamente sus niveles. La combinación con ácido metilmalónico aumenta su especificidad.13
Propionilcarnitina. Se utiliza en los programas de pesquisa de recién nacidos como un marcador de aciduria metilmalónica y acidemia propiónica, por lo que es un biomarcador altamente sensible pero poco específico para distinguir la causa, ya que se encuentra elevado en condiciones adquiridas y genéticas.14
Trastornos adquiridos y congénitos
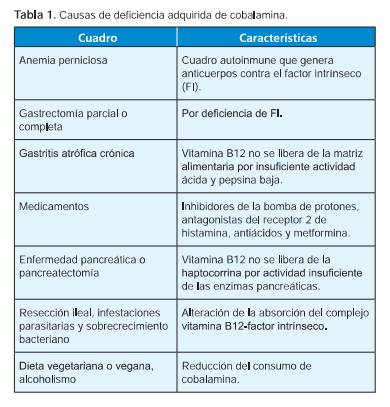
Deficiencia adquirida de cobalamina
La ingesta inadecuada es la causa principal de niveles bajos de cobalamina en la población y la principal causa en los países subdesarrollados.10 En la mayoría de los lactantes la clínica aparece entre los 4 y los 10 meses de vida, con falta de crecimiento, apatía, anorexia, anemia megaloblástica, hipotonía y retraso en el desarrollo.6 En la Argentina, según la Encuesta Nacional de Nutrición y Salud de 2007, el 4.7% de los niños presentaba ingesta de vitamina B12 por debajo del requerimiento. El porcentaje de mujeres con ingesta menor que el requerimiento fue del 25.8%.15 Esto denota la importancia de pesquisar la deficiencia materna, en cuyo caso hay que tratar esta en primer lugar, sin necesidad de continuar el estudio de un lactante (Tabla 1).
Diagnóstico diferencial
Defectos congénitos frente a condiciones adquiridas
Los síntomas hematológicos y neurológicos no son útiles para distinguir las condiciones congénitas de las adquiridas. Ambas pueden manifestarse clínicamente durante el primer año de vida con síntomas de letargo, fallo de medro, hipotonía y vómitos recurrentes.1
Para poder distinguir ambas situaciones es fundamental recabar datos relacionados con riesgo de deficiencia (lactantes amantados de madres deficientes, antecedentes alimentarios, enfermedades crónicas, medicamentos) que orienten hacia la falta de provisión de vitamina B12. En caso de que esto sea descartado y la determinación de vitamina B12 sea baja, se debe contemplar la posibilidad de que se trate de defectos de absorción o transporte de la cobalamina.
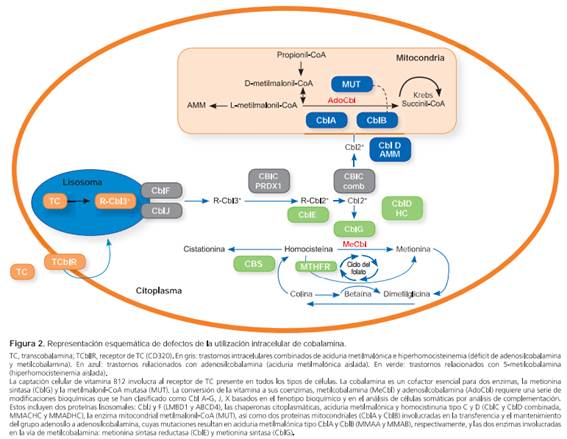
En el caso de los defectos de la utilización intracelular de cobalamina, las determinaciones de vitamina B12 son normales, ya que este biomarcador no refleja su estado intracelular. Como excepción, existen defectos de metabolismo intracelular que pueden cursar con bajos niveles de vitamina B12: cobalamina F y J; en estos pacientes persiste eliminación de ácido metilmalónico luego de administrar vitamina B12 y presentarán daño neurológico a pesar del tratamiento.
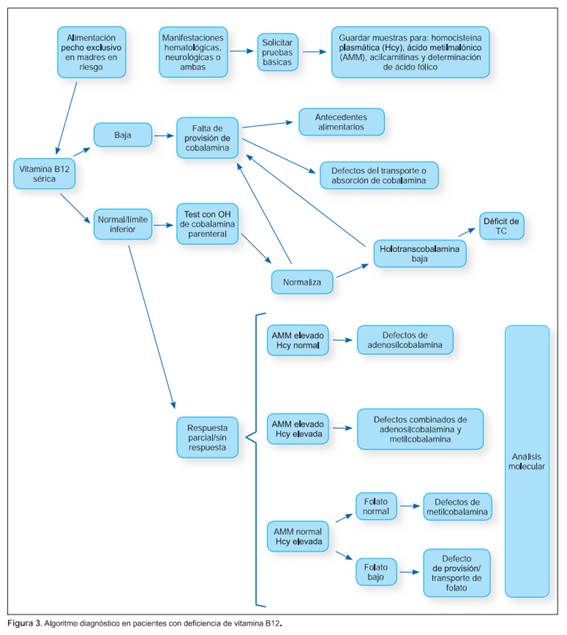
En los defectos intracelulares, los niveles de ácido metilmalónico son considerablemente más altos que los que se ven en pacientes con deficiencia adquirida de cobalamina.14 Otra distinción bioquímica son los valores de homocisteína; en las condiciones adquiridas, el déficit de absorción y las deficiencias combinadas de adenosil y metilcobalamina, la homocisteína está elevada; en cambio, existen formas de aciduria metilmalónica aislada que no elevan la homocisteína ya que no está afectada la vía de la metilcobalamina, pero sí la de la adenosilcobalamina (Figura 3). Además, los pacientes con defectos de cobalamina C, A, B y mutasa son susceptibles a crisis acidóticas metabólicas en respuesta a una enfermedad infecciosa o a un cambio en la dieta, que puede poner en peligro la vida.2 En muchas ocasiones, a pesar de contar con los datos clínicos y bioquímicos, no es posible hacer la distinción entre estos trastornos, por lo que es prioritario comenzar el tratamiento cuanto antes. En estos casos, la respuesta a la administración de hidroxocobalamina puede guiar hacia el diagnóstico.14
Algoritmo diagnóstico
La sospecha de deficiencia de cobalamina puede estar sustentada por manifestaciones hematológicas, neurológicas o ambas. La causa de la deficiencia puede surgir a partir de que los niños son alimentados de forma exclusiva con pecho materno y la madre presenta factores de riesgo para deficiencia de cobalamina. Si la madre presenta deficiencia, se debe iniciar el tratamiento en ambos sin necesidad de continuar con estudios. En el caso de síntomas compatibles con deficiencia de vitamina B12 es factible iniciar el tratamiento con dosis altas a la espera los resultados de pruebas más específicas.
Toma de la muestra en caso de sospecha
Ante la sospecha de déficit de vitamina B12 debe solicitarse hemograma con frotis, reticulocitos, lactato deshidrogenasa (LDH), haptoglobina solo en mayores de 1 año, vitamina B12 sérica y holoTC. En lactantes se solicitará hemograma, y a la madre, vitamina B12 total y activa. Las muestras que se deben conservar aguardando los resultados son: homocisteína plasmática, ácido metilmalónico, acilcarnitinas y ácido fólico. El procesamiento de estas determinaciones está supeditado al resultado de la cobalamina.
Es fundamental guardar estas muestras antes de iniciar el tratamiento con vitamina B12 ya que este modifica los valores y puede entorpecer el proceso diagnóstico. Si la determinación de vitamina B12 es baja, se planteará como etiología la falta de provisión de cobalamina, ya sea por carencia en la dieta o, con menos frecuencia, por defectos en la absorción. Si la determinación de holoTC muestra valores disminuidos y la determinación de vitamina es normal, se planteará como etiología la falta de provisión, pero también disfunción de la transcobalamina. Si la determinación de vitamina B12 se encuentra dentro del rango de referencia, deben procesarse las muestras guardadas para homocisteína plasmática, ácido metilmalónico, acilcarnitinas y ácido fólico. Si el perfil resulta en un aumento de ácido metilmalónico y homocisteína, podríamos estar en presencia de un defecto combinado de adenosilcobalamina y metilcobalamina. Si hay antecedentes de acidosis metabólica con brecha aniónica (gap) elevada, hiperlactacidemia e hiperamonemia asociada con homocisteína normal, aciduria metilmalónica y propionilcarnitina muy elevada, debe sospecharse que está comprometida la vía de la adenosilcobalamina (Figura 2). Si no hay presencia de ácido metilmalónico y la homocisteína se encuentra elevada, será relevante evaluar el nivel de folato; si este es normal, podría tratarse de un defecto de metilcobalamina. Si los niveles de ácido fólico están disminuidos, podría tratarse de un defecto de provisión o de transporte de folato.
Prueba de respuesta a hidroxocobalamina
La prueba de hidroxocobalamina es útil en caso de valores de vitamina B12 normales o en el límite inferior y en presencia de sintomatología compatible. Sirve como guía para diferenciar la etiología, pero también para definir qué pacientes podrían beneficiarse con hidroxocobalamina.14 La prueba de respuesta a la hidroxocobalamina se basa en la administración de 1 mg de esta sustancia por vía intramuscular, durante tres días consecutivos. Después de la inyección de cobalamina se procede a la recolección de orina o plasma luego de diez días. Las muestras de orina o plasma deben analizarse en el mismo laboratorio. Una disminución de la media de las concentraciones de ácido metilmalónico en orina o plasma de más del 50% debe ser considerada como respuesta positiva.14 Pueden diferenciarse dos resultados posibles: respuesta positiva o parcial/ausencia de respuesta según la normalización del ácido metilmalónico y la homocisteína. Si hay desaparición de ácido metilmalónico y se normaliza la homocisteína, podría tratarse de una falta de provisión de cobalamina. En caso de respuesta parcial o falta de respuesta, se plantea que se podría estar frente a un defecto intracelular de cobalamina, aunque existen algunos defectos con respuesta positiva como excepción (cobalamina A, MUT-).2
Tratamiento
Para el tratamiento de la deficiencia de vitamina B12 se utilizan dos preparados farmacológicos: cianocobalamina e hidroxocobalamina. La elección del preparado farmacológico, la vía y el tiempo de administración estarán supeditados a la causa subyacente de la deficiencia. Si se detecta la falta de provisión de cobalamina y no hay presencia de síntomas hematológicos o neurológicos, puede ser válida la introducción de alimentos de origen animal en la dieta, sumado a la suplementación de la madre en niños alimentados a pecho, y la administración por vía oral de suplementos de cianocobalamina.17 En el caso de deficiencia carencial, la cobalamina se puede administrar de manera intramuscular mediante inyecciones de cianocobalamina o hidroxocobalamina, en dosis que van desde 250 hasta 1000 µg de tres a siete veces por semana durante 1 a 2 semanas, luego una vez por semana durante un mes o hasta que el hemograma sea normal. Las dosis de mantenimiento cada dos a tres meses son necesarias si la condición subyacente no se corrige.17,18 El tratamiento de los defectos de absorción y transporte consiste en la administración parenteral de cobalamina en dosis variables, sin que exista consenso en cuanto a intervalos y dosis.16
En términos generales, la hidroxocobalamina es la vitamina metabólicamente activa que se utiliza de manera electiva en los defectos intracelulares de vitamina B12. El tratamiento de estos defectos se basa en su administración en dosis variables.14-16 La respuesta es efectiva en la mayoría de los pacientes tipo cobalamina A y MUT-, poniéndose de manifiesto un descenso pronunciado del ácido metilmalónico, pero su relevancia clínica está en discusión. El tratamiento de las formas combinadas incluye, además, betaína, L-carnitina y ácido fólico.2
Otra indicación absoluta de este preparado son los casos de compromiso neurológico grave por la deficiencia, más allá de la causa subyacente, para evitar las secuelas permanentes. Los efectos adversos incluyen prurito, exantema, fiebre, náuseas, mareos y, excepcionalmente, anafilaxia por hipersensibilidad al cobalto.17,18
Conclusiones
El diagnóstico de deficiencia de vitamina B12 es un desafío, ya que los parámetros clínicos y bioquímicos que la definen presentan límites poco claros. Tanto las manifestaciones hematológicas como neurológicas de la deficiencia de cobalamina pueden ser sutiles y, por lo tanto, difíciles de reconocer.
En los casos de deficiencia adquirida, aunque el tratamiento se haya efectivizado y los cambios morfológicos en el sistema nervioso detectables por resonancia magnética desaparezcan, las consecuencias a largo plazo del deterioro neurológico pueden persistir después de que la deficiencia ha sido tratada.18 Por lo tanto, consideramos de vital importancia el monitoreo de los niveles de cobalamina para el adecuado neurodesarrollo, y señalamos que hasta incluso una deficiencia moderada puede resultar perjudicial para los niños.
El diagnóstico bioquímico de la deficiencia es complejo y existe controversia sobre cuál es el método más sensible y específico. La medición de vitamina B12 tiene falsos positivos, además de no estar claro si el valor de corte de 200 pg/ml es correcto para diagnosticar deficiencia.12 Por eso, es fundamental, en presencia de valores limítrofes, solicitar otros biomarcadores para aumentar su especificidad.9 Estas dificultades ilustran aún más la necesidad de establecer intervalos de referencia en los niños.21 A pesar de que los niveles bajos de vitamina B12 se consideran diagnósticos, hay una escasa correlación entre estos niveles y los síntomas.
Por lo tanto, el diagnóstico de deficiencia va a estar sustentado en tres pilares fundamentales: las manifestaciones clínicas, los valores de los biomarcadores y la respuesta de los síntomas clínicos después de la institución de vitamina parenteral. Los defectos congénitos intracelulares presentan compromiso del sistema nervioso central en grado variable, así como respuestas bioquímicas diversas. Es fundamental el diagnóstico diferencial entre estas entidades para evaluar el tratamiento, definir el pronóstico y dar asesoramiento genético adecuado.