La incidencia de endocarditis infecciosa (EI) ha aumentado con el tiempo, con una mortalidad reportada de hasta el 30% a 30 días.
Durante las últimas 3 décadas, se ha identificado más de 25 especies de Actinomyces en humanos. Su detección en laboratorio y reconocimiento como patógenos en entornos clínicos pueden ser un desafío 1. Se trata de un bacilo Gram positivo. El primer microorganismo de esta familia fue descrito en 1896, pero solo en 1958 fue reportado el Actinomyces denticolens por I. Batty. El principal reservorio es el ser humano; se aloja principalmente en la boca desde muy temprana edad, también se ha descrito en la faringe y el esófago 2
La actinomicosis es una enfermedad granulomatosa rara, crónica y de progresión lenta. Frecuentemente se diagnostica erróneamente porque puede imitar otras afecciones como tuberculosis e incluso cuadros malignos3. Las tasas de prevalencia no están disponibles. Se clasifica en distintas formas clínicas según el sitio anatómico infectado o diseminado, siendo el A.Israelli el principal agente etiológico en la mayoría de las presentaciones3.
Hasta el momento en la literatura se describen 26 casos de Actinomyces sp. como causante de EI, con aislamientos de A.neuii, A.funkei, A.israelii, A.viscosus, A.meyeri.
No se ha descrito Actinomyces denticolens como causante de EI, por lo que el que presentamos es el primer caso reportado en la literatura.
Paciente de 39 años sin antecedentes, agricultor, originario de zona rural, que presenta cuadro de 3 meses de evolución consistente en disnea, fiebre y pérdida de peso. Consulta inicialmente en otra institución, donde se detecta derrame pleural bilateral manejado con drenaje percutáneo. Presenta como complicación deterioro hemodinámico y respiratorio, que requiere soporte vasopresor y ventilatorio. Se realiza un ecocardiograma transtorácico que evidencia insuficiencia aórtica grave con hipertrofia excéntrica y fracción de eyección ventricular izquierda (FEVI) 37%. Tras lograrse estabilidad hemodinámica y destete de inotrópicos es trasladado a nuestra institución para manejo integral en alto nivel de complejidad.
El examen físico de ingreso evidencia danza carotídea y soplo diastólico en foco aórtico, pulsos saltones, estertores inspiratorios bibasales, uso de músculos accesorios y anasarca
El ecocardiograma transesofágico evidencia aurícula izquierda dilatada, trombo intracavitario, VI dilatado con hipertrofia excéntrica (volumen de fin de diástole 383 ml por método biplano) y FEVI 30%. En la válvula mitral se ve vegetación en la cara auricular, insuficiencia funcional moderada. Válvula aórtica bicúspide, con vegetaciones adheridas a ambas valvas, la mayor de 23 mm, insuficiencia grave, tiempo de hemipresión de 114 m/s. Cavidades derechas dilatadas con contractilidad conservada. Presión pulmonar sistólica: 69 mm Hg. Se solicitan hemocultivos con resultado negativo.
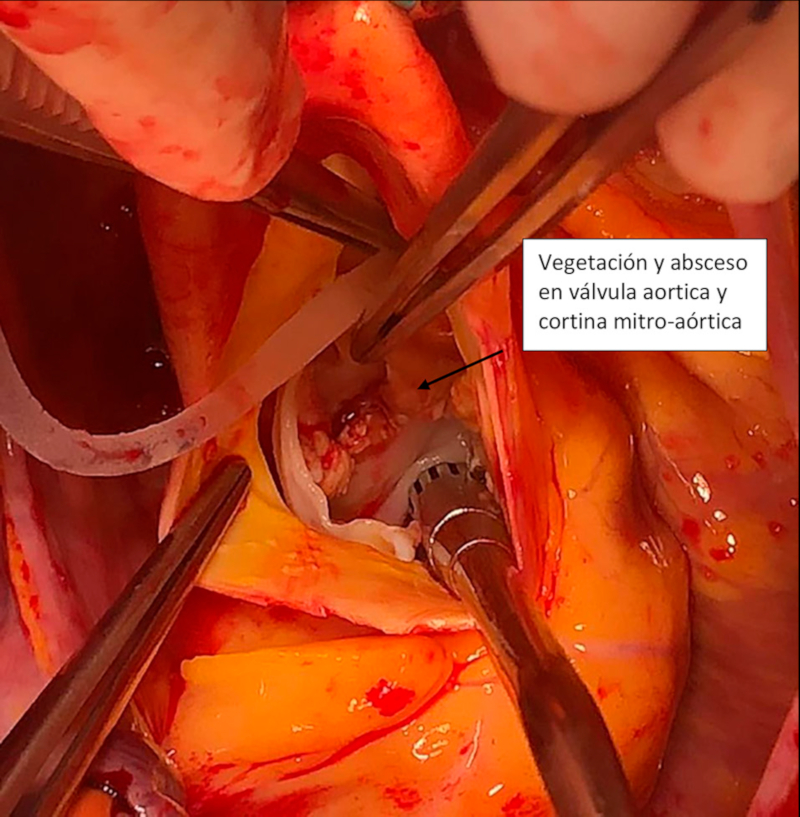
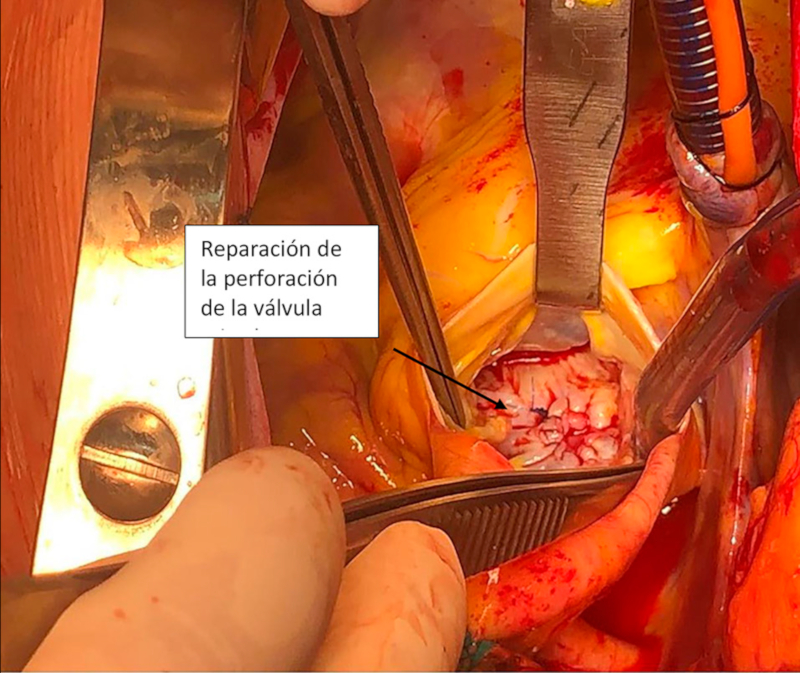
Se lleva el paciente a cirugía. Se confirma válvula aortica bivalva Sievers I por fusión de las valvas coronarianas con calcificaciones en la carilla aórtica y ruptura parcial del rafe cerca del punto de coaptación. En su aspecto ventricular se observan vegetaciones grumosas con formación trombótica en su borde libre. En la unión mitroaórtica se observa un bolsillo que invade la valva anterior de la válvula mitral, donde se encuentran vegetaciones y secreción purulenta (Figura 1). Al retirar el material infeccioso se observa una perforación de la valva anterior de la válvula mitral que también involucra la valva no coronaria de la válvula aórtica. Se reseca la válvula aórtica, se realiza reparo de la válvula mitral, se cierra la perforación y se interpone un parche de pericardio autólogo (Figura 2). Se realiza reemplazo valvular aórtico con prótesis mecánica y exclusión de la orejuela izquierda. El ecocardiograma intraoperatorio evidencia válvula aórtica protésica bien posicionada y ausencia de insuficiencia mitral.
El curso posoperatorio es favorable, con retiro de la ventilación mecánica en las primeras horas. Requiere milrinona durante 3 días. El ecocardiograma de control no evidencia vegetaciones residuales y se confirman hallazgos del ecocardiograma intraoperatorio. En el cultivo de la válvula aórtica se evidencia crecimiento de Actinomyces Denticolens. Se ajusta el manejo antibiótico endovenoso con penicilina y doxiciclina por 6 semanas, posteriormente con amoxicilina y oxacilina oral, y completa 6 meses según recomendación de Infectología
Actualmente se encuentra en buenas condiciones generales, anticoagulado con warfarina en rango terapéutico.
La EI valvular nativa del lado izquierdo sigue siendo la presentación más común de EI, y representa el 70% de todos los casos 5. En la válvula aórtica el principal factor predisponente es la bicuspidización de la válvula, como en este caso. El tratamiento de este paciente generó retos quirúrgicos dado que hubo demora en la consulta por condiciones sociales. Cuando finalmente consultó, estaba en falla cardiaca y edema pulmonar, requiriendo manejo en Cuidados Intensivos por el deterioro agudo de la función del ventrículo izquierdo.
En los casos de EI en la valvula aórtica no hay evidencia de superioridad de la reparación vs el reemplazo4. En este paciente la destrucción valvular aórtica extensa no permitió conducta diferente del reemplazo.
La decisión sobre qué tipo de prótesis valvular elegir se basa en los criterios usuales5. Sin embargo, hay que tener algunas consideraciones en los pacientes con EI, como el compromiso neurológico actual, otras indicaciones de anticoagulación prolongada y el riesgo de un evento hemorrágico cerebral. En estos casos, la anticoagulación podría traer mayores complicaciones y es preferible el implante de una prótesis biológica. En este paciente dada la edad, presencia de trombo intracavitario e integralidad de su estado neurológico, se decidió el reemplazo valvular aórtico mecánico.
Para la EI de válvula mitral nativa las guías de práctica clínica sugieren la reparación siempre que sea posible, cuando no haya abscesos valvulares o compromiso grave del aparato subvalvular 5,6.
En este caso consideramos que la enfermedad mitral era una extensión de la infección aórtica. Se optó por la reparación de la válvula mitral dado que la perforación estaba bien delimitada, los bordes eran fuertes y la exposición quirúrgica era favorable. Se logró una limpieza exhaustiva del tracto de salida y el absceso estaba bien delimitado lo cual permitió el debridamiento fino de sus bordes y la colocación de un parche de pericardio.
Este es el primer caso reportado en la literatura de EI subaguda por A.Denticolens, el cual debe tenerse en cuenta cuando se trate de endocarditis con cultivos negativos. Adicionalmente se presenta el manejo quirúrgico exitoso en un cuadro complejo, que puede servir como referencia en próximos casos.