INTRODUCCIÓN
El síndrome INOCA (por sus siglas en inglés: Ischemia with Non-Obstructive Coronary Arteries) se define por la presencia de signos o síntomas de isquemia sin enfermedad coronaria epicárdica obstructiva y es un hallazgo cada vez más frecuente, principalmente en mujeres. 1,2,3
La prevalencia global se estima cercana al 39%, sin embargo, varía notablemente según el sexo, hallándose en el 33% de los hombres y hasta en un 65% de las mujeres sintomáticas estudiados electivamente con cinecoronariografía. 1,2,3
Entre las distintas causas fisiopatológicas propuestas para explicar estos síndromes, se plantean principalmente dos mecanismos: la ocurrencia de vasoespasmo epicárdico o la presencia de disfunción microvascular (DMV). 4,5
La vasorreactividad coronaria puede evaluarse en forma invasiva, mediante angiografía coronaria. Otra alternativa para valorar la función microvascular es a través de métodos de imágenes, de manera no invasiva, siendo actualmente la PET (Positron Emission Tomography) cardíaca el método de referencia y con mayor validación, a través de la cuantificación del flujo sanguíneo miocárdico (FSM) y la reserva de flujo miocárdica (RFM). 6,7,8,9,10
Las nuevas cámaras gamma con detectores CZTSPECT, poseen mayor sensibilidad y resolución que las tradicionales cámaras con detectores de yoduro de sodio y cuentan con la capacidad de realizar una adquisición dinámica que permite la cuantificación del FSM y el cálculo de la RFM de manera análoga a la PET. 11,12,13
Para cuantificar el FSM y la RFM, es necesario provocar una hiperemia máxima, que puede alcanzarse por diferentes estímulos, con la evaluación de diferentes mecanismos fisiológicos: la administración de dipiridamol actúa inhibiendo la recaptación de la adenosina endógena, y genera vasodilatación microvascular por inhibición del flujo de entrada de calcio en las células del músculo liso, mientras que la prueba de frío (PF), es un potente factor estresante del sistema simpático que conduce a la liberación de óxido nítrico (de manera similar a la acetilcolina) y factores hiperpolarizantes derivados del endotelio. 7,14,15,16,17
La realización de pruebas no invasivas de medición del FSM y la RFM con el uso de ambos apremios, podría resultar útil para establecer el diagnóstico de DMV y diferenciar el o los mecanismos fisiopatológicos involucrados.
El objetivo de esta investigación fue determinar la prevalencia de DMV en pacientes con INOCA, a través de la medición de la RFM con dipiridamol y la variación del FSM (∆FSM) con PF, de manera no invasiva.
MATERIAL Y MÉTODOS
Diseño del estudio: unicéntrico, cohorte única prospectiva.
Población: Se incluyeron en forma consecutiva 93 pacientes con INOCA, en quienes se había descartado la presencia de lesiones coronarias obstructivas (mayor o igual a 50%), mediante angiografía coronaria electiva (n=83) o tomografía coronaria multicorte (n=10). Se excluyeron los pacientes con evidencia de infarto de miocardio, miocardiopatías, deterioro de la fracción de eyección y valvulopatías.
Método para adquisición y procesamiento de imágenes
A todos los pacientes se les realizó un estudio de perfusión miocárdica con CZT-SPECT mediante protocolo de dos días, sin suspender la medicación habitual.
En el primer día, se obtuvieron los valores hemodinámicos basales tras lo cual se inyectaron 7mCi de Tc99m-MIBI en reposo y se obtuvieron imágenes dinámicas para la determinación de FSM basal, seguidas de las imágenes de perfusión miocárdica (IPM) convencionales. A los 60 minutos, se les administró 0,56 mg/kg de dipiridamol endovenoso en 4 minutos, seguidos de 21mCi de Tc99m-MIBI y se obtuvieron nuevamente los valores hemodinámicos e imágenes dinámicas para la determinación del FSM tras el apremio e IPM.
En el segundo día, se obtuvieron nuevamente los valores hemodinámicos basales y se los comparó con los obtenidos el día previo. Como no hubo variación significativa y por acuerdo con el comité de ética de la institución, siguiendo las normas regulatorias establecidas de administrar la menor dosis de material radiactivo que sea posible, no se volvió a inyectar Tc99m-MIBI a los pacientes en reposo, sino que directamente se inició el protocolo con el segundo apremio.
La PF se realizó sumergiendo la mano a temperatura de 4 ºC durante 2 minutos, tras lo cual se inyectaron 21mCi de Tc99m-MIBI y se obtuvieron nuevamente valores hemodinámicos, imágenes dinámicas para la determinación del FSM, seguidas de las IPM convencionales.
Las imágenes y la cuantificación del FSM en reposo y tras ambos apremios fueron procesadas con el software 4DM®. El FSM se expresó en ml/min/gr. La RFM se expresa como la relación entre el FSM con dipiridamol/ FSM reposo, mientras que la ∆FSM con PF se expresa como la relación FSM PF/FSM de reposo.
Se consideró anormal a una RFM con valor menor a 2, y a una ∆FSM a la PF al valor menor a 1,5. 14,15,16,17 Se definió como DMV a la presencia de una o ambas respuestas anormales. Combinando estos resultados obtenidos en nuestra muestra de pacientes, se obtuvieron 4 grupos: 1) RFM normal y ∆FSM anormal, 2) RFM anormal y ∆FSM anormal, 3) RFM anormal y ∆FSM normal, y 4) RFM y ∆FSM normales.
Análisis estadístico
Las variables cuantitativas se expresaron como mediana con su correspondiente rango intercuartilo (RIC), de acuerdo a su distribución y para la comparación entre grupos se utilizó el test de Kruskal-Wallis. Las variables cualitativas se expresaron en porcentajes y fueron comparadas mediante Chi-square test múltiple. Se utilizó el test de Bonferroni para la comparación inter grupos.
Se estableció el nivel de significancia estadística como p <0.05. Para los análisis se utilizó StatsDirect version 3.3.5.
RESULTADOS
Fueron analizados 93 pacientes. No se observaron diferencias significativas entre las características basales ni la medicación de los pacientes entre los diferentes grupos, a excepción del uso de estatinas (Tabla 1). Ningún paciente formó parte del grupo 3.
Tabla 1 Características basales de los pacientes
| Grupo 1 | Grupo 2 | Grupo 4 | p | |
|---|---|---|---|---|
| (n = 40) | (n = 39) | (n = 14) | ||
| Edad (a.) (media ± DE) | 59 ± 11 | 58 ± 12 | 56 ± 10 | ns |
| Sexo: | ||||
| Masculino | 12 (30%) | 16 (41%) | 6 (43%) | ns |
| Femenino | 28 (70%) | 23 (59%) | 8 (57%) | ns |
| Síntomas o cambios en ECG: | ||||
| Angina atípica | 34 (74%) | 28 (72%) | 10 (71%) | ns |
| Angina típica | 3 (8%) | 9 (23%) | 4 (29%) | ns |
| IST >3mm | 3 (8%) | 2 (5%) | 0 | ns |
| FRCV presentes: | ||||
| Diabetes | 5 (12%) | 5 (13%) | 1 (7%) | ns |
| Hipertensión | 19 (48%) | 19 (48%) | 6 (43%) | ns |
| Tabaquismo | 14 (35%) | 15 (38%) | 5 (36%) | ns |
| Dislipemia | 24 (60%) | 24 (62%) | 7 (50%) | ns |
| 4 FRCV | 1 (2%) | 3 (8%) | 0 | ns |
| 3 FRCV | 5 (12%) | 6 (16%) | 3 (21%) | ns |
| 2 FRCV | 17 (43%) | 10 (25%) | 3 (21%) | ns |
| 1 FRCV | 9 (23%) | 13 (33%) | 4 (29%) | ns |
| Sin FRCV | 8 (20%) | 7 (18%) | 4 (29%) | ns |
| Menopausia | 25 (89%) | 18 (78%) | 8 (100%) | ns |
| Medicación habitual: | ||||
| Aspirina | 16 (40%) | 17 (44%) | 7 (50%) | ns |
| Beta-bloqueantes | 11(28%) | 15 (38%) | 9 (64%) | ns |
| IECA | 11(28%) | 9 (23%) | 9 (64%) | ns |
| ARA II | 6 (15%) | 5 (13%) | 0 | ns |
| Clopidogrel | 2 (5%) | 2 (5%) | 2 (5%) | ns |
| Bloqueantes cálcicos | 6 (15%) | 12 (31%) | 2 (5%) | ns |
| Trimetazidina | 4 (10%) | 6 (15%) | 2 (5%) | ns |
| Dinitrato de Isosorbide | 2 (5%) | 7 (18%) | 0 | ns |
| Estatinas | 25 (63%) | 20 (51%) | 14 (100%) | 0.005 |
DE: desviación estándar, ECG: Electrocardiograma, IST: Infradesnivel del segmento ST, FRCV: Factores de riesgo cardiovascular, IECA: Inhibidores de la enzima convertidora de angiotensina, ARA II: Antagonistas de receptores de angiotensina II
Ochenta y ocho pacientes eran sintomáticos. La DMV fue evaluada luego de haber tenido el primer episodio de dolor precordial en 32, mientras que en los 56 restantes la evaluación se realizó luego de varios episodios sintomáticos. Incluso, a 18 de ellos, se les realizó angiografía diagnóstica en más de una oportunidad. Todos los casos tuvieron el último episodio de dolor precordial, al menos 30 días previos al estudio. Cinco pacientes fueron considerados INOCA por antecedentes de infradesnivel del segmento ST (IST) asintomático en pruebas de esfuerzo (3 pacientes del grupo 1 y 2 pacientes de grupo 2)
Las IPM fueron normales en reposo y con ambos apremios en todos los pacientes. Se consideró IPM normal a aquella que no mostraba defectos segmentarios de la captación de Tc99m-MIBI, valorado en forma cuantitativa por una escala de suma tras cada apremio y en reposo igual a cero y en forma cualitativa, comparando los mapas polares de cada paciente con los de referencia del software. Tampoco debían presentar trastornos en la motilidad parietal regional o global ni fracción de eyección ventricular izquierda < 55%.
Cinco pacientes manifestaron molestia precordial durante el apremio con dipiridamol y ninguno presentó alteraciones en el electrocardiograma durante ambos apremios.
Se observaron 79 (85%) pacientes con DMV. Hubo 40 pacientes (43%) en el grupo 1, 39 pacientes (42%) en el grupo 2, ningún paciente en el grupo 3, y 14 pacientes (15%) en el grupo 4.
Los parámetros hemodinámicos basales y tras ambos apremios no mostraron diferencias estadísticamente significativas entre los grupos, a excepción del FSM en reposo entre los grupos 2 y 4 (p< 0,05), tras el dipiridamol entre el grupo 1 vs el 2 (p< 0,0001) y vs el 4 (p<0,05), como así también entre los grupo2 y 4 (p<0,05), y en la PF entre los grupos 1 y 2 vs el grupo 4 (p<0,0001).
Encontramos diferencia significativa en la RFM entre el grupo 1 y el 2 (p < 0,0001) y entre el grupo 2 y el 4 (p < 0,0001), así como en la ∆FSM con PF entre el grupo 1 vs. el grupo 2 (p = 0,0013), el grupo1 vs. el grupo 4 (p < 0,0001) y entre el grupo 2 vs. el grupo 4 (p < 0,0001). Los valores de ∆FSM menores a 1 también mostraron diferencia significativa entre los grupos 1 y 2 (p< 0,0001) (Tabla 2).
Tabla 2 Valores hemodinámicos y resultados obtenidos por grupos
| Grupo 1 | Grupo 2 | Grupo 4 | |
|---|---|---|---|
| (n = 40) | (n = 39) | (n = 14) | |
| Reposo | |||
| FC (lpm) | 65 (58-75) | 64 (59-70) | 62 (59-71) |
| TAS (mmHg) | 130 (120-135) | 130 (120-130) | 130 (120-140) |
| TAD (mmHg) | 80 (80-80) | 80 (80-80) | 80 (70-90) |
| DP | 7975 (7450-10010) | 8160 (7200-9100) | 8305 (7080-9230) |
| FEVI(%) | 75 (68-83) | 71 (66-71) | 70 (67-77) |
| FSM (ml/min/gr) | 1,05 (0,81-1,29) | 1,18 (0,93-1,32) *vs G4 | 0,71 (0,66-1,15) |
| Dipiridamol: | |||
| FC (lpm) | 80 (68-93) | 74 (68-80) | 75 (64-86) |
| TAS (mmHg) | 120 (117-130) | 130 (120-140) | 125 (110-140) |
| TAD (mmHg) | 80 (75-80) | 80 (80-80) | 80 (70-80) |
| DP | 9615 (8425-11850) | 9000 (8360-10200) | 9030 (7920-10360) |
| FEVI(%) | 73 (70- 82) | 74 (70-80) | 75 (70-81) |
| FSM (ml/min/gr) | 2,69 (2,15-3,32) †vs G2*vs G4 | 1,84 (1,49-2,07) *vs G4 | 2,09 (1,72-2,84) |
| PF: | |||
| FC (lpm) | 70 (61-80) | 72 (67-78) | 70 (66-80) |
| TAS (mmHg) | 120 (110-130) | 120 (120-130) | 125 (120-140) |
| TAD (mmHg) | 80 (75-80) | 80 (70-80) | 80 (80-80) |
| DP | 8400 (7250-9610) | 8760 (8040-9620) | 9045 (8260-9940) |
| FEVI(%) | 74 (69-81) | 72 (67-77) | 73 (69-80) |
| FSM (ml/min/gr) | 1,04 (0,83-1,59) †vs G4 | 0,99 (0,77-1,23) †vs G4 | 1,70 (1,19-1,96) |
| RFM | 2,58 (2,13-3,26) | 1,56 (1,41-1,69 †vs G1 y G4 | 2,53 (2,25-3,18) |
| ∆FSM | 1,08 (0,95-1,26) *vs G2 †vs G4 | 0,87 (0,72-1,11) †vs G4 | 1,79 (1,54-2,02) |
| ∆FSM<1 | 0,87 (0,71-0,94) | 0,79 (0,69-0,87) †vs.G1 | - |
*p< 0,05 †p< 0,0001
Todos los valores se presentan como mediana y rango intercuartilo
FC: Frecuencia cardíaca TAS: Tensión arterial sistólica, TAD: Tensión arterial diastólica, DP: doble producto (TASmáx x FCmáx), FEVI: fracción de eyección ventricular izquierda, FSM: Flujo sanguíneo miocárdico, RFM: Reserva de flujo miocárdica, ∆FSM: variación del flujo sanguíneo miocárdico, PF: prueba de frío
DISCUSIÓN
En nuestro trabajo, la mayoría (n=79) de los pacientes con INOCA estudiados con CZT-SPECT, tuvieron respuesta vasodilatadora anormal con el PF, lo que pone en evidencia, una DMV endotelio dependiente. Los pacientes del grupo 2 además, tuvieron RFM con dipiridamol disminuida, evidenciándose un doble componente fisiopatológico en este subgrupo (Figura 1).

Fig. 1 Paciente con DMV músculo liso y endotelio dependiente. A. Dipiridamol (RFM: 1,84) B. Prueba de frío (ΔFSM: 0,71)
La realización de ambos apremios en nuestros pacientes, nos permitió evaluar diferentes mecanismos fisiopatológicos posibles de la DMV: dependiente del endotelio o dependiente del músculo liso. Con el agregado de la PF, pudimos detectar una DMV en la mayoría de los casos, aún en aquellos pacientes con respuesta vasodilatadora normal al dipiridamol, como fueron los pacientes del grupo 1.
La respuesta del FSM con PF fue anormal no solo porque no aumentó el 50% esperado, sino que además en 38 pacientes, el FSM disminuyó con respecto del valor basal, lo que podría interpretarse como un vasoespasmo microvascular endotelio dependiente (Figura 2). De estos 38 pacientes, 12 (32%) pertenecían al grupo 1 y 26 pacientes (68%), al grupo 2 (p< 0,001), lo que podría reflejar una mayor afectación microvascular en este último grupo de pacientes, con un compromiso tanto funcional como estructural.18
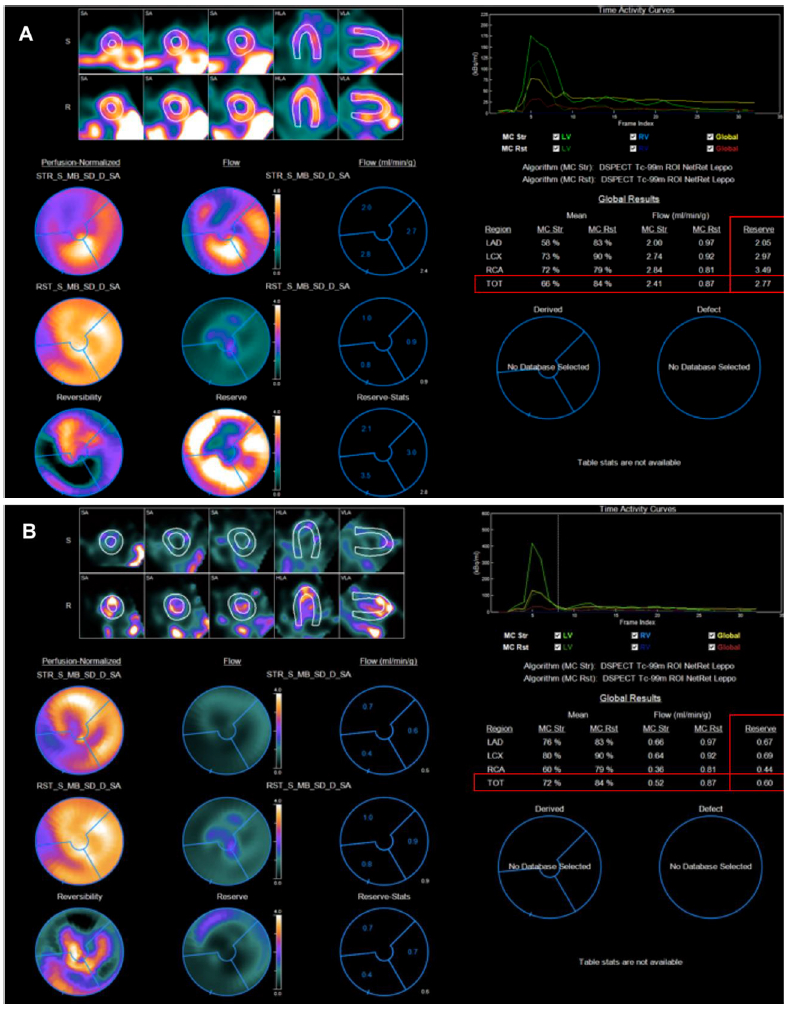
Fig. 2 Paciente con vasoespasmo microvascular endotelio dependiente. A. Dipiridamol (RFM: 2,77) B. Prueba de frío (ΔFSM: 0,60)
En los pacientes (n=14) que tuvieron ∆FSM con PF y RFM con dipiridamol normales, no pudimos establecer características clínicas ni metodológicas que justifiquen una diferencia con el resto de los pacientes. Sin embargo, ello podría estar relacionado a la existencia de una angina de origen vasoespástico, no detectable por este método, o bien podría deberse a la existencia de otras causas de dolor precordial, como el de origen neuropático. Sólo podemos mencionar como dato distintivo, que este grupo de pacientes en su totalidad estaban medicados con estatinas.
En ninguno de nuestros pacientes se realizó prueba de acetilcolina ni ergonovina intracoronaria durante el estudio angiográfico invasivo inicial, por lo que no podemos afirmar que la DMV sea el único mecanismo fisiopatológico involucrado, ya que un pequeño porcentaje de los pacientes que padecen este síndrome, pueden presentar angina vasoespástica asociada a la angina microvascular. 8,9
Existe evidencia actual de que la DMV está presente en las primeras etapas de la aterogénesis como consecuencia de cambios estructurales y funcionales que se producen en las paredes de las arteriolas y capilares intramurales, con frecuencia relacionada a la presencia de factores de riesgo cardiovascular (FRCV). 7
Los FRCV aumentan las especies reactivas de oxígeno con lo que el endotelio vascular se vuelve disfuncional. Como consecuencia de esta disfunción endotelial, se libera menor cantidad de sustancias vasodilatadoras como el óxido nítrico, por lo que disminuye la relajación de las células musculares lisas. De manera tal que la estimulación con PF al evaluar la respuesta vasodilatadora dependiente del endotelio, podría detectar estadios más precoces de la DMV aún en presencia de una respuesta vasodilatadora músculo liso dependiente normal. Además, cuanto mayor es el tiempo de exposición a estos FRCV, mayor será el deterioro vascular. 7
La población estudiada en nuestro trabajo presentaba en su mayoría uno o más FRCV. De los 19 pacientes que no tenían ninguno de los FRCV clásicos, 9 eran mujeres en período de menopausia. Numerosos estudios con PET demostraron que la disminución de estrógenos en mujeres post- menopaúsicas es de por sí, un factor que predispone a una menor vasodilatación coronaria similar a la observada en pacientes diabéticas premenopáusicas. (19,20,21
En cuanto a las manifestaciones clínicas de la DMV, los pacientes pueden presentar angina típica inducida por esfuerzo, en la recuperación inmediata post-ejercicio o incluso durante el reposo, pero también pueden referir dolor atípico o síntomas equivalentes de angina, tales como disnea al esfuerzo. Ante esta gran variedad de síntomas, fue que se establecieron diferentes criterios para del diagnóstico de angina microvascular, donde no solo se tienen en cuenta aspectos clínicos, sino que también se incorporaron valores anormales de vasorreactividad coronaria según los diferentes métodos, dentro de los cuales encontramos el FSM y RFM. 9,21,22
Si bien es sabido que la presencia de DMV empeora el pronóstico, tanto en pacientes con o sin enfermedad coronaria obstructiva y más aún cuando producen síntomas, actualmente no contamos con un tratamiento específico. Esto trae aparejado, la existencia de múltiples combinaciones de diferentes fármacos, tal como mostraban nuestros pacientes, incluso algunos sin una evidencia certera de su beneficio. 23,24
La importancia de conocer los mecanismos fisiopatológicos involucrados en los síndromes INOCA, radica en la posibilidad de poder ajustar el tratamiento en cada caso en particular. Existen estudios que demostraron mejoría en la calidad de vida de estos pacientes, cuando se evalúan los diferentes mecanismos y se medica según la causa fisiopatológica involucrada. El CormicA trial evaluó la función coronaria de 151 pacientes con INOCA durante la angiografía diagnóstica invasiva inicial, y los asignó aleatoriamente a dos grupos: 1) manejo terapéutico orientado por los resultados fisiopatológicos invasivos y 2) grupo control. Se compararon los efectos sobre la calidad de vida y los eventos clínicos a largo plazo entre ambos grupos, y se demostró en el seguimiento que el grupo 1 presentó una mejoría clínica marcada y sostenida y una mejor calidad de vida frente al grupo control.2,25
Presentamos un algoritmo diagnóstico sencillo y no invasivo, que incluye la realización de ambos apremios para poder estudiar los dos mecanismos posibles de vasorreactividad coronaria que producen DMV en pacientes con INOCA (Figura 3).

Fig. 3 Algoritmo diagnóstico propuesto para la evaluación no invasiva de la función microvascular en pacientes con INOCA
Limitaciones
La población estudiada fue pequeña y la metodología utilizada es relativamente reciente, aunque con validación y reproducibilidad actualmente aceptadas. Serán necesarios estudios en poblaciones más numerosas para evaluar la utilidad de esta metodología de estudio en pacientes con INOCA.
Si bien en nuestro país no se realiza de forma rutinaria la evaluación funcional coronaria invasiva en los pacientes con INOCA, consideramos que sería conveniente realizarla durante la angiografía coronaria diagnóstica, para descartar el vasoespasmo epicárdico como causa probable o concomitante.
CONCLUSIONES
En nuestra experiencia, el uso de CZT-SPECT detectó DMV en el 85% de los pacientes estudiados con INOCA.
El uso de ambos apremios permitió evaluar dos mecanismos fisiopatológicos diferentes de DMV, dependiente del músculo liso y dependiente del endotelio.
La evaluación con PF debería incluirse en el estudio no invasivo de pacientes con INOCA, ya que la DMV puede estar presente aún con RFM conservada con dipiridamol.















