INTRODUCCIÓN
Desde la aparición del virus SARS-CoV-2 en diciembre de 2019 se han descripto múltiples formas de presentación y síndromes asociados al mismo. Uno de los más agresivos en niños es el síndrome de inflamación multisistémico pediátrico (SIM-C o PIMS). Es una rara complicación que suele aparecer de 2 a 6 semanas luego de haber presentado una infección por SARS-CoV-2.
Inicialmente se pudo observar que los casos graves pediátricos eran escasos y que el virus productor de la enfermedad COVID-19, por lo general, no afectaba en forma grave a la población infantil. Luego comenzaron los reportes aislados sobre un síndrome símil enferme dad de Kawasaki incompleto o atípico, y un síndrome de shock tóxico, temporalmente relacionados a la infección por SARS-CoV-2. 1,2
En la actualidad se considera que el espectro de presentación del SIM-C es amplio, desde un síndrome Kawasaki like a la afectación multisistémica con shock. La incidencia del cuadro Kawasaki like llega a ser de 3,7 a 30 veces mayor respecto a la incidencia habitual de enfermedad típica. 2,3 La afectación cardíaca -de cualquier índole- producida por el SIM-C es mayor a la producida por el Kawasaki típico;4 varía entre el 30% y el 80% de los casos, 2,5-7 y es una de las que mayor morbimortalidad genera.
Se han descripto asociaciones entre valores de laboratorio y mala evolución de la enfermedad, 8,9 pero no existen puntos de corte definidos que predigan la misma.
El objetivo primario del estudio fue describir la pre sentación clínica y comparar parámetros de laboratorio iniciales entre pacientes con diagnóstico de SIM-C que presentaron shock y quienes no, en un centro pediátrico de referencia de la Ciudad Autónoma de Buenos Aires. El objetivo secundario fue analizar la diferencia de positividad de troponina y del fragmento amino terminal del péptido B (NT-proBNP), y establecer puntos de corte para dichos parámetros.
MATERIAL Y MÉTODOS
Se realizó un estudio analítico y retrospectivo de los pacientes internados entre mayo del 2020 y junio de 2021 con diagnóstico de SIM-C en el Hospital General de Niños Dr. Ricardo Gutiérrez. En dicho período se internaron 32 pacientes.
La definición adoptada para la confirmación de casos de SIM-C fue la del Ministerio de Salud de la Nación (https://www.argentina.gob.ar/salud/coronavirus-COVID-19/casos-pediatria):
- Presencia de fiebre por 3 o más días en pacientes entre 0-18 años con evidencia de haber padecido enfermedad por SARS-CoV-2; acompañado de dos o más de:
1. Erupción cutánea o conjuntivitis bilateral no purulenta o signos de inflamación mucocutánea (boca, manos o pies).
2. Hipotensión o shock.
3. Signos de disfunción miocárdica, pericarditis, valvulitis o anomalías coronarias (incluidos los hallazgos ecocardiográficos o elevación de la troponina y de BNP).
4. Evidencia de coagulopatía: elevación de tiempo de pro trombina (TP),tiempo de tromboplastina parcial (TTP), dímero D.
5. Síntomas gastrointestinales agudos (diarreas, vómitos o dolor abdominal)
- Junto a la presencia de marcadores de inflamación ele vados: proteína C reactiva (PCR), velocidad de sedimen tación globular (VSG) o procalcitonina, y la ausencia de alguna causa evidente de inflamación.
Se obtuvieron datos clínicos, cardiológicos y de laboratorio de cada paciente a través del acceso a las historias clínicas (HC). Se clasificó a los pacientes en dos grupos de acuerdo a si presentaron shock durante la internación (Grupo 1) o no (Grupo 2- Control). Se consideró como shock a la hipotensión arterial (presión arterial <-2 DE del percentilo 50 por sexo, talla y edad, Sociedad Argentina de Pediatría) refractaria a volumen, que haya requerido el uso de algún agente vasoactivo constatado en la HC.
Los parámetros de laboratorio analizados fueron la troponina I ultrasensible (reactivo VIDAS® TNHS, troponina I de alta sensibilidad- BioMerieux), NT-proBNP (VIDAS® NT-proBNP2- BioMerieux), plaquetas y linfocitos al momento del diagnóstico. Para el análisis de estos valores se utilizaron puntos de corte del laboratorio de referencia para catalogar los como alterados: troponina >19 ng/L; linfopenia: <1000 linfocitos/mm3; trombocitopenia: plaquetas < 150.000/mm3 y NT-proBNP >300 pg./mL.
Se consideraron estos parámetros, pues según la bibliografía la troponina es marcador de daño cardíaco; la trombocitopenia presenta alto valor predictivo positivo para compromiso cardíaco; el NT-proBNP demostró tener correlación con disfunción cardíaca y la linfopenia grave tiene alta asociación con shock. 8-10
En forma concomitante se evaluaron los estudios cardiológicos complementarios electrocardiograma (ECG) y ecocardiografía, para valorar parámetros de afectación cardíaca durante el proceso de la enfermedad. Para la definición de compromiso cardiológico se utilizó una síntesis de las definiciones aportadas por Pignatelli 5 y por Valverde 7: presencia de alguna arritmia, extrasístoles supraventriculares o ventriculares, taquicardias auriculares o ventriculares -sos tenidas o no-, bloqueo aurículo-ventricular (AV) de cualquier grado, alteraciones en la repolarización ventricular; caída en la función sistólica ventricular izquierda (medida por algún método); dilatación del ventrículo izquierdo (VI) por arriba de Z score + 2; insuficiencias valvulares; derrame pericárdico de cualquier índole; dilatación de arterias coronarias; o elevación de enzimas cardíacas - CPK-MB, troponina. No se incluyó la taquicardia sinusal como daño de órgano dado lo inespecífico de dicho síntoma en paciente febriles.
Para la medición de la función ventricular sistólica izquierda se utilizó la fracción de acortamiento (FA) medida en modo M en un corte circunferencial del ventrículo izquierdo a nivel de los músculos papilares utilizando como referencia el diámetro diastólico del ventrículo izquierdo (DDVI) y el diámetro sistólico del ventrículo izquierdo (DSVI): (DDVI-DSVI) /DDVI × 100. Se interpretó como disfunción sistólica a la caída de la FA por debajo de 30%.
Análisis estadístico
En primer lugar, se realizó un análisis descriptivo de la pobla ción incluida y se estudiaron las diferencias entre el Grupo 1 y el Grupo 2. Las variables cualitativas se presentan como valor absoluto y porcentaje, y se compararon con la prueba de chi cuadrado o la prueba exacta de Fisher. Las variables cuantitativas se presentan como media y desviación estándar y se comparan con la prueba de t. Finalmente, a través de la construcción de curvas ROC, se analizó la capacidad de discriminación para troponina y NT-proBNP entre ambos grupos, y se establecieron valores de corte. El análisis estadístico se llevó a cabo mediante el programa SPSS 25 Statistics (IBM, Chicago, IL).
Consideraciones éticas
El trabajo de investigación fue observacional y retrospectivo, no se realizaron intervenciones en los pacientes por fuera de las normas y consensos de práctica clínica acorde a la patología. Se tomó como referencia a la ley 3301 de La Ciudad Autónoma de Buenos Aires, la Declaración de Helsinki y a las guías de Buenas Prácticas Clínicas. Los datos se encuentran codificados de forma tal de mantener la confidencialidad de los pacientes (Ley n° 25.326).
RESULTADOS
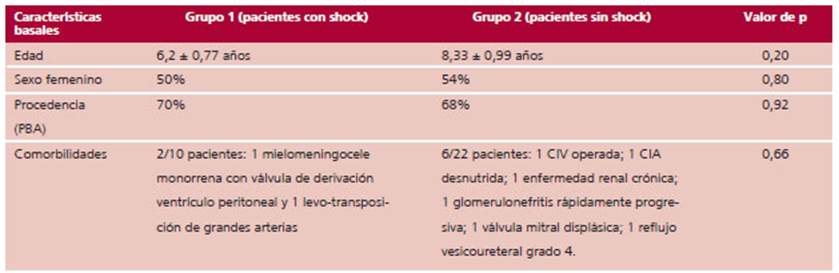
Se analizaron 32 pacientes con diagnóstico de SIM-C, de los cuales 15 fueron masculinos (46,9%) y 17 femeninos (53,1%). La edad promedio de presentación fue de 7,67 años (rango de 0,5 a 14,91 años). Las comorbilidades más frecuentes fueron cardiológicas y nefro-urológicas (Tabla 1). La mayoría de los pacientes presentaron serología positiva para SARS-CoV-2 (28 pacientes de 32); de los restantes cuatro, 2 tuvieron infección documentada previamente y los otros 2 nexo epidemiológico positivo para COVID-19.
En el Grupo 1 hubo 10 pacientes (31,2%) y 22 en el Grupo 2 (68,8%). No se obtuvo el valor inicial de NT-proBNP en tres pacientes (los tres del Grupo 2) y en solo un paciente no se registraron los valores ini ciales de linfocitos y plaquetas (paciente del Grupo 1). La edad promedio en el Grupo 1 fue de 6,2 años, con rango de 2,41 a 10,16 años; para el Grupo 2 el rango fue más amplio, desde 0,5 a 14,91 años, con un pro medio de 8,33 años. Cerca del 70% de los pacientes en ambos grupos eran de la Provincia de Buenos Aires. Al comparar las características basales de cada Grupo no se hallaron diferencias significativas en términos de edad, distribución por sexo, procedencia y comor bilidades (Tabla 1).
Las comorbilidades más frecuentes fueron las cardio patías congénitas (levo transposición de grandes vasos, comunicación interauricular, comunicación interventricular -operada, sin patología residual- y válvula mitral displásica sin disfunción), y antecedentes nefrourológicos (glomerulonefritis rápidamente progresiva, reflujo vesicoureteral grado 3, enfermedad renal crónica y una paciente monorrena con mielomeningocele).
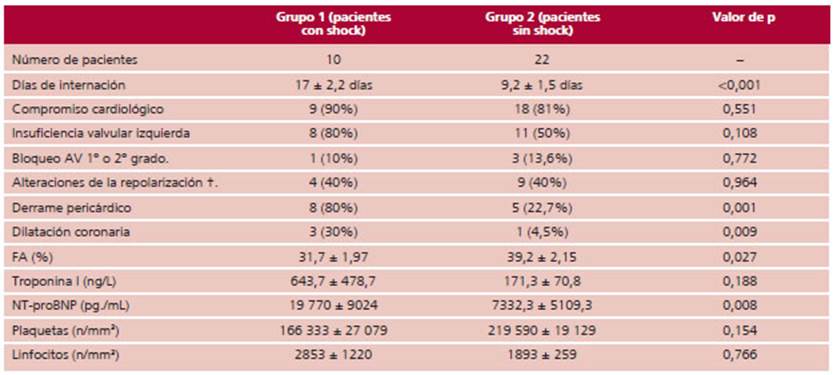
Luego de obtener los datos clínicos, ecocardiográficos y de laboratorio de los pacientes, se compararon los resultados medios en cada grupo (Tabla 2, Figura 1). La estadía hospitalaria media fue de 11,6 días, significativamente mayor en los pacientes que presentaron shock con requerimiento de Unidad de Cuidados Intensivos Pediátrica (UCIP): 17 días vs. 9,2 días (p <0,001). En el Grupo 2 hubo dos pacientes con internaciones prolongadas de causa social. Un total de 13 niños re quirieron el uso de algún agente inotrópico (por shock o por disfunción miocárdica sin shock).

Fig. 1 A la izquierda de cada fila se muestra la distribución de un determinado valor (plaquetas, proBNP, troponina I de alta sensibilidad y linfocitos) expresado como media y error estándar según la presencia (1 o SI) o ausencia (0 o NO) de shock. A la derecha se muestra el gráfico de distribución de cada valor expresado como mediana y la dispersión de los valores también según la pre sencia (1 o SI) o ausencia (0 o NO) de shock
La incidencia de afectación cardíaca fue del 84,4% (27 pacientes), todos ellos presentaron al menos un parámetro alterado. Dentro de los trastornos más frecuentemente observados encontramos la elevación de los valores de troponina I ultrasensible por encima de los valores de referencia del laboratorio (21 pacientes, 77%), insuficiencias valvulares mitral o aórtica de cualquier índole en 19 pacientes (70%), alteraciones de la repolarización en el electrocardiograma (13 pacien tes,48%) y la disfunción sistólica (8 pacientes, 29,6%). La dilatación de las arterias coronarias se pudo apreciar en 4 pacientes (12,5%): 3 del Grupo 1 y 1 del Grupo 2 (p = 0,009). Otras alteraciones observadas fueron el bloqueo AV de primer o segundo grado y el bloqueo incompleto de rama derecha; todos estos hallazgos se normalizaron luego de iniciado el tratamiento adecuado. La función ventricular medida por FA fue menor en pacientes del Grupo 1: 31,7 ±1,97 vs. 39,2 ± 2,15% (p = 0,027). La presencia de derrame pericárdico cons tatado por ecocardiografía fue significativamente ma yor en pacientes con shock (80% vs 22,7%; p = 0,001)
El 30% (3/10) de los pacientes con shock presentaron trombocitopenia (recuento plaquetario <150 mil/ mm3) al ingreso, mientras que en el Grupo 2 la inciden cia fue 13% (3/22), p = 0,138. La linfopenia (linfocitos <1.000/mm3) se encontró presente en 4 pacientes del Grupo 1 (40%) y en 4 del grupo control (18%), sin diferencia estadísticamente significativa (p = 0,14). Entre quienes requirieron algún agente inotrópico, 7 de los 12 pacientes en quienes se obtuvo el valor inicial de linfocitos presentaron linfopenia (58,3%), mientras que entre los 19 pacientes que no requirieron drogas inotrópicas, solo 1 (5,2%) presentó linfopenia al momento del diagnóstico (p = 0,006). La linfopenia presentó especificidad de 95% y valor predictivo positivo de 88% para el uso de inotrópicos. En términos de valores absolutos de plaquetas y linfocitos no hubo diferencias entre ambos grupos.
La troponina I Ultrasensible se encontró elevada (>19 ng/L) en 21/32 pacientes (65,6%), en el 80% (8/10) de los pacientes del Grupo 1 y en el 59% (13/22) del Grupo 2. El valor medio de troponina varió entre am bos grupos, si bien fue mayor en el Grupo 1, no hubo diferencia estadísticamente significativa (p = 0,188). Al definir el mejor valor de corte por curva ROC -troponina I 50 ng/l- y emplearlo en forma dicotómica (positivo-negativo) pudimos apreciar una tasa de positividad en el Grupo 1 del 80% y del 31,8% en Grupo 2 (p = 0,01).
Con el punto de corte establecido para NT-proBNP por el laboratorio de referencia (se considera elevado un valor >300 pg./mL), se observó una positividad al inicio del 90% (9/10) en pacientes con shock, y del 89% (17/19 testeados) en el grupo control. El valor medio de NT-proBNP fue significativamente más elevado en los pacientes con shock (19.770 vs 7.332 pg./mL, p = 0,008).
En análisis con curva ROC, el mejor valor de corte de NT-proBNP para predecir shock fue 3900 pg./mL. Se utilizaron conjuntamente este valor de corte y el de troponina I ultrasensible ajustada (50 ng/L), y se analizó a los pacientes en forma dicotómica: ambos valores positivos vs. cualquier otra combinación. La combinación presentó un valor predictivo negativo (VPN) del 86% para shock.
DISCUSIÓN
Describimos 32 pacientes que reunieron criterios de SIM-C. Las características de la población en cuanto a edad de presentación y distribución por sexo son similares a las descriptas en otras series, 6-8,11-13 con un ligero predominio de pacientes femeninos. Los pacientes del Grupo 1 presentaron una edad promedio menor. En tanto que el 31% presentó shock durante su evolución, el 40% de los pacientes requirió el uso de algún agente inotrópico.
El compromiso cardíaco no difirió respecto de otras publicaciones y se manifestó en torno al 84%; en tanto que la incidencia reportada internacionalmente de dilatación de arterias coronarias fue del 8-24%, en nuestra serie el valor alcanzó el 12,5%. 4,5,8,11,14,15 El derrame pericárdico estuvo presente en el 40% de los pacientes, y se encontraron diferencias significativas en la presencia de este entre el Grupo 1 y el Grupo 2.
La gran diferencia entre los trabajos de Valverde y Pignatelli en la definición de compromiso cardiológico radica en la clasificación de las insuficiencias valvulares; es más restrictivo el criterio de Pignatelli al incluir únicamente insuficiencias moderadas o graves. Si bien amplía el número total de pacientes con compromiso cardíaco, creemos que las insuficiencias valvulares izquierdas triviales, leves o moderadas, al haber revertido una vez cumplido el tratamiento, deben ser consideradas como marcador de daño de órgano.
Pese a haber sido reportadas muertes debido a esta patología, en nuestra serie no hubo óbitos. 5
Pignatelli encontró que los valores elevados de troponina y la trombocitopenia tuvieron alta sensibilidad y valor predictivo negativo para requerimiento de estadía en UCIP. En nuestra serie los pacientes con valores promedio más altos de Troponina y NT-proBNP y con valores más bajos de plaquetas presentaron una evolución desfavorable con shock, aunque el único valor estadísticamente significativo fue el de NT-proBNP. Tras ajustar por curvas ROC, la troponina elevada también mostró estar relacionada con shock.
Al analizar datos de laboratorio en relación con el uso de agentes inotrópicos los resultados son similares a la bibliografía internacional (descrita en pacientes con requerimiento de UCIP): tanto la troponina I ultrasensible (p = 0,029), como el NT-proBNP (p = 0,002) y la linfopenia (p <0,001), mostraron una diferencia estadísticamente significativa entre pacientes que requirieron el uso de algún agente inotrópico y quiénes no.
De acuerdo a nuestra experiencia, consideramos que el rol del cardiólogo infantil sigue siendo clave a la hora de pensar la mejor terapéutica para cada paciente. El posible compromiso cardiológico hace que tanto la toma de muestra para laboratorio como la realización de un ECG y un ecocardiograma deban ser rutinarios al ingreso hospitalario.
La fortaleza de este estudio radica en la adquisición de la mayoría de datos buscados, ya que fueron pocos los valores perdidos en contexto de la emergencia sanitaria por la pandemia. Las características generales de la población no fueron significativamente diferentes a las poblaciones reportadas en otros estudios. Los datos obtenidos que fueron estadísticamente significativos pueden correlacionarse con peor evolución clínica de los pacientes con SIM-C.
La principal debilidad es el número de pacientes y el diseño retrospectivo del estudio. Si bien no todos los centros tienen la disponibilidad de dosar troponina o NT-proBNP, la fórmula leucocitaria y el recuento de plaquetas se encuentran ampliamente disponibles.
CONCLUSIÓN
El SIM-C puede afectar cualquier órgano. En nuestro estudio observamos una alta incidencia de compro miso cardiológico y diferencias significativas en la dilatación de arterias coronarias y la presencia de derrame pericárdico entre quienes presentaron shock y quienes no; por lo que consideramos que la evaluación inicial por un cardiólogo infantil es vital en el manejo de los pacientes. La presencia de linfopenia o valores elevados de NT-proBNP y troponina deben ser tenidos en cuenta para el abordaje terapéutico inicial tanto en centros periféricos como en hospitales de referencia.